Изобретение относится к производным кетоноксимов, в частности к O-[(4-карбометоксииминофенокси)-этил]алканальдокси-мам общей формулы I
4-MeON=C(R)-C6H4OCH2CH2ON=CHR', где R атом водорода, фенил;
R1 этил, пропил, изо-пропил, обладающим инсектицидной активностью.
Предлагаемые соединения могут быть использованы в сельском хозяйстве в качестве средств борьбы с вредителями растений.
Известен метопрен формулы II
MeO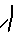

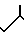

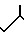
 O
O обладающий инсектицидной активностью. Соединение формулы II недостаточно активно. В концентрации растворов 3.10-3 мг/л он вызывает метаморфоз и гибель 40% личинок комнатной мухи.
обладающий инсектицидной активностью. Соединение формулы II недостаточно активно. В концентрации растворов 3.10-3 мг/л он вызывает метаморфоз и гибель 40% личинок комнатной мухи.
Известен О-эфир феноксифеноксиалканальдоксима формулы III
4-PhO-C6H4OCH2CH2ON=CHEt, обладающий инсектицидной активностью. Соединение формулы III в концентрации 0,3 мг/л вызывает 100%-ную гибель личиной комнатной мухи.
Известен феноксикарб формулы IV
4-РhOC6H4OCH2CH2NHCO2Et, обладающий инсектицидной активностью. Однако аналог формулы IV менее активен. Так, феноксикарб в растворах при концентрации 1.10-2 мг/л вызывает метаморфоз и гибель 50% личиной хлопковой совки.
Цель изобретения создание новых производных альдоксимов, обладающих более высокой инсектицидной активностью. Указанная цель достигается синтезом соединений формулы I.
Соединения формулы I могут быть получены следующим способом:
O=C(R)C6H4ONa  O=C(R)C
O=C(R)C C
C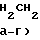 ON=CHR′
ON=CHR′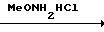 MeON=C(R)C6H4OCH2CH2ON=CHR′
MeON=C(R)C6H4OCH2CH2ON=CHR′
R=Ph(a-в), H(г); R1 Et(a), Pr(б, г), изо-Pr(a).
Фенол (II, R=Ph или Н) обрабатывают сначала метилатом натрия и затем в растворе диметилформамида -β -хлорэтиловым эфиром алканальдоксима формулы III. Образующийся при этом эфир формулы IV нагревают с солянокислым О-метиловым эфиром гидроксиламина в спиртово-пиридиновом растворе, что приводит к образованию соединений формулы I.
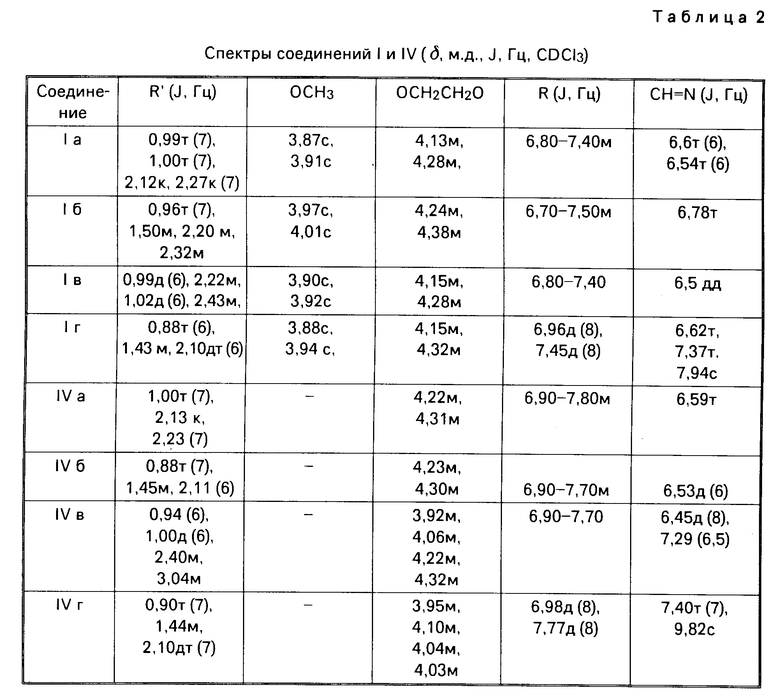
Строение соединений доказано с помощью спектров ЯМР и элементного анализа. Спектры ЯМР записаны на приборе Varian VXR-300 (300 МГц).
Чистота и индивидуальность соединений установлены с помощью газожидкостной и высокоэффективной хроматографии на приборах "Chrom 5" (3,5 м колонка с сорбентом OV-1), "Милихром 1А" (10 см колонка с обращенно-фазовым сорбентом Sеparon C18). Элюент ацетонитрил + вода в соотношении 5:1. Было установлено, что диоксимы формулы I существуют в виде смеси син- и анти-изомеров по кетоксимной и альдоксимной группам, которые можно наблюдать с помощью спектров ПМР. Однако, по-видимому, в связи с легкой син- анти-изомеризацией на хроматограммах соединений формулы I имеется один пик и интервалы температур кипения изменяются в узких пределах (1-2оС).
П р и м е р 1. 0-[(4-оксибензофенон)этил]пропиональдоксим (IVa).
9,5 г 4-гидроксибензофенона в 15 мл метанола обработали 2,7 г метилата натрия в 15 мл метанола, раствор упарили. К остатку прибавили 35 мл диметилформамида, 10,0 г β -хлорэтилового эфира пропиональдоксима и 0,1-0,2 г иодистого калия. Реакционную смесь кипятили 5-6 ч. Затем смесь охладили, вылили в воду и экстрагировали продукт 50 мл диэтилового эфира. Эфирный экстракт промыли 10%-ным водным раствором КОН, водой, высушили сульфатом натрия. Эфир упарили, остаток перегнали в вакууме, т.кип. 186-189оС (0,01 мм рт.ст.), выход 5,1 г.
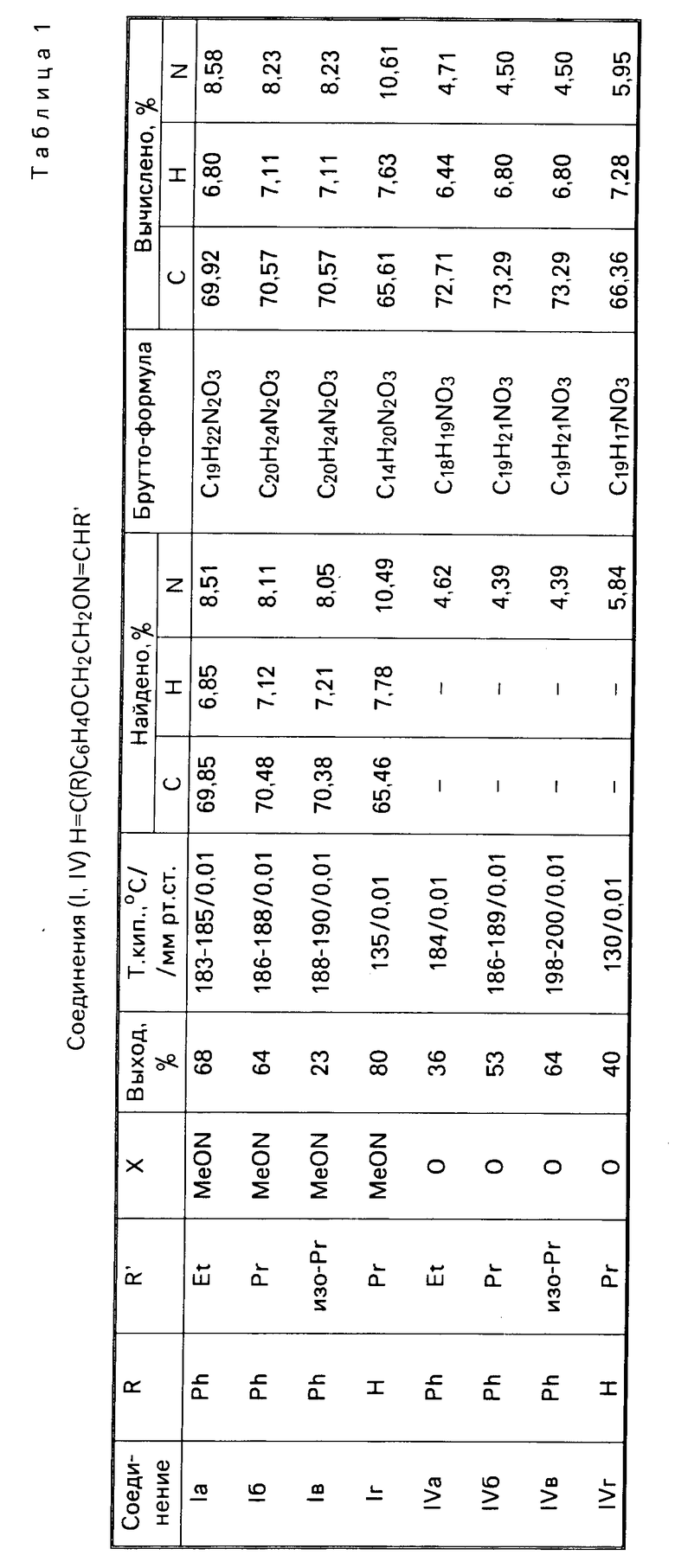
Аналогично получили соединения IV б-г. Константы соединений приведены в табл.1 и 2.
П р и м е р 2, [(0-метил-4-оксибензофеноноксим)этил]пропиональдоксим (Ia).
К 3,6 г кетона IVa, 1,4 г 0-метилового эфира солянокислого гидроксиламина в 12 мл этанола прибавили 1,6 мл пиридина и смесь кипятили 3,5 ч. Затем смесь охладили, упарили, остаток подкислили разбавленной соляной кислотой до рН 1-2. Экстрагировали эфиром, экстракт промыли водой, высушили сульфатом натрия, эфир упарили. Остаток хроматографировали на колонке с силикагелем (элюент гексан-этилацетат, 10:1) или перегоняли в вакууме. Выход 2,5 г, светло-желтое масло.
Аналогично получили соединения Iб-г, константы которых помещены в табл.1 и 2.
Инсектицидную активность полученных соединений изучали в лабораторных условиях, используя методики, описанные в монографии Бурова.
П р и м е р 3. Действие предлагаемых соединений на личинок комнатной мухи Musca domastica).
Объектом исследований служили личинки последнего возраста комнатной мухи. Растворили 1 мг испытываемого соединения в 1 мл ацетона. Ацетоновый раствор разбавили водой до концентрации 10-10-7 мг/л. Полученным водно-ацетоновым раствором (3 мл) смочили бумажный фильтр, который внесли в чашку Петри. На фильтр поместили 20 личинок мухи и оставили в контакте с действующим веществом на 1 сут. Затем перенесли личинки в чистую чашку Петри и дали насекомым корм (смесь отрубей с мукой), не содержащий химических препаратов. Оценку действия препаратов по отношению к контролю производили на 8-10 сут. Контролем служили 20 личинок, помещенных в фильтр, смоченный 1%-ным водным раствором ацетона, не содержащим испытываемого вещества.
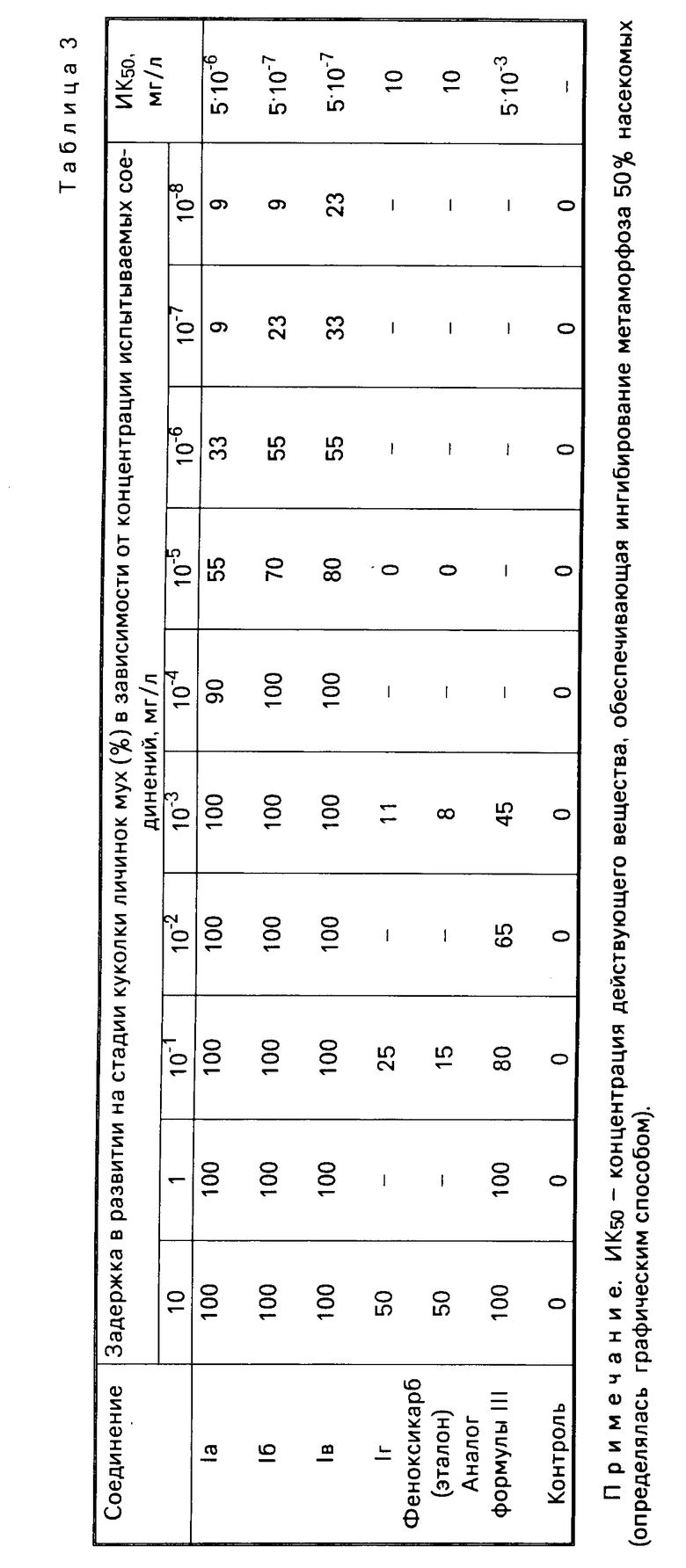
Отмечали значительную задержку в развитии насекомых, обработанных испытуемым соединением, появление уродливых форм и быструю гибель насекомых на стадии куколки. Действие соединений сравнивали с эталоном, которым служили феноксикарб и аналог формулы III. Результаты помещены в табл.3.
Из табл.3 видно, что по уровню инсектицидной активности предлагаемые соединения превосходили эталон на несколько порядков.
П р и м е р 4. Действие соединений на хлопковую совку (Spodoptera litteralis).
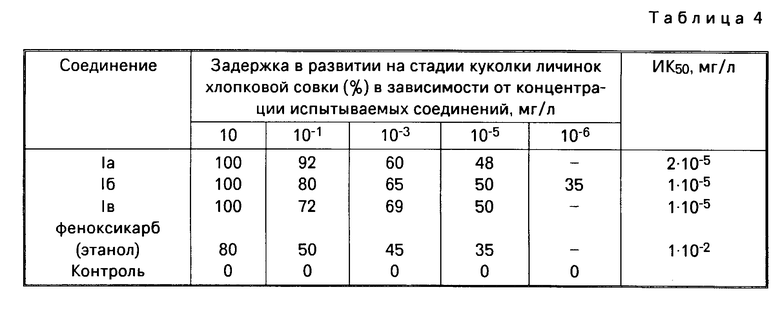
Объектом исследований служили личинки хлопковой совки четвертого возраста. Водно-ацетоновый раствор, содержащий 10-1.10-5 мг/л испытываемого соединения, добавляли в пищу насекомым, которую вносили в чашки Петри, содержащие 20 личинок. Оценку действия препаратов по отношению к контролю производили на 14 сутки. Контролем служили 20 личинок, помещенных в чашки Петри, которых кормили пищей, не содержащей испытуемого вещества. Действие соединений сравнивали с эталоном, которым служил феноксикарб. Результаты помещены в табл.4.
Из данных табл.4 видно, что предлагаемые соединения по действию на хлопковую совку в 1000 раз превосходили эталон.
П р и м е р 5. Острая токсичность предлагаемых соединений.
Острая токсичность определялась на белых мышах-самцах и самках массой 17-19 г при внутримышечном способе введения водных растворов соединений формулы I. Испытываемые соединения в дозах 1000, 3000, 5000 мг/кг не вызывали гибели животных или каких-либо заметных вредных на него воздействий по истечении 96 ч с момента введения. Установлено, что предложенные соединения не токсичны для теплокровных.
Таким образом, соединения формулы I являются высокоактивными ингибиторами роста и развития насекомых, обладающими низкой токсичностью по отношению к теплокровным. Поэтому соединения формулы I могут быть предложены как перспективное средство борьбы с вредными насекомыми.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Алкил-2-(4-фторметокси-4-фтортио)-фенилуксусная кислота в качестве промежуточного вещества для инсектицидов | 1978 |
|
SU1221220A1 |
| Способ получения ароматических соединений | 1985 |
|
SU1402252A3 |
| @ -Этинильные эфиры дитиофосфорной кислоты,обладающие инсектоакарицидной активностью | 1980 |
|
SU948107A1 |
| ПРОИЗВОДНЫЕ 1-ПИРИДИЛИМИДАЗОЛА И ИНСЕКТИЦИДНАЯ КОМПОЗИЦИЯ | 1991 |
|
RU2026294C1 |
| Мета-феноксибензиловые или @ -циано-мета-феноксибензиловые сложные эфиры 2-галоидалкил (окси-,тио-,сульфинил-или сульфонил) фенилалкановых кислот,проявляющие инсектицидную,иксодицидную активность | 1978 |
|
SU1082782A1 |
| ДИЭТИЛОВЫЙ ЭФИР ОКСИ[(1-МЕТИЛ-2-МОРФОЛИНОКАРБОНИЛ)ВИНИЛ]-ФОСФОРНОЙ КИСЛОТЫ, ОБЛАДАЮЩИЙ ИНСЕКТОАКАРИЦИДНОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2007412C1 |
| Инсектицидная композиция | 1977 |
|
SU667109A3 |
| ШТАММ XC 22-А ВИРУСА ЯДЕРНОГО ПОЛИЭДРОЗА ХЛОПКОВОЙ СОВКИ HELICOVERPA ARMIGERA HBN., ИСПОЛЬЗУЕМЫЙ ДЛЯ ПОЛУЧЕНИЯ ИНСЕКТИЦИДНОГО ПРЕПАРАТА | 2017 |
|
RU2652879C1 |
| ПРОИЗВОДНЫЕ 1-АРИЛИМИДАЗОЛОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ИНСЕКТОАКАРИЦИДОНЕМАТОЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ, КЛЕЩАМИ И НЕМАТОДАМИ | 1991 |
|
RU2072992C1 |
| Инсектицидная композиция | 1983 |
|
SU1340569A3 |
Сущность изобретения: продукты формулы: 4 MeON=C(R) C6H4OCH2CH2ON=CHR′, где R-водород, фенил; R′-этил, пропил или изопропил, БФ C9H22N2O3, выход 68% т. кип. 183 185°С; БФ C20H24N2O3, выход 64% т. кип. 186 - 188°С; БФ C14H20N2O3, выход 80% т. кип. 135°С; БФ C18H19NO3, выход 26% т. кип. 184°С; БФ C19H21NO3, выход 53% т. кип. 189 200°С; БФ C13H17NO3, выход 40% т. кип. 130°С. Реагент 1: 4-гидроксибензофенон. Реагент 2: β -хлорэтиловый эфир пропиональдоксима. Условия реакции: металат натрия, метанол, диметилформамид, йодистый калий. 4 табл.
0-[(4-Карбометоксииминофенокси)этил]алканальдоксимы общей формулы
4-MeON=C(R)C6H4OCH2CH2ON= CHR′,
где R атом водорода или фенил;
R' этил, пропил или изопропил,
обладающие инсектицидной активностью.
| Doph S., Frischkne, M.L | |||
| Maptinez Vetal, Z.Pflanzenkrank, Pflanzenschutz, B.88, 1981, S.569. |
Авторы
Даты
1995-10-27—Публикация
1990-09-29—Подача