ел
С
кислоты в присутствии основания в среде органического растворителя с последующим выделением целевых продуктов известными приемами.
П р и м е р 1. Получение 3-амино-2-(2-ме- токсифенил)-7-нитро-4-фенил-1(2Н)изохин- олона.
К смеси 1,45 г (0,005 моль) Ы-(2-метокси- фенил)амида 5-нитро-2-хлорбензойной кислоты, 0,6 г (0,005 моль) фенилацетонитрила и 70 мл диметилформамида прибавляют 1,38 г (0,01 моль) поташа и нагревают при температуре 153°С в течение 3 ч. Растворитель упаривают в вакууме, остаток обрабатывают 90 мл воды, подкисляют уксусной кислотой до рН 7 и отфильтровывают выпавший осадок, промывают водой и сушат, Выход 3,71 г (96%). Т.пл, 244°С (красные кристаллы из изо-пропилового спирта).
Вычислено, %: С 68,21; Н 4,42; N 10,85.
С22Нп№04.
Найдено, %: С 67,93; Н 4,15; N 10,90.
ИК-спектр: 3250 ср., 1660 ср., 1590 с., 1520 ср., 1490 с., 1480 ел., 1320 с„ 1290 ел.. 1100 ел.. 1060 сл„ 940 ел., 850 ел., 775 ср. (, КВч, табл.) Pay Unlearn Sp3-300.
П р и м е р 2, Получение 3-амино-2-( токсифенил)-7-нитро-4-(2,3,4-триметоксцф- енил)-1(2Н)изохинолона.
К смеси 1,45 г (0,005 моль) Ы-(3-метокси- фенил)амида 5-нитро-2-хлорбензойной кислоты, 1 г (0,005 моль) 2,3,4-триметоксифенилацето- нитрила и 100 мл ацетонитрила прибавляют 1,38 г (0,01 моль) поташа и нагревают при температуре 80°С в течение 7 ч. Растворитель упаривают в вакууме, остаток обрабатывают 80 мл воды, подкисляют уксусной кислотой до рН 7, отфильтровывают выпавший осадок, промывают водой сушат. Выход 4,31 г (91%). Т.пл. 155°С (Красные кристаллы из ацетонитрила).
Вычислено, %: С 63,0; Н 4,86; N 8,80.
С25НгзМзО.
Найдено, %: С 62,81; Н 4,74; N 9,05.
ИК-спектр: 3350 ш.ср., 1670 ср., 1620 с„ 1520с., 1330с.. 1280 ср., 1190 ср., 1110 сл„
1040 ел., 880 ел., 740 ел. (см 1, К.Вч, табл.) Pay Unlearn Sp3-300.
ПримерЗ. Испытание биологической активности 3-амино-2-(2-метоксифенил)-7-нитро-4-фенил-1(2Н)изохинолона и 3-амино-2-{2- метоксифенил-7-нитро-4-(2,3,4-триметоксифе- нил)-1(2Н)изохинолона. Заявляемые соединения -3-амино-2-(2-метоксифенйл)-7-нитро-4- фенил-1(2Н) изохинолон (соединение-1) и
3-амино-2-(2-метЬксифенил-7-нитро-4(2,3,4- -триметоксифенил)-1(2Н) изохинолон (соединение II) были изучены на модели аналеп- тической активности. Опыты проводились на 18 белых крысах обоего пола массой 180220 г. В качестве снотворного средства, при проведении методики, был использован не- мбутал в дозе 25 мг/кг массы тела животного. Новые синтезированные вещества и рекомендуемый препарат кофеин-бензоат
натрия вводили в одинаковой дозе по 10 мг/кг подкожно в виде 20% растворов.
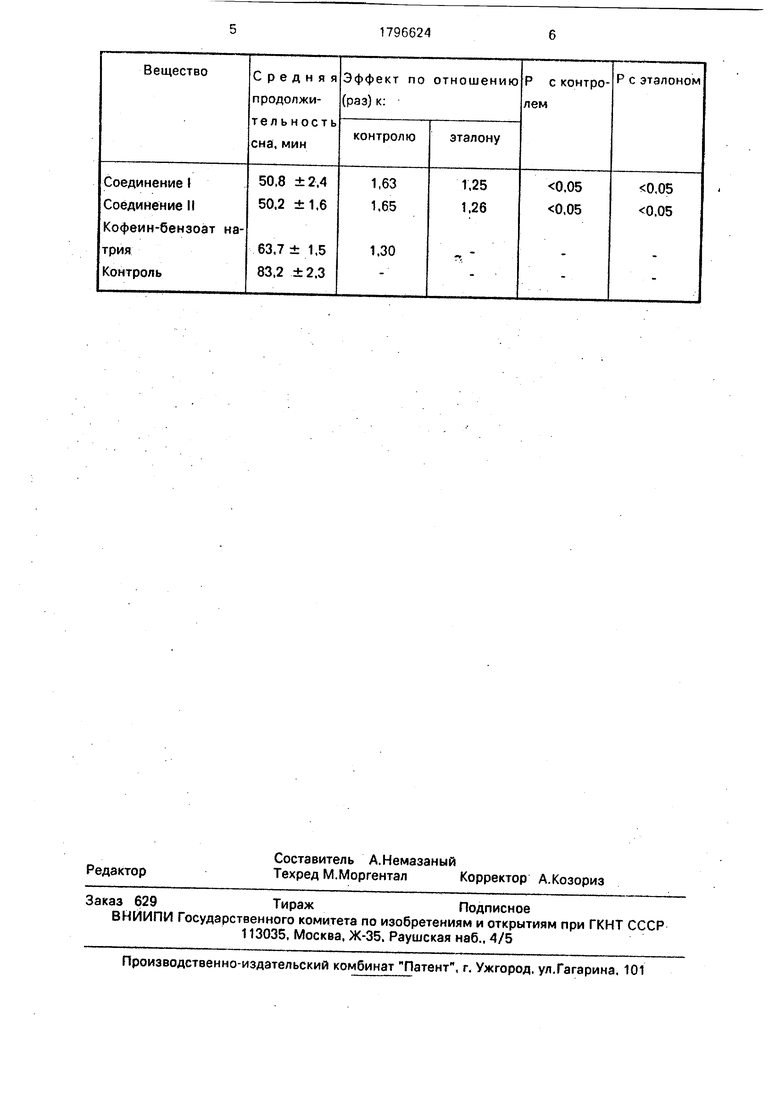
Статистически обработанные данные экспериментальных исследований представлены в таблице.
Как видно из представленных данных, новые вещества обладают стимулирующим действием на центральную нервную систему, укорачивают барбитуровый сон в 1,63 раза по сравнению с контролем и в 1,25 раза
в сравнении с эталонным препаратом кофе- ин-бензратом натрия.
Заявляемые соединения низкотоксич- иы, их ЛДзо 600-620 мг/кг.
Заявляемые соединения могут быть легко получены на любом химико-фармакологическом заводе, так как способ их получения не требует дополнительной разработки и установки оборудования, вследствие своей простоты и отсутствия особых
условий- проведения синтеза (т.к. высокий вакуум, инертная атмосфера, лакримоген- ность исходных полупродуктов и т.д.). Технологичность предлагаемого способа подтверждается также и тем, что исходные
соединения просты, дешевы и выпускаются отечественной промышленностью.

| название | год | авторы | номер документа |
|---|---|---|---|
| 3-Амино-7-нитро-4(2,3,4-триметоксифенил)-2-фенил-1(2Н)изохинолон, обладающий аналептическим действием | 1990 |
|
SU1796625A1 |
| Способ получения 3-амино-1/2Н/-изохинолонов | 1989 |
|
SU1728242A1 |
| Способ получения производных тетрагидроизохинолина или их фармацевтически приемлемых кислотно-аддитивных солей | 1986 |
|
SU1598875A3 |
| Способ получения производных 1-/3-(3,4,5-триметоксифенокси)-2-пропил/-4-арилпиперазина | 1978 |
|
SU893133A3 |
| Ацилированные 1,5,5-триметилбицикло[2,2,1]гепт-2-ил-экзо-амины, проявляющие гипноседативную активность | 1985 |
|
SU1705279A1 |
| 4-(4-МЕТОКСИФЕНИЛ)-4-ОКСО-N-ФЕНИЛ-2-((3-ЦИАНО-4,5,6,7-ТЕТРАГИДРОБЕНЗО[b]ТИОФЕН-2-ИЛ)АМИНО)БУТ-2-ЕНАМИД, ОБЛАДАЮЩИЙ АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ. | 2023 |
|
RU2810072C1 |
| ПРОИЗВОДНЫЕ 2-ОКСО-1-ПИРРОЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ | 2001 |
|
RU2355680C2 |
| Способ получения производных триазолоизохинолина | 1974 |
|
SU591149A3 |
| ПРОИЗВОДНЫЕ 1,3,4-ТИОДИАЗОЛ-2-КАРБОНОВЫХ КИСЛОТ | 1992 |
|
RU2050357C1 |
| ПРОИЗВОДНЫЕ 2-ОКСО-1-ПИРРОЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2001 |
|
RU2292336C2 |
Использование: в качестве биологически активного соединения. Сущность изобретения: 3-амино-2-(2-метоксифенил)-7-нитро-4- фенил-1(2Н)изохинолон: продукт 2-3-амино-2 2-метоксифенил}-7-нитрЬ-4-(2 ,3,4-триметоксифенияЗ-1(2Н)изохинолон. 1) Т.лл.244°С, БФС22Н17М304;2)Т.пл. 155°С, БФС25Н23М307. Реагент 1: амид 5-нитро-2- хлорбензойной кислоты. Реагент 2: фенила- цетонитрил в диметилформамиде в присутствии поташа при 153°С. 1 табл.
Формула изобретения 3-Амино-4-арил-2-(2-метоксифенил)-7- нитро-1(2Н)изохинолоны общей формулы
о rfj)
. QM осн. -.
Т vtt-i
R Нг
где R - CeHs,
СН30 ОСН3
V.
V .
(-оснл
обладающие аналептическим действием,
| Kimoto S., Kamoto М. | |||
| Noglmof К., Usaml Н., Jakugaku Zasshf, 1976, 96(2), p | |||
| Способ приготовления кирпичей для футеровки печей, служащих для получения сернистого натрия из серно-натриевой соли | 1921 |
|
SU154A1 |
| Goya S., Jakudate A., Janoka J., Jsuruda J,, Ogato H., Jakugaku Zasshl, 1980,100(8) | |||
| p | |||
| Накладной замок с электрической сигнализацией | 1923 |
|
SU819A1 |
| Машковекий М.Д | |||
| Лекарственные средства.- М.: Медицина, 1987, т | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Парный рычажный домкрат | 1919 |
|
SU209A1 |
Авторы
Даты
1993-02-23—Публикация
1990-06-11—Подача