Изобретение относится к синтетическим пептидным антигенам, последовательности которых соответствуют областям HJV - 1 белков, и к их применению в качестве диагностических реагентов для определения наличия антител к HJV- 1. Петиды также могут быть использованы в качестве иммуногенов в композициях для стимуляции продуцирования антител против HJV-1.
HJV - 1 (человеческий вирус иммуноде- фицита-1) является названием данным группе высоки родственных вирусов, которые были идентифицированы как первичный этиологический агент для синдрома приобретенного иммунодефицита (AIDS) у людей
(СПИДа). HJV - 1, который также известен как HTLY - III, LAV и AKV, является главной проблемой мирового здравоохранения. С тех пор как HJV - 1 был впервые идентифицирован как этиологический агент СПИДа, значительный прогресс был достигнут в исследованиях вируса как такосого и механизмов, с помощью которых вирус вызывает заболевание, и в разработке диагностических тестов для определения наличия вируса или инфекции.
Методы определения заражения вирусом HJV - 1 в общем заключается в измерении наличия вируса путем обнаружения и количественного определения антител к HJV - 1 - антигенам в крови, сыворотке и
ы
веществах, вырабатываемых из крови. Такие методы используют с целью диагностики AIDS (СПИДа)/и ARC (AIDS - родственного комплекса) и для скрининга крови и продуктов из крови на предшествующее воздействие HJV - 1.
Диагностику HJV - 1 инфекций и скри- нирование крови на наличие HJV-1 обычно осуществляют с помощью методик иммуно- ферментного анализа (Е LISA), чтобы определить наличие антител к иммуногенным компонентам HJV - 1 в испытуемом образце.
Другие методы включают использование блоттинговых методик Вестерна для определения HJV - специфических антител в испытуемых образцах. В общем может быть применен почти любой известный им- муноанализ, такой как радиоиммуноанализ, при использовании специфических реагентов для детектирования HJV - 1 и антител к нему.
Источником антигенов в первой генерации этих анализов обычно являлись антигенные белки, полученные из HJV - 1, продуцированного линиями человеческих хелперных Т-лимфобластоидных клеток, таких как Н9. Хотя эти первые генерации тестов ELISA на HJV - 1 являлись достаточно чувствительными и специфическими, использование этих антигенов, полученных из живых вирусных препаратов, вызывает серьезные существенные трудности.
Продуцирование самого.HJV - 1 в непрерывных клеточных линиях может быть осуществлено с высокой степенью (РЗ компонент) в лабораториях из-за опасности для исследователей подвергнуться вредному воздействию вируса. Кроме того, имеются четкие ложные отрицательные и ложные положительные результаты, которые были получены в тестах ELISA с использованием целых антигенов вируса.
Блрт-анализ Вестерна с использованием цельных вирусных антигенов обеспечивает более высокую специфичность, но он более трудоемок и требует больших затрат времени, чем ELISA тесты. Кроме того, так как Н9 и другие HJV - 1 продуцирующие клетки являются линиями человеческих клеток, если они не подвергнуты дорогостоящей очистке, они могут загрязнены обычными клеточными антигенами, такими как HLA антигены, которые могут вызвать ложную положительную реакцию в тесте ELISA.
Дорогостоящая очистка вирусных антигенов из клеточных линий также может предположительно разрушать иммуноген- ность иммунологически важных белков или,
другими словами, дезактивировать антигены, в результате чего продуцируются реагенты, которые приводят к ложным отрицательным реакциям. Дополнительно,
ложные отрицательные реакции с использованием антигенов, полученных из интакт- ных вирусных препаратов, могут встречаться из-за стерических затруднений, из-за которых антитела к вирусным антиге0 на не могут взаимодействовать со своим специфическим антигеном, потому что реакция заблокирована наличием других вирусных антигенов и антител в реакционной смеси.. ...
5 Во второй генерации тестов ELISA для определения HJV - 1 инфекции применяют иммунологически важные вирусные белки, которые могут быть продуцированы клонирующими участками HJ V -1 генома в бакте0 рии. Вирусный этиологический агент AIDS (т.е. вирусы, ранее называемые HTLY-III, LAV и ARV) из различных источников был изолирован, клонирован и была определена нуклеотидная последовательность.
5 Как показано на фиг.1, HJV - 1 является относительно сложным ретровирусом. содержащим по крайней мере семь генов. Вирусные структуральные гены, обозначенные gag, poJ и env соответственно, кодируют
0 белки вирусного ядра, обратную транскрип- тазу и вирусные гликопротеины вирусной оболочки. Другие гены, показанные на фиг.1, являются вспомогательными генами, включенными в репликацию вируса Гены
5 gag и env кодируют полипротеины, синтезированные из каждого из этих генов, являются пост-трансляционно расщепляемыми на несколько малых протеинов. Предыдущие исследования показали, что белки, кодиро0 ванные gag и особенно env - областями HJV - t - генома, являются иммунологически важными, так как антитела к продуктам gag и env генов найдены в сыворотке AIDS и ARC пациентов.,
5 env - ген кодирует гликопротеин (д р160) с кажущейся молекулярной массой (Mr) около 160 000 дальтон, который является пост синтетически расщепляемым на два гликопротеина, g р 120 и др 41 с молекуляр0 ной массой 120 000 и 41 000 соответствен но. Гликопротеин др 120 является по-видимому наружным белком вирусной оболочки, тогда как др 41 по-видимому является трансмембранным белком. И др 120 и др 41 являются
5 иммуногенными с антителами к обоим белкам, которые легко определяются в сыворотке больных AIDS и ARC.
Поскольку антитела к др 120 и др 160 в сыворотке больных AIDS и ARC, а также асимптоматических индивидуумов, зараженных вирусом, являются нейтрализующими, т.е. ингибируют связывание вируса, др 120, др 160 или их участки являются кандидатами для субединицы вакцины. Трансмембранный гликопротеин др 41 является HJV - 1 антигеном, более последовательно распознаваемым антителами в сыворотке больных AIDS и ARC (5). Кроме того, антите - ла в сыворотке больного также распознают эпитопы белков ядра вируса, кодируемых gag - геном.
Иммунологически важные Н J V -1 антигены для применения в диагностике и как потенциальные композиции вакцины были приготовлены путем клонирования участков HJV - 1 генома в различных экспрессирую- щйе системы, такие как бактерии, дрожжи или vaccinia, HJV - 1 антигены, продуцированные по методикам рекомбинантной ДНК, однако, должны еще пройти дорогостоящую очистку, чтобы избежать ложных положительных реакций в ELISA из-за реактивности любого антитела к антигенам системы экспрессии, которые могут загрязнять препарат HJV - 1 антигена. Также денатурация HJV - 1 антигенов во время очистки может разрушить важную антигенную активность.
Белок антигенов содержит ряд зпито- по в или антигенных детерминант, которые являются областями в белках, которые содержат сайты связывания для специфических антител. В общем белковые антигены содержат 5-10 эпитопов, каждый из которых содержит последовательность из 6-8 аминокислот. Эпитопы могут быть или непрерывными, в которых 6-8 аминокислот имеются в последовательности, или периодическими, в которых аминокислоты, которые образуют эпитоп, связаны вместе трехмерной укладкой белков. Хотя эпитоп состоиттолько из относительно небольшого числа аминокислот, их реактивность с антителом находится под влиянием аминокислот в белке, который окружают эпитоп.
Исследования, направленные на картирование антигенных сайтов или эпитопов белков, были выполнены с использованием синтетических пептидов, соответствующих различным областям интересующих белков.
Помимо их полезности в исследованиях для картирования эпитопов синтетические пептиды, если они охватывают основные антигенные детерминанты белка, обладают потенциалом в качестве вакцин и диагностических агентов. Синтетические пептид- ные антигены обладают некоторыми преимуществами в отношении продуцирования специфических антител и реактивности. Последовательность синтезированного пентида может быть выбрана среди аминокислотных последовательностей, которые фактически определены при аминокислот- 5 ном секвенсировании белка, или выводятся из последовательности ДНК, кодирующей белок. Использование специфических синтетических пептидов устраняет необходимость в использовании белка полной длины
0 при продуцировании или для анализа спе-. цифических антител. Кроме того, методика синтеза пептидов в твердой фазе позволяет получать химически практически неограниченные количества интересующего пепти5 да. Доступность автоматизированных синтезаторов пептидов является дополнительным преимуществом таких методик.
В некоторых публикациях представлены данные, показывающие иммунологиче0 скую реактивность выбранных синтетических пептидов, соответствующих антигенным белкам HJV - 1, В одном исследовании был синтезирован пептид, имеющий аминокислотную последовательность
5 Tyr-Asp-Arg-Pro-Glu-Glu-GIy-lie-Giu-GIu- Gly-Glu-Arg-Asp-Arp-Asp-Arg-Ser-Giy-Cys, которая соответствует ами+юкислотым остаткам 735-752 HJV - 1. Этот пептид, который является частью др 41, использовали
иммунизации кроликов в попытке вызвать нейтрализующий антитела ответ в HJV-1.
Кроме того, несколько сывороток от больных AIDS, про которых было известно,
5 что они содержат анти-др 41 антитела, были мало реактивными с этим пептидом; это указывает, что этот пептид содержит по крайней мере один эпитоп, распознаваемый до некоторой степени антителами к нативному
0 др 160/др4 1.
Недавно вышедшая работа относится к обеспечению синтетических пептидов для диагностики AIDS в дополнение к разработке композиций вакцины. В одном исследо5 ва нии был синтезирован пептид из 21 аминокислоты, названный SM284, с аминокислотной последовательностью Arg-lle- Leu-Ala-Val-Glu-Arg-Tyr-Leu-Lys-Asp-Glu-Le u-Leu-Gly-Ile-Gly-Cys-Ser.
0
Этот пептид, который соответствует аминокислотам 586-606 в др 160 и содержит антигеннь1й сегмент др 41, является реактивным с HJV - 1 положительной сыворот5 кой от больных AIDS/ARC при анализе методами ELISA и блоттиг-анализе Вестерна. SM284 пептид благоприятно выдерживает сравнение с протеинами, происходящим из НJV - 1, при детектирова- нии HJV - 1 антител по методу ELISA.
Например, в методе ELISA с использованием SM284 детектируют антитела D образцах сыворотки у 96,5% больных AIDS/ARC и 34,6% здоровых асимптомати- ческих с высоким риском индивидуумов. Не имелось ложных положительных в 387 сыворотках от контрольных индивидуумов.
Серологический и химический анализы SM284 пе.птйда и родственных пептидов показали, что некоторые аминокислоты по-ви- димому являются более важными, чем другие при взаимодействии антителоанти- ген пептидэ. .
. Деления остатков Arg-1, He-2- n Lys-10 из пептида значительно снижает.или ун ич- тожает серологическую реактивность. Деле- ция ТГУ-GIy-Cys-Ser остатков у карбоксильного конца, пептида, с другой .стороны, приводит в результате к умеренной потере серологической активности, ука- зывая,.что аминеконцевая часть пептида является по-видимому более важной, чем карбоксильная концевая часть для иммуно- логической реактивности.
Предлагается несколько иммунологиче- ски реактивных синтетических.пептидов, соответствующих областям HJV - 1 белков .для детектирования AIDS и AIDS - родственной болезни. Особенно интересным является пептид V (39), имеющий последовательность Arg-lle-Leu-AJa-Val-Glu- Arg-Tyr-Leu-Lys-Asp-Glu-GIu-Leu-Leu-Gly- e-Trp-Gly-Cys-Ser-Gly-Lys-Leu-Ne-Cys X, где X является ОН или NH2, который соответст- вует участку др 41, кодируемому парами ос- нрваний 7516-7593 HIV- 1 генома. Пептид V (39) реагирует с 23/24(95,8%) образцами сыворотки от больных с достоверной HJV - 1 инфекцией.
В соответствии с настоящим изобрете- нием предлагаются новые синтетические пептиды, соответствующие антигенным HJV- 1 белкам, которые являются полезными и превышают по селективности диагно,- стические методы для детектирования HJV - 1 инфекций.
Найдены новые синтетические пептид- ные антигены, соответствующие гликопро- теину др 41, кодированному HJV - 1 env геном.
Эти пептиды используются для диагностики AIDS у подозрительных индивидуумов и в методах для скрининга на воздействие HJV - 1 крови и происходящих из крови продуктов с высокой степенью на- дежности и очень незначительным количе- .ством ложных результатов.
Пептиды могут быть использованы в методах определения антител к HJV - 1 в образцах. Методы включают контактирование
образца с пептидными антигенами в условиях, которые позволяют образоваться имму- нологичесокму комплексу между пептидом и любым HJV-1 специфическим антителом в образце. Измерение образования комплекса с помощью любого детектирующего (Средства указывает на наличие или отсутствие антител к HJV.- 1 в образце.
Также могут быть использованы новые пептиды в качестве иммуногенов в композициях вакцины для иммунизации против HJV - 1 инфекции или для продуцирования у животных HJV - 1 специфических антител против HJV - 1 антигенов.
На фиг. 1 схематически представлены гены HJV - 1; на фиг.2 - ген др 41 HJV - 1, изображенный в виде частично перекрывающих пептидов, синтезированных в соответствии с изобретением, и сравнение известных пептидов, соответствующих др 41; на фиг.З - гистограмма, показывающая величины EL ISA, полученные с использованием дР41А5 в качестве антигена.
Изобретение посвящено ряду пептидов длиной 15-27 аминокислот, соответствующих областям белкового продукта целого HJV - 1 gag гена и др 41 HJV - 1, которые были синтезированы и испытаны на имму- нореактивность к HJV - 1 положительным образцам сыворотки, полученным из Соединенных Штатов/Великобритании, Израиля, Африки и Швеции. Новые пептиды являются полезными в тестах на диагностику HJV- 1 инфекции или на предшествующее воздействие вируса и в качестве иммуногенов в композициях, чтобы вызвать продуцирование у животных и людей антител против HJV-1. Пептиды, соответствующие gag белкам и в частности др 41 были собраны и синтезированы, потому что эти HJV- t белки показывают меньшую вариацию от штамма к штамму характеристик, чем другие иммунологически важные HJV - 1 антигенные белки, такие как др 120. Пептиды, охватываемые изобретением, включают олигопептиды, имеющие аминокислотные последовательности, содержащие такие последовательности, которые содержат непрерывные (линейные) эпитопы, реактивные с HJV - 1 специфическими антителами.
Следовательно, изобретение охватывает группу иммунологически реактивных пептидов и функционально эквивалентных вариантов их, которые не ухудшают в значительной мере антигенные свойства пептида, соответствующего др 41, кодируемого env геном HJV- 1.
Области др 41, соответствующие каждому пептиду, детально описанному ниже, показаны на фиг.2. Все пептиды синтезированы по известным методикам синтеза пептидов на твердой фазе. Синтез также позволяет, чтобы одна или две аминокислоты, несоответствующие первоначальной последовательности белка, были добавлены к NH2 - или СООН - концу пептидов. Такие наружные аминокислоты являются полез. ными для сочетания пептидов друг с другом, для содержания с. белковым носителем или с подложкой. Аминокислоты, которые являются полезными для этих целей, включают тирозин, лизин, глютаминовую кислоту, ас- паргиновую кислоту, цистеин и их производные. Могут быть .использованы дополнительные методики модификации белков, например, NH2 - ацетилирование или СООН - концевое змидироваиие, чтобы обеспечить дополнительное средство для сочетания пептидов с другим белком или
молекулой пептида или подложкой.
Новые пептиды, соответствующие др 41, представлены ниже:
др41А5. X-Asp-Gln-Gln-Leu-Leu-G y-l1e-Trp-G y- Cys-Ser-Gly-Lys-Leu-l e-Cys-Thr-Thr-Ala-Val
Pro-Trp-Asn-l-Z, где X является или Н концевой амино NHa - группы пептида, или дополнительной аминокислотой, связанной с аминоконцевой NHa - труппой пептида, дополнительную аминокислоту выбирают для облегчения сочетания пептида с носителем белка; J - отсутствует или является Суз; a..Z является ОН или NH2.
Пептид др41А5, который соответствует аминокислотам 596-618. кодируемым парами оснований (по) 7563 по 7632 HJV - 1 генома, соответствующими env гену является особенно предпочтительным вариантом настоящего изобретения. Пептид др41А5 в котором X является Н2, J является Суз и Z является ОН, является особенно предпочтительным.
др41СТ4
Пептид др41СТ4, который соответству- етобластидр41 белка, кодируемого по при-, мерно от 8173 до 8238 HJV- 1 геиома, имеет формулу: X-AIa-Leu-Lys-Tyr-Trp-Trp-Asn- Leu-Leu-Glu-Tyr-Trp-Ser-Gln-Glu-Leu-Lys-A sn-Ser-Ala-Val-Ser-J-Z, где X, J и Z имеют указанные ранее значения,
др41СТЗ
Пептид др41СТЗМ, который соответствует области дР41, кодируемой по от примерно 8220 до 8280 Н J V - 1, имеет формулу: X-Lys-Asn-Ser-A a-Val-Ser-Leu-Leu-Asn-Ala
-Thr-Ala-lle-A a-Val-Ala-Glu-GIy-Thr-Asp-J-Z, где X, J и Z имеют указанные ранее значения,
др41В1
Пептид др41В1, который соответствует области др41, кодируемой от примерно по 7614 до 7686 Н J V -1 генома env гена, имеет формулу; X-Thr-Ala-Val-Pro-Trp-Asn-A a-Ser- 5 Trp-Ser-Asn-Lys-Ser-Leu-GIu-Glu-Ile-Trp-As n-Asn-Met-Trp:Trp-Met-J-Z, где X, J и Z имеют указанные ранее значения.
др41ВЗ.- ...
Пептид др41 ВЗ, который соответствует 0 области дР 41, кодируемой примерно по 7705 до 7773 HJV-1 генома, имеет формулу: X-lle-Asn-Tyr-Thr-Ser-Leu-tie-His-Ser-Leu-ll e-Glu-Glu-Ser-Gin-Asn-Gln-Gln-Glrt-Lys-Asn
-Glu-J-Z, где X, J и Z имеют указанные ранее 5 значения.
Кроме того, изобретение охватывает некоторые иммунологически реактивные пептиды и их функциональные варианты, соответствующие областям белковых про- 0 дуктов, кодируемых gag геном HIV - 1 (фиг.1). Эти новые пептиды представлены1 ниже: . GAG 2 .
Пептид GAG 2, который соответствует
5 области gag генного продукта, кодируемого
по примерно 779 до 840 gag гена H1V - 1,
имеет формулу: X-Pro-Arg-Tlir-Leu-Ash-AlaТф-Val-Val-Glu-Glu-Lys-Ala-Phe-Ser-Pro -Giu
-VaKl-Z, где X, J nZ имеют указанные ранее 0 значения. GAG3
Пептид GAG 3, который соответствует области gag генного белкового продукта, кодируемого по примерно 810 до 870.gag гена, 5 имеет формулу: X-Val-GIu-GIu-Lys-Ala-Phe- Ser-Pro-Glu-Val-IIe- Pro-Met-Phe-Ser-Aia- Leu-Ser-Glu-Giy-J-Z, где X, J и Z имеют . указанные ранее значения.
GAG 14 . .- ; 0- Пептид GAG 14, который соответствует области gag генного продукта, кодируемого по примерно 1368 до 1430 HJV- 1 gag гена, имеет формулу:. X-Glu-Met-Met-Thr-Ala-Cys- Gin-Gly-Val-GIy-Gly-Pro-Giy-His-Lys-Ala-Arg 5 -Val-Leu-Ala-Glu-J-Z, где X, J и Z имеют указанные ранее значения. P17-D
Пептид P17-D, который соответствует
области gag генного белкового продукта, ко0 дируемой по примерно 495 до 560 HJV - 1
оао гена, имеет формулу: X-Ser-Glu-Gly-Cys Arg-Gln-lle-Leu-Gly-Gln-Leu-Gln-Pro-Ser-Leu
-Gln-Thr-Gly-Ser-Gln-Leu-J-Z, гдеХ, J игиме-. ют указанные ранее значен ия. 5 P17-F
Пеприд P17-F, который соответствует области оао генного белкового продукта, кодируемой по примерно 588 до 647 HJV - 1 оао гена, имеет формулу: X-Leu-Tyr-Cys-Vai- His-Gln-Arg-lle-Gin-ile-Lys-Asn-Thr-Lys-Glu
-Ala-Leu-Asp-Lys-lle-J-Z, где X, J и Z имеют указанные ранее значения.
Пептиды могут быть использованы в способах детектирования антител к HJV - 1 или ассоциированным HJv - 1 антигенам. Предпочтительно методы, которые используют пептиды для детектирования наличия HJV - 1 специфических антител в образце, включают контактирование образца с по крайней мере, одним из пептидов в условиях, которые допускают образование имму- нологического комплекса между пептидным антигеном и любыми антителами к HJV - 1, которые могут присутствовать в образце. Образование иммунологического комплекса, если оно происходит, указывает на наличие антител к HJV - 1 в образце, затем оно детектируется и измеряется подходящими средствами.
Такие методы включают, среди прочих, иммуноанализ гемогенного и гетерогенного связывания, такой как радиоиммуноанализ (РИА), ELISA, и блот-анализ Вестерна. Кроме того, протоколы анализов с использованием новых пептидов позволяют провести исследование конкурентного и неконкурентного связывания.
Пептиды могут быть мечеными (ненери- рующими сигнал) или немеченными в зависимости от типа используемого анализа. Метки, которые могут быть соединены с пептидом, хорошо известны на данном уровне техники и включают, среди прочих, ферменты, радионуклиды, флюорогенные и хромогенные субстраты, кофаткоры, био- тин/авидин, коллоидное золото и магнитные частицы. Модификация новых пептидов позволяет сочетать их известными методами с носителями белков или пептидов или с известными подложками, например, поли- стирольными или поливинилхлоридными плашками для микротирования, стеклянны-. ми трубками или стеклянными шариками и хроматографическими носителями, таким как бумага, целлюлоза и производные целлюлозы, и оксид кремния.
Предпочтительной аналитической методикой, особенно для широко масштабного клинического скрининга сыворотки и крови и происходящих из крови продуктов больных являются ELISA и блот-аналйз Вестерна, особенно предпочтительной является методика ELISA, ELISA тесты, применяю- ш,ие описанные выше пептиды, основаны обычно на тестах с использованием HJV- 1 белков или их частей, происходящих из че- ,ловеческих клеток или полученных по методике рекомбинатной ДНК, в качестве антигенов. При использовании в качестве реагентов в этих анализах пептиды обычно
связывают с внешней поверхностью стенок микротитратора. Пептиды могут быть непосредственно связаны со стенкой микротитратора. Однако было обнаружено, что
максимальное связывание пептидов со стенками может быть осуществлено при предварительной обработке стенок полилизином перед добавлением пептидов.
Дополнительно новые пептиды могут
0 быть ковалентно присоединены с помощью известных средств к белковому носителю, такому как БСА, полученный в результате конъюгат используют для покрытия стенок. Обычно пептиды используют в концёнтра5 ции между 10 и 100 мкг/мл для покрытия, хотя некоторые пептиды для успешного анализа имеют концентрации порядка 500 мкг/мл.
Образцы затем наносят на покрытые
0 пептидом стенки, где образуется иммуноло- гический комплекс, если в образце имеются антитела к HJV- 1. Могут быть добавлены генерирующие сигнал средства, чтобы способствовать определению образования
5 комплекса. Детектируемый сигнал продуцируется, если в образце имеются специфические к HJV-1 антитела.
Изобретение далее иллюстрируется следующими конкретными примерами, ко0 торые ни в коей мере не должны рассматриваться как ограничивающие область изобретения.
Пример 1. Для синтеза всех пептидов используют Эпплайд Биосистем пептидсин5 тезизер Модель 430 А. В каждом синтезе используют п-метилбензилгидриламинную твердую фазу - подложку из смолы Пеп- тидс Интернейшнл Луисвилль, КИ). Пептиды были синтезированы в соотвествии с
0 Инструкцией для пользователя для Пептид Синтезизер Модель 430 А, Эпплайд Биоси- стемс, 1986г.
Все аминокислоты для использования в синтезе, содержащие трет.-бутилкарбо5 нильную группу (т-Вос), защищающую а - NH2- группу, были получены из Новабиохем АГ, Швейцария, Аминокислоты с реактивными боковыми группами, содержат дополни- тельные защищающие группы для
0 предотвращения нежелательных и вредных реакций в боковых цепях.
Индивидуальные защищенные аминокислоты, использованные для синтезе всех пептидов, приведены в таблице 1| находя5 щейся в приложении.
После завершения конкретного синтеза удаляют защищающие группы их синтезированного пептида и пептид отщепляют от смолы твердого носителя с помощью обработки безводной фтористоводородной кислотой (HF) при 0°С в сочетании с 10% анизола и 10% диметилсульфоксида в качестве очищающих агентов. Затем прибавляют 2% Тиокрезола для цистеин-содержащих пеп- тидов, отдувают током азота HF из образца, удаление любого остаточного YF осуществляют путем вакуумирования образца при 0°С. Пептиды экстрагируют из смолы при обработке трифторуксусной кислотой (ТФУК), которую затем удаляют выпариванием при комнатной температуре. После удаления ТФУК пептиды осаждают и промывают безводным эфиром.
Таблица1
Аминокислоты, использованные для синтеза пептидов
Boc-Ala-OH Boc-Arg(Tos)-OH .5 Boc-Asn-OH
Boc-Asp-(OBzl)-OH Boc-Cys(pMeOBzl)-0 Boc-Glu(OBzl)-OH Boc-Gln-OH 10 Bpc-Gly-OH
Boc-His(Tos)-OH .Bqc-lle-OH 1/2 HaO
Boc-Leu-OH H20 . Bqc-Lys(2-OZ)-OH (cryst.) 15 Bqc-Met-OH Boc-Phe-OH Boc-Pro-OH Boc-Ser(Bzl)-OH DCHA Boc-Thr(BzI)-OH 20 Boc-Trp(Formyl)-OH Boc-Tyr(2-Br-z)-OH Boc-Val-QH
То$ тозил или п-толуолсульфоновая кислота oBzl бензилокси . pMeoBzl n-метилбензилокси 2-CI-z карбобензоксихлорид 2-Br-z карбобензоксибромид
Перед использованием в конкретном анализе пептиды могут быть дополнительно очищены, при желании, с помоа ю высоко эффективной жидкостной хроматографии с обратимой фазой (HPLC). Особенно пригодной колонкой для такой очистки является колонка с обратимой фазой Видек С-18, для элюированмя пептидов используют градиент вода (ТФУК) - ацетонитрил (ТФУК).
П р и м е р 2. Синтезируют пептид др41А5, имеющий аминокислотную последовательность Asn-Gln-GIn-Leu-Leu-Gly-ile- Trp-Gly-Cys-Ser-Gly-Lys-Leu-lle-Cys-Thr-Thr -Ala-Va -Pro-Trp-Axn-Cys-OH, по методике примера 1 и используют его в ELISA для измерения его иммунологической реактивности.
На плашки для микротитрования наносят полилизин в концентрации 1 мг/мл и инкубируют 30 мин. Затем полилизин сбрасывают и на стенки плашки наносят пептид 5 др41А5 в концентрации от 10 до 100 мкг/мл для покрытия. После инкубирования пепти- да на стенках в течение периода времени, достаточного для связывания со стенкой, удаляют раствор пептида и прибавляют в
10 течение 15 минут раствор глутарового альдегида, который стабилизирует присоединение пептида к стенкам. Затем удаляют раствор глутарового альдегида, стенки промывают буфером и прибавляют смесь глици15 на.и бычьего сывороточного альбумина (БСА), который служит для блокирования несвязанных сайтов на стенках и сводит к минимуму нееспецифмческое связывание антител во время самого теста ELiSA. После
0 стадии окончательной промывки плашки готовы к использованию. Покрытые пептидом плашки для микротмтрования могуг храниться несколько месяцев без какого-либо снижения энтигенной активности пептида 5 др41А5, покрывающего стенки.
Используют обычный вариант известных методов ELISA с плашками для микротитрования, приготовленными, как описано выше. Образцы сыворотки от индивидуу0 мов, которые были разбавлены 1:50 в РВ5 (фосфатный буферный солевой раствор), содержащем 0,05% лолиоксиэтиленсорбитан мсзнолаурата (Твин 20), прибавляют 1 % БСА на каждую стенку и инкубируют 30 мин при
5 37°С во влажной атмосфере. Разбавленные образцы сыворотки затем удаляют из плашек и три раза промывают стенки PBS, содержащим 0,05% Твин 20. Затем прибавляют конъюгированное анти-челов е0 чес кий Ig антитело на стенки и инкубируют 30 мин. Конъюгированные антитела были получены у коз или кроликов, они являются специфическими для человеческого IgC, IgM, легких иммуноглобулиновых цепей и их
5 сочетаний. Предпочтительно в ELISA используют коньюгированную щелочную фос- фотазу с анти-человеческим IgC (от Дакопаттс), разбавленную 1:500 для использования в PBS, содержащем 0,05% Твин 20
0 и 1% БСА. Затем конъюгат инкубируют в
течение достаточного периода времени,
чтобы прошла реакция со связанными чело веческиМи антителами, плашки три раза
промывают, как указано выше. Для того,
5 чтобы детектировать антитела к JV - 1 в человеческой сыворотке, которая реагирует с пептидом др41А5, использованным в качестве антигена (т.е. положительная реакция), прибавляют хромогениый субстрат субстрата щелочной фосфатазы (Сигма, кат, № 104,
151802871 16
таблетки), растворяют в натрийкарбонат- реакции были подвергнуты блот-анализом ном (MgCI буфере и доводят концентрацию Вестерна.
до 1 мкл/мл, которая расщепляется фермен-Кроме того из фиг.2 видно, что др41А5 том, воздействующим на античеловеческий имеет частичное перекрывание в аминокис- д с получением окрашенного продукта. По- 5 лотной последовательности с пептидом SM еле инкубации примерно в течение 40 мин 284 и пептидом (39) Козанда. Следовательно при комнатной температуре положитель- пептид gp 41A5 содержит аминокислотную ные реакции указывают на наличие антител последовательность у карбоксил-концевого в образце, реактивных к антигену. Желтую участка двух известных пептидов плюс до- до оранжевой до красно-коричневой окра- 10 полнительную последовательность, соот- ску на каждой стенке, указывающую на по- ветствующую области дР41 с ложительную реакцию, регистрируют на карбоксил-концевой стороны пептидов спектрофотометре при 405 нмдля количест- 5М284и V(39). Как обсуждалось ранее, Вонг венного определения реакции. Спектрофо- сссотр, рассматривал карбоксил-концевой тометрические показатели регулируют для 15 участок пептида SM284 как иммунологиче- корректйровки основных реакций. ски менее важный при сравнении с аминоНа фиг.З представлена гистограмма, по- концевым участком пептида р М 284, В казывающая количества антител, получен- противоположность Вонгу с сотрудниками, ные из четырех отдельных ELISA однако, расширение замен др41А5 к карбок- определений с использованием р 41А5 в 20 сильному концу дР41 приводит в результате качестве антигена. 101 истинной положи- к пептиду, имеющему отличные антигенные тельная (по блот-анализу Вестерна) сыво- свойства для детектирования AJDS-специ- ротка от больных AIDS и ARC и 179 истинно фических антител в человеческой еыворот- отрицательных сывороток вводят в реакцию ке. Этот пептид показывает как более в системе ELISA с др41А5. Среднее отклоне- 25 высокую степень реактивности, так и более ние для положительных реакций было опре- высокую специфичность в ELISA ив блот- делено равным О.Д.405 0,376. На фиг.З анализе Вестерна, чем у обоих пептидов V показано, что др41А5 дает положительную (39) и SM 284.
реакцию со 100% (101/101) истинно поло-Таблица 2 показывает, что др41А5 реа- жительных сывороток и 0% (0/179) с истин- 30 гирует со всеми 233 (100%) достоверно по- но отрицательными сыворотками. ложительными HJV - 1 сыворотками. Эти
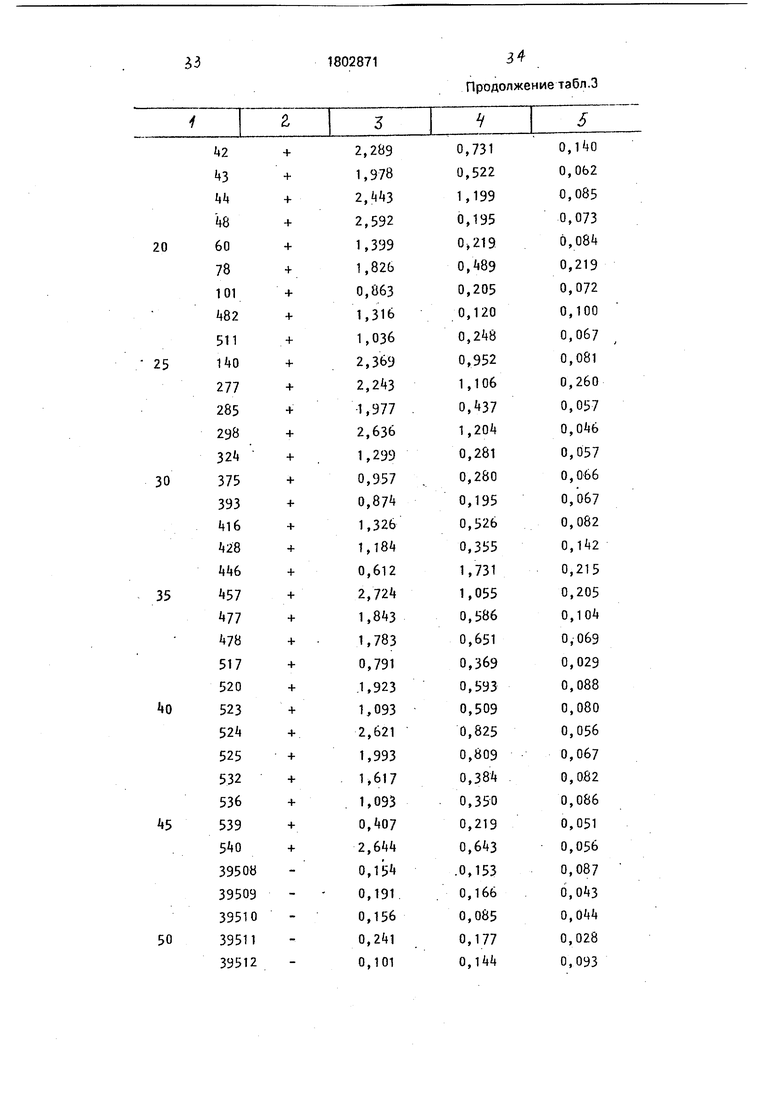
Пример 3. Для Сравнения с новыми результаты были получены с теми же 233 лептидами был синтезирован известный сыворотками, испытанными против пептида пептид V (39) Козанда, как описано в.приме- V (39), который дали 12 ложных отрицатель- ре 1, в соответствии с его аминокислотной 35 ных реакций. Среднее отклонение величин последовательностью, описанной в патенте для положительной реакции в тестах ELISA США N2 4629783. Относительная локализа- составило О.Д.405 примерно 0,3. Любое ция этого пептидз в др41 показана на фиг.2, значение ниже 0,3 рассматривается как от- на котором приведена относительная лока- рицательная реакция. Легко видеть, что об- лизация последовательности др41А5 и дру- 40 разцы сывороток №№ 7, 19, 40, 44t 60, 101, гих пептидов, соответствующих gp41 HJV- 482, 511, 324, 375 и 393 четко показывают 1. Козанд сообщил, что пептид V (39) реаги- отсутствие реактивности с пептидом V (39), рует с 23/24 (95,8%) достоверно положи- но высокую реактивность с дР41А5. Таблица тельными сыворотками (т.е. при одной находится в приложении. ложной отрицательной реакции). Пептид 45 В таблице 3 приведено дополнительное был использован в ELISA, описанной в при- сравнение более высокой иммунологиче- мере 2, с заменой на пептид V (39) пептида ской реактивности др41А5 по сравнению с др41А5.. пептидом V (39) Козанда. Из 233 образцов
Пептид (V) (39) дает 221/233 (94,8%) по- сывороток, представленных в таблице 2, 38 ложительных реакций с известными HJV-1 50 были удостоверены как положительные по положительными образцами сыворотки. блот-анализу Вестерна. Эти положительные Было отмечено 12 ложных отрицательных сыворотки плюс 8 подтвержденных отрицэ- реакций, как показано в таблице 2. Кроме тельных образцов сыворотки (по блот-ана- того, пептид V (39) дал ложную положитель- лизу Вестерна) вводят в реакцию с ную реакцию в одной из 102 (0,98%) досто- 55 пептидами др41А5 и V (39) в параллельных верно отрицательных сывороток. Образцы тестах ELISA с положительными реакциями, сывороток были удостоверены как положи- имеющими О.Д.405 примерно 0.3. тельные и отрицательные с помощью блот-Кроме того, не-HIV- 1 антиген (отрица- анализа Вестерна с HJV - 1 белками. Все тельный антиген) используют в качестве ложные положительные и отрицательные контроля. Легко видеть, что др41А5 не дает
ни ложных отрицательных ни ложных положительных реакций. Следовательно, неожиданно др41А5 дает по методике ELISA результаты, которые являются четко на 100% точными. Диагностическая и скри- нирующая способности в анализах с использованием др41А5 четко выше, чем у обычных используемых в анализе пепти- дов V (39) и SM284 или любого другого HJV- 1 антигена.
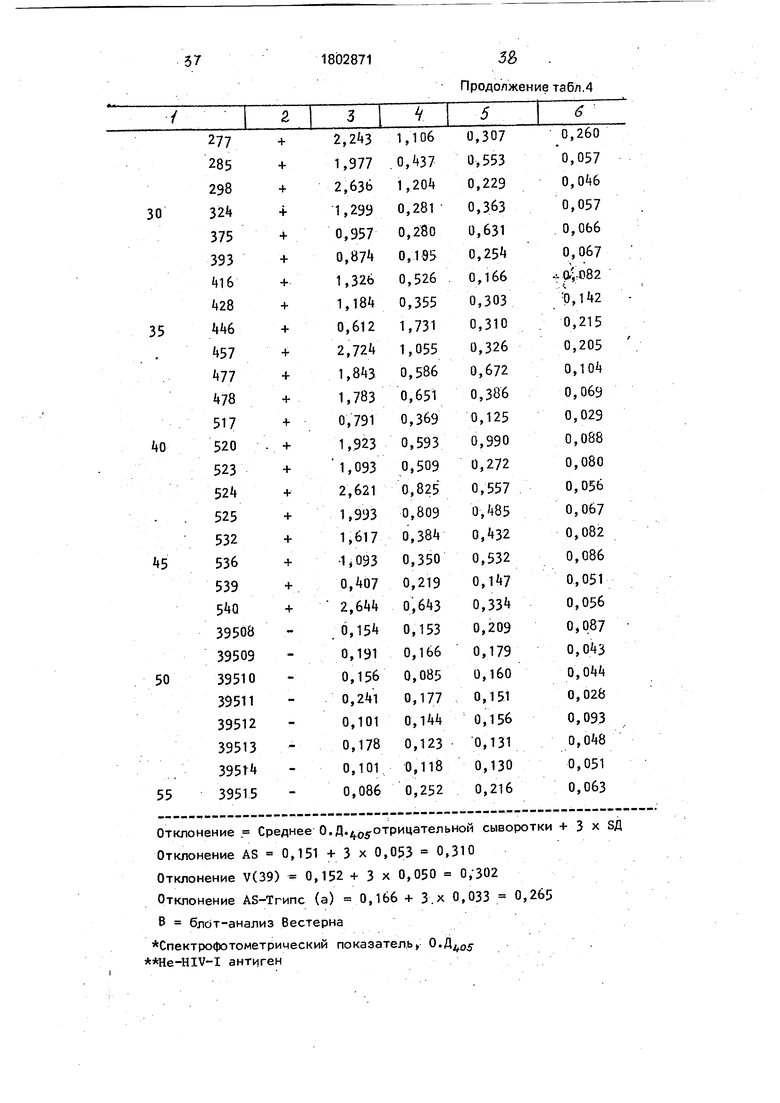
П р и м е р 4. Пептид AS-Trun с/а/ с пропущенным карбоксильным концевым участком др31А5 фиг.2 также синтезируют по методике примера 1 и используют в тестах ELISA, как описано в примере 2, не за- менив пептид др41А5 на AS-trunc/a/, для измерения антигенной активности. Из результатов ELISA, представленных в таблицах 4, легко видеть, что очевидно, что карбоксильная концевая часть др41А5 тре- буется для высокой степени реактивности и специфичности этого пептида.
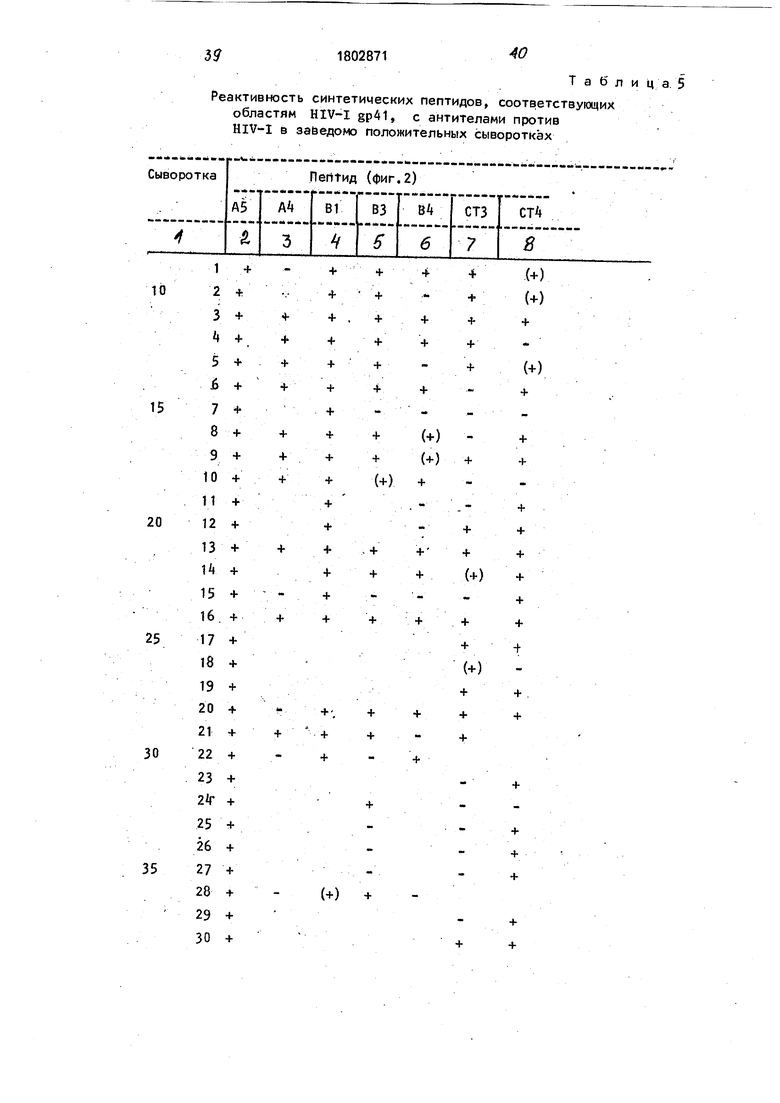
П р и м е р 5. Синтезируют по методике примере 1 пептид др41СТ4, имеющий аминокислотную последовательность, пред- ставленную выше, и испытывают в анализе ELISA по методике примера 2 (заменив др41А5 на др41СТ4 против 105 HJV- 1 по- ложительных.сывороток(всеони реагировали с др41А5). Наносят покрытие на плашки для микротирования по методике примера 2 при концентрации пептида между 10 и 100 мкг/мл. Как показано в таблице 5, этот пептид реагирует с 68/106 (64,8%) положительными сыворотками. Не наблюдалось ложных положительных реакций при испытании этого пептида против 28 достоверно отрицательных сывороток.
П р и м е р 6. Синтезируют по методике примера 1 пептид др41СТЗ, имеющий ами- нокислотную последовательность, представленную выше, и показывают им плашки для микротитрования по методике примера 2 (заменив gp41 A5 на др41 СТЗ). Как показано в таблице 5, др41СТЗ реагирует с 38/80 (48,8%) образцами заведомо положитель-. ных сывороток в анализе ELISA, как описано в примерах 2 и 3. Пептид дает только одну ложную положительную реакцию при испытании против 20 заведомо отрицательных сывороток.
П риме р7. Покрывают плашки микро- титраторапептидомдр41В1, синтезированным по методике примера 1, с концентрацией 10-100 мкг/мл, покрытие проводят по поисанной выше методике и используют в анализе ELISA, как описано в примере 2 (заменив др41А5 на др41В1). Этот пептид реагирует с 45/95 (47,4 %) образцов достоверных HJV - 1 положитель-
ных сывороток (таблица 5). Не имелось ложных положительных сывороток (таблица 5), Не имелось ложных положительных реакций с двумя отрицательными сыворотками.
Примере. Покрывают пептидом др41ВЗ, синтезированным по методике примера 1, с концентрацией 10-100 мкг/мл плашки микротитратора. Он дает положительные реакции с 22/32 (68,8%) заведомо положительными HJV - 1 образцами сыворотки в анализе ELISA, как описано в примерах 2 и 3 (таблица 5). Не наблюдали ложных положительных реакций с двумя заведомо отрицательными сыворотками.
. П р и м е р 9. Синтезируют GAG 2 и GAG 3 и GAG 14пептиды по методике примера 1. Наносят покрытие на плашки микротитра- тора из каждого пептида при концентрации 10-100 мкг/мл и используют в анализе ELISA, как описано в примере 2, но изменив др41А5 на GAG 2, GAG 3 или GAG 14 как антиген. Пептид GAG 2 также анализируют против HJV - 1 положительных образцов сывороток. Результаты анализов приведены в таблице 6.
ПримерЮ. Синтезируют пептиды P17-D и P17-F по методике примера 1 и покрывают каждый пептидом при концентрации 500 мкг/мл плашки микротитратора, используют в анализе ELISA по. методике примера 2, но заменив др41А5 на P17-D и P17-F в качестве антигена. Эти пептиды также анализируют против HJV - 2 положительных образцов сывороток. Результаты представлены в таблице 7.
НJV - 2, родственных ретровирус, но не идентичный HJV - 1, недавно был выделен у больных AIDS из Западной Африки, кот.о- рый в анализе ELISA дает отрицательный ответ при использовании HIB -1 антигенов.
Из данных таблиц 6 и 7 можно видеть по данным примеров 9 и 10, что пептиды GAG 2, P17-D и P17-F каждый содержит эпитопы, распознаваемые антителами как к HJV - 1, так и к HJV - 2. .Следовательно, эти три пептида могут быть полезными для диагностики и композиций вакцин при обеих инфекциях HJV - 1 и HJV - 2.
Из приведенных выше результатов очевидно, что новые синтетические пептиды, описанные здесь, которые соответствуют областям иммунологически важных белков HIV - 1, например др41 и оао генным продуктам, обеспечивают более чувствительный и селективный анализ на наличие антител к HJV- 1.
Ф о р м у л а и з о б р е т е н и я
Способ определения антител к HJV - 1 путем взаимодействия с антигеном в иммунологмческой реакции, о т л и ч a rout и и с я тем, что, с целью повышения точности, в качестве антигена используют один или более полипептидов формулы
X-Asp-Glu-Glu-Leu-Leu-Gly-lle-Trp-Gly-Cy S-Ser-Gly- Lys-LeiHIe-Cys-Tbr-Thr-Ala- Val-Pro-Trp-Asn-Y-, Asp-Gln-Gln-Leu- Leu-Gly-Trp-Gly-Cys-Ser-Gly- Lys-Leu-He-Cys-Thr-Ala-Val-Pro-Trp- Asn-Cys-OH, X-Ala-Leu-Lys-Tyr-Trp- Asn-Leu-Leu-Gln-Tyr- Trp-Ser-Gln- Glu-Leu-Lys-Asn-Ser-Ala-Val-Ser-Y-Z, X-Lys-Asn-Ser-Ala-Val-Ser-Leu-Leu-Asn-A la-Thr- Ala-lle-Ala-Val-Ala-Glu-Gly-Thr- Asp-Y-Z, X-Thr-Ala-Val-Pro-Trp-Asn-Ala- S e r-Trp-Ser-Asn-Lys- Ser-Leu-Glu-Glu-lle-Trp-Asn-Asn-Met-Thr
-Trp-Met-Y-Z, X-lle-Asn-Tyf-Thr-Ser-Leu- lle-Hls-Ser-Leu-lle- Glu-Glu-Ser-Glu-Asn-GIn- G I n - G I u - L y-s - A s n - G I u - Y - Z , X-Pro-Arg-Thr-Leu-Asn-Ala-Trp
-Val-Lys-Val-Val-Gru- Glu-Lys- Ala-Phe-Ser-Pzo-Glu-Val-Y-Z, X-Val-Glu-Gly-Lys-Ala-Phe-Ser-Pro-G lu - Val-lle- Pro-Met-Phe-Ser-Ala-Leu-Ser- Glu-G y-Y-Z, X-Glu-Met-Met-Thr-Ala-Cys- G I n - G I у - V a I - G I у - G I y - Pro-Gly-Hls-Lys-Ala-Arg-Val-Leu-Ala-Glu
-Y-Z, X-Ser-Glu-Gly-Cys-Arg-Gln-lte-Leu- Gly-Gln-Leu-GIn- Pro-Ser-Leu-Gln-Thr-Gly- Ser-Glu-Glu-Leu-Y-Z.
и/или
X-Leu-Tyr-Cys-Val-Hls-Gln-Arg-lle-GI u-lle-Lys- Asp-Thr-Lys-Glu-Ala-Leu-Asp- Lys-lle-Y-Z,
где Х- или Н в аминоконцевой NHa-rpynne пептида, или аминокислота, связанная с аминоконцевой МНа-группой пептида, причем кислота выбрана для обеспечения связывания пептида с белковым носителем;
J- или Cys, или отсутствует,
Z - или ОН, или NH2.
Приоритет по признакам
27.03.87 - пептид Asp-GIn-Gln-Leu-Leu- Gly-lle-Tzp-Gly-Cys-Ser-Gly-Lys-Leu-lle-Cys- Thr-Thr-Ala-Val-Pro-Trp-Asn-Cys-OH.
18.05.87 Все другие признаки формулы изобретения.
Таблица2




















| название | год | авторы | номер документа |
|---|---|---|---|
| ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ С ВЫСОКОПЛОТНЫМ ПОКРЫТИЕМ ДЛЯ ИНДУКЦИИ ЭКСПРЕССИИ АНТИТЕЛ | 2017 |
|
RU2813282C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ И/ИЛИ ПРЕДОТВРАЩЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2016 |
|
RU2714205C2 |
| Антитела против белка р17 ВИЧ-1 субтипа А | 2019 |
|
RU2727673C1 |
| Эпитоп тиоредоксина-1, специфично связывающийся с моноклональным антителом | 2018 |
|
RU2804772C2 |
| ЭПИТОП ТИОРЕДОКСИНА-1, СПЕЦИФИЧНО СВЯЗЫВАЮЩИЙСЯ С МОНОКЛОНАЛЬНЫМ АНТИТЕЛОМ | 2018 |
|
RU2804126C2 |
| Эпитоп тиоредоксина-1 и моноклональное антитело, специфически связывающееся с ним | 2018 |
|
RU2797266C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ И ПРЕДОТВРАЩЕНИЯ ГЕПАТИТА В И D | 2021 |
|
RU2812764C1 |
| ЭПИТОП ТИОРЕДОКСИНА-1, СПЕЦИФИЧНО СВЯЗЫВАЮЩИЙСЯ С МОНОКЛОНАЛЬНЫМ АНТИТЕЛОМ | 2023 |
|
RU2802944C1 |
| Моноклональное антитело, специфично связывающееся с эпитопом тиоредоксина-1, его получение и применение | 2018 |
|
RU2790687C2 |
| Моноклональное антитело, специфично связывающееся с эпитопом тиоредоксина-1, его получение и применение | 2018 |
|
RU2791264C2 |

Использование: иммунология, диагностика СПИДа. Сущность изобретения: пред- лагаются синтетические пептмды, соответствующие областям иммунологиче- ски реактивных белков HJV-1, используемые при дигностике HJV-1-инфекции. 7 табл., 3 ил.
Иммунологическая реактивность, определенная EL1SA между HIV-1 антителами в 233 образцах достоверно положительных сывороток и синтетическими пелтидными антигенами, соответствующими областям
. 1802871 24
Продолжение табл.2
25
180287126
Продолжение табл. 2
271802871 28
Продолжение табл.2
31
Т а б л и ц а 3
EL1 SA тесты сравнения специфичности и селективности синтетических пептидных антигенов
1802871
32
Продолжение табл.2
33
1802871
It Продолжение табл.3
S5
Спектрофотометрический показатель, О.Д. He-H4V I антиген
Отклонение Среднее 0.Д.отрицательной сыворотки ч+ Зх9Д .
Отклонение AS - 0,151 + 3 х 0,053 « 0,310 (О.ДЧ0 )
Отклонение V(39) -0,152,+ 3 х 0,050 0,302 (О.ДЧв..)
WB блот-аналиэ Вестерна с использованием HIV-I антигенов
Таблица
Реактивность антител в образцах сыворотки с синтетическими пептидными антигенами, соответствующими HIV-I антигенам
1802871
36 Продолжение .З
Отклонение . Среднее 0.Д.отрицательной сыворотки +3 х 8Д Отклонение AS 0,151 + 3 х 0,053 я 0,ЗЮ Отклонение V(39) 0,152 + 3 х 0,050 0;302 Отклонение AS-Тгипс (а) 0,166 + 3.x 0,033 0,265 В блбт-анализ Вестерна
Спектрофотометрический показател.ь О. He-HIV-I антиген
3 1802871 4°
Т а б л и ц а. 5
Реактивность синтетических пептидов, соответствующих областям HIV-I gp41, с антителами против HIV-I в заведомо положительных сыворотках
41
1802871
0
5
31
32
33
34
35
36
37
38
39
40
41
+ 4- + 44- +
4+ 4- + 4(+)
4- 4(+) (+)
05
10
15
42 +
43 4А
45
46
47
48
49
50
51
52
53
54
55
56
57
58
59
60
61
62
63 6V
65
66
+ +
4- 4- 4- + + 4- + 4- 4- 4- 44- 4- 4- 4- 4- 4- 4- 4- 4- 4- 4(4-) (+)
4(+)
4- 4- 4(+) 44(+) . (+) 4(f)
44444
4- 4- 4- 4- 4- + 44- 44- + 44(f)
(+)
43
1802871
0
5
0
5
Ю
5
50
67
68
69
70
71
72
73 7 V
75
76,
77
78
79
80
81
82
83 8k
85
86
87
. 88
89
90
91
92
93
9
95
- 96
97
98
99
100
101
102
103
+
4 4 4 4- 4- 4- 4 4 4- 4- + 4 +
. 4 4- 4- 4 4- 4
4- 4 4 4 4 4 4 4 4
4
4
4
4
4
}
4
(+) (+)
4 (+)
()
4 4- 4 4 44
44
4
4- 4 4м
4- 4 4
4
4
4
4
4
4
(+)
.,-- „
LLiLliJjd lLd,
Продолжение таб
- отрицательная реакция (+) слабая положительная реакция
f сильная положительная реакция
Иммунологическая реактивность пептидных антигентов,
соответствующих HjV-1 GAG генному продукту
Источник сыворотки
„
lLd,
Продолжение табл.5 8
Таблица б
Иммунблогическая реактивность антител в образцах
сывороток от больных HIV-1 и HIV-2 с пептидами,
соотвбтствующими HIV-1 и HIV-2 генными продуктами
Т а б лица 7
Фиг.1
СТ6
ПТ-Ю
аз. 19А др41
СТ4
Ш
СТ5
стз
СТ1
BAR 20 за
COOH-ferminus SP4-1
Фиг. 2
| Schorr et al, N | |||
| Engl.J | |||
| Приспособление для установки двигателя в топках с получающими возвратно-поступательное перемещение колосниками | 1917 |
|
SU1985A1 |
| Popovlc et a,, Science, 1984, 224; 497- 500 | |||
| Kuhni et at., Lancet I, 1985, 1222-1223 | |||
| Gallo et al., Science, 1984, 224; 503 | |||
| Allan et al., Science, 1985-228; 1091- 1094 | |||
| Wang et.al | |||
| Proc | |||
| Nate | |||
| Acad | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| Центробежный тахометр | 1927 |
|
SU6159A1 |
| Патент США N° 4629783, кл | |||
| Шпалорезный станок | 1921 |
|
SU530A1 |
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1993-03-15—Публикация
1988-03-25—Подача