ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №62/966970, поданной 28 января 2020 г., содержание которой настоящим явно полностью включено в данную заявку посредством ссылки.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка подана вместе с Перечнем последовательностей в электронном формате. Перечень последовательностей представлен в виде файла с названием SVF005SeqListing.TXT, который был создан и последний раз изменен 26 января 2021 г., размер которого составляет 141377 байт. Информация, представленная в электронном Перечне последовательностей, настоящим полностью включена в данную заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0003] В аспектах настоящего изобретения в общем предложены иммуногенные композиции или комбинации продуктов сконструированных нуклеиновых кислот, генов, пептидов или белков гепатита В (HBV) и гепатита D (HDV), которые можно применять, чтобы вызвать иммунный ответ против инфекции HBV и/или HDV. Этот иммунный ответ включает, состоит по существу из или состоит из активированных иммунных клеток, которые продуцируют нейтрализующие антитела, и активированных иммунных клеток, таких как Т-клетки и В-клетки, против HBV и/или HDV. В соответствии с настоящим изобретением также в общем предложены способы применения указанных иммуногенных композиций или комбинаций продуктов у субъектов, чтобы индуцировать иммунные ответы против HBV и/или HDV путем введения указанных композиций или комбинаций с применением подхода, включающего примирование (прайм) гомологичной или гетерологичной нуклеиновой кислотой и/или полипептидом и стимулирование (буст) нуклеиновой кислотой и/или полипептидом.
УРОВЕНЬ ТЕХНИКИ
[0004] Гепатит представляет собой заболевание, приводящее к отечности и воспалению печени. Это расстройство обычно вызывается вирусами, пять типов которых известно на сегодняшний день (вирусы гепатита А, В, С, D и Е). Инфицирование вирусом гепатита В может быть либо острым, либо хроническим, причем тяжелые хронические инфекции вызывают хроническое воспаление, фиброз, цирроз и гепатоцеллюлярную карциному. Вирус гепатита В имеет геном из частично двухцепочечной кольцевой ДНК, который проникает в ядро хозяина и транскрибируется РНК-полимеразой хозяина с образованием четырех молекул вирусной мРНК. Они используются для трансляции вирусных белков, таких как белки капсида и поверхностные антигены, а также для продукции большего количества ДНК-геномов с применением обратной транскриптазы. Гепатит D представляет собой вирусоид, для репликации которого требуется коинфекция или суперинфекция гепатитом В. Кольцевая одноцепочечная РНК гепатита D амплифицируется, используя РНК-полимеразы хозяев, но также содержит отдельный ген антигена гепатита D (HDAg). Во время коинфекции или суперинфекции вирусами гепатита В и D, интактные вирусы гепатита D пакуются в оболочку, содержащую поверхностные антигены гепатита В, окружающие РНК-геном, покрытый белком HDAg. Включение поверхностных антигенов гепатита В необходимо для инфекционности вируса гепатита D, так как вирус гепатита D не кодирует собственные белки связывания с рецептором. Коинфекция или суперинфекция вирусом гепатита D вызывает более тяжелые осложнения, с повышенным риском печеночной недостаточности, цирроза и рака печени. Существует потребность в эффективных иммуногенных композициях и вакцинах для создания профилактического иммунитета против обеих инфекций вирусами гепатита В и D.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0005] В настоящем изобретении в общем предложено применение рекомбинантных нуклеиновых кислот, ДНК, РНК, белков, полипептидов или пептидов, содержащих антигены HBV и/или HDV, чтобы вызвать иммунные ответы, продукцию антител, иммунную защиту или иммунитет против инфекций HBV или HDV. В некоторых вариантах реализации рекомбинантные нуклеиновые кислоты, ДНК, РНК, белки, полипептиды или пептиды, содержащие антигены HBV и/или HDV, применяют в подходе, включающем композицию для примирования ДНК/стимулирования белком. В некоторых вариантах реализации такой подход с композицией для примирования ДНК/стимулирования белком приводит к большему иммунному ответу, продукции антител, иммунной защите или иммунитету против инфекций HBV или HDV по сравнению с иммуногенными композициями на основе только ДНК, только белка или организма.
[0006] Хронические инфекции вирусами гепатита В и D (HBV/HDV) могут вызывать рак. Современная терапия HBV с применением аналогов нуклеозидов (NA) пожизненная и снижает, но не устраняет риск рака. Отличительной особенностью хронического гепатита В является нарушенный ответ специфичных к HBV Т-клеток. В некоторых вариантах реализации предложена иммунотерапия, запускаемая непримированными здоровыми Т-клетками, специфичными к антигену HDV (HDAg), чтобы обойти потребность в специфичных к HBV Т-клетках для примирования специфичных к PreS1 Т-клеток и продукции антител против PreS1, блокирующих проникновение HBV. В некоторых вариантах реализации оценивали индукцию антител против PreS1 и специфичных к HBV и HDV Т-клеток комбинациями последовательностей PreS1 и/или HDAg in vitro и in vivo. В некоторых вариантах реализации нейтрализацию HBV специфичными к PreS1 антителами мыши и кролика оценивали в культуре клеток, и исследовали нейтрализацию HBV антителами кролика против PreS1 у мышей, которых репопулировали гепатоцитами человека. В некоторых вариантах реализации адоптивный перенос антител против PreS1 предотвращал или модулировал инфекцию HBV после последующей провокации у гуманизированных мышей.
[0007] В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов содержат последовательности, гены или полипептиды HBV, HDV, PreS1 или HDAg. В некоторых вариантах реализации PreS1 представляет собой PreS1 А или PreS1 В. В некоторых вариантах реализации HDAg представляет собой HDAg генотипа 1 штамма А (1A), HDAg генотипа 1 штамма В (1В), HDAg генотипа 2 штамма А (2А) или HDAg генотипа 2 штамма В (2В). В некоторых вариантах реализации композиции также содержат сайт аутокаталитического расщепления пептида. В некоторых вариантах реализации сайт аутокаталитического расщепления пептида представляет собой сайт аутокаталитического расщепления пептида Р2А. В некоторых вариантах реализации компоненты PreS1 и HDAg сгруппированы друг с другом в композициях. В некоторых вариантах реализации PreS1 находится по ходу транскрипции или непосредственно по ходу транскрипции от последовательности HDAg. В некоторых вариантах реализации группы PreS1 и HDAg разделены сайтом аутокаталитического расщепления пептида. В некоторых вариантах реализации группы PreS1 и HDAg разделены сайтом аутокаталитического расщепления пептида Р2А.
[0008] В некоторых вариантах реализации композиции нуклеиновых кислот представляют собой плазмиду, вирус, бактериофаг, космиду, фосмиду, фагмиду, бактериальную искусственную хромосому (ВАС), дрожжевую искусственную хромосому (YAC) или искусственную хромосому человека (НАС). В некоторых вариантах реализации композиции нуклеиновых кислот являются кольцевыми или линейными. В некоторых вариантах реализации композиции нуклеиновых кислот получены в биологической системе, включая, но не ограничиваясь клетками млекопитающих, клетками человека, клетками бактерий, Е. coli, дрожжей, S. cerevisiae или другими подходящими биологическими системами. В некоторых вариантах реализации нуклеиновые кислоты или гены HBV и/или HDV находятся в кассете, которая содержит элементы, необходимые для транскрипции и трансляции нуклеиновых кислот или генов в биологической системе.
[0009] В некоторых вариантах реализации композиции полипептидов правильно свернуты (уложены) или денатурированы. В некоторых вариантах реализации композиции полипептидов получены в биологической системе, включая, но не ограничиваясь рекомбинантными системами экспрессии в млекопитающих, бактериях, дрожжах, насекомых или в бесклеточной системе. В некоторых вариантах реализации композиции полипептидов получают в клетках млекопитающего, человека, первичных, иммортализованных клетках, клетках рака, стволовых клетках, фибробластах, клетках эмбриональной почки человека (HEK) 293, клетках яичника китайского хомячка (СНО), бактериальных клетках, Escherichia coli, клетках дрожжей, Saccharomyces cerevisiae, Pichia pastoris, клетках насекомого, Spodoptera frugiperda Sf9 или S. frugiperda Sf21, или в бесклеточной системе. В некоторых вариантах реализации композиции полипептидов очищают, применяя методики, известные в данной области техники, включая, но не ограничиваясь перечисленным, экстрагирование, замораживание/размораживание, гомогенизацию, пермеабилизацию, центрифугирование, центрифугирование в градиенте плотности, ультрацентрифугирование, преципитацию, электрофорез в полиакриламидном геле в денатурирующих условиях (ПААГ/ДСН), нативный ЭФ в ПААГ, эксклюзионную хроматографию, жидкостную хроматографию, газовую хроматографию, хроматографию гидрофобных взаимодействий, ионообменную хроматографию, анионообменную хроматографию, катионообменную хроматографию, аффинную хроматографию, иммуноаффинную хроматографию, металл-аффинную хроматографию, хроматографию на никелевой колонке, очистку с помощью эпитопной метки или лиофилизацию.
[0010] В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов вводят животному, включая, но не ограничиваясь перечисленным, людей, мышей, крыс, кроликов, кошек, собак, лошадей, коров, свиней, овец, обезьян, приматов или кур. В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов вводят с интервалами в 1, 2, 3, 4, 5, 6 или 7 дней, или 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 недель, или 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 месяцев или в любой момент времени в пределах диапазона, заданного любыми двумя из указанных выше временных точек между каждой дозой. В некоторых вариантах реализации композиции нуклеиновых кислот вводят перед введением композиций полипептидов. В некоторых вариантах реализации композиции полипептидов вводят перед введением композиций нуклеиновых кислот.
[0011] В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов вводят в количестве 1, 10, 100, 1000 нг, или 1, 10, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 мкг, или 1, 10, 100 или 1000 мг или в любом количестве в пределах диапазона, заданного любыми двумя из указанных выше количеств. В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов вводят со вспомогательными веществами. В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов вводят с адъювантами. В некоторых вариантах реализации композиции нуклеиновых кислот вводят путем электропорации in vivo.
[0012] В некоторых вариантах реализации иммуногенность композиций нуклеиновых кислот или полипептидов оценивают путем измерения продуцирующих интерферон гамма (IFNγ) иммунных клеток, применяя методики, известные в данной области, включая метод иммуноферментных пятен (ELISpot), измерение титра антитела IgG, специфичного к HBV, HDV, белков HBV, нуклеиновых кислот HBV, белков HDV, нуклеиновых кислот HDV, PreS1 или HDAg, или измерение нейтрализующей активности сывороток или очищенных антител из иммунизированных животных в анализе in vitro или in vivo.
[0013] В некоторых вариантах реализации введение композиций нуклеиновых кислот или полипептидов обеспечивает временную, продолжительную или постоянную защиту против инфекции HBV или HDV. В некоторых вариантах реализации временная, продолжительная или постоянная защита против инфекции HBV или HDV превосходит таковую у других иммуногенных композиций. В некоторых вариантах реализации введение композиций нуклеиновых кислот или полипептидов осуществляют в сочетании с противовирусной терапией. В некоторых вариантах реализации введение композиций нуклеиновых кислот или полипептидов для обеспечения временной, продолжительной или постоянной защиты против инфекции HBV или HDV эффективно у людей. В некоторых вариантах реализации композиции нуклеиновых кислот или полипептидов применяют в качестве вакцин против HBV или HDV.
[0014] Предпочтительные аспекты настоящего изобретения имеют отношение к следующим пронумерованным альтернативам:
[0015] 1. Иммуногенная композиция или комбинация продуктов, содержащие:
(a) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и
(b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1.
[0016] 2. Иммуногенная композиция или комбинация продуктов согласно альтернативе 1, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4, или любую их комбинацию.
[0017] 3. Иммуногенная композиция или комбинация продуктов согласно альтернативе 1 или 2, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе.
[0018] 4. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-3, отличающиеся тем, что нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и тем, что последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от последовательности нуклеиновой кислоты HDAg.
[0019] 5. Иммуногенная композиция или комбинация продуктов согласно альтернативе 4, дополнительно содержащая по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида.
[0020] 6. Иммуногенная композиция или комбинация продуктов согласно альтернативе 5, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2А тешовируса свиней-1 (Р2А), 2А вируса ящура (F2A), 2А вируса ринита лошадей A (ERAV) (Е2А) и 2А вируса Thosea asigna (Т2А), и тем, что каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце.
[0021] 7. Иммуногенная композиция или комбинация продуктов согласно альтернативе 5 или 6, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ ID NO: 13.
[0022] 8. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-7, отличающиеся тем, что нуклеиновая кислота кодон-оптимизирована для экспрессии у человека.
[0023] 9. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-8, отличающиеся тем, что нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35-36.
[0024] 10. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-9, отличающиеся тем, что нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 18 или SEQ ID NO: 35-36.
[0025] 11. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-10, отличающиеся тем, что по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию.
[0026] 12. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-11, отличающиеся тем, что по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе.
[0027] 13. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-12, отличающиеся тем, что по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от по меньшей мере одной последовательности полипептида HDAg.
[0028] 14. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-13, отличающиеся тем, что полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37.
[0029] 15. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-14, отличающиеся тем, что полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37.
[0030] 16. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-15, отличающиеся тем, что полипептид экспрессирован рекомбинантным способом.
[0031] 17. Иммуногенная композиция или комбинация продуктов согласно альтернативе 16, отличающиеся тем, что полипептид экспрессирован рекомбинантным способом в системе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе.
[0032] 18. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-17, дополнительно содержащие адъювант.
[0033] 19. Иммуногенная композиция или комбинация продуктов согласно альтернативе 18, отличающиеся тем, что адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
[0034] 20. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-19, отличающиеся тем, что нуклеиновая кислота включает ДНК.
[0035] 21. Иммуногенная композиция или комбинация продуктов согласно любой из альтернатив 1-20, отличающиеся тем, что нуклеиновая кислота предоставлена в рекомбинантном векторе.
[0036] 22. Способ индуцирования иммунного ответа у субъекта с применением иммуногенной композиции или комбинации продуктов, представленных в любой из альтернатив 1-21, включающий:
введение указанному субъекту по меньшей мере одной примирующей дозы, содержащей нуклеиновую кислоту; и
введение указанному субъекту по меньшей мере одной стимулирующей дозы, содержащей полипептид.
[0037] 23. Способ согласно альтернативе 22, отличающийся тем, что по меньшей мере одна стимулирующая доза дополнительно содержит адъювант.
[0038] 24. Способ согласно альтернативе 23, отличающийся тем, что адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
[0039] 25. Способ согласно любой из альтернатив 22-24, отличающийся тем, что по меньшей мере одну стимулирующую дозу вводят по меньшей мере через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель после введения по меньшей мере одной примирующей дозы или в пределах диапазона времени, заданного любыми двумя из указанных выше моментов времени, например, в пределах 1-48 дней или 1-48 недель.
[0040] 26. Способ согласно любой из альтернатив 22-25, отличающийся тем, что введение осуществляют энтерально, перорально, интраназально, парентерально, подкожно, внутримышечно, внутрикожно или внутривенно, или любой комбинацией перечисленных путей.
[0041] 27. Способ согласно любой из альтернатив 22-26, отличающийся тем, что введение осуществляют в сочетании с противовирусной терапией.
100421 28. Способ согласно альтернативе 27, отличающийся тем, что противовирусная терапия включает введение энтекавира, тенофовира, ламивудина, адефовира, телбивудина, эмтрицитабина, интерферона-а, пегилированного интерферона-а или интерферона альфа-2b, или любой их комбинации.
10043] 29. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D, содержащая:
[0044] (а) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и
[0045] (b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1.
[0046] 30. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 29, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4, или любую их комбинацию.
[0047] 31. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 29 или 30, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе.
[0048] 32. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-31, отличающиеся тем, что нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и тем, что последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от последовательности нуклеиновой кислоты HDAg.
10049] 33. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 32, дополнительно содержащие по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида.
[0050] 34. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 33, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2А тешовируса свиней-1 (Р2А), 2А вируса ящура (F2A), 2А вируса ринита лошадей A (ERAV) (Е2А) и 2А вируса Thosea asigna (Т2А), и тем, что каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце.
[0051] 35. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 33 или 34, отличающиеся тем, что по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ IDNO: 13.
[0052] 36. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-35, отличающиеся тем, что нуклеиновая кислота кодон-оптимизирована для экспрессии у человека.
[0053] 37. Иммуногенная композиция или комбинация продуктов для применения для лечения или ингибирования гепатита В или гепатита D согласно любой из альтернатив 29-36, отличающиеся тем, что нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35-36.
[0054] 38. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-37, отличающиеся тем, что нуклеиновая кислота содержит SEQ ID NO: 18 или SEQ ID NO: 35-36.
[0055] 39. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-38, отличающиеся тем, что по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию.
[0056] 40. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-39, отличающиеся тем, что по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе.
[0057] 41. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-40, отличающиеся тем, что по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от по меньшей мере одной последовательности полипептида HDAg.
[0058] 42. Иммуногенная композиция или комбинация продуктов для применения для лечения или ингибирования гепатита В или гепатита D согласно любой из альтернатив 29-41, отличающиеся тем, что полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37.
[0059] 43. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-42, отличающиеся тем, что полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37.
[0060] 44. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-43, отличающиеся тем, что полипептид экспрессирован рекомбинантным способом.
[0061] 45. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 44, отличающиеся тем, что полипептид экспрессирован рекомбинантным способом в системе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе.
[0062] 46. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-45, дополнительно содержащие адъювант.
[0063] 47. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно альтернативе 46, отличающиеся тем, что адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
[0064] 48. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-47, отличающиеся тем, что нуклеиновая кислота включает ДНК.
[0065] 49. Иммуногенная композиция или комбинация продуктов для применения для лечения гепатита В или гепатита D согласно любой из альтернатив 29-48, отличающиеся тем, что нуклеиновая кислота предоставлена в рекомбинантном векторе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0066] Дополнительно к описанным выше признакам, дополнительные признаки и варианты будут однозначно следовать из приведенного далее описания чертежей и типичных вариантов реализации. Должно быть понятно, что на данных чертежах изображены типичные варианты реализации, и они не предназначены для ограничения объема изобретения.
[0067] На ФИГУРАХ 1A-В изображены конструкции нуклеиновых кислот или полипептидов, содержащие антигены HBV и/или HDV, используемые в данной заявке. Представлены десять конструкций: Дельта-1 (Δ-1, D1), Дельта-2 (Δ-2, D2), Дельта-3 (Δ-3, D3), Дельта-4 (Δ-4, D4), Дельта-5 (Δ-5, D5), Дельта-6 (Δ-6, D6), Дельта-7 (Δ-7, D7), Дельта-8 (Δ-8, D8), Дельта-9 (Δ-9, D9), и Дельта-10 (Δ-10, D10) (ФИГУРА 1А). Вестерн-блоттинг подтвердил, что указанные десять полипептидных конструкций правильно экспрессируются (ФИГУРА 1B). GFP использовали в качестве контроля для вестерн-блоттинга.
[0068] На ФИГУРЕ 2 изображены конструкции, используемые для подхода с композицией для примирования ДНК/стимулирования белком. Композиция ДНК содержит последовательность нуклеиновой кислоты Δ-4, и белковая композиция содержит полипептидную последовательность либо Δ-7, либо Δ-8, либо слитых Δ-7 и Δ-8.
[0069] На ФИГУРАХ 3A-3Е изображен количественный анализ образующихся пятен интерферона гамма (IFNγ) на 106 клеток в анализе ELISpot, которые соответствуют активации Т-лимфоцитов, очищенной популяции лейкоцитов из сывороток, происходящих из мышей, иммунизированных композициями ДНК HBV/HDV, в ответ на контакт с различными антигенами HBV или HDV. Антигены включают очищенные полипептиды, включая PreS1 A (SEQ ID NO: 11), PreS1 A (SEQ ID NO: 12), HDAg генотипа 1 A (SEQ ID NO: 5, «HDAg гтп 1A-пул 1» и «HDAg гтп 1A-пул 2»), HDAg генотипа 1 В (SEQ ID NO: 6, «HDAg гтп 1B-пул 3» и «HDAg гтп 1B-пул 4»), HDAg генотипа 2 A (SEQ ID NO: 7, «HDAg гтп 2С-пул 5» и «HDAg гтп 2С-пул 6») и HDAg генотипа 2 В (SEQ ID NO: 8, «HDAg гтп 20-пул 7» и «HDAg гтп 20-пул 8»). Мышей умерщвляли через 6 недель после первой иммунизации и объединенные в пулы спленоциты из каждой группы стимулировали в течение 48 часов пулами пептидов HDV 18, соответствующими генотипу 1 (пулы 1-4) и генотипу 2 (пулы 5-8). Пулы 1 и 2 генотипа 1 относятся к последовательности/изоляту А, тогда как пулы 3 и 4 соответствуют последовательности/изоляту В. Аналогично, пулы 5 и 6 генотипа 2 относятся к последовательности/изоляту С и пулы 7 и 8 генотипа 2 относятся к последовательности/изоляту D. Каждый пул содержал 20 или 221 (для пулов 1 и 5) 15-мерный пептид с перекрыванием 10 АК. Конканавалин А («КонА») использовали в качестве положительного контроля, и два пептида овальбумина («OVA Th» и «OVA CTL») и ростовую среду («среда») использовали в качестве отрицательных контролей. Для каждой стимулированной пептидом группы проводили запуск в трех повторах, и столбики показывают среднее количество образующих пятна IFNγ клеток (SFC) на 106 клеток со стандартной ошибкой. Отсечка была установлена на 100 SFC/106 спленоцитов. Концентрации антигенов представлены.
[0070] На ФИГУРАХ 4A-4С изображен количественный анализ титра антитела IgG против PreS1 в сыворотках, происходящих из мышей, иммунизированных композициями ДНК HBV/HDV. Конструкции Δ-1-Δ-10 исследовали на выработку антител IgG против консенсусных последовательностей PreS1 А и PreS1 В у мышей (по 5 мышей на группу). На ФИГУРАХ 4A-4В рассмотрена реактивность против аминокислот 2-48 PreS1. На ФИГУРЕ 4С рассмотрена перекрестная реактивность против (под-)генотипов HBV A1, А2, В, В2, С, D1, E1 hF.
[0071] На ФИГУРАХ 5A-5С изображен количественный анализ образующихся пятен интерферона гамма (IFNγ) на 106 клеток в анализе ELISpot очищенной популяции лейкоцитов из сывороток, происходящих из мышей C57BL/6 или трансгенных по HLA-A2 мышей HHD, иммунизированных композицией ДНК Δ-4, или непримированных мышей C57BL/6, в ответ на контакт с различными антигенами или пептидами HBV или HDV. Антигены включают очищенные полипептиды, включая PreS1 A (SEQ ID NO: 11), PreS1 A (SEQ ID NO: 12), пул, содержащий генотипы HDAg 1 А и 1 В (SEQ ID NO: 5 и 6, «гтп 1-пул 1», «гтп 1-пул 2», «гтп 1-пул 3», «гтп 1-пул 4»), пул, содержащий генотипы HDAg 2 А и 2 В (SEQ ID NO: 7 и 8, «гтп 2-пул В1», «гтп 2-пул В2», «гтп 2-пул В3», «гтп 2-пул В4»), пулы фрагментов пептидов HDAg, содержащие пептиды KLEDDNPWL, KLEEENPWL и FPWDILFPA («пеп-3-пул»), и отдельные пептиды HDAg KLEDDNPWL, KLEEENPWL и FPWDILFPA. Конканавалин А («КонА») использовали в качестве положительного контроля, и два пептида овальбумина («OVA Th» и «OVA CTL») и ростовую среду («среда») использовали в качестве отрицательных контролей. Концентрации антигенов представлены.
[0072] На ФИГУРАХ 6A-6С изображен количественный анализ титра IgG против PreS1 у Новозеландских белых кроликов, иммунизированных композициями ДНК Δ-3 или Δ-4. Собирали сыворотки из кроликов и исследовали с помощью ELISA против консенсусных пептидов PreS1А и PreS1B (ФИГУРА 6В). Антисыворотку вакцинированных кроликов также исследовали на перекрестную реактивность с (под-)генотипами HBV A1, А2, В, В2, С, D1, Е1 и F (ФИГУРА 6С). Столбики диаграммы показывают средние конечные титры против PreS1 для каждой группы, определенные как конечное последнее разведение сыворотки, дающее ОП на 405 нм в три раза выше, чем ОП неиммунизированных сывороток при таком же разведении. Сыворотки серийно титровали шестикратными разведениями, начиная с 1:60.
[0073] На ФИГУРЕ 6D показан процент реактивности антисывороток вакцинированных D-4 кроликов против PreS1 различных (под-)генотипов HBV. Антисыворотки вакцинированных D-4 кроликов в возрасте шести недель исследовали на реактивность (ОП на 405 нм) против (под-)генотипов HBV D1, F, А1, С, А2, В, В2 и Е1 с помощью ELISA. Используя отдельные 20-мерные пептиды PreS1 с перекрыванием десяти АК, соответствующие каждому типу HBV из АК 2-21, 12-31, 22-41 и 32-48, нейтрализующие эпитопы преимущественно локализовали на участке АК 22-41 и 32-48 генотипа D1, о чем свидетельствует наиболее высокий процент реактивности, за которым следовали (под-)типы С, Е1 и А1 на том же участке АК.
[0074] На ФИГУРАХ 7A-7С изображен количественный анализ образующихся пятен интерферона гамма (IFNy) в анализе ELISpot на 106 клеток очищенной популяции лейкоцитов из сывороток, полученных из мышей C57BL/6, иммунизированных только ДНК Д-4, только белком Δ-7 или примирующей/стимулирующей композицией ДНК Δ-4/белок Δ-8. Антигены включают очищенные полипептиды, включая PreS1 A (SEQ ID NO: 11), PreS1 A (SEQ ID NO: 12), пул, содержащий генотипы HDAg 1 А и 1 В (SEQ ID NO: 5 и 6, «гтп 1-пул 1», «гтп 1-пул 2», «гтп 1-пул 3», «гтп 1-пул 4»), и пул, содержащий генотипы HDAg 2 А и 2 В (SEQ ID NO: 7 и 8, «гтп 2-пул 5», «гтп 2-пул 6», «гтп 2-пул 7»з «гтп 2-пул 8»). Конканавалин А («КонА») использовали в качестве положительного контроля, и два пептида овальбумина («OVA Th» и «OVA CTL»), ДМСО и ростовую среду («среда») использовали в качестве отрицательных контролей. Концентрации антигенов представлены.
[0075] На ФИГУРАХ 8A-8С изображен количественный анализ титра IgG против PreS1 у мышей C57BL/6, иммунизированных только ДНК, только белком или композициями для примирования ДНК/стимулирования белком HBV/HDV.
[0076] На ФИГУРЕ 9 изображен количественный анализ титра IgG против PreS1 у кроликов, иммунизированных только ДНК, только белком или композициями для примирования ДНК/стимулирования белком HBV/HDV.
[00771 На ФИГУРАХ 10A-10В изображено защитное действие против инфекции HBV через 1, 2, 3, 4, 6 и 8 недель после первой инокуляции, что определили на основании титров HBV в каждый момент времени. Каждая линия показывает одну отдельную мышь (ФИГУРА 10А). Две мыши отрицательного контроля (серые линии) получили IgG неиммунизированных кроликов и три мыши (красные линии) получили D4 PreS1 IgG. Одна мышь из группы, которой вводили PreS1-IgG, умерла на 4 неделе, следовательно, для этой мыши доступны только измерения на 1, 2 и 3 неделе. Не наблюдали значимых различий между группами в отношении уровней в сыворотке аланинтрансферазы, аспарагинтрансферазы, щелочной фосфатазы или билирубина (ФИГУРА 10В).
[0078] На ФИГУРАХ 11A-D изображена оценка смесей пептидов D-7 и D-8 (10 мкг каждого для введения мышам) с различными адъювантами. Исследовали адъюванты QS-21, MF59 и квасцы. Композиции ДНК D-4, которые вводили внутримышечно с помощью электропорации, использовали в качестве контроля. На ФИГУРЕ 11А показан график введения доз и примеры конечных титров с исследованными адъювантами. На ФИГУРЕ 11В показан % реактивности у отдельных мышей для каждого условия, который оценивали с помощью ELISA. Ось х («1, 3, 10, 30, 0») соответствует идентификационным номерам отдельных мышей. На ФИГУРЕ ПС показана активация IFNy спленоцитов консенсусными пептидами PreS1 HBV и антигенов HDV, что оценивали с помощью ELISpot. На ФИГУРЕ 11D показаны конечные титры антитела против PreS1 против пептидов PreS1А и PreS1B.
[0079] На ФИГУРАХ 12A-D изображено сравнение примирования/стимулирования только смесью пептидов D-7 и D-8, только слитым пептидом D-7+D-8 и примирования ДНК D-4 и стимулирования смесью пептидов D-7 и D-8 с примированием/стимулированием только ДНК D-4 и непримированными контролями. На ФИГУРЕ 12А показана активация IFNγ спленоцитов консенсусными пептидами PreS1 HBV и антигенов HDV, что оценивали с помощью ELISpot. На ФИГУРЕ 12 В показаны уровни антитела против PreS1А, которые оценивали через 2 недели после первого раунда введения. На ФИГУРЕ 12С показаны уровни антитела против PreS1А, которые оценивали через 2 недели после второго раунда введения. На ФИГУРЕ 12D показаны уровни антитела против PreS1B, которые оценивали через 2 недели после второго раунда введения. Подписи к ФИГУРАМ 12В-D соответствуют идентификационным номерам отдельных мышей.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0080] Несмотря на профилактические вакцины и противовирусные методы лечения, хроническая инфекция вирусом гепатита В (HBV) на сегодняшний день поражает более 250 миллионов людей по всему миру. Один миллион хронических носителей погибают каждый год вследствие связанных с печенью осложнений, вызванных HBV, таких как цирроз печени и, в конечном счете, гепатоцеллюлярная карцинома (ГЦК). Вирус гепатита D (HDV), РНК-сателлитный вирус для HBV, который «крадет» поверхностный антиген у HBV (HBsAg), коинфицирует 15-25 миллионов носителей HBV во всем мире и усугубляет прогрессирование заболевания. До сих пор не существует эффективного функционального лечения хронической инфекции HBV или HDV. Современное стандартное лечение HBV состоит из аналогов нуклеозидов (NA), которые ингибируют функцию обратной транскриптазы (ОТ) полимеразы HBV. Это предотвращает созревание вируса посредством блокирования синтеза частично дцДНК внутри капсида. Таким образом, NA только подавляют репликацию вируса во время терапии. Это является следствием того, что блокирование ОТ не влияет ни на продукцию и высвобождение белка (включая HBsAg), ни на синтез ковалентно замкнутой кольцевой ДНК, главной причины персистенции HBV. Пожизненный прием NA снижает, но не исключает риск ГКК. Режим, включающий по меньшей мере один год введения пегилированного интерферона (1Г>1)-альфа, на сегодняшний день является рекомендуемым лечением хронического HDV; тем не менее, стойкие ответы редки. Было показано, что комбинированное лечение пегилированным IFN-альфа и NA имеет ограниченную эффективность против HDV и HBV.
[0081] HBV использует несколько стратегий, чтобы ускользнуть от иммунного ответа хозяина. Хроническое присутствие белков HBV вызывает дисфункцию Т-клеток. Инфицированные HBV клетки продуцируют в повышенном количестве субвирусные частицы HBsAg, преимущественно содержащие малый HBsAg (SHBsAg), чтобы блокировать популяцию нейтрализующих антител, направленных против SHBsAg. Это гарантирует выживаемость вирусных частиц, на поверхности которых содержится больше средних белков HBsAg (MHBsAg; содержащих S и PreS2) и больших белков HBsAg (LHBsAg; содержащих S, PreS2 и PreS1). Важно отметить, что домен PreS1 отвечает за связывание с Иа+-таурохолат-котранспортирующим полипептидом (NTCP)-рецептором для HBV на гепатоцитах. Таким образом, явным способом нацеливания на инфекционные частицы HBV и предотвращения инфицирования новых гепатоцитов будет повышение уровня антител против домена PreS1 вируса.
[0082] В настоящей заявке описано, что для создания иммунотерапии, нацеленной на инфекцию как HBV, так и HDV, чтобы вызвать продукцию антител против PreS1 и Т-клеток, специфичных к HBV и HDV, получали химерные гены, содержащие PreS1 и большой антиген HDV в различных комбинациях (Фигура 1А). Преимущество соединения PreS1 с HDAg состоит в том, что HDAg будет действовать как гетерологичный носитель Т-клеточного эпитопа у пациентов, которые моноинфицированы HBV. Таким образом, эти специфичные к HDAg Т-клетки поддерживают длительную эндогенную продукцию антител против PreS1, которые блокируют проникновение вируса и позволяют обойти потребность в специфичных к HBV Т-клетках. В действительности, >90% носителей HBV моноинфицированы HBV, и у этих пациентов гетерологичный HDAg будет примировать здоровые непримированные Т-клетки, которые поддерживают примирование специфичных к HBV ответов. Кроме того, вероятно, что специфичные к HDAg Т-клетки и антитела против PreS1 предотвращают суперинфекцию HDV у этих пациентов. Для того чтобы индуцировать как нейтрализующие антитела, так и Т-клетки, применяли генетическую иммунизацию, так как показали, что эта стратегия активирует иммунный ответ на HBV. В целом, эта стратегия блокирования проникновения вируса дополняет ингибиторы созревания и ингибиторы сборки капсида, которые находятся в разработке на данный момент, чтобы добиться продолжительных ответов вне терапии против инфекции HBD и/или HDV.
[0083] Варианты реализации, предложенные в данной заявке, относятся к иммуногенным композициям или комбинациям продуктов сконструированных нуклеиновых кислот, генов, пептидов или белков гепатита В (HBV) и гепатита D (HDV), которые можно применять, чтобы вызвать иммунный ответ против инфекции HBV или HDV. Применение химерных генов и химерных белков, содержащих нуклеиновые кислоты, гены, пептиды или белки HBV и HDV, было описано, например, в WO 2017/132332, которая настоящим явно полностью включена в данную заявку посредством ссылки.
[0084] В следующем подробном описании есть ссылки на сопроводительные чертежи, которые являются его частью. На чертежах одинаковые символы обычно обозначают одинаковые компоненты, если контекстом не определено иное. Иллюстрирующие варианты реализации, описанные в подробном описании, чертежах и формуле изобретения, не подразумевают ограничения. Можно использовать другие варианты реализации, и можно осуществить другие изменения, не отклоняясь от сущности и объема объекта изобретения, представленного в данной заявке. Будет сразу понятно, что аспекты настоящего изобретения, описанные в общих чертах в данной заявке и проиллюстрированные на Фигурах, можно расположить, заменить, объединить, разделить и разработать в большом разнообразии различных конфигураций, все из которых явно предусмотрены в данной заявке.
[0085] Если не указано иное, все технические и научные термины, используемые в данной заявке, имеют те же значения, которые обычно понимает средний специалист в данной области техники. Все патенты, заявки на патент, опубликованные заявки на патент и другие публикации, на которые ссылаются в данной заявке, явно полностью включены в данную заявку посредством ссылки, если не указано иное. В случае, когда существует множество определений термина в данной заявке, определения, приведенные в данном разделе, имеют преимущественную силу, если не указано иное.
[0086] Формы единственного числа используют в данной заявке по отношению к одному или более чем одному (например, по меньшей мере одному) из грамматических объектов. В качестве примера, «элемент» означает один элемент или более чем один элемент.
[0087] Термины «приблизительно» или «около» в данной заявке относятся к количеству, уровню, значению, числу, частоте, проценту, измерению, размеру, величине, массе или длине, которые варьируются на целые 30, 25, 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1% относительно указанного количества, уровня, значения, числа, частоты, процента, измерения, размера, величины, массы или длины.
[0088] По всему тексту настоящего описания, если по контексту не требуется иное, термины «содержат», «содержит» и «содержащий» следует понимать как подразумевающие включение указанного этапа или элемента или группы этапов или элементов, но не исключение любого другого этапа или элемента или группы этапов или элементов.
[0089] Под формулировкой «состоящий из» подразумевают включающий, и она ограничена тем, что следует за формулировкой «состоящий из». Таким образом, формулировка «состоящий из» указывает на то, что перечисленные элементы необходимы или обязательны, и что другие элементы не могут присутствовать. Под формулировкой «состоящий по существу из» подразумевают включение любых элементов, перечисленных после указанной формулировки, и ограничение такими другими элементами, которые не препятствуют или способствуют активности или действию, указанным в настоящем описании для перечисленных элементов. Таким образом, формулировка «состоящий по существу из» указывает на то, что перечисленные элементы необходимы или обязательны, но что другие элементы необязательны и могут присутствовать или не присутствовать в зависимости от того, оказывают ли они или не оказывают существенного влияния на активность или действие перечисленных элементов.
[0090] При осуществлении настоящего изобретения будут применяться, если конкретно не указано противоположное, обычные способы молекулярной биологии и технологии рекомбинантных ДНК, находящиеся в рамках компетенции в данной области, множество из которых описано ниже с целью иллюстрирования. Такие методики полностью объяснены в литературе. См., например, Sambrook, el al., Molecular Cloning: A Laboratory Manual (Зе издание, 2000); DNA Cloning: A Practical Approach, тома 1 и II (D. Glover, ред.); Oligonucleotide Synthesis (N. Gait, ред., 1984); Oligonucleotide Synthesis: Methods and Applications (P. Herdewijn, ред., 2004); Nucleic Acid Hybridization (B. Hames & S. Higgins, ред., 1985); Nucleic Acid Hybridization: Modern Applications (Buzdin и Lukyanov, ред., 2009); Transcription and Translation (B. Hames & S. Higgins, ред., 1984); Animal Cell Culture (R. Freshney, ред., 1986); Freshney, R.I. (2005) Culture of Animal Cells, a Manual of Basic Technique, 5oe изд. Hoboken NJ, John Wiley & Sons; B. Perbal, A Practical Guide to Molecular Cloning (Зе издание, 2010); Farrell, R., RNA Methodologies: A Laboratory Guide for Isolation and Characterization (3e издание, 2005).
10091] Термин «чистота» любого данного вещества, соединения или материала в данной заявке относится к фактической представленности вещества, соединения или материала по сравнению с ожидаемой представленностью. Например, вещество, соединение или материал может быть по меньшей мере на 80, 85, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 или 100% чистым, включая все десятичные доли между указанными значениями. На чистоту могут влиять нежелательные примеси, включая, но не ограничиваясь побочными продуктами, изомерами, энантиомерами, продуктами деградации, растворителем, носителем, средой или примесями, или любой их комбинацией. Чистоту можно измерить с помощью технологий, включая, но не ограничиваясь хроматографией, жидкостной хроматографией, газовой хроматографией, спектроскопией, спектрометрией в УФ и видимом диапазонах, инфракрасной спектрометрией, масс-спектрометрией, ядерным магнитным резонансом, гравиметрией или титрованием, или любой их комбинацией.
[0092] Термины «функция» и «функциональный» в данной заявке относятся к биологической, ферментативной или терапевтической функции.
[0093] Формулировки «эффективное количество» или «эффективная доза» в данной заявке относятся к количеству, достаточному, чтобы добиться желательного результата и, соответственно, будут зависеть от ингредиента и желательного результата. Тем не менее, после того как станет известен желательный эффект, определение эффективного количества находится в рамках компетенции специалиста в данной области техники.
[0094] Обычно «планки погрешностей», приведенные на фигурах, представляют собой стандартную ошибку среднего значения.
[0095] Термины «состав» и «композиция», используемые взаимозаменяемо в данной заявке, представляют собой эквивалентные термины, относящиеся к смеси химически связанных веществ для введения субъекту.
[0096] Термин «выделенный/изолированный» в данной заявке относится к материалу, который главным образом или по существу свободен от компонентов, которые обычно сопутствуют ему в природном состоянии. Например, «выделенная клетка» в данной заявке включает клетку, которая была очищена из окружения или организмов в ее встречающемся в природе состоянии, клетку, которая была удалена из субъекта или из культуры, например, она в значительной мере не связана с веществами in vivo или in vitro.
[0097] Термин «субъект» в данной заявке имеет обычное значение, которое понятно в свете настоящего описания, и относится к животному, которое является объектом лечения, ингибирования или улучшения, наблюдения или эксперимента. Термин «животное» имеет обычное значение, которое понятно в свете настоящего описания, и включает холоднокровных и теплокровных позвоночных и/или беспозвоночных, таких как рыбы, моллюски или пресмыкающиеся и, в частности, млекопитающие. Термин «млекопитающее» имеет обычное значение, которое понятно в свете настоящего описания, и включает, но не ограничен мышами, крысами, кроликами, морскими свинками, собаками, кошками, овцами, козами, коровами, лошадьми, приматами, такими как люди, обезьяны, шимпанзе или человекообразные обезьяны. В некоторых вариантах реализации субъект представляет собой человека.
[0098] В некоторых вариантах реализации, описанных в данной заявке, предложен выбор нуждающегося субъекта или пациента. В некоторых вариантах реализации выбирают пациента, который нуждается в лечении вирусной инфекции. В некоторых вариантах реализации выбирают пациента, который ранее получал лечение от вирусной инфекции. В некоторых вариантах реализации выбирают пациента, который ранее получал лечение от риска возникновения вирусной инфекции. В некоторых вариантах реализации выбирают пациента, у которого развился рецидив вирусной инфекции. В некоторых вариантах реализации выбирают пациента, у которого развилась устойчивость к методам лечения вирусной инфекции. В некоторых вариантах реализации выбирают пациента, у которого может быть любая комбинация указанных выше критериев селекции.
[0099] Термины «лечить», «лечение», «терапевтический» или «терапия» в данной заявке имеют обычное значение, которое понятно в свете настоящего описания, и не обязательно означают полное излечение или устранение заболевания или состояния. Термин «лечить» или «лечение» (и что хорошо известно в данной области техники) также означает подход к получению полезных или желательных результатов в отношении состояния субъекта, включая клинические результаты. Полезные или желательные клинические результаты могут включать, но не ограничены перечисленными: облегчение или снижение выраженности одного или более симптомов или состояний, уменьшение масштаба заболевания, стабилизацию (т.е., отсутствие ухудшения) состояния заболевания, предотвращение передачи или распространения заболевания, отсрочивание или замедление прогрессирования заболевания, снижение выраженности или временное облегчение болезненного состояния, уменьшение повторной встречаемости заболевания и ремиссию, либо частично, либо полностью и либо детектируемо, либо не детектируемо. Термины «лечить» и «лечение» в данной заявке также включают профилактическое лечение. Способы лечения включают введение субъекту терапевтически эффективного количества активного агента. Этап введения может состоять из однократного введения или может включать серию введений. Композиции вводят субъекту в количестве и в течение периода времени, достаточного для лечения пациента. Протяженность периода лечения зависит от различных факторов, таких как тяжесть состояния, возраст и генетический профиль пациента, концентрация активного агента, активность композиций, применяемых для лечения, или их комбинация. Также будет понятно, что эффективная дозировка агента, применяемого для лечения или профилактики, может повышаться или снижаться в ходе конкретного режима лечения или профилактики. Изменения в дозировке могут являться результатом и становиться ясными после стандартных диагностических анализов, известных в данной области техники. В некоторых случаях может потребоваться постоянное введение.
[0100] Термин «ингибировать» в данной заявке имеет обычное значение, которое понятно в свете настоящего описания, и может относиться к снижению или предотвращению вирусной инфекции. Снижение может быть на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100%, или на величину, которая находится в пределах диапазона, заданного любыми двумя из указанных выше значений. В данной заявке термин «отсрочивать» имеет обычное значение, которое понятно в свете настоящего описания, и относится к замедлению, отсрочке или откладыванию явления, такого как вирусная инфекция, на более позднее время, чем ожидаемое в противном случае. Отсрочивание может представлять собой отсрочивание на 0%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или величину в пределах диапазона, заданного любыми двумя из указанных выше значений. Термины ингибировать и отсрочивать не обязательно указывают на 100% ингибирование или отсрочивание. Может осуществляться частичное ингибирование или отсрочивание.
[0101] Термин «иммуногенная композиция» в данной заявке относится к веществу или смеси веществ, включая, но не ограничиваясь перечисленными: антигены, эпитопы, нуклеиновые кислоты, пептиды, полипептиды, белки, полисахариды, липиды, гаптены, токсоиды, инактивированные организмы или аттенуированные организмы, или любую их комбинацию, предназначенным для того, чтобы вызвать иммунный ответ при введении хозяину. Иммунный ответ включает как врожденный, так и приобретенный иммунный ответ, последний из которых создает продолжительную иммунологическую память посредством клеток, таких как Т-клетки памяти и В-клетки памяти. Антитела, созданные во время первичного иммунного ответа на иммуногенную композицию, можно получить при последующих провокациях теми же антигенами, эпитопами, нуклеиновыми кислотами, пептидами, полипептидами, белками, полисахаридами, липидами, гаптенами, токсоидами, инактивированными организмами или аттенуированными организмами, или живым организмом или патогеном, на котором выставлены указанные антигены, эпитопы, нуклеиновые кислоты, пептиды, полипептиды, белки, полисахариды, липиды, гаптены или токсоиды, или любая их комбинация. Таким образом, иммуногенная композиция может служить в качестве вакцины против определенного патогена. Иммуногенные композиции также могут содержать один или более адъювантов, чтобы стимулировать иммунный ответ и повысить эффективность защитного иммунитета.
[0102] Термин «комбинация продуктов» в данной заявке относится к набору из двух или более отдельных соединений, веществ, материалов или композиций, которые можно применять совместно для единой функции. В некоторых вариантах реализации комбинация продуктов содержит по меньшей мере одну композицию нуклеиновых кислот и по меньшей мере одну композицию полипептидов, которые применяют совместно, чтобы вызвать иммунный ответ при введении хозяину, необязательно в большей степени, чем был бы вызван, если бы только один тип композиции подлежал введению.
[0103] Термины «нуклеиновая кислота» или «молекула нуклеиновой кислоты» в данной заявке относятся к полинуклеотидам, таким как дезоксирибонуклеиновая кислота (ДНК) или рибонуклеиновая кислота (РНК), олигонуклеотидам, фрагментам, полученным в результате полимеразной цепной реакции (ПЦР), и фрагментам, полученным с помощью любого из способов лигирования, расщепления, действия эндонуклеаз и действия экзонуклеаз. Молекулы нуклеиновых кислот могут состоять из мономеров, которые представляют собой встречающиеся в природе нуклеотиды (такие как ДНК и РНК), или аналоги встречающихся в природе нуклеотидов (например, энантиомерные формы встречающихся в природе нуклеотидов), или комбинацию обоих. Модифицированные нуклеотиды могут иметь изменения в сахарных группах и/или в группах пиримидинового или пуринового основания. Модификации сахара включают, например, замену одной или более гидроксильных групп на галогены, алкильные группы, амины и азидогруппы, или сахара могут быть функционализированы с образованием простых или сложных эфиров. Более того, всю сахарную группу можно заменить на стерически и электронно близкие структуры, такие как азасахара и карбоциклические аналоги сахара. Примеры модификаций в группе основания включают алкилированные пурины и пиримидины, ацилированные пурины или пиримидины или другие хорошо известные гетероциклические заместители. Мономеры нуклеиновых кислот могут быть связаны фосфодиэфирными связями или аналогами таких связей. Аналоги фосфодиэфирных связей включают фосфоротиоатную, фосфородитиоатную, фосфороселеноатную, фосфородиселеноатную, фосфороанилотиоатную, фосфоранилидатную или фосфорамидатную связь. Термин «молекула нуклеиновой кислоты» также включает так называемые «пептид-нуклеиновые кислоты», которые содержат встречающиеся в природе или модифицированные основания нуклеиновых кислот, присоединенные к полиамидному остову. Нуклеиновые кислоты могут быть либо одноцепочечными, либо двухцепочечными. Термин «олигонуклеотид» можно использовать взаимозаменяемо с термином «нуклеиновая кислота», и он может относиться либо к двухцепочечной, либо к одноцепочечной ДНК или РНК. Нуклеиновая кислота или нуклеиновые кислоты могут содержаться в векторе нуклеиновых кислот или конструкции нуклеиновых кислот (например, плазмиде, вирусе, бактериофаге, космиде, фосмиде, фагмиде, бактериальной искусственной хромосоме (ВАС), дрожжевой искусственной хромосоме (YAC) или искусственной хромосоме человека (НАС)), которые можно применять для амплификации и/или экспрессии нуклеиновой кислоты или нуклеиновых кислот в различных биологических системах. Обычно, вектор или конструкция также будут содержать элементы включая, но не ограничиваясь перечисленными: промоторы, энхансеры, терминаторы, индукторы, участки связывания рибосомы, сайты инициации трансляции, инициирующие кодоны, стоп-кодоны, сигналы полиаденилирования, точки начала репликации, сайты клонирования, сайты множественного клонирования, сайты ферментов рестрикции, эпитопы, репортерные гены, маркеры селекции, маркеры селекции антибиотиком, нацеливающие последовательности, метки для очистки пептидов или вспомогательные гены, или любую их комбинацию.
[0104] Нуклеиновая кислота или молекула нуклеиновой кислоты может содержать одну или более последовательностей, кодирующих различные пептиды, полипептиды или белки. Такие одна или более последовательностей могут быть соединены в одной и той же нуклеиновой кислоте или молекуле нуклеиновой кислоты рядом друг с другом или с дополнительными нуклеиновыми кислотами между ними, например, линкерами, повторами или сайтами ферментов рестрикции, или любой другой последовательностью, длина которой составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200 или 300 оснований, или любую длину в диапазоне, заданном любыми двумя из указанных выше длин. Термин «по ходу транскрипции» на нуклеиновой кислоте в данной заявке относится к последовательности, которая расположена после 3'-конца предыдущей последовательности, на цепи, содержащей кодирующую последовательность (смысловой цепи), если нуклеиновая кислота двухцепочечная. Термин «против хода транскрипции» на нуклеиновой кислоте в данной заявке относится к последовательности, которая расположена перед 5'-концом следующей последовательности на цепи, содержащей кодирующую последовательность (смысловой цепи), если нуклеиновая кислота двухцепочечная. Термин «сгруппированные» на нуклеиновой кислоте в данной заявке относится к двум или более последовательностям, которые находятся вблизи либо непосредственно, либо с дополнительными нуклеиновыми кислотами между ними, например, линкерами, повторами или сайтами ферментов рестрикции, или любой другой последовательностью, длина которой составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200 или 300 оснований, или любую длину в диапазоне, заданном любыми двумя из указанных выше длин, но, как правило, не с последовательностью между ними, которая кодирует функционирующий или каталитический полипептид, белок или домен белка.
[0105] Термин «кодон-оптимизированный», относящийся к нуклеиновой кислоте, в данной заявке относится к замене кодонов нуклеиновой кислоты, чтобы усилить или максимизировать трансляцию в хозяине конкретного вида без изменения полипептидной последовательности, на основании видоспецифичных предпочтений к использованию кодонов и относительной доступности каждой аминоацил-тРНК в цитоплазме целевой клетки. Оптимизация кодонов и методики осуществления такой оптимизации известны в данной области техники. Программы, содержащие алгоритмы для оптимизации кодонов, известны специалистам в данной области техники. Программы могут включать, например, алгоритмы OptimumGene, GeneGPS® и т.д. Кроме того, синтетические кодон-оптимизированные последовательности можно получить из коммерческих источников, например, от Integrated DNA Technologies и других коммерчески доступных сервисов секвенирования ДНК. Для специалиста в данной области понятно, что уровни экспрессии генов зависят от множества факторов, таких как последовательности промотора и регуляторные элементы. Обнаружили, что у большинства бактерий виды тРНК узнают небольшие подгруппы кодонов, что приводит к трансляционной селекции, которая может послужить важным ограничением экспрессии белка. В данном аспекте, множество синтетических генов можно разработать таким образом, чтобы повысить уровень экспрессии белка с них.
[0106] Нуклеиновые кислоты, описанные в данной заявке, содержат нуклеооснования. Первичные, канонические, природные или немодифицированные основания представляют собой аденин, цитозин, гуанин, тимин и урацил. Другие нуклеооснования включают, но не ограничены перечисленными: пурины, пиримидины, модифицированные нуклеооснования, 5-метилцитозин, псевдоуридин, дигидроуридин, инозин, 7-метилгуанозин, гипоксантин, ксантин, 5,6-дигидроурацил, 5-гидроксиметилцитозин, 5-бромурацил, изогуанин, изоцитозин, аминоаллил-основания, меченые красителем основания, флуоресцентные основания или меченые биотином основания.
[0107] Термины «пептид», «полипептид» и «белок» в данной заявке относятся к макромолекулам, состоящим из аминокислот, связанных пептидными связями. Множество функций пептидов, полипептидов и белков известно в данной области, и они включают, но не ограничены функциями ферментов, структурной, транспортной, защитной функциями, функциями гормонов или сигнальными функциями. Пептиды, полипептиды и белки часто, но не всегда, получают биологическим способом с помощью рибосомного комплекса с применением матрицы нуклеиновой кислоты, хотя способы химического синтеза также доступны. Путем манипуляций над матрицей нуклеиновой кислоты, пептидом, полипептидом и белком можно осуществить мутации, такие как замены, делеции, укорачивания, добавления, дупликации или слияния более чем одного пептида, полипептида или белка. Такие слияния более чем одного пептида, полипептида или белка можно осуществить в одной и той же молекуле рядом друг с другом или с дополнительными аминокислотами между ними, например, линкерами, повторами, эпитопами или метками, или любой другой последовательностью, длина которой составляет 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 150, 200 или 300 оснований, или любую длину в диапазоне, заданном любыми двумя из указанных выше длин.
[0108] В некоторых вариантах реализации последовательности нуклеиновых кислот или пептидов, представленные в данной заявке и используемые в примерах, функциональны в различных биологических системах, включая, но не ограничиваясь клетками человека, мыши, кролика, Е. coli, дрожжей и млекопитающих. В других вариантах реализации последовательности нуклеиновых кислот или пептидов, подобные на 0%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, или 100%, или любой процент в пределах диапазона, заданного любыми двумя из указанных выше процентов подобия, последовательностям нуклеиновых кислот или пептидов, представленным в данной заявке и используемым в примерах, также можно применять, не влияя на функцию последовательностей в биологических системах. В данной заявке термин «подобие» относится к последовательности нуклеиновой кислоты или пептида, имеющей такой же общий порядок нуклеотидов или аминокислот, соответственно, как и в опорной последовательности нуклеиновой кислоты или пептида, с определенными изменениями, такими как замены, делеции, повторы или вставки внутри последовательности. В некоторых вариантах реализации две последовательности нуклеиновых кислот, подобные настолько мало как на 0%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%, могут кодировать такой же полипептид благодаря содержанию различных кодонов, которые кодируют одну и ту же аминокислоту во время трансляции.
[0109] Термин «экспрессирован рекомбинантным способом» в данной заявке относится к получению белков в оптимизированных или приспособленных биологических системах. Эти системы имеют преимущества над экспрессией белка в природном хозяине, включая, но не ограничиваясь высокой экспрессией (сверхэкспрессией), легкостью очистки, легкостью трансформации, способностью к индуцированию, низкой стоимостью или стабильностью белка. В некоторых вариантах реализации белки экспрессируют в системах экспрессии в млекопитающем, бактериях, дрожжах, насекомых или в бесклеточных системах экспрессии рекомбинантных белков. У каждой системы есть свои преимущества или недостатки. Например, бактериальные системы экспрессии сильно оптимизированы для сверхэкспрессии, но могут вызывать неправильное сворачивание или агрегацию полученного белка, дрожжевые системы пригодны, когда требуются посттрансляционные модификации, и системы экспрессии в насекомом и млекопитающем пригодны для правильного сплайсинга РНК, который происходит в организмах более высокого уровня. В некоторых вариантах реализации Δ-7, Δ-8 и другие рекомбинантные полипептиды получают и очищают из клеток млекопитающего, человека, первичных, иммортал изо ванных клеток, клеток рака, стволовых клеток, фибробластов, клеток эмбриональной почки человека (HEK) 293, клеток яичника китайского хомячка (СНО), бактериальных клеток, клеток Escherichia coli, дрожжей, Saccharomyces cerevisiae, Pichia pastoris, насекомого, Spodoptera frugiperda SJ9 или S. frugiperda Sf21l, или из бесклеточной системы. В некоторых вариантах реализации гены, векторы или конструкции для экспрессии доставляют в рекомбинантные системы экспрессии в виде плазмид, бактериофагов, вирусов, аденоассоциированных вирусов (AAV), бакуловируса, космид, фосмид, фагмид, ВАС, YAC или НАС. Более подробное обсуждение рекомбинантных систем экспрессии см. в Gomes et al. «An Overview of Heterologous Expression Host Systems for the Production of Recombinant Proteins» ((2016) Adv. Anim. Vet. Sci. 4(7):346-356), которая настоящим явно полностью включена в данную заявку посредством ссылки.
[0110] Термин «HDAg» в данной заявке относится к гену или белку антигена гепатита D. Существуют малая (24 кДа) и большая (27 кДа, 213 аминокислот, исключая инициирующий кодон-метионин) изоформы HDAg, и они транслируются с одной открытой рамки считывания в геноме HDV. Дезаминирование аденозина в стоп-кодоне UAG в кодоне 196 кодирующей последовательности позволяет трансляции продолжаться, в результате чего образуется большая изоформа. Если явно не указано иное, варианты реализации, описанные в данной заявке, включают большую изоформу HDAg. В некоторых вариантах реализации последовательности HDAg содержат по меньшей мере одну из четырех различных последовательностей штамма HDAg: «HDAg генотипа 1 А», «HDAg генотипа 1 В», «HDAg генотипа 2 А» или «HDAg генотипа 2 В». В некоторых вариантах реализации последовательность нуклеиновой кислоты, кодирующая по меньшей мере один полипептид HDAg, содержит последовательность нуклеиновой кислоты HDAg генотипа 1 A (SEQ ID NO: 1), HDAg генотипа 1 В (SEQ ID NO: 2), HDAg генотипа 2 A (SEQ ID NO: 3) или HDAg генотипа 2 В (SEQ ID NO: 4). В некоторых вариантах реализации полипептид, содержащий по меньшей мере один полипептид HDAg, содержит полипептидную последовательность HDAg генотипа 1 A (SEQ ID NO: 5), HDAg генотипа 1 В (SEQ ID NO: 6), HDAg генотипа 2 A (SEQ ID NO: 7) или HDAg генотипа 2 В (SEQ ID NO: 8).
[0111] Термин «PreS1» в данной заявке относится к фрагменту N-концевого домена на большом поверхностном антигене HBV (HBsAg). Фрагмент PreS1 длиной 47 аминокислот из N-концевого домена длиной 108-119 аминокислот из большого HBsAg эффективно вызывает иммунный ответ и индуцирует высокий титр антител против PreS1/против HBV в моделях у млекопитающих. В некоторых вариантах реализации последовательности PreS1 содержат по меньшей мере одну из двух различных консенсусных последовательностей PreS1: «PreS1 А» и/или «PreS1 В». В некоторых вариантах реализации последовательность нуклеиновой кислоты, кодирующая по меньшей мере один полипептид PreS1, содержит последовательность нуклеиновой кислоты PreS1A (SEQ ID NO: 9) или PreS1 В (SEQ ID NO: 10). В некоторых вариантах реализации полипептид, содержащий по меньшей мере один полипептид PreS1, содержит полипептидную последовательность PreS1 A (SEQ ID NO: 11) или PreS1 В (SEQ ID NO: 12).
[0112] В некоторых вариантах реализации консенсусные последовательности PreS1А и PreS1 В HBV получают или выводят из подобия последовательностей PreS1 в известных генотипах HBV. Существует десять известных или распространенных генотипов HBV (генотипы А, В, С, D, Е, F, G, Н, I и J), имеющих до или приблизительно 8% различий нуклеотидов в геномной последовательности. Среди них существуют дополнительные субгенотипы, у которых выявляют до или приблизительно 4%-8% отличий нуклеотидов в геномной последовательности. Субгенотипы HBV включают, но не ограничены перечисленными: Al, А2, A3, А4, А5, А6, А7, В2, ВЗ, В4, В5, В6, В7, В9, C1, С2, С3, С4, С5, С6, С7, С8, С9, С10, D1, D2, D3, D4, D5, D6, D7, Fl, F2, F2a, F3 или F4. Более подробное обсуждение генотипов HBV, см. в Sunbul «Hepatitis В virus genotypes: Global distribution and clinical importance)) ((2014) World. J. Gastroenterology. 20(18): 5427-5434, которая настоящим явно полностью включена в данную заявку посредством ссылки.
[0113] Термины «сайт аутокаталитического расщепления пептида» или «пептид 2А» в данной заявке относятся к последовательности пептида, в которой происходит расщепление пептидной связи между двумя входящими в его состав аминокислотами, приводящее к разделению двух белков, которые фланкируют последовательность. Полагают, что такое расщепление является результатом «проскока» рибосомы через образованную пептидную связь между С-концевым пролином и глицином в последовательности пептида 2А. Четыре последовательности сайта аутокаталитического расщепления пептида, идентифицированные на данный момент, находят фактическое применение в биомедицинских исследованиях: 2А вируса ящура (F2A); 2А вируса ринита лошадей A (ERAV) (Е2А); 2А тешовируса-1 свиньи (Р2А) и 2А вируса Thosea asigna (Т2А). В некоторых вариантах реализации используют последовательности нуклеиновой кислоты (SEQ ID NO: 13) и полипептида (SEQ ID NO: 14) сайта аутокаталитического расщепления пептида Р2А.
[0114] Термин «HBeAg» в данной заявке относится к белку антигена HBV, находящегося между нуклеокапсидным кором и липидной оболочкой вируса. HBeAg, продуцированный в хозяине, секретируется в сыворотку крови и является надежным маркером активной инфекции HBV. Количественный анализ секреции HBeAg in vitro в модели культуры клеток можно использовать для оценки действия биологических или фармацевтических соединений или композиций на инфекционность HBV.
[0115] Термин «вспомогательное вещество» имеет обычное значение, которое понятно в свете настоящего описания, и относится к другим веществам, соединениям или материалам, находящимся в иммуногенной композиции или вакцине. Вспомогательные вещества с желательными свойствами включают, но не ограничены перечисленными: консерванты, адъюванты, стабилизаторы, растворители, буферы, разбавители, солюбилизирующие агенты, детергенты, поверхностно-активные вещества, хелатирующие агенты, антиоксиданты, спирты, кетоны, альдегиды, этилендиаминтетрауксусную кислоту (ЭДТА), лимонную кислоту, соли, хлорид натрия, бикарбонат натрия, фосфат натрия, борат натрия, цитрат натрия, хлорид калия, фосфат калия, сульфат магния, сахара, декстрозу, фруктозу, маннозу, лактозу, галактозу, сахарозу, сорбит, целлюлозу, сыворотку, аминокислоты, полисорбат 20, полисорбат 80, дезоксихолат натрия, тауродезоксихолат натрия, стеарат магния, этоксилат октилфенола, бензетония хлорид, тимеросал, желатин, сложные эфиры, простые эфиры, 2-феноксиэтанол, мочевину или витамины, или любую их комбинацию. Некоторые вспомогательные вещества могут быть в остаточных количествах или быть примесями, оставшимися от процесса производства иммуногенной композиции или вакцины, включая, но не ограничиваясь перечисленными: сыворотку, альбумин, овальбумин, антибиотики, инактивирующие агенты, формальдегид, глутаральдегид, р-пропиолактон, желатин, обломки клеток, нуклеиновые кислоты, пептиды, аминокислоты или компоненты ростовой среды, или любую их комбинацию. Количество вспомогательного вещества может находиться в иммуногенной композиции или вакцине на уровне процентов: 0%, 0,1%, 0,2%, 0,3%, 0,4%, 0,5%, 0,6%, 0,7%, 0,8%, 0,9%, 1%, 2%, 3%, 4%, 5%, 6%, 7%, 8%, 9%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 100% по массе, или любого процента по массе в диапазоне, заданном любыми двумя из указанных выше значений.
[0116] Термин «адъювант» в данной заявке относится к веществу, соединению или материалу, который стимулирует иммунный ответ и повышение эффективности защитного иммунитета и который вводят в сочетании с иммуногенным антигеном, эпитопом или композицией. Адъюванты служат для улучшения иммунных ответов, позволяя непрерывное высвобождение антигена, повышающую регуляцию цитокинов и хемокинов, привлечение клеток в место введения, повышенное поглощение антигена и его представление в антигенпредставляющих клетках или активацию антигенпредставляющих клеток и инфламмасом. Широко применяемые адъюванты включают, но не ограничены перечисленными: квасцы, соли алюминия, сульфат алюминия, гидроксид алюминия, фосфат алюминия, гидроксифосфат кальция, алюмосульфат калия, масла, минеральное масло, парафиновое масло, эмульсии типа масло в воде, детергенты, MF59®, сквален, AS03, α-токоферол, полисорбат 80, AS04, монофосфорил-липид А, виросомы, нуклеиновые кислоты, полиинозиновая:полицитидиловая кислота, сапонины, QS-21, белки, флагеллин, цитокины, хемокины, IL-1, IL-2, IL-12, IL-15, IL-21, имидазохинолины, олигонуклеотиды CpG, липиды, фосфолипиды, диолеоил-фосфатидилхолин (DOPC), димиколят трегалозы, пептид о гликаны, экстракты бактерий, липополисахариды или адъювант Фрейнда, или любую их комбинацию.
[0117] Термины «примирование» и «стимулирование» в данной заявке относятся к отдельным иммуногенным композициям, применяемым в гетерологичном подходе иммунизации путем примирования-стимулирования. Иммунизациям или вакцинам обычно требуется более чем одно введение иммуногенной композиции, чтобы вызвать эффективный иммунитет к целевому патогену у хозяина. По сравнению с этим гомологичным подходом, в котором для всех введений предоставляется одна и та же композиция, проведение гетерологичного примирования-стимулирования может более эффективно создавать сильный иммунитет с большими уровнями антител и улучшенным клиренсом или устойчивостью к некоторым патогенам, таким как HBV или HDV. При проведении гетерологичного примирования-стимулирования сначала предоставляют по меньшей мере одну примирующую дозу, содержащую один тип иммуногенной композиции. После предоставления указанной по меньшей мере одной примирующей дозы затем предоставляют по меньшей мере одну стимулирующую дозу, содержащую другой тип иммуногенной композиции. Введение по меньшей мере одной стимулирующей дозы осуществляют по меньшей мере через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель после введения по меньшей мере одной примирующей дозы или в пределах диапазона времени, заданного любыми двумя из указанных выше временных точек, например, в пределах 1-48 дней или 1-48 недель. В некоторых вариантах реализации примирующая доза содержит нуклеиновую кислоту (например, ДНК или РНК), которая кодирует один или более антигенов или эпитопов, и стимулирующая доза содержит полипептид, который содержит один или более антигенов или эпитопов. В хозяине примирующая нуклеиновая кислота транслируется in vivo, чтобы вызвать иммунную реакцию, и вызывает больший ответ против последующего стимулирования полипептидом. В некоторых вариантах реализации примирующая нуклеиновая кислота содержит последовательности, которые кодируют по меньшей мере один полипептид HDAg, по меньшей мере один пептид PreS1 и по меньшей мере один сайт аутокаталитического расщепления пептида. В некоторых вариантах реализации стимулирующий полипептид содержит по меньшей мере один полипептид HDAg и по меньшей мере один полипептид PreS1.
[0118] В некоторых вариантах реализации введение примирующей нуклеиновой кислоты и стимулирующего полипептида, содержащих компоненты HBV и HDV, экспериментальному организму приводит к большему титру антител против HDAg, против PreS1, против HBV или против HDV при отношении, составляющем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 50, 100, 150, 200, 300, 400, 500, 600, 700, 800, 900, 1000, 5000, 10000, 100000 или 1000000, или любом отношении в пределах диапазона, заданного любыми двумя из указанных выше отношений, к таковому для иммунизированного только нуклеиновой кислотой или только полипептидом или не иммунизированного контрольного организма, что анализировали количественно с помощью методик, известных в данной области техники, таких как ELISA. В некоторых вариантах реализации введение примирующей нуклеиновой кислоты и стимулирующего полипептида, содержащих компоненты HBV и HDV, экспериментальному организму приводит к тому, что сыворотка нейтрализует инфекционность HBV или HDV in vitro более эффективно и снижает частоту инфицирования до отношения, составляющего 0,00001, 0,00005, 0,0001, 0,0005, 0,001, 0,005, 0,01, 0,02, 0,03, 0,04, 0,05, 0,06, 0,07, 0,08, 0,09, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9 или 1,0, или любого отношения в пределах диапазона, заданного любыми двумя из указанных выше отношений, по сравнению с сыворотками из иммунизированного только нуклеиновой кислотой или только полипептидом или неиммунизированного контрольного организма. В некоторых вариантах реализации введение примирующей нуклеиновой кислоты и стимулирующего полипептида, содержащих компоненты HBV и HDV, экспериментальному организму приводит к большему количеству положительных по интерферону гамма (IFNγ) клеток (например, Т-клеток) при отношении, составляющем 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 200, 250, 300, 350, 400, 450, 500, 550, 600, 650, 700, 750, 800, 850, 900, 950, 1000, 5000 или 10000, или любом отношении в пределах диапазона, заданного любыми двумя из указанных выше отношений, по сравнению с иммунизированным только нуклеиновой кислотой или только полипептидом или неиммунизированным контрольным организмом.
[0119] В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов вводят с адъювантом. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов вводят энтерально, перорально, интраназально, парентерально, подкожно, внутримышечно, внутрикожно или внутривенно, или любой комбинацией перечисленных путей. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов вводят в сочетании с соединением для противовирусной терапии, у которого есть известное действие против HBV или HDV, включая, но не ограничиваясь перечисленными соединениями: энтекавир, тенофовир, ламивудин, адефовир, телбивудин, эмтрицитабин, интерферон-α, пегилированный интерферон-α или интерферон альфа-2b, или любую их комбинацию.
[0120] Термины «электропорация in vivo», «электропорация» и «ЭП» в данной заявке относятся к доставке генов, нуклеиновых кислот, ДНК, РНК, белков или векторов в клетки живых тканей или организмов с помощью электрических токов, применяя методики, известные в данной области техники. Электропорацию можно использовать в качестве альтернативы другим способам переноса генов, таким как вирусы (трансдукция), липофекция, генная пушка (биолистика), микроинъекция, слияние везикул или химическая трансформация. Электропорация ограничивает риск иммуногенности и неблагоприятного встраивания или мутагенеза генома клетки. ДНК-векторы, такие как плазмиды, способны проникнуть в ядро клетки, позволяя транскрипцию и трансляцию составляющих их генов. В некоторых вариантах реализации гены, нуклеиновые кислоты, ДНК, РНК, белки или векторы вводят в целевую ткань или целевой организм путем подкожной, внутримышечной или внутрикожной инъекции. Электропоратор затем доставляет короткие электрические импульсы посредством электродов, размещенных внутри или вблизи от введенного путем инъекции образца. В данной заявке термин «вм/ЭП» относится к электропорации in vivo образца, доставленного внутримышечно («вм»).
[0121] Термин «uPA+/+-SCID» в данной заявке относится к модели иммунодефицита у мышей, используемой для исследования заболеваний печени, включая инфекции вирусами гепатита. Эти мыши гомозиготны по Prkdc^, что вызывает недостаточность функциональных Т- и В-лимфоцитов. Сверхэкспрессия активатора плазминогена урокиназного типа (иРА) также вызывает тяжелую цитотоксичность печени и печеночную недостаточность в процессе развития. Последующая трансплантация и прививка ткани печени человека этим мышам приводит к получению модели, идеальной для исследования болезней печени у людей. Дополнительные сведения о мышах uPA+/+-SCID см. в Meuleman и др. «The human liver-uPA-SCID mouse: A model for the evaluation of antiviral compounds against HBV and HCV» ((2008) Antiviral Research 80(3): 231-238), которая настоящим явно полностью включена в данную заявку посредством ссылки.
[0122] Термин «% по массе» или «% масса/масса» в данной заявке имеет обычное значение, которое понятно в свете настоящего описания, и относится к проценту, выраженному в виде массы ингредиента или агента от общей массы композиции, умноженной на 100. Термин «% по объему» или «% об/об» в данной заявке имеет обычное значение, которое понятно в свете настоящего описания, и относится к проценту, выраженному в виде объема жидкости соединения, вещества, ингредиента или агента от общего объема жидкости композиции, умноженного на 100.
[0123] Настоящее изобретение описано в данной заявке в общих чертах с использованием утвердительной терминологии для описания множества вариантов реализации. В объем настоящего изобретения также входят варианты реализации, в которых предмет рассмотрения исключен, полностью или частично, например, вещества или материалы, этапы способа и условия, протоколы или процедуры.
Иммуногенные композиции и комбинации продуктов.
[0124] В данной заявке предложены иммуногенные композиции или комбинации продуктов. В некоторых вариантах реализации указанные иммуногенные композиции или комбинации продуктов предназначены для индукции иммуногенного ответа на конкретный антиген. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов содержат (а) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и (b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4, или любую их комбинацию. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе. В некоторых вариантах реализации нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и что последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от последовательности нуклеиновой кислоты HDAg. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов дополнительно содержат по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2А тешовируса свиней-1 (Р2А), 2А вируса ящура (F2A), 2А вируса ринита лошадей A (ERAV) (Е2А) и 2А вируса Thosea asigna (Т2А), и при этом каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ ID NO: 13. В некоторых вариантах реализации нуклеиновая кислота кодон-оптимизирована для экспрессии у человека. В некоторых вариантах реализации нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35-36. В некоторых вариантах реализации нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 18 или SEQ ID NO: 35-36. В некоторых вариантах реализации по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию. В некоторых вариантах реализации по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе. В некоторых вариантах реализации по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от по меньшей мере одной последовательности полипептида HDAg. В некоторых вариантах реализации полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37. В некоторых вариантах реализации полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37. В некоторых вариантах реализации полипептид экспрессирован рекомбинантным способом. В некоторых вариантах реализации полипептид экспрессирован рекомбинантным способом в системе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов дополнительно содержат адъювант.В некоторых вариантах реализации адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию. В некоторых вариантах реализации нуклеиновая кислота содержит ДНК. В некоторых вариантах реализации нуклеиновая кислота предоставлена в рекомбинантном векторе.
[0125] Также в данной заявке предложены способы индуцирования иммунного ответа у субъекта с применением иммуногенной композиции или комбинации продуктов. В некоторых вариантах реализации иммуногенная композиция или комбинация продуктов представляет собой любую из иммуногенных композиций или комбинаций продуктов, описанных в данной заявке. В некоторых вариантах реализации указанные способы включают введение указанному субъекту по меньшей мере одной примирующей дозы, содержащей нуклеиновую кислоту; и введение указанному субъекту по меньшей мере одной стимулирующей дозы, содержащей полипептид. В некоторых вариантах реализации указанная по меньшей мере одна стимулирующая доза дополнительно содержит адъювант.В некоторых вариантах реализации адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию. В некоторых вариантах реализации по меньшей мере одну стимулирующую дозу вводят по меньшей мере через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель после введения по меньшей мере одной примирующей дозы или в пределах диапазона времени, заданного любыми двумя из указанных выше временных точек, например, в пределах 1-48 дней или 1-48 недель. В некоторых вариантах реализации введение осуществляют энтерально, перорально, интраназально, парентерально, подкожно, внутримышечно, внутрикожно или внутривенно, или любой комбинацией перечисленных путей. В некоторых вариантах реализации введение осуществляют в сочетании с противовирусной терапией. В некоторых вариантах реализации противовирусная терапия включает введение энтекавира, тенофовира, ламивудина, адефовира, телбивудина, эмтрицитабина, интерферона-а, пегилированного интерферона-а или интерферона альфа-2b, или любой их комбинации.
[0126] Также в данной заявке предложены иммуногенные композиции или комбинации продуктов для применения для лечения или ингибирования гепатита В или гепатита D. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов представляют собой любую из иммуногенных композиций или комбинаций продуктов, описанных в данной заявке. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов содержат (а) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и (b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе. В некоторых вариантах реализации нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и что последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от последовательности нуклеиновой кислоты HDAg. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов дополнительно содержат по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2А тешовируса свиней-1 (Р2А), 2А вируса ящура (F2A), 2А вируса ринита лошадей A (ERAV) (Е2А) и 2А вируса Thosea asigna (Т2А), и при этом каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце. В некоторых вариантах реализации указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ ID NO: 13. В некоторых вариантах реализации нуклеиновая кислота кодон-оптимизирована для экспрессии у человека. В некоторых вариантах реализации нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35-36. В некоторых вариантах реализации нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 18, или SEQ ID NO: 35-36. В некоторых вариантах реализации по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию. В некоторых вариантах реализации по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе. В некоторых вариантах реализации по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от по меньшей мере одной последовательности полипептида HDAg. В некоторых вариантах реализации полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37. В некоторых вариантах реализации полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37. В некоторых вариантах реализации полипептид экспрессирован рекомбинантным способом. В некоторых вариантах реализации полипептид экспрессирован рекомбинантным способом в системе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе. В некоторых вариантах реализации иммуногенные композиции или комбинации продуктов дополнительно содержат адъювант.В некоторых вариантах реализации адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию. В некоторых вариантах реализации нуклеиновая кислота содержит ДНК. В некоторых вариантах реализации нуклеиновая кислота предоставлена в рекомбинантном векторе.
ПРИМЕРЫ
[0127] Некоторые аспекты вариантов реализации, обсуждаемые выше, описаны более подробно в следующих примерах, которые ни коим образом не предназначены для ограничения объема настоящего изобретения. Специалистам в данной области будет понятно, что множество других вариантов реализации также входят в объем настоящего изобретения, описанного в данной заявке выше и в формуле изобретения.
Пример 1. Методика.
Животные.
[0128] Самок мышей C57BL/6 (Н-2b) получали от Charles River Laboratories.
Трансгенных по человеческому лейкоцитарному антигену А2 (HLA-A2) мышей HHD выводили самостоятельно. Все мыши были в возрасте 8-10 недель в начале экспериментов, и их содержали при стандартных условиях. Получали и содержали мышеи uPA+/+-SCID с гуманизированной печенью. Новозеландских белых кроликов приобретали у коммерческих поставщиков.
Плазмиды ДНК.
[0129] Плазмиды, кодирующие генотипы 1 и 2 L-HDAg и домен PreS1 (АК 2 -48) HBsAg, использовали в этом исследовании в виде слитых конструкций, необязательно расщепляемых посредством Р2А, состоящих из различных комбинаций последовательностей HDAg/PreS1. Последовательности HDAg генотипов 1 и 2 получали из четырех различных клинических изолятов; US-2 и СВ, и 7/18/83 и TW2476, соответственно. Все гены клонировали в остов pVAXl (Invitrogen, Карлсбад, Калифорния), используя сайты рестрикции EcoR I и HindIII. Плазмиды наращивали в клетках ТОР10 E.coli (Life Technologies, Карлсбад, Калифорния) и очищали для инъекции in vivo, применяя набор для очистки ДНК Qiagen Endofree (Qiagen GmbH), следуя инструкциям производителя. Правильность размера гена подтверждали с помощью расщепления ферментами рестрикции, применяя EcoR I и HindIII (Fast Digest, Thermo Fisher Scientific).
Вестерн-блоттинг.
[0130] Вестерн-блоттинг проводили по существу как широко известно в данной области техники. Клетки Hela трансфицировали каждой из плазмидных ДНК pVAXl Dl-D10 и pVAX1 с репортерным геном GFP в качестве контроля, применяя реагент для трансфекции липофектамин® 3000 (Thermo Fisher Scientific). Для детектирования белка использовали сыворотку из вакцинированных D4 кроликов, разбавленную 1:1000 (первичное антитело), и антитело козы против иммуноглобулинов кролика-HRP, 0,25 г/л (DAKO), разбавленное 1:4000 (вторичное антитело). Для детектирования хемилюминесценции применяли субстрат Pierce™ ECL Plus Western Blotting Substrate, и изображения накапливали с помощью системы Gel Doc XR+ (Biorad).
Пептиды.
[0131] Всего 168 15-мерных пептидов HDAg с перекрыванием 10 АК приобретали у Sigma-Aldrich (Сент-Луис, Миссури). Указанные 168 пептидов разделяли на 8 пулов, каждый из которых содержал 20 или 21 пептид. Четыре пула соответствовали генотипу 1 (пул 11-21, пул 222-42, пул 343-63 и пул 464-84) и четыре пула соответствовали генотипу 2 (пул 11-21, пул 222-42, пул 343-63 и пул 464-84) Для последовательностей А, В, С и D, причем каждая последовательность относится к каждому клиническому изоляту.
[0132] Две консенсусные последовательности PreS1 HBsAg (PreS1A и PreS1B), состоящие из 47 АК, и 20-мерные пептиды PreS1 с перекрыванием 10 АК для (под-)генотипов HBV A1, А2, В, В2, С, Dl, Е1 и F, приобретали в Sigma-Aldrich (Сент-Луис, Миссури). Все пептиды прошли контроль качества (КК) (Sigma-Aldrich PEPscreen® Directory) и имели чистоту >70%. Пептиды овальбумина OVA 257-264 CTL (SIINFEKL (SEQ ID NO: 38)) и OVA 323-339 Th (ISQAVHAAHAEINEAGR (SEQ ID NO: 39)) использовали в качестве отрицательных контролей пептидов, тогда как конканавалин А (КонА), приобретенный в Sigma Aldrich (Сент-Луис, Миссури), использовали в качестве положительного контроля в конечной концентрации, равной 0,5 мкг/мкл.
Протоколы иммунизации для оценки иммуногенности плазмид HBV/HDV у мышей и кроликов.
[0133] Для оценки иммуногенности конструкций in vivo, мышей и кроликов иммунизировали по существу как описано, стимулировали с интервалами в один месяц и умерщвляли через две недели для сбора селезенок и крови. Вкратце, самок мышей C57BL/6 (пять на группу) иммунизировали внутримышечно (в/м) в переднюю болыпеберцовую мышцу (ТА) 50 мкг плазмидной ДНК в объеме 50 мкл в стерильном ФБР с помощью обычной инъекции иглой (27G), с последующей электропорацией (ЭП) in vivo с применением устройства Cliniporator2 (IGEA, Карпи, Италия). Во время электропорации in vivo использовали паттерн импульса 1 мс 600 В/см с последующим импульсом 400 мс 60 В/см, чтобы способствовать лучшему поглощению ДНК. Перед инъекцией вакцины мышам давали анальгетик и держали их под анестезией изофлураном во время вакцинаций. Для исследований на кроликах, по два Новозеландских белых кролика на группу иммунизировали 300 мкг вакцин ДНК D3 и D4. Вакцины вводили путем в/м инъекции в 300 мкл стерильного ФБР в правую мышцу ТА, а затем проводили ЭП in vivo.
Детектирование продуцирующих IFNy Т-клеток с помощью анализа методом иммуноферментных пятен (ELISpot).
[0134] Через две недели после последней вакцинации, спленоциты из каждой иммунизированной группы мышей объединяли (по пять мышей/группу) и исследовали их способность индуцировать специфичные к HBV/HDV Т-клетки на основании секреции IFN-y после стимуляции пептидом в течение 48 ч, как известно в данной области техники, применяя доступный для приобретения набор для анализа ELISpot (Mabtech, Нака Странд, Швеция).
Детектирование антитела с помощью ELISA.
[0135] Детектирование IgG мыши и кролика против консенсуса PreS1 и перекрывающихся 20-мерных пептидов (10 мкг/мл) осуществляли, применяя протоколы, известные в данной области техники. Титры антител определяли как конечную точку титрования сывороток, при которой значение ОП на 405 нм по меньшей мере в два раза превышало ОП отрицательного контроля (сыворотки неиммунизированного или контрольного животного) при таком же разведении.
Анализ нейтрализации HBV в модели на мышах uPA-SCID с печенью человека.
[0136] HepG2-NTCP-A3 представляет собой прошедший селекцию клон клеток, происходящий из клетки HepG2, экспрессирующей NTCP человека, как описано ранее. Его культивировали в среде DMEM, дополненной 10% эмбриональной сывороткой крупного рогатого скота, 2 мМ L-глутамином, 50 Ед/мл пенициллина и 50 мкг/мл стрептомицина. Во время и после инокуляции в среду добавляли 2,5% ДМСО, чтобы улучшить инфицирование и репликацию HBV. Исходный раствор вируса HBV, применяемый для инфекции, получали из клеток HepAD38 путем преципитации ПЭГ, как описано. Собирали культуральную среду между 3 и 6 днем после инфекции и разбавляли 1:5 ФБР для количественного анализа HBeAg с помощью ELISA, применяя доступные для приобретения антитела.
Статистический анализ.
[0137] Результаты анализировали, применяя программное обеспечение GraphPad Prism V.5 и V.8 и Microsoft Excel V. 16.13.1.
Пример 2. Иммуногенные конструкции HBV и HDV.
[0138] Было показано, что применение рекомбинантных конструкций полипептидов HBV и HDV эффективно вызывало образование антител и иммунную защиту от указанных двух вирусов гепатита, например, в WO 2017/132332, которая настоящим явно полностью включена в данную заявку посредством ссылки. Эти рекомбинантные конструкции полипептидов собирали путем объединения HDAg, выбранного из четырех различных генотипов HDV (HDAg генотипа 1 A, HDAg генотипа 1 В, HDAg генотипа 2 А и HDAg генотипа 2 В), PreS1, выбранного из двух генотипов консенсусных последовательностей (PreS1А и PreS1B), и одного или более сайтов аутокаталитического расщепления пептида Р2А. Схематические изображения одиннадцати рекомбинантных конструкций показаны на фигурах 1А и 2, и соответствующие SEQ ID NO последовательностей ДНК и полипептидов, если возможно, представлены в таблице 1. С помощью вестерн-блоттинга подтвердили, что полипептиды правильно экспрессируются с рекомбинантных конструкций Δ-1-Δ-10 (Фигура 1В).
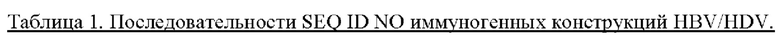
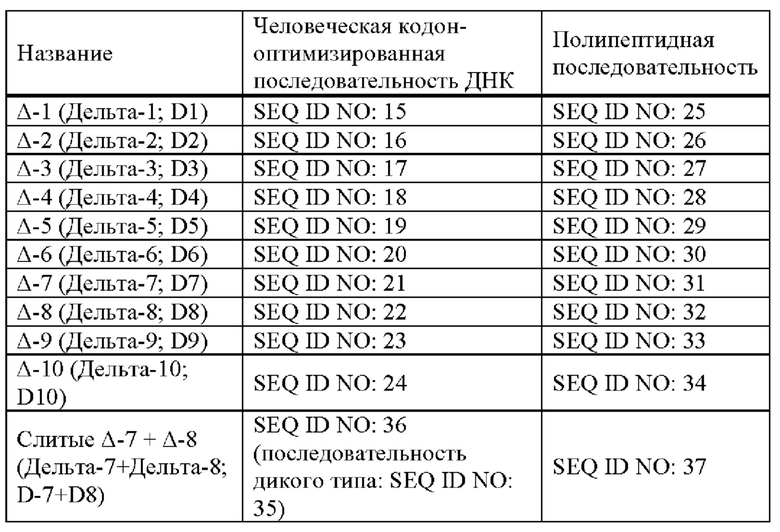
Пример 3. Композиции ДНК HBV/HDV вызывают иммуногенный ответ у мышей.
[0139] Хотя иммуногенные композиции и вакцины традиционно представляли собой либо целые организмы, либо антигенные белки, недавно было показано, что введение ДНК in vivo в живую ткань и последующая транскрипция и трансляция антигенных белков также высоко эффективно запускает иммунный ответ.Такие иммуногенные композиции ДНК исследовались как потенциальные кандидатные вакцины против различных заболеваний.
[0140] Через 2 недели после второго введения композиций конструкций ДНК, оценивали иммунитет мышей против антигенов HBV и HDV. Лейкоциты очищали из образцов цельной крови мышей и инкубировали с очищенными полипептидными антигенами, включая PreS1 A, PreS1 В, HDAg генотипов 1 А, 1 В, 2 А и 2 В. Клетки также инкубировали с конканавалином А («КонА») в качестве положительного контроля и двумя пептидами овальбумина («OVA Th» и «OVA CTL») в качестве отрицательных контролей. Частота встречаемости продуцирующих интерферон гамма (IFNγ) клеток в популяции в ответ на контакт с антигеном оценивали с помощью анализа методом иммуноферментных пятен (ELISpot). Вкратце, лейкоциты инкубировали с антигеном в лунках, покрытых антителами против IFNγ. Затем клетки удаляли и последовательно добавляли в лунки биотинилированные антитела против IFNγ, связанный перекрестными связями с щелочной фосфатазой стрептавидин и субстраты щелочной фосфатазы-колориметрические реагенты, с тщательной промывкой между указанными реагентами. Планшету затем позволяли высохнуть, и оставшиеся окрашенные пятна, которые соответствовали секретирующим IFNγ клеткам, подсчитывали с помощью микроскопии. Подсчитанные общие количества образующих пятна IFNγ клеток на 106 всех клеток в ответ на различные пептидные антигены для каждой из мышей показаны на фигурах 3А (Δ-1 и Δ-2), 3В (Δ-3 и Δ-4),3 (Δ-5 и Δ-6), 3D (Δ-7 и Δ-8) и 3Е (Δ-9 и Δ-10).
[0141] Исследовали реактивность антисывороток против консенсусных пептидов PreS1A и PreS1B (АК 2-48) и их перекрестную реактивность с (под-)типами HBV A1, А2, В, В2, С, D1, Е1 и F, используя пулы 20-мерных пептидов PreS1. Иммуногенные композиции, содержащие Δ-1, Δ-2, Δ-3, Δ-4, Δ-7 и Δ-8, приводили к сильной иммуногенности против обоих антигенов PreS1 HBV (Фигуры 4A-В). Δ-3 и Δ-4 вызывали титры антител >104 у мышей, затем следовали конструкции Δ-1, Δ-2, Δ-7 и Δ-8. Важно отметить, что антисыворотки из иммунизированных Δ-4 и Δ-7 мышей эффективно давали перекрестную реакцию со всеми исследованными типами HBV (Фигура 4С). Иммунный ответ на пептиды HDAg был более изменчивым, вероятно вследствие различий в последовательностях генотипов, но обычно был больше, чем для контрольных овальбуминов. Примечательно, что в группах, которым вводили Δ-3 и Δ-4, наблюдали небольшое снижение ответов Т-клеток на HDV, например, по сравнению с конструкциями, которые содержали только HDAg (Δ-5, Δ-6, Δ-9, Δ-10), что можно объяснить конкурированием за распознавание эпитопа при одновременном примировании специфичных к PreS1 Т-клеток. В целом, это показывает, что активная иммунизация способна индуцировать функциональные Т-клетки против антигенов PreS1 и HDAg, и приводит к предположению, что широко функциональная иммунотерапия должна содержать оба генотипа 1 и 2 HDV, чтобы гарантировать индукцию специфичных Т-клеток.
[0142] Сходные эксперименты проводили с рестриктированными по HLA-A2 Т-клетками, очищенными из трансгенных по HLA-A2 мышей HHD. ELISpot IFNγ для нормальных мышей C57BL/6 (Фигура 5А) и HLA-A2 HHD (Фигура 5В), которым вводили с помощью электропорации композицию, содержащую Δ-4, наряду с непримированными мышами HLA-A2 HHD в качестве контроля (Фигура 5С), подтвердил иммуногенность у трансгенных мышей, позволяя предложить эффективность композиций ДНК для лечения людей.
Пример 4. Композиции ДНК HBV/HDV вызывают иммуногенный ответ у кроликов.
[0143] Эксперименты, соответствующие таковым, описанным в Примере 3, также проводили с кроликами (Oryctolagus cuniculus). Новозеландским белым кроликам вводили путем внутримышечной инъекции солевой раствор, содержащий 900 мкг композиций ДНК, содержащих либо Δ-3, либо Δ-4, и проводили электропорацию. Дозы вводили на 0 и 4 неделях. После иммунизации титры антител против PreS1 в сыворотках кроликов наблюдали для обеих композиций ДНК, содержащих Δ-3 или Δ-4, причем Δ-4 оказался более эффективным (>103) (Фигуры 6A-В). Также исследовали перекрестную реактивность антисывороток кролика против (под-)типов HBV A1, А2, В, В2, С, D1, Е1 и F, используя пулы 20-мерных пептидов PreS1 (Фигура 6С). Точную специфичность антисывороток кролика против D4 определяли, используя отдельные 20-мерные пептиды PreS1 HBV типа A1, А2, В, В2, С, Dl, Е1 и F (Фигура 6D). Это позволило картировать эпитопы на PreS1, расположенные на участке 22-48 АК в генотипе D1, о чем свидетельствовала более высокая реактивность, за которой следовала более низкая реактивность по отношению к генотипам С, Е1 и А1. Это перекрывается с сайтом связывания NTCP и частично с ранее идентифицированными эпитопами, распознаваемыми нейтрализующими антителами.
[0144] В Таблице 2 сведены действия на иммунитет десяти иммуногенных композиций ДНК. Композиции ДНК, содержащие Д-4, приводили к наибольшему титру антител против PreS1/против HBV как у мышей, так и у кроликов, и их использовали для иммунизаций путем примирования/стимулирования в следующих Примерах. Для Д-4 также выявили наиболее широкую реактивность по отношению к различным генотипам HBV. «н/д» означает низкие или недетектируемые уровни активности антитела, «н/о» означает, что эксперимент не осуществляли.


Пример 5. Подход примирования ДНК/стимулирования белком с помощью конструкций HBV/HDV улучшает иммуногенный ответ у мышей.
[0145] Композиции ДНК, содержащие Δ-4 (SEQ ID NO: 18), и композиции полипептидов, содержащие Δ-7 (SEQ ID NO: 31) или Δ-8 (SEQ ID NO: 32), применяли в подходе иммунизации путем примирования ДНК/стимулирования белком, чтобы создать приобретенный иммунитет и вызвать продукцию антител против HBV и/или HDV in vivo (Фигура 2).
[0146] Мышей C57BL/6 иммунизировали (1) композицией ДНК, содержащей Δ-4 (3 последовательные дозы по 50 мкг ДНК), (2) композицией полипептида, содержащей Δ-7 (3 последовательные дозы по 20 мкг белка с квасцами в качестве адъюванта), или (3) композицией ДНК, содержащей Δ-4, а затем композицией полипептида, содержащей Δ-8 (2 дозы по 50 мкг ДНК, затем 2 дозы по 20 мкг белка с квасцами). После введения соединений исследовали продукцию IFNγ очищенными лейкоцитами в ответ на антигены HBV и HDV с помощью ELISpot (как описано в Примерах 1 и 2). У мышей, которых лечили (1), выявили ответ на антигены гепатита (Фигура 7А), сопоставимый с таковым, наблюдаемым в Примере 3 и на Фигуре 3В, но у мышей, которых лечили композициями для примирования ДНК/стимулирования белком (3), выявили сравнительно более сильный общий ответ иммунных клеток (Фигура 7С). Так как Δ-8 содержит последовательности полипептидов HDAg генотипа 2, проанализированный иммунный ответ особенно улучшился против этих антигенов (Фигура 7С, гтп 2-пул 5, 6, 7 и 8). Напротив, подход только с белком (2) с применением полипептидов Δ-7 не был способен вызвать столь же эффективный иммунный ответ к обоим антигенам HBV и HDV (Фигура 7В). Это демонстрирует, что указанный подход примирования ДНК/стимулирования белком может эффективно вызывать сильный иммуногенный ответ, больший, чем обычные композиции на основе белка или организма, на некоторые патогены, включая HBV и HDV.
[0147] Другие комбинации примирования ДНК/стимулирования белком также оценивали на мышах. Титры IgG против PreS1 у мышей измеряли после иммунизации (1) композицией только ДНК, содержащей Δ-4 («D4»), (2) композициями только белка, содержащими Δ-7 («D7-D7»), Δ-8 («D8-D8»), Δ-9 («D9-D9») или Δ-10 («D10-D10»), или (3) композициями ДНК-белка, содержащими ДНК Δ-4 с белком Δ-7 («D4-D7»), Δ-8 («D4-D8»), Δ-9 («D4-D9») или Δ-10 («D4-D10»). Композиции вводили три раза на 0, 4 и 8 неделях, с введением либо 50 мкг ДНК вм/ЭП, либо 20 мкг белка с квасцами в каждой дозе. Для композиций ДНК-белка (3), вводили 50 мкг ДНК вм/ЭП в качестве первой дозы на 0 неделе и вводили 20 мкг белка с квасцами в качестве второй и третьей дозы на 4 и 8 неделях. Титры IgG против PreS1 в сыворотках оценивали через 2 недели (Фигура 8А), 6 недель (Фигура 8В) и 10 недель (Фигура 8С) после введения первой дозы (т.е., через 2 недели после введения каждой дозы). Композиция для примирования ДНК/стимулирования белком D4-D7 приводила к более высоким титрам против PreS1 после завершения графика введения доз.
Пример 6. Подход примирования ДНК/стимулирования белком с помощью конструкций HBV/HDV улучшал иммуногенный ответ у кроликов.
[0148] Новозеландских белых кроликов иммунизировали (1) композицией только ДНК, содержащей Δ-4, (2) композицией только белка, содержащей Δ-4, или (3) композицией для примирования ДНК/стимулирования белком, содержащей ДНК Δ-4 и белок Δ-4. Композиции вводили четыре раза на 0, 4, 8 и 12 неделях, причем вводили либо 900 мкг ДНК вм/ЭП, либо 300 мкг белка с квасцами в каждой дозе. Для композиций ДНК-белка (3), 900 мкг ДНК вм/ЭП вводили в качестве первой дозы на 0 неделе, и 300 мкг белка с квасцами вводили в качестве второй, третьей и четвертой доз на 4, 8 и 12 неделях. Титры IgG против PreS1 в сыворотках оценивали на 0, 2, 10 и 14 неделях (т.е., через 2 недели после введения каждой дозы) (Фигура 9). Композиция примирования ДНК/стимулирования белком (3) не только приводила к большим общим титрам по сравнению с композициями только ДНК (1) и только белка (2), но и вызывала сильную продукцию антител более быстро, ко 2 неделе, по сравнению с композицией только белка.
Пример 7. Адоптивный перенос сывороток или очищенного IgG из иммунизированных животных защищал гуманизированных мышей от провокаций HBV и HDV.
[0149] Способность индуцированных D4 антител нейтрализовать инфекцию HBV in vivo определяли, применяя химерную модель на мышах uPA+/+-SCID с печенью человека, как описано. Общий IgG очищали из иммунизированных D4 и неиммунизированных кроликов и вводили путем инъекции мышам uPA+/+-SCID, которых репопулировали гепатоцитами человека за три дня до провокации HBV. Индуцированные D4 антитела IgG против PreS1 защищали или значительно отсрочивали пик виремии у всех получивших провокацию мышей (Фигура 10А). Из трех получивших провокацию мышей, одна была защищена (недели 1-3), тогда как у других двух выявили уровни HBV в сыворотке <104 МЕ/мл вплоть до ежемесячного скрининга, и они оставались ниже по сравнению с контролями вплоть до 8 недель последующего наблюдения. У всех контрольных мышей, которым вводили IgG из непримированного кролика, достигались уровни ДНК HBV в сыворотке, превышающие 108 МЕ/мл. Не наблюдали значимых различий между группами в отношении уровней в сыворотке аланинтрансферазы, аспарагинтрансферазы, щелочной фосфатазы или билирубина (Фигура 10В). В заключение, пассивная иммунизация специфичными к D4 антителами IgG против PreS1, которую проводили в виде разовой дозы, была способна предотвращать, или значительно отсрочивать инфицирование HBV in vivo у мышей, которых репопулировали гепатоцитами человека (Таблица 3). Важно отметить, что инокулят содержал высокие уровни субвирусных частиц SHBsAg, показывая, что эти антитела в действительности избегали блокирования посредством SHBsAg. Антитела против PreS1, присутствующие при инокуляции и в течение первых недель, явно блокировали инфекцию, или первые раунды инфекции, и ограничивали количество инфицированных гепатоцитов. Это ограничивало распространение вируса и отсрочивало развитие пика виремии.
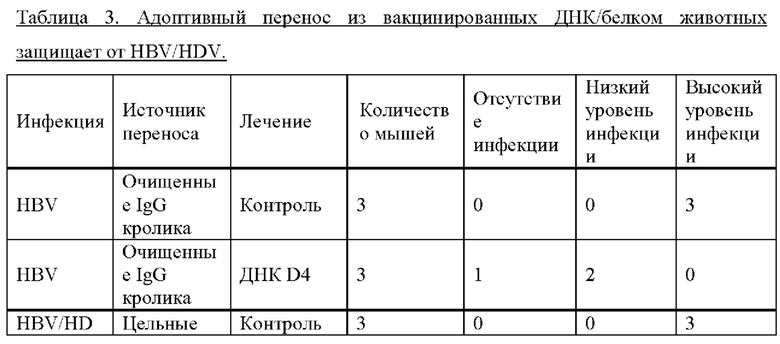
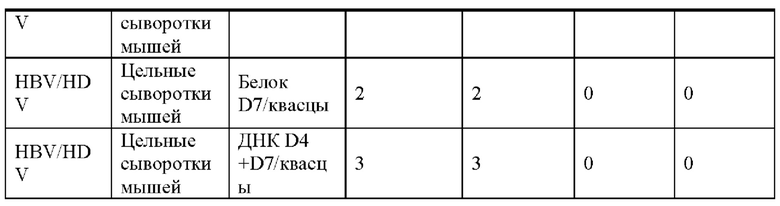
Пример 8. Провокация пептидными конструкциями HBV/HDV с различными адъювантами.
[0150] Смеси пептидов D-7 и D-8 оценивали, применяя различные адъюванты. Мышам C57BL/6J вводили 2 раундами по 20 мкг смеси пептидов D-7 и D-8 (10 мкг каждого из D-7 и D-8) на 0 неделе и 3 неделе (Фигура 11А). Образцы периферической крови брали на 2 неделе (между двумя раундами), чтобы определить конечные титры реактивности против HBV и HDV с помощью ELISA (Фигура 11А и 11В), и выделяли спленоциты для определения реактивности против HBV и HDV с помощью ELISpot (Фигура 11С-D) на 5 неделе. Пептидные композиции вводили подкожно с адъювантами QS-21, MF59 и квасцами. Непримированных мышей и мышей, которым вводили ДНК-плазмиду D-4 путем внутримышечной электропорации, использовали в качестве контролей. ELISpot IFNγ проводили, как описано выше, используя пулы пептидов HDAg, пептидов PreS1A и PreS1B, с пептидами OVA и конканавалином А в качестве контролей (Фигуры 11С-D). Для композиций, которые вводили с адъювантом QS-21, выявили повышенную реактивность против HDAg по сравнению с другими адъювантами. Исследовали по 5 мышей на группу.
Пример 9. Сравнение типичных конструкций ДНК и/или пептида HBV/HDV.
[0151] Проводили сравнение иммуногенности для 1) только смеси пептидов D-7 и D-8, 2) только слитого пептида D-7+D-8, 3) примирования ДНК D-4 и стимулирования смесью пептидов D-7 и D-8, используя только ДНК D-4 и условия без примирования в качестве контролей. Мышам вводили либо 20 мкг слитого белка D-7+D-8, либо 10 мкг каждого из пептидов D-7 и D-8 в смешанных условиях с адъювантом QS-21, подкожно в основание хвоста в объеме 100 мкл. Проводили 2 раунда введения на 0 и 4 неделях. Контрольную ДНК D-4 вводили в дозе 50 мкг внутримышечно в 50 мкл ФБР с электропорацией. На 6 неделе (после двух раундов введения) определяли ответ Т-клеток на PreS1 и антиген HDV генотипов 1 и 2 с помощью ELISpot IFNγ (Фигура 12А). Кроме того, на 2 неделе (после одного раунда введения) и 6 неделе (после двух раундов введения) оценивали уровни антител против консенсусных пептидов PreS1А (Фигура 12В-С) и PreS1B (Фигура 12D). Наибольшую реактивность по отношению к HBV и HDV наблюдали в условиях примирования ДНК и стимулирования пептидом.
Пример 10. Иммунизация путем примирования ДНК или белком со стимулированием ДНК или белком против HBV и/или HDV в клинических испытаниях на людях.
[0152] В следующем примере описаны варианты реализации с применением иммуногенной композиции или комбинации продуктов, необязательно состоящих из компонента нуклеиновой кислоты и компонента полипептида, для лечения или предотвращения вирусных инфекций, вызванных такими вирусами, как HBV и HDV.
[0153] Композиции для примирования ДНК/стимулирования белком, описанные в Примере 5, вводят пациентам-людям энтерально, перорально, интраназально, парентерально, подкожно, внутримышечно, внутрикожно или внутривенно. Эти пациенты-люди могут быть на данный момент инфицированы HBV и/или HDV, ранее инфицированы HBV и/или HDV, иметь риск инфицирования HBV и/или HDV или не инфицированы HBV и/или HDV.
[0154] Сначала вводят дозы примирования ДНК в количестве, составляющем 1, 10, 100, 1000 нг, или 1, 10, 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 мкг, или 1, 10, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 мг, или в любом количестве в диапазоне, заданном любыми двумя из указанных выше количеств, или в любом другом количестве, подходящем для оптимальной эффективности у людей. После первой примирующей дозы ДНК можно вводить 1, 2, 3, 4 или 5 дополнительных примирующих доз ДНК через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель, или через любое время в диапазоне, заданном любыми двумя из указанных выше времен, после введения предыдущей примирующей дозы ДНК, например, в пределах 1-48 дней или 1-48 недель. Дозы стимулирования белком вводят после доз примирования ДНК в количестве, составляющем 1, 10, 100, 1000 нг, или 1, 10, 50, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 мкг, или 1, 10, 100, 200, 300, 400, 500, 600, 700, 800, 900, 1000 мг, или в любом количестве в диапазоне, заданном любыми двумя из указанных выше количеств, или в любом другом количестве, подходящем для оптимальной эффективности у людей. Первую стимулирующую дозу белка вводят через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель или через любое время в диапазоне, заданном любыми двумя из указанных выше времен, после введения последней примирующей дозы ДНК. После первой стимулирующей дозы белка можно вводить 1, 2, 3, 4 или 5 дополнительных стимулирующих доз белка через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель или через любое время в диапазоне, заданном любыми двумя из указанных выше времен, после введения предыдущей стимулирующей дозы белка.
[0155] Пациентов будут отслеживать для выявления успешного ответа, направленного против HBV и/или HDV, например, продукции антител против HBV, против HDV, против PreS1 или против HDAg в сыворотках, быстрой активации Т-клеток и других иммунных клеток после контакта с антигенами HBV и/или HDV, и защиты от будущих инфекций HBV и/или HDV.
[0156] У пациентов, на данный момент инфицированных, ранее инфицированных или имеющих риск инфицирования HBV и/или HDV, введение композиций для примирования ДНК/стимулирования белком можно осуществить в сочетании с противовирусной терапией. Потенциальные лекарства противовирусной терапии, у которых выявили эффективность против HBV или HDV, включают, но не ограничены перечисленными лекарствами: энтекавир, тенофовир, ламивудин, адефовир, телбивудин, эмтрицитабин, интерферон-а, пегилированный интерферон-а или интерферон альфа-2b, или любой их комбинацией. У пациентов будут отслеживать побочные действия, такие как головокружение, тошнота, диарея, депрессия, нарушение сна, головные боли, зуд, сыпь, жар или другие известные побочные действия предложенных противовирусных лекарств.
[0157] В по меньшей мере некоторых из ранее описанных вариантов реализации один или более элементов, используемых в некотором варианте реализации, можно взаимозаменяемо применять в другом варианте реализации, кроме тех случаев, когда такая замена технически невозможна. Для специалистов в данной области должно быть понятно, что можно осуществить различные другие опущения, добавления и модификации способов и структур, описанных выше, не отклоняясь от объема заявленного объекта изобретения. Предполагается, что все такие модификации и изменения входят в объем объекта изобретения, который определяется прилагаемой формулой изобретения.
[0158] Касательно использования в настоящей заявке по существу любых терминов во множественном и/или единственном числе, специалисты в данной области техники могут перейти от множественного числа к единственному числу и/или от единственного числа к множественному числу, если это уместно для данного контекста и/или применения. Различные преобразования единственного числа во множественное число и наоборот могут быть явно указаны в данной заявке для полной ясности.
[0159] Специалистам в данной области техники будет понятно, что в общем термины, используемые в данной заявке и особенно в прилагаемой формуле изобретения (например, в ограничительной части прилагаемой формулы изобретения), как правило, считают «открытыми» терминами (например, термин «включающий» следует понимать как «включающий, но не ограниченный этим», термин «обладающий» следует понимать как «обладающий по меньшей мере», термин «включает» следует понимать как «включает, но не ограничен этим», и т.д.). Специалистам в данной области техники дополнительно будет понятно, что если предполагается перечисление определенного числа пунктов формулы изобретения, то такое число пунктов будет практически перечислено в формуле изобретения, а отсутствие такого перечисления указывает на то, что данное намерение отсутствовало. Например, для облегчения понимания, в следующей прилагаемой формуле изобретения могут использоваться вводные фразы «по меньшей мере один» и «один или более», чтобы представить перечисленные пункты формулы изобретения. Тем не менее, использование таких фраз не должно истолковываться как подразумевающее, что представление в форме единственного числа перечисленного пункта формулы изобретения ограничивает какой-либо конкретный пункт формулы изобретения, содержащий такое перечисление пункта формулы изобретения, альтернативными вариантами реализации, содержащими только одно такое перечисление, даже если тот же пункт формулы изобретения содержит вводные фразы «один или более» или «по меньшей мере один» и формы единственного числа (например, форму единственного числа следует истолковывать как «по меньшей мере один» или «один или более») для перечисления пунктов формулы изобретения. Кроме того, даже при указании в явном виде конкретного номера перечисленного пункта формулы изобретения специалисты в данной области техники поймут, что такое перечисление следует понимать, как по меньшей мере перечисленный номер (например, простое перечисление «двух перечислений», без других модификаторов, обычно означает по меньшей мере два перечисления или два или более двух перечислений). Более того, в случаях, когда используют устоявшееся выражение, аналогичное «по меньшей мере один из А, В и С, и т.д.», обычно такая формулировка подразумевается в смысле, который поймет специалист в данной области техники (например, формулировка «система, содержащая по меньшей мере один из А, В и С» будет включать, но не будет ограничена системами, которые содержат А отдельно, В отдельно, С отдельно, А и В вместе, А и С вместе, В и С вместе и/или А, В и С вместе, и т.д.). В случаях, когда используют устоявшееся выражение, аналогичное «по меньшей мере один из А, В или С, и т.д.», обычно такая формулировка подразумевается в смысле, который поймет специалист в данной области техники (например, формулировка «система, содержащая по меньшей мере один из А, В или С» будет включать, но не будет ограничена системами, которые содержат А отдельно, В отдельно, С отдельно, А и В вместе, А и С вместе, В и С вместе и/или А, В и С вместе, и т.д. Специалисты в данной области техники дополнительно поймут, что практически любое разделительное слово и/или формулировка, представляющие два или более альтернативных терминов, либо в описании, либо в формуле изобретения, либо на фигурах, следует понимать как возможность включения одного из терминов, любого из данных терминов или обоих терминов. Например, следует понимать, что формулировка «А или В» включает возможные варианты «А» или «В» или «А и В».
[0160] Кроме того, если свойства или аспекты настоящего описания представлены в виде групп Маркуша, то специалисты в данной области техники поймут, что настоящее описание, тем самым, также описано в виде любого отдельного представителя или подгруппы представителей группы Маркуша.
[0161] Специалист в данной области техники поймет, что для любых и всех целей, например, в части предоставления письменного описания, все диапазоны, описанные в данной заявке, также включают любой и все возможные поддиапазоны и комбинации поддиапазонов. Любой перечисленный диапазон может быть легко расценен как описывающий в достаточной степени и позволяющий разбить этот диапазон на по меньшей мере равные половины, трети, четверти, пятые части, десятые части и т.д. В качестве неограничивающего примера, каждый диапазон, обсуждаемый в настоящей заявке, можно легко разбить на нижнюю треть, среднюю треть и верхнюю треть, и т.д. Специалист в данной области техники также поймет, что все формулировки, такие как «вплоть до», «по меньшей мере», «более чем», «менее чем» и тому подобные формулировки, включают указанное число и относятся к диапазонам, которые затем можно разбить на поддиапазоны, как обсуждалось выше. Наконец, специалист в данной области техники поймет, что диапазон содержит каждого отдельного представителя. Таким образом, например, группа, содержащая 1 -3 элемента, относится к группам, содержащим 1, 2 или 3 элемента. Аналогично, группа, содержащая 1-5 элементов, относится к группам, содержащим 1, 2, 3, 4 или 5 элементов, и так далее.
[0162] Хотя различные аспекты и варианты реализации были описаны в данной заявке, другие аспекты и варианты реализации должны быть понятны специалистам в данной области техники. Указанные различные аспекты и варианты реализации, раскрытые в данной заявке, предложены с целью иллюстрирования и не предназначены для ограничения, при этом фактические объем и сущность настоящего изобретения задаются следующей формулой изобретения.
[0163] Все ссылочные материалы, цитированные в данной заявке, включая, но не ограничиваясь опубликованными и неопубликованными заявками на патент, патентами и литературными источниками, полностью включены в данную заявку посредством ссылки и настоящим сделаны частью настоящего описания. В случаях, когда публикации и патенты или заявки на патент, включенные в данную заявку посредством ссылки, противоречат раскрытию, содержащемуся в настоящем описании, предполагается, что настоящее описание замещает и/или имеет преимущественную силу над любым таким противоречащим материалом.
Ссылочные материалы
Razavi-Shearer D, Gamkrelidze I, Nguyen MH, Chen D-S, Van Damme P, Abbas Z, et al. Global prevalence, treatment, and prevention of hepatitis В virus infection in 2016: a modelling study. Lancet Gastroenterol Hepatol 2018; 3:383-403.
Trepo C, Chan HLY, Lok A. Hepatitis В virus infection. Lancet 2014; 384:2053-2063.
WHO I Global hepatitis report, 2017. WHO 2018.
Mitra B, Thapa RJ, Guo H, Block TM. Host functions used by hepatitis В virus to complete its life cycle: Implications for developing host-targeting agents to treat chronic hepatitis B. Antiviral Res 2018; 158:185-198.
Chen H-Y, Shen D-T, Ji D-Z, Han P-C, Zhang W-M, Ma J-F, et al. Prevalence and burden of hepatitis D virus infection in the global population: a systematic review and metaanalysis. Gw?2018;:gutjnl-2018-316601.
Liu J, Li T, Zhang L, Xu A. The Role of Hepatitis В Surface Antigen in Nucleos(t)ide Analogues Cessation among Asian Chronic Hepatitis В Patients: A Systematic Review. Hepatology Published Online First: 18 December 2018. doi: 10.1002/hep.30474
Nassal M. HBV cccDNA: viral persistence reservoir and key obstacle for a cure of chronic hepatitis B. Gut 2015; 64: 1972-1984.
Papatheodoridis G V., Manolakopoulos S, Touloumi G, Vourli G, Raptopoulou-Gigi M, Vafiadis-Zoumbouli I, et al. Virological suppression does not prevent the development of hepatocellular carcinoma in HBeAg-negative chronic hepatitis В patients with cirrhosis receiving oral antiviral(s) starting with lamivudine monotherapy: results of the nationwide HEPNET. Greece cohort study. Gut 2011; 60: 1109-1116.
Zoulim F, Mason WS. Reasons to consider earlier treatment of chronic HBV infections. Gut 2012; 61: 333-336.
Heidrich B, Yurdaydin C, Kabacam G, Ratsch BA, Zachou K, Bremer B, et al. Late HDV RNA relapse after peginterferon alpha-based therapy of chronic hepatitis delta. Hepatology 2014; 60: 87-97.
Wedemeyer H, Yurdaydin C, Dalekos GN, Erhardt A, Cakaloglu Y, Degertekin H, et al. Peginterferon plus Adefovir versus Either Drug Alone for Hepatitis Delta. N Engl J Med 2011; 364: 322-331.
Feld JJ, Terrault NA, Lin HS, Belle SH, Chung RT, Tsai N, et al. Entecavir and peginterferon alfa-2a in adults with HB eAg-positive immune tolerant chronic hepatitis В virus infection. Hepatology 2018;:hep. 30417.
Chen M, Sallberg M, Thung SN, Hughes J, Jones J, Milich DR. Nondeletional T-cell receptor transgenic mice: model for the CD4(+) T-cell repertoire in chronic hepatitis В virus infection. J Virol 2000; 74: 7587-99.
Chen M, Sallberg M, Hughes J, Jones J, Guidotti LG, Chisari F V., et al. Immune Tolerance Split between Hepatitis В Virus Precore and Core Proteins. J Virol 2005; 79: 3016-3027.
Chen MT, Billaud J-N, Sallberg M, Guidotti LG, Chisari F V., Jones J, et al. A function of the hepatitis В virus precore protein is to regulate the immune response to the core antigen. Proc NatlAcadSci 2004; 101: 14913-14918.
Mason WS, Gill US, Litwin S, Zhou Y, Peri S, Pop O, et al. HBV DNA Integration and Clonal Hepatocyte Expansion in Chronic Hepatitis В Patients Considered Immune Tolerant. Gastroenterology 2016; 151: 986-998.e4.
Milich DR. The Concept of Immune Tolerance in Chronic Hepatitis В Virus Infection Is Alive and Well. Gastroenterology 2016; 151: 801-804.
Short JM, Chen S, Roseman AM, Butler PJG, Crowther RA. Structure of Hepatitis В Surface Antigen from Subviral Tubes Determined by Electron Cryomicroscopy. J Mol Biol 2009; 390: 135-141.
Rydell GE, Prakash K, Norder H, Lindh M. Hepatitis В surface antigen on subviral particles reduces the neutralizing effect of anti-HBs antibodies on hepatitis В viral particles in vitro. Virology 2017; 509: 67-70.
Dryden KA, Wieland SF, Whitten-Bauer C, Gerin JL, Chisari F V., Yeager M. Native Hepatitis В Virions and Capsids Visualized by Electron Cryomicroscopy. Mol Cell 2006; 22: 843-850.
Ni Y, Sonnabend J, Seitz S, Urban S. The Pre-S2 Domain of the Hepatitis В Virus Is Dispensable for Infectivity but Serves a Spacer Function for L-Protein-Connected Virus Assembly. J Virol 2010; 84: 3879-3888.
Ni Y, Lempp FA, Mehrle S, Nkongolo S, Kaufman C, Faith M, et al. Hepatitis В and D Viruses Exploit Sodium Taurocholate Co-transporting Polypeptide for Species-Specific Entry into Hepatocytes. Gastroenterology 2014; 146:1070-1083.e6.
Chen A, Allien G, Brenndorfer ED, Brass A, Holmstrom F, Chen M, et al. Heterologous T Cells Can Help Restore Function in Dysfunctional Hepatitis С Virus Nonstructural 3/4A-Specific T Cells during Therapeutic Vaccination. J Immunol 2011; 186: 5107-5118.
Mancini-Bourgine M, Fontaine H, Scott-Algara D, Pol S, Brechot C, Michel M-L. Induction or expansion of T-cell responses by a hepatitis В DNA vaccine administered to chronic HBV carriers. Hepatology 2004; 40: 874-882.
Kosinska AD, Zhang E, Johrden L, Liu J, Seiz PL, Zhang X, et al. Combination of DNA Prime Adenovirus Boost Immunization with Entecavir Elicits Sustained Control of Chronic Hepatitis В in the Woodchuck Model. PLoSPathog 2013; 9:el003391.
Brass A, Frelin L, Milich DR, Sallberg M, Ahlen G. Functional Aspects of Intrahepatic Hepatitis В Virus-specific T Cells Induced by Therapeutic DNA Vaccination. Mol Ther 2015; 23: 578-590.
Yuen MF, Gane EJ, Kim DJ, Weilert F, Chan HLY, Lalezari J, et al. Antiviral Activity, Safety, and Pharmacokinetics of Capsid Assembly Modulator NVR 3-778 in Patients with Chronic HBV Infection. Gastroenterology Published Online First: 6 January 2019. doi: 10.1053/J.GASTRO.2018.12.023
Liang TJ, Block TM, McMahon BJ, Ghany MG, Urban S, Guo J-T, et al. Present and future therapies of hepatitis B: From discovery to cure. Hepatology 2015; 62: 1893-1908.
Meuleman P, Vanlandschoot P, Leroux-Roels G. A simple and rapid method to determine the zygosity of uPA-transgenie SCID mice, doi: 10.1016/S0006-291X(03)01388-3
Meuleman P, Libbrecht L, De Vos R, de Hemptirme B, Gevaert K, Vandekerckhove J, et al. Morphological and biochemical characterization of a human liver in a uPA-SCID mouse chimera. Hepatology 2005; 41: 847-856.
Levander S, Holmstrom F, Frelin L, Ahlen G, Rupp D, Long G, et al. Immune-mediated effects targeting hepatitis С virus in a syngeneic replicon cell transplantation mouse model. Gut 2018; 67: 1525-1535.
 Tjelle T, Kjeken R, Frelin L, Hoglund U, et al. hi vivo electroporation enhances the immunogenicity of hepatitis С virus nonstructural 3/4A DNA by increased local DNA uptake, protein expression, inflammation, and infiltration of CD3+T cells. J Immunol 2007; 179: 4741-53.
Tjelle T, Kjeken R, Frelin L, Hoglund U, et al. hi vivo electroporation enhances the immunogenicity of hepatitis С virus nonstructural 3/4A DNA by increased local DNA uptake, protein expression, inflammation, and infiltration of CD3+T cells. J Immunol 2007; 179: 4741-53.
Ni Y, Urban S. Hepatitis В Virus Infection of HepaRG Cells, HepaRG-hNTCP Cells, and Primary Human Hepatocytes. In: Methods in molecular biology (Clifton, N.J.).; 2017. pp. 15-25.
Donkers JM, Zehnder B, van Westen GJP, Kwakkenbos MJ, IJzerman AP, Oude Elferink RPJ, et al. Reduced hepatitis В and D viral entry using clinically applied drugs as novel inhibitors of the bile acid transporter NTCP. Sci Rep 2017; 7: 15307.
Meuleman P, Lerouxroels G. The human liver-uPA-SCID mouse: A model for the evaluation of antiviral compounds against HBV and HCV. Antiviral Res 2008; 80: 231-238.
Wi J, Jeong MS, Hong HJ. Construction and characterization of an anti-hepatitis В virus preS 1 humanized antibody that binds to the essential receptor binding site. J Microbiol Biotechnol 2017; 27: 1336-1344.
Lok ASF, McMahon BJ, Brown RS, Wong JB, Ahmed AT, Farah W, et al. Antiviral therapy for chronic hepatitis В viral infection in adults: A systematic review and metaanalysis. Hepatology 2016; 63: 284-306.
Revill PA, Chisari F V, Block JM, Dandri M, Gehring AJ, Guo H, et al. A global scientific strategy to cure hepatitis B. Lancet Gastroenterol Hepatol Published Online First: 10 April 2019. doi:10.1016/S2468-1253(19)30119-0
Neurath AR, Kent SB, Strick N, Parker K. Identification and chemical synthesis of a host cell receptor binding site on hepatitis В virus. Cell 1986; 46: 429 36.
Gripon P, Le Seyec J, Rumin S, Guguen-Guillouzo C. Myristylation of the Hepatitis В Virus Large Surface Protein Is Essential for Viral Infectivity. Virology 1995; 213: 292-299.
Hong HJ, Ryu CJ, Hur H, Kim S, Oh HK, Oh MS, et al. In vivo neutralization of hepatitis В virus infection by an anti-preSl humanized antibody in chimpanzees. Virology 2004; 318: 134-141.
Bogomolov P, Alexandrov A, Voronkova N, Macievich M, Kokina K, Petrachenkova M, et al. Treatment of chronic hepatitis D with the entry inhibitor myrcludex B: First results of a phase lb/Па study. J Hepatol 2016; 65: 490-498.
Blank A, Eidam A, Haag M, Hohmann N, Burhenne J, Schwab M, et al. The NTCP-inhibitor Myrcludex B: Effects on Bile Acid Disposition and Tenofovir Pharmacokinetics. Clin Pharmacol Ther 2018; 103: 341-348.
Passioura T, Watashi K, Fukano K, Sureau C, Suga H, Correspondence TW. De Novo Macrocyclic Peptide Inhibitors of Hepatitis В Virus Cellular Entry. Cell Chem Biol 2018; 25:906-915.
Bian Y, Zhang Z, Sun Z, Zhao J, Zhu D, Wang Y, et al. Vaccines Targeting PreS1 Domain Overcome Immune Tolerance in HBV Carrier Mice HHS Public Access. 2017; 66: 1067-1082.
Chen M, Jagya N, Bansal R, Frelin L, Sallberg M. Prospects and progress of DNA vaccines for treating hepatitis B. Expert Rev Vaccines 2016; 15:629-640.
Yalcin K, Danis R, Degertekin H, Alp MN, Tekes S, Budak T. The lack of effect of therapeutic vaccination with a pre-S2/S HBV vaccine in the immune tolerant phase of chronic HBV infection. J Clin Gastroenterol 2003; 37: 330-5.
Zhao H-J, Han Q-J, Wang G, Lin A, Xu D-Q, Wang Y-Q, et al. I:C-based rHBVvac therapeutic vaccine eliminates HBV via generatioPolyn of HBV-specific CD8+ effector memory T cells. Gut20l9;:gutjnl-2017-315588.
Suslov A, Boldanova T, Wang X, Wieland S, Heim MH. Hepatitis В Virus Does Not Interfere With Innate Immune Responses in the Human Liver. Gastroenterology 2018; 154: 1778-1790.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Svenska Vaccinfabriken Produktion AB
<120> КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ И ПРЕДОТВРАЩЕНИЯ ГЕПАТИТА B И
D
<130> SVF.005WO
<150> US 62/966970
<151> 2020-01-28
<160> 39
<170> PatentIn версии 3.5
<210> 1
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК HDAg генотипа 1 A
<400> 1
agccgcagcg aaagcaaaaa aaaccgcggc ggccgcgaag aaattctgga acagtgggtg
60
ggcgcgcgca aaaaactgga agaactggaa cgcgatctgc gcaaaattaa aaaaaaaatt
120
aaaaaactgg aagaagaaaa cccgtggctg ggcaacatta aaggcattct gggcaaaaaa
180
gatcgcgaag gcgaaggcgc gccgccggcg aaacgcgcgc gcgcggatca gatggaagtg
240
gatagcggcc cgcgcaaacg cccgtttcgc ggcgaattta ccgataaaga acgccgcgat
300
catcgccgcc gcaaagcgct ggaaaacaaa cgcaaacagc tgagcagcgg cggcaaaagc
360
ctgagcaaag aagaagaaga agaactgcgc aaactgaccg aagaagatga acgccgcgaa
420
cgccgcgtgg cgggcccgcg cgtgggcggc gtgaacccgc tggaaggcgg cacccgcggc
480
gcgccgggcg gcggctttgt gccgagcatg cagggcgtgc cggaaagccc gtttgcgcgc
540
accggcgaag gcctggatgt gcgcggcaac cagggctttc cgtgggatat tctgtttccg
600
gcggatccgc cgtttagccc gcagagctgc cgcccgcag
639
<210> 2
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК HDAg генотипа 1 B
<400> 2
agccgcagcg aaagcaaaaa aaaccgcggc ggccgcgaag aagtgctgga acagtgggtg
60
aacggccgca aaaaactgga agaactggaa cgcgaactgc gccgcgcgcg caaaaaaatt
120
aaaaaactgg aagatgataa cccgtggctg ggcaacgtga aaggcattct gggcaaaaaa
180
gataaagatg gcgaaggcgc gccgccggcg aaacgcgcgc gcaccgatca gatggaaatt
240
gatagcggcc cgcgcaaacg cccgctgcgc ggcggcttta ccgatcgcga acgccaggat
300
catcgccgcc gcaaagcgct gaaaaacaaa aaaaaacagc tgagcgcggg cggcaaaagc
360
ctgagcaaag aagaagaaga agaactgaaa cgcctgaccc gcgaagatga agaacgcaaa
420
aaagaagaac atggcccgag ccgcctgggc gtgaacccga gcgaaggcgg cccgcgcggc
480
gcgccgggcg gcggctttgt gccgagcatg cagggcattc cggaaagccg ctttacccgc
540
accggcgaag gcctggatgt gcgcggcagc cgcggctttc cgcaggatat tctgtttccg
600
agcgatccgc cgtttagccc gcagagctgc cgcccgcag
639
<210> 3
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК HDAg генотипа 2 A
<400> 3
agccagagcg aaacccgccg cggccgccgc ggcacccgcg aagaaaccct ggaaaaatgg
60
attaccgcgc gcaaaaaagc ggaagaactg gaaaaagatc tgcgcaaaac ccgcaaaacc
120
attaaaaaac tggaagaaga aaacccgtgg ctgggcaaca ttgtgggcat tattcgcaaa
180
ggcaaagatg gcgaaggcgc gccgccggcg aaacgcccgc gcaccgatca gatggaagtg
240
gatagcggcc cgggcaaacg cccgcataaa agcggcttta ccgataaaga acgcgaagat
300
catcgccgcc gcaaagcgct ggaaaacaaa aaaaaacagc tgagcgcggg cggcaaaatt
360
ctgagcaaag aagaagaaga agaactgcgc cgcctgaccg atgaagatga agaacgcaaa
420
cgccgcgtgg cgggcccgcg cgtgggcgat gtgaacccga gccgcggcgg cccgcgcggc
480
gcgccgggcg gcggctttgt gccgcagatg gcgggcgtgc cggaaagccc gtttagccgc
540
accggcgaag gcctggatat tcgcggcacc cagggctttc cgtgggtgag cccgagcccg
600
ccgcagcagc gcctgccgct gctggaatgc accccgcag
639
<210> 4
<211> 639
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК HDAg генотипа 2 B
<400> 4
agccagagcg aaagcaaaaa aaaccgccgc ggcggccgcg aagatattct ggaaaaatgg
60
attaccaccc gccgcaaagc ggaagaactg gaaaaagatc tgcgcaaagc gcgcaaaacc
120
attaaaaaac tggaagatga aaacccgtgg ctgggcaaca ttattggcat tattcgcaaa
180
ggcaaagatg gcgaaggcgc gccgccggcg aaacgcccgc gcaccgatca gatggaaatt
240
gatagcggca ccggcaaacg cccgcataaa agcggcttta ccgataaaga acgcgaagat
300
catcgccgcc gcaaagcgct ggaaaacaaa aaaaaacagc tgagcagcgg cggcaaaaac
360
ctgagccgcg aagaagaaga agaactgggc cgcctgaccg tggaagatga agaacgccgc
420
cgccgcgtgg cgggcccgcg caccggcgat gtgaacctga gcggcggcgg cccgcgcggc
480
gcgccgggcg gcggctttgt gccgcgcatg gaaggcgtgc cggaaagccc gtttacccgc
540
accggcgaag gcctggatat tcgcggcaac cagggctttc cgtgggtgcg cccgagcccg
600
ccgcagcagc gcctgccgct gctggaatgc accccgcag
639
<210> 5
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность HDAg генотипа 1 A
<400> 5
Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Ile Leu
1 5 10 15
Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu Arg Asp
20 25 30
Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu Asn Pro
35 40 45
Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg Glu Gly
50 55 60
Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met Glu Val
65 70 75 80
Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr Asp Lys
85 90 95
Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Arg Lys
100 105 110
Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu
115 120 125
Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg Val Ala
130 135 140
Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr Arg Gly
145 150 155 160
Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro Glu Ser
165 170 175
Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn Gln Gly
180 185 190
Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser Pro Gln
195 200 205
Ser Cys Arg Pro Gln
210
<210> 6
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность HDAg генотипа 1 B
<400> 6
Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Val Leu
1 5 10 15
Glu Gln Trp Val Asn Gly Arg Lys Lys Leu Glu Glu Leu Glu Arg Glu
20 25 30
Leu Arg Arg Ala Arg Lys Lys Ile Lys Lys Leu Glu Asp Asp Asn Pro
35 40 45
Trp Leu Gly Asn Val Lys Gly Ile Leu Gly Lys Lys Asp Lys Asp Gly
50 55 60
Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Thr Asp Gln Met Glu Ile
65 70 75 80
Asp Ser Gly Pro Arg Lys Arg Pro Leu Arg Gly Gly Phe Thr Asp Arg
85 90 95
Glu Arg Gln Asp His Arg Arg Arg Lys Ala Leu Lys Asn Lys Lys Lys
100 105 110
Gln Leu Ser Ala Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu
115 120 125
Leu Lys Arg Leu Thr Arg Glu Asp Glu Glu Arg Lys Lys Glu Glu His
130 135 140
Gly Pro Ser Arg Leu Gly Val Asn Pro Ser Glu Gly Gly Pro Arg Gly
145 150 155 160
Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Ile Pro Glu Ser
165 170 175
Arg Phe Thr Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Ser Arg Gly
180 185 190
Phe Pro Gln Asp Ile Leu Phe Pro Ser Asp Pro Pro Phe Ser Pro Gln
195 200 205
Ser Cys Arg Pro Gln
210
<210> 7
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность HDAg генотипа 2 A
<400> 7
Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu Glu Thr
1 5 10 15
Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu Glu Lys
20 25 30
Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu Glu Asn
35 40 45
Pro Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys Asp Gly
50 55 60
Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu Val
65 70 75 80
Asp Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp Lys
85 90 95
Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys
100 105 110
Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu Glu Glu
115 120 125
Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg Val Ala
130 135 140
Gly Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro Arg Gly
145 150 155 160
Ala Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro Glu Ser
165 170 175
Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr Gln Gly
180 185 190
Phe Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu
195 200 205
Glu Cys Thr Pro Gln
210
<210> 8
<211> 213
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность HDAg генотипа 2 B
<400> 8
Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg Gly Gly Arg Glu Asp Ile
1 5 10 15
Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys Ala Glu Glu Leu Glu Lys
20 25 30
Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys Lys Leu Glu Asp Glu Asn
35 40 45
Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile Arg Lys Gly Lys Asp Gly
50 55 60
Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu Ile
65 70 75 80
Asp Ser Gly Thr Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp Lys
85 90 95
Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys
100 105 110
Gln Leu Ser Ser Gly Gly Lys Asn Leu Ser Arg Glu Glu Glu Glu Glu
115 120 125
Leu Gly Arg Leu Thr Val Glu Asp Glu Glu Arg Arg Arg Arg Val Ala
130 135 140
Gly Pro Arg Thr Gly Asp Val Asn Leu Ser Gly Gly Gly Pro Arg Gly
145 150 155 160
Ala Pro Gly Gly Gly Phe Val Pro Arg Met Glu Gly Val Pro Glu Ser
165 170 175
Pro Phe Thr Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Asn Gln Gly
180 185 190
Phe Pro Trp Val Arg Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu
195 200 205
Glu Cys Thr Pro Gln
210
<210> 9
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК PreS1 A
<400> 9
ggcaccaacc tgagcaccag caacccgctg ggcttttttc cggatcatca gctggatccg
60
gcgtttcgcg cgaacagcgc gaacccggat tgggatttta acccgaacaa agatacctgg
120
ccggatgcga acaaagtggg c
141
<210> 10
<211> 141
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК PreS1 B
<400> 10
ggccagaacc tgagcaccag caacccgctg ggcttttttc cggatcatca gctggatccg
60
gcgtttcgcg cgaacaccgc gaacccggat tgggatttta acccgaacaa agatacctgg
120
ccggatgcga acaaagtggg c
141
<210> 11
<211> 47
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность PreS1 A
<400> 11
Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His
1 5 10 15
Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp
20 25 30
Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
35 40 45
<210> 12
<211> 47
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность PreS1 B
<400> 12
Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His
1 5 10 15
Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp
20 25 30
Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
35 40 45
<210> 13
<211> 66
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность ДНК сайта автокаталитического расщепления
пептида P2A
<400> 13
ggaagcggag ctactaactt cagcctgctg aagcaggctg gagacgtgga ggagaaccct
60
ggacct
66
<210> 14
<211> 22
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность сайта автокаталитического
расщепления пептида P2A
<400> 14
Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val
1 5 10 15
Glu Glu Asn Pro Gly Pro
20
<210> 15
<211> 3198
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-1
<400> 15
atggccagca gaagtgaatc aaaaaagaat cggggagggc gggaagaaat cctggaacag
60
tgggtcggag cacggaagaa actggaagaa ctggagaggg acctgcgcaa gatcaagaag
120
aagatcaaga agctggagga ggagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggatc gggagggaga gggagcacca cctgcaaaga gggccagagc cgaccagatg
240
gaggtggata gcggaccaag gaagcgccct ttcagaggag agtttaccga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagagga agcagctgag ctccggcggc
360
aagtccctgt ctaaggagga ggaggaggag ctgcgcaagc tgacagagga ggacgagaga
420
agggagagga gggtggcagg acctagggtg ggaggcgtga acccactgga gggaggaacc
480
agaggagcac ctggaggagg attcgtgcca tccatgcagg gagtgcccga gtctcctttt
540
gcccggacag gcgagggcct ggatgtgaga ggcaatcagg gcttcccctg ggacatcctg
600
tttcctgccg atccaccctt ctctcctcag agctgccggc cacagagcag atccgagtct
660
aagaagaaca ggggaggaag agaggaggtg ctggagcagt gggtgaatgg ccggaagaag
720
ctggaggagc tggagcggga gctgagaagg gccagaaaga agatcaagaa gctggaagac
780
gataatcctt ggctgggcaa tgtgaaaggc atcctgggca agaaggacaa ggatggagag
840
ggagcacctc cagcaaagag ggcaagaacc gaccagatgg agatcgattc tggaccaagg
900
aagcgccccc tgagaggagg cttcacagac cgggagagac aggatcaccg ccggagaaag
960
gccctgaaga acaagaagaa gcagctgtcc gccggaggca agagcctgtc caaagaagag
1020
gaagaggagc tgaagaggct gacccgcgag gacgaggaga ggaagaagga ggagcacgga
1080
ccaagcaggc tgggagtgaa tccttccgag ggaggaccta ggggagcacc aggaggaggc
1140
ttcgtgccat ctatgcaggg catccccgag agccggttta ccagaacagg agagggcctg
1200
gacgtgaggg gctcccgcgg ctttcctcag gacatcctgt tcccatctga tccccctttt
1260
tccccccagt cttgtaggcc tcagggcacc aacctgtcta caagcaatcc actgggcttc
1320
tttcccgacc accagctgga tcctgccttc cgcgccaaca gcgccaatcc cgactgggac
1380
ttcaacccaa ataaggacac ctggccagat gccaacaagg tcggcggcca gaacctgtcc
1440
acatctaatc ctctgggctt ctttccagac caccagctgg atccagcctt ccgggccaac
1500
acagctaacc ctgactggga cttcaacccc aataaggata cttggcccga cgccaacaag
1560
gtcggcggaa gcggagctac taacttcagc ctgctgaagc aggctggaga cgtggaggag
1620
aaccctggac ctatgagcca gtccgagaca aggaggggcc ggagaggaac cagggaggag
1680
acactggaga agtggatcac agcccgcaag aaggccgagg agctggagaa ggacctgcgg
1740
aagaccagaa agacaatcaa gaagctggaa gaagagaacc catggctggg caatatcgtg
1800
ggcatcatca gaaagggcaa ggacggcgag ggagcaccac cagcaaagag gcccaggact
1860
gatcagatgg aagtcgatag cggaccaggc aagcggcctc acaagtccgg cttcacagac
1920
aaggagagag aggaccatag gcgccggaag gccctggaaa acaagaagaa gcaattatcc
1980
gccggcggca agatcctgtc caaagaggaa gaagaggagc tgagaaggct gaccgacgag
2040
gatgaggaga ggaaaagaag ggtggcagga ccaagggtgg gcgacgtgaa tcccagcagg
2100
ggaggaccaa gaggcgcccc tggcggcggc ttcgtgccac agatggcagg agtgccagag
2160
agcccctttt ccaggacagg agagggcctg gatatcagag gcacccaggg ctttccttgg
2220
gtgtctccaa gccctccaca gcagcggctg ccactgctgg agtgcacccc tcagtcccag
2280
tctgagagca agaagaacag aaggggcggc agagaggaca tcctggagaa gtggatcacc
2340
acacgcagaa aagctgaaga actggaaaag gacctgagga aggcccgcaa aacaatcaag
2400
aagctggagg atgaaaatcc atggctggga aacatcatcg gcatcatcag gaagggcaag
2460
gacggggaag gcgcaccacc tgcaaagcgg cctagaacag atcagatgga aatcgattct
2520
ggcaccggca agaggccaca caagagcggc ttcaccgaca aggagcgcga ggatcacaga
2580
aggcgcaagg ccctggagaa caagaagaag caattaagca gcggcggcaa gaatctgtcc
2640
agagaagaag aggaggagct gggccgcctg accgtggagg acgaggagcg gagaaggcgc
2700
gtggcaggac cacgcacagg cgatgtgaac ctgtccggag gaggaccaag gggagcacct
2760
ggaggcggct tcgtgcctag aatggaggga gtgcctgagt cccccttcac ccgcaccgga
2820
gagggcctgg acatcagagg caatcaggga ttcccatggg tgaggcccag cccaccacag
2880
cagcgcctgc cactgctgga gtgtaccccc cagggcacaa acctgtccac ctctaatccc
2940
ctgggcttct ttcctgatca tcagctggac ccagccttca gggccaactc cgccaatcca
3000
gattgggact tcaacccgaa taaggatact tggccagatg caaacaaggt cggaggacag
3060
aacctgagca catccaaccc tctgggcttc tttcctgacc atcagctgga tcccgccttt
3120
cgcgccaata ccgccaaccc tgattgggac ttcaacccta ataaggatac ttggcctgat
3180
gctaataagg tcgggtga
3198
<210> 16
<211> 3198
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-2
<400> 16
atggccggca ctaacctgtc tacatcaaac cctctgggat ttttccccga tcatcagctg
60
gaccccgcat ttcgcgctaa ctctgctaac cctgactggg atttcaaccc taataaggac
120
acatggccag atgccaacaa ggtcggcggc cagaacctgt ccacctctaa tcccctgggc
180
ttctttcctg accaccagct ggatcctgcc ttcagggcca acaccgccaa tcccgactgg
240
gacttcaacc caaataagga tacctggcct gacgctaaca aggtcggcag ccggtccgag
300
tctaagaaga ataggggagg aagggaggag atcctggagc agtgggtggg cgccagaaag
360
aagctggagg agctggagcg ggacctgaga aagatcaaga agaagatcaa gaagctggag
420
gaggagaacc cctggctggg caatatcaag ggcatcctgg gcaagaagga tcgggaggga
480
gagggagcac cacctgcaaa gagggccaga gccgaccaga tggaggtgga ttccggccct
540
aggaagcgcc cattcagagg cgagtttaca gacaaggagc ggagagatca caggcgccgg
600
aaggccctgg agaacaagag gaagcagctg agctccggcg gcaagagcct gtccaaggag
660
gaggaggagg agctgcgcaa gctgaccgag gaggacgaga gaagggagag gagggtggca
720
ggacctaggg tgggaggcgt gaacccactg gagggaggaa caagaggagc acccggagga
780
ggcttcgtgc cttctatgca gggcgtgcct gagagcccat ttgccaggac cggagagggc
840
ctggacgtga gaggcaatca gggcttccca tgggacatcc tgtttcccgc cgatccaccc
900
ttcagcccac agtcctgcag gccccagtct cgcagcgagt ccaagaagaa cagaggcgga
960
agggaggagg tgctggagca gtgggtgaat ggcaggaaga agctggaaga actggagagg
1020
gagctgagaa gggcccgcaa gaagatcaag aagctggaag acgataatcc ttggctgggc
1080
aatgtgaaag gcatcctggg caagaaggac aaggatggag agggagcacc tccagcaaag
1140
agggcaagaa cagaccagat ggagatcgat tccggaccaa ggaagcgccc tctgagggga
1200
ggcttcaccg accgggagag acaggatcac cgccggagaa aggccctgaa gaacaagaag
1260
aagcagctga gcgccggcgg caagtctctg agtaaagaag aagaggagga gctgaagcgg
1320
ctgacaagag aggacgagga gaggaagaag gaggagcacg gaccatccag gctgggagtg
1380
aatccttctg agggaggacc aaggggcgcc cctggcggag gcttcgtgcc tagcatgcag
1440
ggcatcccag agtccaggtt taccaggaca ggcgaaggcc tggacgtgcg gggctctaga
1500
ggctttcccc aggacatcct gttccctagc gatccccctt tttctcctca gagctgtaga
1560
ccacagggaa gcggagctac taacttcagc ctgctgaagc aggctggaga cgtggaggag
1620
aaccctggac ctatgggcac caacctgtcc acatctaacc ctctgggctt ctttccagat
1680
catcagctgg acccagcctt cagggccaac agcgccaatc cagactggga cttcaacccc
1740
aataaggaca catggcctga cgcaaacaag gtcggaggac agaacctgag cacctccaat
1800
ccactgggct tctttcccga ccaccagctg gatccagcct tccgcgccaa cactgctaac
1860
cctgattggg acttcaaccc taataaggat acatggcctg atgccaataa ggtcggctct
1920
cagagcgaga caaggagggg ccggagagga accagggagg agacactgga gaagtggatc
1980
accgcccgca agaaggccga ggagctggag aaggacctga ggaagacccg caagacaatc
2040
aagaagctgg aagaagagaa cccatggctg ggcaatatcg tgggcatcat cagaaagggc
2100
aaggacggcg agggagcacc accagcaaag aggccccgca cagatcagat ggaagtggat
2160
tccggacctg gcaagcggcc acacaagtct ggcttcaccg acaaggagag agaggaccat
2220
aggcgccgga aggccctgga aaacaagaag aagcaattat ctgccggcgg caagatcctg
2280
agtaaagaag aggaagagga gctgagaagg ctgaccgacg aggatgagga gaggaagcgc
2340
cgggtggccg gcccacgcgt gggcgacgtg aatccctcca ggggaggacc aagaggagca
2400
cctggaggcg gcttcgtgcc ccagatggcc ggcgtgcccg agtccccttt ttctcggacc
2460
ggcgagggcc tggatatcag aggcacacag ggctttccat gggtgtcccc ctctcctcca
2520
cagcagaggc tgccactgct ggagtgcaca ccccagagcc agagcgaatc taagaagaac
2580
agaaggggag gccgcgagga catcctggaa aaatggatca ccacacgcag aaaagctgaa
2640
gaactggaaa aggacctgcg gaaggccaga aagaccatca agaagctgga ggatgaaaat
2700
ccatggctgg gaaacatcat cggcatcatc cggaagggca aggacgggga aggcgcacca
2760
cctgcaaagc ggcctagaac cgatcagatg gaaatcgata gcggcacagg caagaggcca
2820
cacaagtccg gcttcaccga taaagagcgc gaggatcaca gaaggcgcaa ggccctggag
2880
aacaagaaga agcaattaag cagcggcggc aagaatctgt ccagagaaga ggaggaagag
2940
ctgggccgcc tgacagtgga ggacgaggag cggagaaggc gcgtggcagg acccagaacc
3000
ggcgatgtga acctgtccgg aggaggacct aggggagcac caggaggcgg cttcgtgcct
3060
agaatggagg gcgtgccaga gtctcccttt acccggacag gcgagggcct ggacatcaga
3120
ggcaatcagg gctttccctg ggtccgcccc tccccccctc agcagagact gccactgctg
3180
gaatgcacac cacagtga
3198
<210> 17
<211> 3762
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-3
<400> 17
atggccggca ccaatctgtc tacctcaaat cccctgggct tcttccccga tcatcagctg
60
gaccctgcct tccgagcaaa ttccgctaat cctgattggg atttcaaccc aaataaggac
120
acatggccag atgccaacaa ggtcggcggc cagaacctgt ccacctctaa tcctctgggc
180
ttctttccag accaccagct ggatcccgcc ttcagggcca acacagccaa tcccgactgg
240
gacttcaacc ctaataagga cacctggcct gacgccaaca aggtcggcag caggtccgag
300
tctaagaaga ataggggagg aagggaggag atcctggagc agtgggtggg agcacgcaag
360
aagctggagg agctggagcg ggacctgaga aagatcaaga agaagatcaa gaagctggag
420
gaggagaacc cctggctggg caatatcaag ggcatcctgg gcaagaagga tcgggaggga
480
gagggagcac cacctgcaaa gagggccaga gccgaccaga tggaggtgga ttccggacca
540
aggaagcgcc ctttcagagg agagtttaca gacaaggagc ggagagatca caggcgccgg
600
aaggccctgg agaacaagcg gaagcagctg agctccggcg gcaagagcct gtccaaggag
660
gaggaggagg agctgagaaa gctgaccgag gaggacgaga gaagggagag gagggtggcc
720
ggccccaggg tgggcggcgt gaaccctctg gagggaggaa caaggggagc accaggagga
780
ggcttcgtgc cttccatgca gggcgtgccc gagtctcctt ttgccaggac cggagagggc
840
ctggacgtgc gcggcaatca gggcttccca tgggacatcc tgtttcccgc cgatccaccc
900
ttctctcccc agagctgcag gcctcagtct cgcagcgagt ccaagaagaa cagaggcgga
960
agggaggagg tgctggagca gtgggtgaat ggcaggaaga agctggaaga actggagagg
1020
gagctgagaa gggcccgcaa gaagatcaag aagctggaag acgataatcc ttggctgggc
1080
aatgtgaaag gcatcctggg caagaaggac aaggatggag agggagcacc tccagcaaag
1140
agggcaagaa cagaccagat ggagatcgat tctggaccaa ggaagcgccc cctgagggga
1200
ggcttcaccg accgggagag acaggatcac cgccggagaa aggccctgaa gaacaagaag
1260
aagcagctga gcgccggcgg caagtctctg agtaaagaag aagaggagga gctgaagcgg
1320
ctgaccagag aggacgagga gcggaagaag gaggagcacg gcccaagcag actgggagtg
1380
aatccatccg agggaggacc tagaggcgcc cctggcggcg gcttcgtgcc ttctatgcag
1440
ggcatcccag agagcaggtt taccaggaca ggcgaaggcc tggacgtgcg gggctccaga
1500
ggctttcccc aggacatcct gttcccttct gatccccctt tttccccaca gtcttgtagg
1560
ccccagggca ccaacctgtc cacatctaac ccactgggct tctttcctga tcaccagctg
1620
gatccagcct tccgcgccaa ctccgccaat ccagactggg acttcaaccc caataaggac
1680
acatggcctg atgctaacaa ggtcggaggc cagaacctga gcacctccaa tcccctgggc
1740
ttctttcctg accaccagct ggatcctgcc ttccgcgcca acacagctaa ccctgattgg
1800
gacttcaacc caaataagga tacctggcct gatgcaaaca aggtcggagg aagcggagct
1860
actaacttca gcctgctgaa gcaggctgga gacgtggagg agaaccctgg acctatgggc
1920
accaacctgt ctacaagcaa tccactgggc ttctttcccg accatcagct ggacccagcc
1980
ttcagggcca acagcgccaa ccctgactgg gacttcaacc caaataagga cacgtggcct
2040
gatgccaaca aggtcggagg acaaaacctg tccacctcta accccctggg cttctttccc
2100
gatcatcaat tagacccagc cttccgcgct aacactgcta accctgactg ggacttcaac
2160
ccgaataagg atacttggcc tgatgccaat aaggtcggca gccagtccga gacaaggagg
2220
ggccggagag gaaccaggga ggagacactg gagaagtgga tcaccgccag aaagaaggcc
2280
gaggagctgg agaaggacct gaggaagacc cgcaagacaa tcaagaagct ggaagaagag
2340
aacccttggc tgggcaatat cgtgggcatc atcagaaagg gcaaggacgg cgagggagca
2400
ccaccagcca agaggccacg cacagatcag atggaagtgg atagcggacc aggcaagagg
2460
cctcacaagt ccggcttcac cgacaaggag agggaggacc ataggcgccg gaaggccctg
2520
gaaaacaaga agaagcaatt atccgccggc ggcaagatcc tgtctaaaga agaggaagaa
2580
gagctgagaa ggctgaccga cgaggatgag gagaggaaga ggagggtggc aggacctaga
2640
gtgggcgacg tgaatccatc caggggagga ccaagaggag caccaggagg cggcttcgtg
2700
ccacagatgg caggagtgcc agagagcccc ttttccagga caggagaggg cctggatatc
2760
aggggaaccc agggctttcc ttgggtgtct ccaagccctc cacagcagcg gctgccactg
2820
ctggagtgca caccccagtc ccagtctgag agcaagaaga acagaagggg cggcagagag
2880
gacatcctgg aaaaatggat caccacacgc agaaaagctg aagaactgga aaaggacctg
2940
cggaaggcca gaaagaccat caagaagctg gaggatgaaa atccatggct gggaaatatc
3000
atcggcatca tccggaaggg caaggacggg gaaggcgcac cacctgcaaa gcggcccagg
3060
accgatcaga tggaaatcga ttctggaacc ggcaagcggc ctcacaagag tggcttcacc
3120
gataaggaga gagaggatca cagaaggcgc aaggccctgg agaacaagaa gaagcaatta
3180
agcagcggcg gcaagaatct gtccagagaa gaggaagagg agctgggcag actgacagtg
3240
gaggacgagg agcggagaag gcgcgtggca ggaccaagaa ccggcgatgt gaacctgtcc
3300
ggaggaggac caaggggagc acctggggga ggcttcgtgc caaggatgga gggagtgcct
3360
gagtccccct tcaccagaac cggcgaaggc ctggacatca ggggcaatca gggattccca
3420
tgggtgcggc cctccccacc ccagcagaga ctgcctctgc tggagtgtac cccacagggc
3480
actaacctgt ccacctctaa cccgttaggc ttctttcctg accatcaatt agatcccgcc
3540
ttccgggcca acagcgccaa tcctgattgg gacttcaacc cgaataagga cacctggccc
3600
gacgcaaaca aggtcggagg gcaaaacctg agcacctcca accctttagg cttctttcca
3660
gatcatcagc tggatccagc ctttagagcc aataccgcca accctgactg ggatttcaac
3720
cctaacaaag atacctggcc cgacgctaac aaagtgggat ga
3762
<210> 18
<211> 3900
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-4
<400> 18
atggccagtc ggagcgaatc aaagaaaaat aggggagggc gggaagaaat cctggagcag
60
tgggtcggag cacgaaagaa actggaagaa ctggagaggg acctgcgcaa gatcaagaag
120
aagatcaaga agctggagga ggagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggatc gggagggaga gggagcacca cctgcaaaga gggccagagc cgaccagatg
240
gaggtggata gcggccctag gaagcgccca ttcagaggcg agtttacaga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagcgga agcagctgag ctccggcggc
360
aagtccctgt ctaaggagga ggaggaggag ctgagaaagc tgaccgagga ggacgagaga
420
agggagagga gggtggcagg acctagggtg ggaggcgtga acccactgga gggaggaaca
480
aggggagcac ctggaggagg attcgtgcca tccatgcagg gagtgcctga gtctccattt
540
gccaggaccg gagagggcct ggatgtgcgc ggaaatcagg gcttcccctg ggacatcctg
600
tttcctgccg atccaccctt ctccccacag tcttgcaggc cacagggaac caacctgagc
660
acatccaatc ctctgggctt ctttccagac caccagctgg atcctgcctt cagagccaac
720
tccgccaatc cagactggga cttcaacccc aataaggaca catggcctga tgccaacaag
780
gtcggcggcc agaacctgtc taccagcaat cccctgggct tctttcctga ccaccagctg
840
gatccagcct tccgggccaa cactgctaac cctgattggg acttcaaccc taataaggat
900
acctggccag acgccaacaa ggtcggcgga agcggagcta ctaacttcag cctgctgaag
960
caggctggag acgtggagga gaaccctgga cctatgtcca ggtctgagag caagaagaat
1020
aggggaggaa gagaggaggt gctggagcag tgggtgaacg gccgcaagaa gctggaggag
1080
ctggagaggg agctgagaag ggcccgcaag aagatcaaga agctggaaga cgataatcct
1140
tggctgggca atgtgaaagg catcctgggc aagaaggaca aggatggaga gggagcacct
1200
ccagcaaaga gggcaagaac agaccagatg gagatcgatt ctggaccaag gaagcgccct
1260
ctgaggggag gcttcaccga ccgggagaga caggatcacc gccggagaaa ggccctgaag
1320
aacaagaaga agcagctgtc cgccggcggc aagtccctga gcaaagaaga ggaagaggag
1380
ctgaagaggc tgacccgcga ggacgaggag cggaagaagg aggagcacgg accaagcaga
1440
ctgggagtga atccttccga gggaggacca agaggagcac ccggaggagg cttcgtgcca
1500
tctatgcagg gcatccccga gagccggttt accagaacag gagagggcct ggacgtgagg
1560
ggctcccgcg gctttcctca ggacatcctg ttcccatctg atcccccttt tagcccacag
1620
tcctgtaggc cccagggcac taacctgagc acatccaacc cactgggctt ctttcctgat
1680
catcagctgg acccagcctt ccgcgccaac agcgccaacc ctgactggga cttcaaccca
1740
aataaggaca catggccaga tgctaacaag gtcggaggac aaaacctgtc taccagcaac
1800
cctctgggct tctttcccga tcatcagctg gaccccgcct tcagggccaa cacagccaat
1860
cccgactggg acttcaaccc gaataaggac acctggccag atgcaaacaa ggtcggagga
1920
agcggagcta ctaacttcag cctgctgaag caggctggag acgtggagga gaaccctgga
1980
cctatgagcc agtctgagac aaggaggggc cggagaggaa ccagggagga gacactggag
2040
aagtggatca ccgccagaaa gaaggccgag gagctggaga aggacctgcg gaagaccaga
2100
aagacaatca agaagctgga agaagagaac ccatggctgg gcaatatcgt gggcatcatc
2160
cgcaagggca aggacggcga gggagcacca ccagcaaaga ggccccgcac agatcagatg
2220
gaagtggata gcggccctgg caagaggcca cacaagtccg gcttcaccga caaggagagg
2280
gaggaccata ggcgccggaa ggccctggaa aacaagaaga agcaattatc cgccggcggc
2340
aagatcctgt ccaaagagga agaagaggag ctgagaaggc tgaccgacga ggatgaggag
2400
aggaaaagaa gggtggcagg accaagagtg ggcgacgtga atcccagcag aggcggacca
2460
agaggagcac ctggaggcgg cttcgtgccc cagatggccg gcgtgcccga gtctcctttt
2520
agcagaactg gagagggcct ggatatcagg ggaacacagg gctttccatg ggtgagccca
2580
tcccctccac agcagaggct gccactgctg gagtgcaccc ctcagggaac caacctgtct
2640
accagcaacc cgctgggctt ctttcccgac catcagctgg accctgcctt ccgcgccaac
2700
tccgccaacc ctgattggga cttcaacccg aataaggata cctggcccga cgctaacaag
2760
gtcggaggcc agaacctgtc cacctctaac cccttaggct tctttcccga tcaccagctg
2820
gatcccgcct tcagagccaa cactgctaac cccgattggg acttcaaccc gaataaggac
2880
acgtggccag acgctaacaa ggtcggggga agcggagcta ctaacttcag cctgctgaag
2940
caggctggag acgtggagga gaaccctgga cctatgtcgc agtccgagtc taagaagaat
3000
agaaggggcg gccgggagga tatcctggaa aaatggatca ccacacgcag aaaagctgaa
3060
gaactggaaa aggacctgag gaaggcccgc aagaccatca agaagctgga ggatgaaaat
3120
ccatggctgg gaaacatcat cggcatcatc agaaagggca aggacgggga aggcgcccca
3180
cctgcaaagc ggcctagaac cgatcagatg gaaatcgatt ctggcacagg caagcggcca
3240
cacaagagtg gcttcaccga taaggagaga gaggatcaca gaaggcgcaa ggccctggag
3300
aacaagaaga agcaattaag cagcggcggc aagaatctgt ccagagaaga agaggaggag
3360
ctgggcagac tgacagtgga ggacgaggag cggagaaggc gcgtggcagg accaaggacc
3420
ggcgatgtga acctgagcgg aggaggacct aggggagcac caggaggcgg cttcgtgcct
3480
aggatggagg gagtgccaga gtcccccttt accaggactg gcgagggcct ggacatcagg
3540
ggaaatcagg gattcccatg ggtgcggcct agcccaccac agcagagact gccactgctg
3600
gagtgtacac cccagggcac aaacctgagc acatccaatc cgctgggctt ctttccagat
3660
catcaattag atccagcctt cagggccaac tccgccaatc cggattggga cttcaacccg
3720
aataaggaca cttggcccga cgcaaacaag gtcggagggc aaaacctgtc taccagcaat
3780
ccacttggct tctttcctga ccatcagctg gatcccgcct ttcgcgccaa taccgccaat
3840
cctgactggg acttcaatcc taacaaagac acctggcccg acgcaaacaa agtgggatga
3900
<210> 19
<211> 2634
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-5
<400> 19
atggcctcac ggtcagagtc aaagaaaaat aggggggggc gggaagaaat cctggaacag
60
tgggtcggag cacggaaaaa actggaagag ctggagaggg acctgcgcaa gatcaagaag
120
aagatcaaga agctggagga ggagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggatc gggagggaga gggagcacca cctgcaaaga gggccagagc cgaccagatg
240
gaggtggata gcggccctag gaagcgccca ttcagaggcg agtttaccga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagcgga agcagctgag ctccggcggc
360
aagtccctgt ctaaggagga ggaggaggag ctgagaaagc tgacagagga ggacgagaga
420
agggagcgcc gggtggccgg cccaagggtg ggcggcgtga accccctgga gggaggaacc
480
aggggagcac ctggaggagg cttcgtgcca tctatgcagg gcgtgcctga gagcccattt
540
gccaggacag gagagggcct ggatgtgcgc ggcaatcagg gcttcccctg ggacatcctg
600
tttcctgccg atccaccctt cagcccacag tcctgcaggc ctcagagcag atccgagtct
660
aagaagaaca ggggaggaag agaggaggtg ctggagcagt gggtgaatgg ccggaagaag
720
ctggaggagc tggagcggga gctgagaagg gccagaaaga agatcaagaa gctggaagac
780
gataatcctt ggctgggcaa tgtgaaaggc atcctgggca agaaggacaa ggatggagag
840
ggagcacctc cagcaaagag ggcaagaacc gaccagatgg agatcgatag cggaccaagg
900
aagcgccctc tgagaggagg cttcacagac cgggagagac aggatcaccg ccggagaaag
960
gccctgaaga acaagaagaa gcagctgtcc gccggaggca agagcctgtc caaagaagag
1020
gaagaggagc tgaagaggct gacccgcgag gacgaggagc ggaagaagga ggagcacggc
1080
ccttccagac tgggcgtgaa tccatctgag ggaggaccaa ggggagcacc aggcggcggc
1140
ttcgtgccaa gcatgcaggg catccccgag tcccggttta ccagaacagg agagggcctg
1200
gacgtgaggg gctctcgcgg ctttcctcag gacatcctgt tcccaagcga tccccctttt
1260
tctccacaga gctgtcgccc ccagggaagc ggagctacta acttcagcct gctgaagcag
1320
gctggagacg tggaggagaa ccctggacct atgtctcaga gcgagacaag gaggggccgg
1380
agaggaacca gggaggagac actggagaag tggatcacag ccagaaagaa ggccgaggag
1440
ctggagaagg acctgcggaa gaccagaaag acaatcaaga agctggaaga agaaaatcca
1500
tggctgggaa atatcgtggg catcatcagg aagggcaagg acggcgaggg agcaccacca
1560
gccaagaggc ctcgcactga tcagatggag gtggattccg gccctggcaa gaggccacac
1620
aagtctggct tcacagacaa ggagagggag gaccataggc gccggaaggc cctggaaaac
1680
aagaagaagc aattatctgc cggcggcaag atcctgagca aagaggaaga ggaggagctg
1740
agaaggctga ccgacgagga tgaggagagg aagaggaggg tggcaggacc aagagtgggc
1800
gacgtgaatc ctagcagagg cggaccaaga ggcgccccag gcgggggctt cgtgccacag
1860
atggcaggag tgccagagtc ccctttttct aggaccggag agggcctgga tatcagggga
1920
acacagggct ttccatgggt gtccccatct cctccacagc agaggctgcc actgctggag
1980
tgcacccctc agagccagtc cgagtctaag aagaatagaa ggggcggccg cgaggacatc
2040
ctggagaagt ggatcaccac acgcagaaaa gctgaagaac tggaaaagga cctgaggaag
2100
gcccgcaaaa caatcaagaa gctggaggat gagaaccctt ggctgggcaa tatcatcgga
2160
attatcagga agggcaagga tggcgaaggc gccccacctg caaagcggcc aaggactgat
2220
cagatggaaa tcgatagcgg aacaggcaag cggccccaca agtccggctt caccgacaag
2280
gagagagagg atcacagaag gcgcaaggcc ctggagaaca agaagaagca attaagcagc
2340
ggcggcaaga atctgtccag agaagaagag gaggagctgg gcagactgac cgtggaggac
2400
gaggagcgga gaaggcgcgt ggcaggacct cgcacaggcg atgtgaacct gtccggagga
2460
ggacctaggg gagcaccagg aggcggcttc gtgccacgca tggagggcgt gccagagtct
2520
ccctttaccc gcaccggaga gggcctggac atcaggggca atcagggctt tccctgggtc
2580
cgcccctccc cccctcagca gagactgccc ctgctggaat gcacaccaca gtga
2634
<210> 20
<211> 2772
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-6
<400> 20
atggcctcac ggtcagagtc aaagaagaac agaggcggaa gagaagaaat cctggagcag
60
tgggtcggag cacggaaaaa gctggaagaa ctggagaggg acctgcgcaa gatcaagaag
120
aagatcaaga agctggagga ggagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggata gggagggaga gggagcacca cctgcaaaga gggccagagc cgaccagatg
240
gaggtggata gcggaccaag gaagcgcccc ttccgcggag agtttaccga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagagga agcagctgag ctccggcggc
360
aagtccctgt ctaaggagga ggaggaggag ctgcgcaagc tgacagagga ggacgagaga
420
agggagagga gggtggcagg accaagggtg ggaggagtga atcctctgga gggaggaacc
480
agaggagcac caggaggagg cttcgtgcca agcatgcagg gagtgccaga gtcccccttt
540
gccaggacag gagagggcct ggacgtgaga ggcaaccagg gcttcccttg ggacatcctg
600
tttccagccg atccaccctt cagccctcag tcctgcaggc cacagggaag cggagctact
660
aacttcagcc tgctgaagca ggctggagac gtggaggaga accctggacc tatgagccgg
720
tccgagtcta agaagaatag gggaggaaga gaggaggtgc tggagcagtg ggtgaacggc
780
agaaagaagc tggaggagct ggagagggag ctgagaaggg cccgcaagaa gatcaagaag
840
ctggaagacg ataatccttg gctgggcaat gtgaaaggca tcctgggcaa gaaggacaag
900
gatggagagg gagcacctcc agcaaagagg gcaagaaccg accagatgga gatcgatagc
960
ggacctagga agcgcccact gaggggaggc tttacagacc gggagagaca ggatcaccgc
1020
cggagaaagg ccctgaagaa caagaagaag cagctgtccg ccggaggcaa gagcctgtcc
1080
aaagaagagg aagaggagct gaagaggctg acccgcgagg acgaggagag gaagaaggag
1140
gagcacggac catctaggct gggagtgaat cccagcgagg gaggaccaag gggagcacct
1200
ggaggaggct tcgtgccctc catgcagggc atccctgagt ctcggtttac cagaaccggc
1260
gagggcctgg acgtgagggg cagccgcggc tttccacagg acatcctgtt cccctccgat
1320
cccccttttt ctccccagag ctgtcgccct caaggaagcg gagctactaa cttcagcctg
1380
ctgaagcagg ctggagacgt ggaggagaac cctggaccta tgtctcagag cgagacaagg
1440
aggggccgga gaggaaccag ggaggagaca ctggagaagt ggatcacagc ccgcaagaag
1500
gccgaggagc tggagaagga cctgcggaag accagaaaga caatcaagaa gctggaagaa
1560
gagaaccctt ggctgggcaa tatcgtgggc atcatcagga agggcaagga cggcgaggga
1620
gcaccaccag ccaagaggcc acgcactgat cagatggagg tggattctgg accaggcaag
1680
cggccccaca agagcggctt cacagacaag gagagagagg accataggcg ccggaaggcc
1740
ctggaaaaca agaagaagca attaagcgcc ggcggcaaga tcctgtccaa agaggaagag
1800
gaggagctga gaaggctgac cgacgaggat gaggagagga aaagaagggt ggcaggacct
1860
agggtgggcg acgtgaatcc aagcagggga ggacctagag gagcaccagg aggcggcttc
1920
gtgccacaga tggcaggagt gcctgagtcc ccattttctc ggaccggcga gggcctggat
1980
atcagaggca cacagggctt cccctgggtg tccccttctc ctccacagca gcggctgcct
2040
ctgctggagt gcacccctca gggaagcgga gctactaact tcagcctgct gaagcaggct
2100
ggagacgtgg aggagaaccc tggacctatg tcgcagagcg aatctaagaa gaatagaagg
2160
ggcggcagag aggatatcct ggagaagtgg atcaccacac gcagaaaagc tgaagaactg
2220
gaaaaggacc tgaggaaggc ccgcaagacc atcaagaagc tggaggatga aaatccatgg
2280
ctgggaaata tcatcggcat catccggaag ggcaaggacg gggaaggcgc cccacctgca
2340
aagcggccca ggactgatca gatggaaatc gattccggca caggcaagag gcctcacaag
2400
tctggcttca cagataaaga gcgcgaggat cacagaaggc gcaaggccct ggagaacaag
2460
aagaagcaat tatctagcgg cggcaagaat ctgtccagag aagaagagga ggagctgggc
2520
cgcctgaccg tggaggacga ggagcggaga aggcgcgtgg caggaccaag aacaggcgat
2580
gtgaacctgt ctggaggcgg cccaaggggc gcccccggcg gaggcttcgt gccaagaatg
2640
gaaggcgtgc cagagtcccc ttttacccgg acaggggaag gcctggacat tagaggcaat
2700
cagggctttc cctgggtgcg accaagcccc cctcagcagc gactgcctct gctggagtgt
2760
acccctcagt ga
2772
<210> 21
<211> 1569
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-7
<400> 21
atggcctcac ggtctgagtc aaagaagaat cgggggggaa gagaagaaat cctggaacag
60
tgggtcggcg cacggaaaaa actggaagaa ctggagcggg acctgagaaa gatcaagaag
120
aagatcaaga agctggagga agagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggatc gggagggcga gggagcacca cctgcaaaga gggcaagggc agaccagatg
240
gaggtggatt ccggacctag gaagcggccc ttccggggag agtttaccga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagcgga agcagctgag ctccggcggc
360
aagtctctga gcaaggagga ggaggaggag ctgagaaagc tgacagagga ggacgagaga
420
agggagcgcc gggtggccgg cccaagggtg ggcggcgtga accccctgga gggaggaacc
480
aggggagcac caggaggagg cttcgtgcct tctatgcagg gcgtgccaga gagccccttt
540
gccaggacag gagagggcct ggatgtgcgc ggcaatcagg gcttcccatg ggacatcctg
600
tttcccgccg atccaccctt ctcccctcag tcttgcaggc cacagtcccg ctctgagagc
660
aagaagaaca ggggaggaag ggaggaggtg ctggagcagt gggtgaatgg caggaagaag
720
ctggaggagc tggagcggga gctgagaagg gccagaaaga agatcaagaa gctggaagac
780
gataatcctt ggctgggcaa tgtgaaaggc atcctgggca agaaggacaa ggatggagag
840
ggagcacctc cagcaaagag ggcacgcacc gaccagatgg agatcgattc cggaccaagg
900
aagcggcccc tgaggggagg cttcacagac agggagcgcc aggatcaccg ccggagaaag
960
gccctgaaga acaagaagaa gcagctgtct gccggcggca agtccctgtc taaagaagag
1020
gaggaggagc tgaagcggct gaccagagag gacgaggagc ggaagaagga ggagcacggc
1080
ccttccagac tgggcgtgaa tccatctgag ggaggaccaa gaggcgcccc tggcggaggc
1140
ttcgtgccta gcatgcaggg catcccagag tccaggttta ccagaaccgg agagggcctg
1200
gacgtgcggg gctctagagg ctttccccag gacatcctgt tccctagcga tccccctttt
1260
agcccccagt cctgtaggcc tcagggcacc aacctgagca catccaatcc actgggcttc
1320
tttccagacc accagctgga tccagccttc cgcgccaaca gcgccaatcc agactgggac
1380
ttcaacccca ataaggacac ctggcctgat gccaacaagg tcggcggcca gaacctgtct
1440
acaagcaatc ctctgggctt ctttcctgat caccagctgg atcctgcctt tcgggccaat
1500
acagccaacc ctgactggga cttcaatcct aacaaagaca cttggcccga tgctaataag
1560
gtcggctga
1569
<210> 22
<211> 1569
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-8
<400> 22
atggccagtc agagcgagac ccgcagagga cggagaggaa cacgagaaga gacactggag
60
aaatggatta cagcacggaa gaaggcagaa gagctggaga aggacctgag gaagacccgc
120
aagacaatca agaagctgga ggaggagaac ccctggctgg gcaatatcgt gggcatcatc
180
aggaagggca aggatggaga gggagcacca cctgccaaga ggcctcgcac agaccagatg
240
gaggtggata gcggaccagg caagcggcct cacaagtccg gcttcaccga caaggagaga
300
gaggatcacc ggagaaggaa ggccctggag aacaagaaga agcagctgtc cgccggcggc
360
aagatcctgt ctaaggagga ggaggaggag ctgcgccggc tgacagacga ggatgaggag
420
aggaagagaa gggtggcagg accaagggtg ggcgacgtga atccttctag gggaggacca
480
aggggagcac caggaggagg cttcgtgcct cagatggccg gcgtgccaga gtctcccttt
540
agccggacag gcgagggcct ggatatcaga ggcacccagg gctttccttg ggtgtctcca
600
agcccaccac agcagcggct gccactgctg gagtgcacac cccagtccca gtctgagagc
660
aagaagaaca ggaggggagg aagagaggac atcctggaga agtggatcac cacaagaagg
720
aaggccgagg agctggagaa ggacctgcgg aaggccagaa agaccatcaa gaagctggag
780
gatgaaaatc cttggctggg aaatatcatc ggaattatta gaaaaggcaa ggacggagag
840
ggagcacctc cagcaaagcg gccaagaaca gaccagatgg agatcgattc tggaaccggc
900
aagaggcccc acaagagtgg cttcaccgat aaggagcgcg aggatcaccg ccggagaaag
960
gccctggaaa acaagaagaa gcaattaagc tccggcggca agaatctgag cagagaagaa
1020
gaggaggagc tgggccgcct gacagtggag gacgaggaga ggcgccggag agtggcagga
1080
cctagaaccg gcgatgtgaa cctgtccgga ggcggcccaa ggggagcacc tggaggcggc
1140
ttcgtgccac gcatggaggg cgtgcctgag tctcccttca ccaggacagg agagggcctg
1200
gacatcagag gcaatcaggg attcccatgg gtgcggccca gcccacctca gcagagactg
1260
cctctgctgg agtgtacccc acagggcaca aacctgtcca cctctaatcc tctgggcttc
1320
tttccagacc accagctgga tccagccttc agggccaact ccgccaaccc tgactgggac
1380
ttcaacccta ataaggacac atggccagat gccaacaagg tcggcggcca gaacctgagc
1440
acctccaatc ccctgggctt ctttcctgac caccagctgg atcccgcctt tcgcgccaat
1500
accgccaatc ccgactggga cttcaatcca aataaggaca cctggcccga tgctaacaaa
1560
gtgggatga
1569
<210> 23
<211> 1287
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-9
<400> 23
atggccagtc ggagcgaatc aaagaaaaat agagggggaa gagaagaaat cctggagcag
60
tgggtcgggg cacggaaaaa actggaagaa ctggagcggg acctgagaaa gatcaagaag
120
aagatcaaga agctggagga agagaacccc tggctgggca atatcaaggg catcctgggc
180
aagaaggata gggagggcga gggagcacca cctgcaaaga gggcaagggc agaccagatg
240
gaggtggatt ccggaccaag gaagcggccc ttccggggag agtttaccga caaggagcgg
300
agagatcaca ggcgccggaa ggccctggag aacaagcgga agcagctgag ctccggcggc
360
aagtctctga gcaaggagga ggaggaggag ctgagaaagc tgacagagga ggacgagaga
420
agggagagga gggtggcagg acctagggtg ggaggcgtga acccactgga gggaggaacc
480
aggggagcac ctggaggagg ctttgtgcca tctatgcagg gagtgccaga gagccctttc
540
gccaggacag gagagggcct ggatgtgcgc ggcaatcagg gcttcccctg ggacatcctg
600
tttcctgccg atccaccctt cagcccacag tcctgcaggc cacagtcccg ctctgagagc
660
aagaagaaca ggggaggaag ggaggaggtg ctggagcagt gggtgaatgg ccggaagaag
720
ctggaggagc tggagcggga gctgagaagg gccagaaaga agatcaagaa gctggaagac
780
gataatcctt ggctgggcaa tgtgaaaggc atcctgggca agaaggacaa ggatggagag
840
ggagcacctc cagcaaagag ggcacgcacc gaccagatgg agatcgattc tggacctagg
900
aagcggcccc tgagaggagg ctttacagac agggagcgcc aggatcaccg ccggagaaag
960
gccctgaaga acaagaagaa gcagctgagc gccggcggca agtccctgtc taaagaagag
1020
gaggaggagc tgaagcggct gaccagagag gacgaggagc ggaagaagga ggagcacgga
1080
ccatccagac tgggagtgaa tccttctgag ggaggaccaa gaggcgcccc aggcggcggc
1140
tttgtgccaa gcatgcaggg catccccgag tccaggttca ccagaaccgg cgaaggcctg
1200
gatgtgcggg gcagcagagg cttcccccag gatattctgt ttccctccga cccccccttc
1260
agtccccagt cttgccgacc tcagtga
1287
<210> 24
<211> 1287
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность ДНК Дельта-10
<400> 24
atggcctcac agagcgaaac acggcggggg cggaggggaa ctagagagga aacactggaa
60
aaatggatta cagcacggaa aaaggcagag gaactggaga aggacctgag gaagacccgc
120
aagacaatca agaagctgga ggaggagaac ccatggctgg gcaatatcgt gggcatcatc
180
cggaagggca aggatggaga gggagcacca cctgcaaaga ggccccgcac cgaccagatg
240
gaggtggatt ctggccctgg caagaggcca cacaagagcg gcttcacaga caaggagcgc
300
gaggatcacc ggagaaggaa ggccctggag aacaagaaga agcagctgag cgccggcggc
360
aagatcctgt ccaaggagga ggaggaggag ctgcgccggc tgaccgacga ggatgaggag
420
cggaagagaa gggtggcagg accaagagtg ggcgacgtga atccctctag gggaggacca
480
aggggagcac ctggaggagg cttcgtgcct cagatggcag gagtgccaga gtcccctttt
540
tctaggaccg gagagggcct ggatatcagg ggaacacagg gctttccatg ggtgtctcca
600
agcccaccac agcagaggct gccactgctg gagtgcaccc ctcagtccca gtctgagagc
660
aagaagaaca ggaggggagg aagggaggac atcctggaga agtggatcac cacaagaagg
720
aaggccgagg agctggagaa ggacctgcgg aaggccagaa aaacaatcaa gaagctggaa
780
gatgagaacc cctggctggg caatatcatc ggcatcatca gaaaaggcaa ggacggcgag
840
ggagcacctc cagcaaagcg gcctagaacc gaccagatgg agatcgattc cggcacaggc
900
aagcggccac acaagtctgg cttcaccgac aaggagagag aggatcaccg ccggagaaag
960
gccctggaaa acaagaagaa gcaattaagc tccggcggca agaatctgag cagagaagaa
1020
gaggaggagc tgggcagact gaccgtggag gacgaggaga ggcgccggag agtggcagga
1080
cccagaacag gcgatgtgaa cctgagcgga ggaggaccta ggggagcacc aggaggcggc
1140
ttcgtgccta gaatggaggg cgtgccagag tcccccttta ccaggacagg agagggcctg
1200
gacatcaggg gcaatcaggg ctttccctgg gtccgccctt caccaccaca gcagagactg
1260
cccctgctgg aatgcacacc acagtga
1287
<210> 25
<211> 1065
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-1
<400> 25
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg
210 215 220
Gly Gly Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys
225 230 235 240
Leu Glu Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys
245 250 255
Lys Leu Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu
260 265 270
Gly Lys Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu
290 295 300
Arg Gly Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu
325 330 335
Ser Lys Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu
340 345 350
Glu Arg Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro
355 360 365
Ser Glu Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser
370 375 380
Met Gln Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Val Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser
405 410 415
Asp Pro Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Thr Asn Leu
420 425 430
Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro
435 440 445
Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn
450 455 460
Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser
465 470 475 480
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala
485 490 495
Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys
500 505 510
Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Ser Gly Ala Thr Asn
515 520 525
Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
530 535 540
Met Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu Glu
545 550 555 560
Thr Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu Glu
565 570 575
Lys Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu Glu
580 585 590
Asn Pro Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys Asp
595 600 605
Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu
610 615 620
Val Asp Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp
625 630 635 640
Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys
645 650 655
Lys Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu Glu
660 665 670
Glu Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg Val
675 680 685
Ala Gly Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro Arg
690 695 700
Gly Ala Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro Glu
705 710 715 720
Ser Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr Gln
725 730 735
Gly Phe Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu
740 745 750
Leu Glu Cys Thr Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg
755 760 765
Gly Gly Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys
770 775 780
Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys
785 790 795 800
Lys Leu Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile
805 810 815
Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg
820 825 830
Thr Asp Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His Lys
835 840 845
Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala
850 855 860
Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu Ser
865 870 875 880
Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu Glu
885 890 895
Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn Leu Ser
900 905 910
Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Arg Met
915 920 925
Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly Leu Asp
930 935 940
Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro Pro Gln
945 950 955 960
Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln Gly Thr Asn Leu Ser
965 970 975
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala
980 985 990
Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys
995 1000 1005
Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser
1010 1015 1020
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro
1025 1030 1035
Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro
1040 1045 1050
Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
1055 1060 1065
<210> 26
<211> 1065
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-2
<400> 26
Met Ala Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro
1 5 10 15
Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp
20 25 30
Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val
35 40 45
Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp
50 55 60
His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp
65 70 75 80
Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
85 90 95
Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Ile Leu
100 105 110
Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu Arg Asp
115 120 125
Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu Asn Pro
130 135 140
Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg Glu Gly
145 150 155 160
Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met Glu Val
165 170 175
Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr Asp Lys
180 185 190
Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Arg Lys
195 200 205
Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu
210 215 220
Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg Val Ala
225 230 235 240
Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr Arg Gly
245 250 255
Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro Glu Ser
260 265 270
Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn Gln Gly
275 280 285
Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser Pro Gln
290 295 300
Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly
305 310 315 320
Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys Leu Glu
325 330 335
Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys Lys Leu
340 345 350
Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu Gly Lys
355 360 365
Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Thr
370 375 380
Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu Arg Gly
385 390 395 400
Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys Ala Leu
405 410 415
Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu Ser Lys
420 425 430
Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu Glu Arg
435 440 445
Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro Ser Glu
450 455 460
Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln
465 470 475 480
Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu Asp Val
485 490 495
Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser Asp Pro
500 505 510
Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Ser Gly Ala Thr Asn
515 520 525
Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
530 535 540
Met Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp
545 550 555 560
His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp
565 570 575
Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
580 585 590
Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His
595 600 605
Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp
610 615 620
Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Ser
625 630 635 640
Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu Glu Thr Leu
645 650 655
Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu Glu Lys Asp
660 665 670
Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu Glu Asn Pro
675 680 685
Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys Asp Gly Glu
690 695 700
Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu Val Asp
705 710 715 720
Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp Lys Glu
725 730 735
Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys Gln
740 745 750
Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu Glu Glu Leu
755 760 765
Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg Val Ala Gly
770 775 780
Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro Arg Gly Ala
785 790 795 800
Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro Glu Ser Pro
805 810 815
Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr Gln Gly Phe
820 825 830
Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu
835 840 845
Cys Thr Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg Gly Gly
850 855 860
Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys Ala Glu
865 870 875 880
Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys Lys Leu
885 890 895
Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile Arg Lys
900 905 910
Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp
915 920 925
Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His Lys Ser Gly
930 935 940
Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu
945 950 955 960
Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu Ser Arg Glu
965 970 975
Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu Glu Arg Arg
980 985 990
Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn Leu Ser Gly Gly
995 1000 1005
Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Arg Met Glu
1010 1015 1020
Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly Leu Asp
1025 1030 1035
Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro Pro
1040 1045 1050
Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln
1055 1060 1065
<210> 27
<211> 1253
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-3
<400> 27
Met Ala Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro
1 5 10 15
Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp
20 25 30
Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val
35 40 45
Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp
50 55 60
His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp
65 70 75 80
Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
85 90 95
Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Ile Leu
100 105 110
Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu Arg Asp
115 120 125
Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu Asn Pro
130 135 140
Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg Glu Gly
145 150 155 160
Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met Glu Val
165 170 175
Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr Asp Lys
180 185 190
Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Arg Lys
195 200 205
Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu
210 215 220
Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg Val Ala
225 230 235 240
Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr Arg Gly
245 250 255
Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro Glu Ser
260 265 270
Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn Gln Gly
275 280 285
Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser Pro Gln
290 295 300
Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly
305 310 315 320
Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys Leu Glu
325 330 335
Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys Lys Leu
340 345 350
Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu Gly Lys
355 360 365
Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Thr
370 375 380
Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu Arg Gly
385 390 395 400
Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys Ala Leu
405 410 415
Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu Ser Lys
420 425 430
Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu Glu Arg
435 440 445
Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro Ser Glu
450 455 460
Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln
465 470 475 480
Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu Asp Val
485 490 495
Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser Asp Pro
500 505 510
Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Thr Asn Leu Ser Thr
515 520 525
Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe
530 535 540
Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp
545 550 555 560
Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser Thr Ser
565 570 575
Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg
580 585 590
Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr
595 600 605
Trp Pro Asp Ala Asn Lys Val Gly Gly Ser Gly Ala Thr Asn Phe Ser
610 615 620
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Gly
625 630 635 640
Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln
645 650 655
Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe
660 665 670
Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln
675 680 685
Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu
690 695 700
Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn
705 710 715 720
Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Ser Gln Ser
725 730 735
Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu Glu Thr Leu Glu Lys
740 745 750
Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg
755 760 765
Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu Glu Asn Pro Trp Leu
770 775 780
Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala
785 790 795 800
Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu Val Asp Ser Gly
805 810 815
Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu
820 825 830
Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser
835 840 845
Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu Glu Glu Leu Arg Arg
850 855 860
Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg Val Ala Gly Pro Arg
865 870 875 880
Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro Arg Gly Ala Pro Gly
885 890 895
Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro Glu Ser Pro Phe Ser
900 905 910
Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr Gln Gly Phe Pro Trp
915 920 925
Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr
930 935 940
Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg Gly Gly Arg Glu
945 950 955 960
Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys Ala Glu Glu Leu
965 970 975
Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys Lys Leu Glu Asp
980 985 990
Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile Arg Lys Gly Lys
995 1000 1005
Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln
1010 1015 1020
Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His Lys Ser Gly
1025 1030 1035
Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu
1040 1045 1050
Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu Ser
1055 1060 1065
Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu
1070 1075 1080
Glu Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn
1085 1090 1095
Leu Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val
1100 1105 1110
Pro Arg Met Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly
1115 1120 1125
Glu Gly Leu Asp Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg
1130 1135 1140
Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro
1145 1150 1155
Gln Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro
1160 1165 1170
Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro
1175 1180 1185
Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn
1190 1195 1200
Lys Val Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe
1205 1210 1215
Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala
1220 1225 1230
Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp
1235 1240 1245
Ala Asn Lys Val Gly
1250
<210> 28
<211> 1299
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-4
<400> 28
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Gly Thr Asn Leu Ser Thr Ser Asn Pro
210 215 220
Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn
225 230 235 240
Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro
245 250 255
Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu
260 265 270
Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr
275 280 285
Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp
290 295 300
Ala Asn Lys Val Gly Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
305 310 315 320
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Ser Arg Ser Glu
325 330 335
Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Val Leu Glu Gln Trp Val
340 345 350
Asn Gly Arg Lys Lys Leu Glu Glu Leu Glu Arg Glu Leu Arg Arg Ala
355 360 365
Arg Lys Lys Ile Lys Lys Leu Glu Asp Asp Asn Pro Trp Leu Gly Asn
370 375 380
Val Lys Gly Ile Leu Gly Lys Lys Asp Lys Asp Gly Glu Gly Ala Pro
385 390 395 400
Pro Ala Lys Arg Ala Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Pro
405 410 415
Arg Lys Arg Pro Leu Arg Gly Gly Phe Thr Asp Arg Glu Arg Gln Asp
420 425 430
His Arg Arg Arg Lys Ala Leu Lys Asn Lys Lys Lys Gln Leu Ser Ala
435 440 445
Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu Leu Lys Arg Leu
450 455 460
Thr Arg Glu Asp Glu Glu Arg Lys Lys Glu Glu His Gly Pro Ser Arg
465 470 475 480
Leu Gly Val Asn Pro Ser Glu Gly Gly Pro Arg Gly Ala Pro Gly Gly
485 490 495
Gly Phe Val Pro Ser Met Gln Gly Ile Pro Glu Ser Arg Phe Thr Arg
500 505 510
Thr Gly Glu Gly Leu Asp Val Arg Gly Ser Arg Gly Phe Pro Gln Asp
515 520 525
Ile Leu Phe Pro Ser Asp Pro Pro Phe Ser Pro Gln Ser Cys Arg Pro
530 535 540
Gln Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp
545 550 555 560
His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp
565 570 575
Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
580 585 590
Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His
595 600 605
Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp
610 615 620
Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly
625 630 635 640
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
645 650 655
Glu Asn Pro Gly Pro Met Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg
660 665 670
Gly Thr Arg Glu Glu Thr Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys
675 680 685
Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys
690 695 700
Lys Leu Glu Glu Glu Asn Pro Trp Leu Gly Asn Ile Val Gly Ile Ile
705 710 715 720
Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg
725 730 735
Thr Asp Gln Met Glu Val Asp Ser Gly Pro Gly Lys Arg Pro His Lys
740 745 750
Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala
755 760 765
Leu Glu Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser
770 775 780
Lys Glu Glu Glu Glu Glu Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu
785 790 795 800
Arg Lys Arg Arg Val Ala Gly Pro Arg Val Gly Asp Val Asn Pro Ser
805 810 815
Arg Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Gln Met
820 825 830
Ala Gly Val Pro Glu Ser Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp
835 840 845
Ile Arg Gly Thr Gln Gly Phe Pro Trp Val Ser Pro Ser Pro Pro Gln
850 855 860
Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln Gly Thr Asn Leu Ser
865 870 875 880
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala
885 890 895
Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys
900 905 910
Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser Thr
915 920 925
Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe
930 935 940
Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp
945 950 955 960
Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Ser Gly Ala Thr Asn Phe
965 970 975
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
980 985 990
Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg Gly Gly Arg Glu Asp Ile
995 1000 1005
Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys Ala Glu Glu Leu Glu
1010 1015 1020
Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys Lys Leu Glu Asp
1025 1030 1035
Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile Arg Lys Gly
1040 1045 1050
Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp
1055 1060 1065
Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His Lys Ser
1070 1075 1080
Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala
1085 1090 1095
Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu
1100 1105 1110
Ser Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp
1115 1120 1125
Glu Glu Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val
1130 1135 1140
Asn Leu Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe
1145 1150 1155
Val Pro Arg Met Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr
1160 1165 1170
Gly Glu Gly Leu Asp Ile Arg Gly Asn Gln Gly Phe Pro Trp Val
1175 1180 1185
Arg Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr
1190 1195 1200
Pro Gln Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe
1205 1210 1215
Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn
1220 1225 1230
Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala
1235 1240 1245
Asn Lys Val Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly
1250 1255 1260
Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr
1265 1270 1275
Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro
1280 1285 1290
Asp Ala Asn Lys Val Gly
1295
<210> 29
<211> 877
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-5
<400> 29
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg
210 215 220
Gly Gly Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys
225 230 235 240
Leu Glu Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys
245 250 255
Lys Leu Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu
260 265 270
Gly Lys Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu
290 295 300
Arg Gly Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu
325 330 335
Ser Lys Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu
340 345 350
Glu Arg Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro
355 360 365
Ser Glu Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser
370 375 380
Met Gln Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Val Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser
405 410 415
Asp Pro Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Ser Gly Ala
420 425 430
Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro
435 440 445
Gly Pro Met Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg
450 455 460
Glu Glu Thr Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu
465 470 475 480
Leu Glu Lys Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu
485 490 495
Glu Glu Asn Pro Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly
500 505 510
Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln
515 520 525
Met Glu Val Asp Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe
530 535 540
Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn
545 550 555 560
Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu
565 570 575
Glu Glu Glu Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg
580 585 590
Arg Val Ala Gly Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly
595 600 605
Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val
610 615 620
Pro Glu Ser Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly
625 630 635 640
Thr Gln Gly Phe Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu
645 650 655
Pro Leu Leu Glu Cys Thr Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn
660 665 670
Arg Arg Gly Gly Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg
675 680 685
Arg Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr
690 695 700
Ile Lys Lys Leu Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly
705 710 715 720
Ile Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg
725 730 735
Pro Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro
740 745 750
His Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg
755 760 765
Lys Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn
770 775 780
Leu Ser Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp
785 790 795 800
Glu Glu Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn
805 810 815
Leu Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro
820 825 830
Arg Met Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly
835 840 845
Leu Asp Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro
850 855 860
Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln
865 870 875
<210> 30
<211> 923
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-6
<400> 30
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Gly Ser Gly Ala Thr Asn Phe Ser Leu
210 215 220
Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Ser Arg
225 230 235 240
Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Val Leu Glu Gln
245 250 255
Trp Val Asn Gly Arg Lys Lys Leu Glu Glu Leu Glu Arg Glu Leu Arg
260 265 270
Arg Ala Arg Lys Lys Ile Lys Lys Leu Glu Asp Asp Asn Pro Trp Leu
275 280 285
Gly Asn Val Lys Gly Ile Leu Gly Lys Lys Asp Lys Asp Gly Glu Gly
290 295 300
Ala Pro Pro Ala Lys Arg Ala Arg Thr Asp Gln Met Glu Ile Asp Ser
305 310 315 320
Gly Pro Arg Lys Arg Pro Leu Arg Gly Gly Phe Thr Asp Arg Glu Arg
325 330 335
Gln Asp His Arg Arg Arg Lys Ala Leu Lys Asn Lys Lys Lys Gln Leu
340 345 350
Ser Ala Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu Leu Lys
355 360 365
Arg Leu Thr Arg Glu Asp Glu Glu Arg Lys Lys Glu Glu His Gly Pro
370 375 380
Ser Arg Leu Gly Val Asn Pro Ser Glu Gly Gly Pro Arg Gly Ala Pro
385 390 395 400
Gly Gly Gly Phe Val Pro Ser Met Gln Gly Ile Pro Glu Ser Arg Phe
405 410 415
Thr Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Ser Arg Gly Phe Pro
420 425 430
Gln Asp Ile Leu Phe Pro Ser Asp Pro Pro Phe Ser Pro Gln Ser Cys
435 440 445
Arg Pro Gln Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
450 455 460
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Ser Gln Ser Glu Thr Arg
465 470 475 480
Arg Gly Arg Arg Gly Thr Arg Glu Glu Thr Leu Glu Lys Trp Ile Thr
485 490 495
Ala Arg Lys Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Thr Arg
500 505 510
Lys Thr Ile Lys Lys Leu Glu Glu Glu Asn Pro Trp Leu Gly Asn Ile
515 520 525
Val Gly Ile Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala
530 535 540
Lys Arg Pro Arg Thr Asp Gln Met Glu Val Asp Ser Gly Pro Gly Lys
545 550 555 560
Arg Pro His Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg
565 570 575
Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly
580 585 590
Lys Ile Leu Ser Lys Glu Glu Glu Glu Glu Leu Arg Arg Leu Thr Asp
595 600 605
Glu Asp Glu Glu Arg Lys Arg Arg Val Ala Gly Pro Arg Val Gly Asp
610 615 620
Val Asn Pro Ser Arg Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe
625 630 635 640
Val Pro Gln Met Ala Gly Val Pro Glu Ser Pro Phe Ser Arg Thr Gly
645 650 655
Glu Gly Leu Asp Ile Arg Gly Thr Gln Gly Phe Pro Trp Val Ser Pro
660 665 670
Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln Gly
675 680 685
Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala Gly Asp Val Glu
690 695 700
Glu Asn Pro Gly Pro Met Ser Gln Ser Glu Ser Lys Lys Asn Arg Arg
705 710 715 720
Gly Gly Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg Lys
725 730 735
Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile Lys
740 745 750
Lys Leu Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile Ile
755 760 765
Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg
770 775 780
Thr Asp Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His Lys
785 790 795 800
Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala
805 810 815
Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu Ser
820 825 830
Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu Glu
835 840 845
Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn Leu Ser
850 855 860
Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Arg Met
865 870 875 880
Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly Leu Asp
885 890 895
Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro Pro Gln
900 905 910
Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln
915 920
<210> 31
<211> 522
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-7
<400> 31
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg
210 215 220
Gly Gly Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys
225 230 235 240
Leu Glu Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys
245 250 255
Lys Leu Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu
260 265 270
Gly Lys Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu
290 295 300
Arg Gly Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu
325 330 335
Ser Lys Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu
340 345 350
Glu Arg Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro
355 360 365
Ser Glu Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser
370 375 380
Met Gln Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Val Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser
405 410 415
Asp Pro Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Thr Asn Leu
420 425 430
Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro
435 440 445
Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn
450 455 460
Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser
465 470 475 480
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala
485 490 495
Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys
500 505 510
Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
515 520
<210> 32
<211> 522
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-8
<400> 32
Met Ala Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu
1 5 10 15
Glu Thr Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu
20 25 30
Glu Lys Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu
35 40 45
Glu Asn Pro Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys
50 55 60
Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr
85 90 95
Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Lys Lys Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro
165 170 175
Glu Ser Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr
180 185 190
Gln Gly Phe Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro
195 200 205
Leu Leu Glu Cys Thr Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn Arg
210 215 220
Arg Gly Gly Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg
225 230 235 240
Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile
245 250 255
Lys Lys Leu Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile
260 265 270
Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His
290 295 300
Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu
325 330 335
Ser Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu
340 345 350
Glu Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn Leu
355 360 365
Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Arg
370 375 380
Met Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro Pro
405 410 415
Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln Gly Thr Asn Leu
420 425 430
Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro
435 440 445
Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn
450 455 460
Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser
465 470 475 480
Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala
485 490 495
Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys
500 505 510
Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
515 520
<210> 33
<211> 428
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-9
<400> 33
Met Ala Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu
1 5 10 15
Ile Leu Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu
20 25 30
Arg Asp Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu
35 40 45
Asn Pro Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg
50 55 60
Glu Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr
85 90 95
Asp Lys Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Arg Lys Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro
165 170 175
Glu Ser Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn
180 185 190
Gln Gly Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser
195 200 205
Pro Gln Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg
210 215 220
Gly Gly Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys
225 230 235 240
Leu Glu Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys
245 250 255
Lys Leu Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu
260 265 270
Gly Lys Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu
290 295 300
Arg Gly Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu
325 330 335
Ser Lys Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu
340 345 350
Glu Arg Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro
355 360 365
Ser Glu Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser
370 375 380
Met Gln Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Val Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser
405 410 415
Asp Pro Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln
420 425
<210> 34
<211> 428
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность Дельта-10
<400> 34
Met Ala Ser Gln Ser Glu Thr Arg Arg Gly Arg Arg Gly Thr Arg Glu
1 5 10 15
Glu Thr Leu Glu Lys Trp Ile Thr Ala Arg Lys Lys Ala Glu Glu Leu
20 25 30
Glu Lys Asp Leu Arg Lys Thr Arg Lys Thr Ile Lys Lys Leu Glu Glu
35 40 45
Glu Asn Pro Trp Leu Gly Asn Ile Val Gly Ile Ile Arg Lys Gly Lys
50 55 60
Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met
65 70 75 80
Glu Val Asp Ser Gly Pro Gly Lys Arg Pro His Lys Ser Gly Phe Thr
85 90 95
Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys
100 105 110
Lys Lys Gln Leu Ser Ala Gly Gly Lys Ile Leu Ser Lys Glu Glu Glu
115 120 125
Glu Glu Leu Arg Arg Leu Thr Asp Glu Asp Glu Glu Arg Lys Arg Arg
130 135 140
Val Ala Gly Pro Arg Val Gly Asp Val Asn Pro Ser Arg Gly Gly Pro
145 150 155 160
Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Gln Met Ala Gly Val Pro
165 170 175
Glu Ser Pro Phe Ser Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Thr
180 185 190
Gln Gly Phe Pro Trp Val Ser Pro Ser Pro Pro Gln Gln Arg Leu Pro
195 200 205
Leu Leu Glu Cys Thr Pro Gln Ser Gln Ser Glu Ser Lys Lys Asn Arg
210 215 220
Arg Gly Gly Arg Glu Asp Ile Leu Glu Lys Trp Ile Thr Thr Arg Arg
225 230 235 240
Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Ala Arg Lys Thr Ile
245 250 255
Lys Lys Leu Glu Asp Glu Asn Pro Trp Leu Gly Asn Ile Ile Gly Ile
260 265 270
Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Pro
275 280 285
Arg Thr Asp Gln Met Glu Ile Asp Ser Gly Thr Gly Lys Arg Pro His
290 295 300
Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg Lys
305 310 315 320
Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser Ser Gly Gly Lys Asn Leu
325 330 335
Ser Arg Glu Glu Glu Glu Glu Leu Gly Arg Leu Thr Val Glu Asp Glu
340 345 350
Glu Arg Arg Arg Arg Val Ala Gly Pro Arg Thr Gly Asp Val Asn Leu
355 360 365
Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Arg
370 375 380
Met Glu Gly Val Pro Glu Ser Pro Phe Thr Arg Thr Gly Glu Gly Leu
385 390 395 400
Asp Ile Arg Gly Asn Gln Gly Phe Pro Trp Val Arg Pro Ser Pro Pro
405 410 415
Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln
420 425
<210> 35
<211> 3434
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность нуклеиновой кислоты слитых
Дельта-7/Дельта-8 дикого типа
<400> 35
aagcttgcac catggccggc accaacctga gcaccagcaa cccgctgggc ttttttccgg
60
atcatcagct ggatccggcg tttcgcgcga acagcgcgaa cccggattgg gattttaacc
120
cgaacaaaga tacctggccg gatgcgaaca aagtgggcgg ccagaacctg agcaccagca
180
acccgctggg cttttttccg gatcatcagc tggatccggc gtttcgcgcg aacaccgcga
240
acccggattg ggattttaac ccgaacaaag atacctggcc ggatgcgaac aaagtgggca
300
gccgcagcga aagcaaaaaa aaccgcggcg gccgcgaaga aattctggaa cagtgggtgg
360
gcgcgcgcaa aaaactggaa gaactggaac gcgatctgcg caaaattaaa aaaaaaatta
420
aaaaactgga agaagaaaac ccgtggctgg gcaacattaa aggcattctg ggcaaaaaag
480
atcgcgaagg cgaaggcgcg ccgccggcga aacgcgcgcg cgcggatcag atggaagtgg
540
atagcggccc gcgcaaacgc ccgtttcgcg gcgaatttac cgataaagaa cgccgcgatc
600
atcgccgccg caaagcgctg gaaaacaaac gcaaacagct gagcagcggc ggcaaaagcc
660
tgagcaaaga agaagaagaa gaactgcgca aactgaccga agaagatgaa cgccgcgaac
720
gccgcgtggc gggcccgcgc gtgggcggcg tgaacccgct ggaaggcggc acccgcggcg
780
cgccgggcgg cggctttgtg ccgagcatgc agggcgtgcc ggaaagcccg tttgcgcgca
840
ccggcgaagg cctggatgtg cgcggcaacc agggctttcc gtgggatatt ctgtttccgg
900
cggatccgcc gtttagcccg cagagctgcc gcccgcagag ccgcagcgaa agcaaaaaaa
960
accgcggcgg ccgcgaagaa gtgctggaac agtgggtgaa cggccgcaaa aaactggaag
1020
aactggaacg cgaactgcgc cgcgcgcgca aaaaaattaa aaaactggaa gatgataacc
1080
cgtggctggg caacgtgaaa ggcattctgg gcaaaaaaga taaagatggc gaaggcgcgc
1140
cgccggcgaa acgcgcgcgc accgatcaga tggaaattga tagcggcccg cgcaaacgcc
1200
cgctgcgcgg cggctttacc gatcgcgaac gccaggatca tcgccgccgc aaagcgctga
1260
aaaacaaaaa aaaacagctg agcgcgggcg gcaaaagcct gagcaaagaa gaagaagaag
1320
aactgaaacg cctgacccgc gaagatgaag aacgcaaaaa agaagaacat ggcccgagcc
1380
gcctgggcgt gaacccgagc gaaggcggcc cgcgcggcgc gccgggcggc ggctttgtgc
1440
cgagcatgca gggcattccg gaaagccgct ttacccgcac cggcgaaggc ctggatgtgc
1500
gcggcagccg cggctttccg caggatattc tgtttccgag cgatccgccg tttagcccgc
1560
agagctgccg cccgcagggc accaacctga gcaccagcaa cccgctgggc ttttttccgg
1620
atcatcagct ggatccggcg tttcgcgcga acagcgcgaa cccggattgg gattttaacc
1680
cgaacaaaga tacctggccg gatgcgaaca aagtgggcgg ccagaacctg agcaccagca
1740
acccgctggg cttttttccg gatcatcagc tggatccggc gtttcgcgcg aacaccgcga
1800
acccggattg ggattttaac ccgaacaaag atacctggcc ggatgcgaac aaagtgggca
1860
gccagagcga aacccgccgc ggccgccgcg gcacccgcga agaaaccctg gaaaaatgga
1920
ttaccgcgcg caaaaaagcg gaagaactgg aaaaagatct gcgcaaaacc cgcaaaacca
1980
ttaaaaaact ggaagaagaa aacccgtggc tgggcaacat tgtgggcatt attcgcaaag
2040
gcaaagatgg cgaaggcgcg ccgccggcga aacgcccgcg caccgatcag atggaagtgg
2100
atagcggccc gggcaaacgc ccgcataaaa gcggctttac cgataaagaa cgcgaagatc
2160
atcgccgccg caaagcgctg gaaaacaaaa aaaaacagct gagcgcgggc ggcaaaattc
2220
tgagcaaaga agaagaagaa gaactgcgcc gcctgaccga tgaagatgaa gaacgcaaac
2280
gccgcgtggc gggcccgcgc gtgggcgatg tgaacccgag ccgcggcggc ccgcgcggcg
2340
cgccgggcgg cggctttgtg ccgcagatgg cgggcgtgcc ggaaagcccg tttagccgca
2400
ccggcgaagg cctggatatt cgcggcaccc agggctttcc gtgggtgagc ccgagcccgc
2460
cgcagcagcg cctgccgctg ctggaatgca ccccgcagag ccagagcgaa agcaaaaaaa
2520
accgccgcgg cggccgcgaa gatattctgg aaaaatggat taccacccgc cgcaaagcgg
2580
aagaactgga aaaagatctg cgcaaagcgc gcaaaaccat taaaaaactg gaagatgaaa
2640
acccgtggct gggcaacatt attggcatta ttcgcaaagg caaagatggc gaaggcgcgc
2700
cgccggcgaa acgcccgcgc accgatcaga tggaaattga tagcggcacc ggcaaacgcc
2760
cgcataaaag cggctttacc gataaagaac gcgaagatca tcgccgccgc aaagcgctgg
2820
aaaacaaaaa aaaacagctg agcagcggcg gcaaaaacct gagccgcgaa gaagaagaag
2880
aactgggccg cctgaccgtg gaagatgaag aacgccgccg ccgcgtggcg ggcccgcgca
2940
ccggcgatgt gaacctgagc ggcggcggcc cgcgcggcgc gccgggcggc ggctttgtgc
3000
cgcgcatgga aggcgtgccg gaaagcccgt ttacccgcac cggcgaaggc ctggatattc
3060
gcggcaacca gggctttccg tgggtgcgcc cgagcccgcc gcagcagcgc ctgccgctgc
3120
tggaatgcac cccgcagggc accaacctga gcaccagcaa cccgctgggc ttttttccgg
3180
atcatcagct ggatccggcg tttcgcgcga acagcgcgaa cccggattgg gattttaacc
3240
cgaacaaaga tacctggccg gatgcgaaca aagtgggcgg ccagaacctg agcaccagca
3300
acccgctggg cttttttccg gatcatcagc tggatccggc gtttcgcgcg aacaccgcga
3360
acccggattg ggattttaac ccgaacaaag atacctggcc ggatgcgaac aaagtgggct
3420
gatgagaatt ccgt
3434
<210> 36
<211> 3431
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Кодон-оптимизированная последовательность нуклеиновой кислоты
слитых Дельта-7/Дельта-8
<400> 36
aagcttgcac catggcaggc accaatctgt caacctctaa ccctctgggc tttttccccg
60
accatcagct ggaccccgca ttccgagcaa actccgctaa ccctgactgg gatttcaacc
120
caaataagga cacctggccc gatgccaata aggtcggcgg ccagaacctg tccacatcta
180
atccactggg cttctttccc gaccaccagc tggatcctgc cttccgggcc aacacagcca
240
atcctgactg ggacttcaac cctaataagg atacctggcc cgatgccaac aaggtcggca
300
gcaggtccga gtctaagaag aataggggag gaagggagga gatcctggag cagtgggtgg
360
gagcacgcaa gaagctggag gagctggagc gggacctgag aaagatcaag aagaagatca
420
agaagctgga ggaggagaac ccctggctgg gcaatatcaa gggcatcctg ggcaagaagg
480
atcgggaggg agagggagca ccacctgcaa agagggccag agccgaccag atggaggtgg
540
attccggccc taggaagcgc ccattcagag gcgagtttac cgacaaggag cggagagatc
600
acaggcgccg gaaggccctg gagaacaagc ggaagcagct gagctccggc ggcaagagcc
660
tgtccaagga ggaggaggag gagctgagaa agctgacaga ggaggacgag agaagggaga
720
ggagggtggc aggacctagg gtgggaggcg tgaacccact ggagggagga accaggggag
780
cacctggagg aggattcgtg ccatccatgc agggagtgcc tgagtctcca tttgccagga
840
caggagaggg cctggacgtg cgcggaaatc agggcttccc ctgggacatc ctgtttcctg
900
ccgatccacc cttctcccct cagtcttgca ggccacagtc tcgcagcgag tccaagaaga
960
acagaggcgg aagggaggag gtgctggagc agtgggtgaa tggccggaag aagctggaag
1020
aactggagag ggagctgaga agggcccgca agaagatcaa gaagctggaa gacgataatc
1080
cttggctggg caatgtgaaa ggcatcctgg gcaagaagga caaggatgga gagggagcac
1140
ctccagcaaa gagggcaaga accgaccaga tggagatcga ttctggacca aggaagcgcc
1200
ctctgagagg aggcttcaca gaccgggaga gacaggatca ccgccggaga aaggccctga
1260
agaacaagaa gaagcagctg agcgccggcg gcaagtctct gagtaaagaa gaagaggagg
1320
agctgaagcg gctgaccaga gaggacgagg agcggaagaa ggaggagcac ggaccaagca
1380
gactgggagt gaatccttcc gagggaggac caagaggagc acccggagga ggcttcgtgc
1440
catctatgca gggcatcccc gagagcaggt ttaccagaac cggcgaaggc ctggacgtgc
1500
ggggctccag aggctttcct caggacatcc tgttcccatc tgatccccct tttagccccc
1560
agtcctgtag gcctcagggc accaacctgt ccacatctaa ccctctgggc ttctttcctg
1620
atcatcagct ggacccagcc ttccgcgcca acagcgccaa tcccgattgg gacttcaacc
1680
caaataagga tacctggcca gacgctaaca aggtcggagg acagaacctg agcacatcca
1740
atcctctggg cttctttcca gaccaccagc tggatccagc cttcagggct aatacagcca
1800
atcccgactg ggacttcaac ccaaataagg acacgtggcc agacgcaaac aaggtcggct
1860
ctcagagcga gacaaggagg ggccggagag gaaccaggga ggagacactg gagaagtgga
1920
tcaccgccag aaagaaggcc gaggagctgg agaaggacct gaggaagacc cgcaagacaa
1980
tcaagaagct ggaagaagag aacccatggc tgggcaatat cgtgggcatc atccgcaagg
2040
gcaaggacgg cgagggagca ccaccagcaa agaggcccag gactgatcag atggaggtgg
2100
atagcggccc tggcaagagg ccacacaagt ccggcttcac agacaaggag agggaggacc
2160
ataggcgccg gaaggccctg gaaaacaaga agaagcaatt atccgccggc ggcaagatcc
2220
tgtctaaaga agaggaagaa gagctgagaa ggctgaccga cgaggatgag gagaggaaaa
2280
gaagggtggc aggaccaaga gtgggcgacg tgaatccctc cagaggcgga ccaagaggag
2340
cacctggagg cggcttcgtg ccccagatgg ccggcgtgcc cgagtctcct tttagcagaa
2400
ccggagaggg cctggatatc aggggaaccc agggctttcc atgggtgtcc ccatctcctc
2460
cacagcagcg gctgccactg ctggagtgca cccctcagag ccagagcgaa tctaagaaga
2520
acagaagggg cggcagagag gacatcctgg aaaaatggat caccacacgc agaaaagctg
2580
aagaactgga aaaggacctg cggaaggcca gaaaaacaat caagaagctg gaggatgaaa
2640
atccatggct gggaaacatc atcggcatca tcagaaaggg caaggacggg gaaggcgcac
2700
cacctgcaaa gcggcctaga acagatcaga tggaaatcga ttctggaacc ggcaagcggc
2760
cacacaagag cggcttcacc gacaaggaga gagaggatca cagaaggcgc aaggccctgg
2820
agaacaagaa gaagcaatta agcagcggcg gcaagaatct gtccagagaa gaggaagagg
2880
agctgggcag actgaccgtg gaggacgagg agcggagaag gcgcgtggca ggacccagga
2940
caggcgatgt gaacctgagc ggaggaggac ctaggggagc accaggaggc ggcttcgtgc
3000
ctaggatgga gggagtgcca gagtccccct ttaccagaac cggcgagggc ctggacatca
3060
ggggaaatca gggattccca tgggtgcggc cttccccacc acagcagaga ctgccactgc
3120
tggagtgtac cccccagggc acaaacctga gcacctccaa tcccctgggc ttctttcctg
3180
accatcagct ggaccctgcc ttcagggcca acagcgccaa cccagattgg gacttcaacc
3240
ctaataagga cacctggcca gatgcaaaca aggtcggcgg ccaaaacctg tctacaagca
3300
accccctggg cttctttcca gatcaccagc tggatcccgc ctttcgcgcc aataccgcca
3360
accctgattg ggatttcaac cctaacaaag acacttggcc tgacgctaat aaggtcggct
3420
gatgagaatt c
3431
<210> 37
<211> 1136
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полипептидная последовательность слитых Дельта-7/Дельта-8
<400> 37
Met Ala Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro
1 5 10 15
Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser Ala Asn Pro Asp
20 25 30
Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val
35 40 45
Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro Leu Gly Phe Phe Pro Asp
50 55 60
His Gln Leu Asp Pro Ala Phe Arg Ala Asn Thr Ala Asn Pro Asp Trp
65 70 75 80
Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro Asp Ala Asn Lys Val Gly
85 90 95
Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly Arg Glu Glu Ile Leu
100 105 110
Glu Gln Trp Val Gly Ala Arg Lys Lys Leu Glu Glu Leu Glu Arg Asp
115 120 125
Leu Arg Lys Ile Lys Lys Lys Ile Lys Lys Leu Glu Glu Glu Asn Pro
130 135 140
Trp Leu Gly Asn Ile Lys Gly Ile Leu Gly Lys Lys Asp Arg Glu Gly
145 150 155 160
Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Ala Asp Gln Met Glu Val
165 170 175
Asp Ser Gly Pro Arg Lys Arg Pro Phe Arg Gly Glu Phe Thr Asp Lys
180 185 190
Glu Arg Arg Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Arg Lys
195 200 205
Gln Leu Ser Ser Gly Gly Lys Ser Leu Ser Lys Glu Glu Glu Glu Glu
210 215 220
Leu Arg Lys Leu Thr Glu Glu Asp Glu Arg Arg Glu Arg Arg Val Ala
225 230 235 240
Gly Pro Arg Val Gly Gly Val Asn Pro Leu Glu Gly Gly Thr Arg Gly
245 250 255
Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln Gly Val Pro Glu Ser
260 265 270
Pro Phe Ala Arg Thr Gly Glu Gly Leu Asp Val Arg Gly Asn Gln Gly
275 280 285
Phe Pro Trp Asp Ile Leu Phe Pro Ala Asp Pro Pro Phe Ser Pro Gln
290 295 300
Ser Cys Arg Pro Gln Ser Arg Ser Glu Ser Lys Lys Asn Arg Gly Gly
305 310 315 320
Arg Glu Glu Val Leu Glu Gln Trp Val Asn Gly Arg Lys Lys Leu Glu
325 330 335
Glu Leu Glu Arg Glu Leu Arg Arg Ala Arg Lys Lys Ile Lys Lys Leu
340 345 350
Glu Asp Asp Asn Pro Trp Leu Gly Asn Val Lys Gly Ile Leu Gly Lys
355 360 365
Lys Asp Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg Ala Arg Thr
370 375 380
Asp Gln Met Glu Ile Asp Ser Gly Pro Arg Lys Arg Pro Leu Arg Gly
385 390 395 400
Gly Phe Thr Asp Arg Glu Arg Gln Asp His Arg Arg Arg Lys Ala Leu
405 410 415
Lys Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ser Leu Ser Lys
420 425 430
Glu Glu Glu Glu Glu Leu Lys Arg Leu Thr Arg Glu Asp Glu Glu Arg
435 440 445
Lys Lys Glu Glu His Gly Pro Ser Arg Leu Gly Val Asn Pro Ser Glu
450 455 460
Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro Ser Met Gln
465 470 475 480
Gly Ile Pro Glu Ser Arg Phe Thr Arg Thr Gly Glu Gly Leu Asp Val
485 490 495
Arg Gly Ser Arg Gly Phe Pro Gln Asp Ile Leu Phe Pro Ser Asp Pro
500 505 510
Pro Phe Ser Pro Gln Ser Cys Arg Pro Gln Gly Thr Asn Leu Ser Thr
515 520 525
Ser Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe
530 535 540
Arg Ala Asn Ser Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp
545 550 555 560
Thr Trp Pro Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser Thr Ser
565 570 575
Asn Pro Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg
580 585 590
Ala Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr
595 600 605
Trp Pro Asp Ala Asn Lys Val Gly Ser Gln Ser Glu Thr Arg Arg Gly
610 615 620
Arg Arg Gly Thr Arg Glu Glu Thr Leu Glu Lys Trp Ile Thr Ala Arg
625 630 635 640
Lys Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg Lys Thr Arg Lys Thr
645 650 655
Ile Lys Lys Leu Glu Glu Glu Asn Pro Trp Leu Gly Asn Ile Val Gly
660 665 670
Ile Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala Pro Pro Ala Lys Arg
675 680 685
Pro Arg Thr Asp Gln Met Glu Val Asp Ser Gly Pro Gly Lys Arg Pro
690 695 700
His Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu Asp His Arg Arg Arg
705 710 715 720
Lys Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser Ala Gly Gly Lys Ile
725 730 735
Leu Ser Lys Glu Glu Glu Glu Glu Leu Arg Arg Leu Thr Asp Glu Asp
740 745 750
Glu Glu Arg Lys Arg Arg Val Ala Gly Pro Arg Val Gly Asp Val Asn
755 760 765
Pro Ser Arg Gly Gly Pro Arg Gly Ala Pro Gly Gly Gly Phe Val Pro
770 775 780
Gln Met Ala Gly Val Pro Glu Ser Pro Phe Ser Arg Thr Gly Glu Gly
785 790 795 800
Leu Asp Ile Arg Gly Thr Gln Gly Phe Pro Trp Val Ser Pro Ser Pro
805 810 815
Pro Gln Gln Arg Leu Pro Leu Leu Glu Cys Thr Pro Gln Ser Gln Ser
820 825 830
Glu Ser Lys Lys Asn Arg Arg Gly Gly Arg Glu Asp Ile Leu Glu Lys
835 840 845
Trp Ile Thr Thr Arg Arg Lys Ala Glu Glu Leu Glu Lys Asp Leu Arg
850 855 860
Lys Ala Arg Lys Thr Ile Lys Lys Leu Glu Asp Glu Asn Pro Trp Leu
865 870 875 880
Gly Asn Ile Ile Gly Ile Ile Arg Lys Gly Lys Asp Gly Glu Gly Ala
885 890 895
Pro Pro Ala Lys Arg Pro Arg Thr Asp Gln Met Glu Ile Asp Ser Gly
900 905 910
Thr Gly Lys Arg Pro His Lys Ser Gly Phe Thr Asp Lys Glu Arg Glu
915 920 925
Asp His Arg Arg Arg Lys Ala Leu Glu Asn Lys Lys Lys Gln Leu Ser
930 935 940
Ser Gly Gly Lys Asn Leu Ser Arg Glu Glu Glu Glu Glu Leu Gly Arg
945 950 955 960
Leu Thr Val Glu Asp Glu Glu Arg Arg Arg Arg Val Ala Gly Pro Arg
965 970 975
Thr Gly Asp Val Asn Leu Ser Gly Gly Gly Pro Arg Gly Ala Pro Gly
980 985 990
Gly Gly Phe Val Pro Arg Met Glu Gly Val Pro Glu Ser Pro Phe Thr
995 1000 1005
Arg Thr Gly Glu Gly Leu Asp Ile Arg Gly Asn Gln Gly Phe Pro
1010 1015 1020
Trp Val Arg Pro Ser Pro Pro Gln Gln Arg Leu Pro Leu Leu Glu
1025 1030 1035
Cys Thr Pro Gln Gly Thr Asn Leu Ser Thr Ser Asn Pro Leu Gly
1040 1045 1050
Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala Asn Ser
1055 1060 1065
Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr Trp Pro
1070 1075 1080
Asp Ala Asn Lys Val Gly Gly Gln Asn Leu Ser Thr Ser Asn Pro
1085 1090 1095
Leu Gly Phe Phe Pro Asp His Gln Leu Asp Pro Ala Phe Arg Ala
1100 1105 1110
Asn Thr Ala Asn Pro Asp Trp Asp Phe Asn Pro Asn Lys Asp Thr
1115 1120 1125
Trp Pro Asp Ala Asn Lys Val Gly
1130 1135
<210> 38
<211> 8
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Овальбумин 257-264 CTL
<400> 38
Ser Ile Ile Asn Phe Glu Lys Leu
1 5
<210> 39
<211> 17
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Овальбумин 323-339 Th
<400> 39
Ile Ser Gln Ala Val His Ala Ala His Ala Glu Ile Asn Glu Ala Gly
1 5 10 15
Arg
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИ-PRE-S1 HBV АНТИТЕЛА | 2016 |
|
RU2739955C2 |
| СЛИТЫЙ БЕЛОК | 2016 |
|
RU2748643C2 |
| СПОСОБ И СРЕДСТВО ДЛЯ БЫСТРОГО ОБНАРУЖЕНИЯ ИНФЕКЦИЙ ВИРУСА ГЕПАТИТА D | 2019 |
|
RU2800845C2 |
| ИНСЕКТИЦИДНЫЕ БЕЛКИ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2740312C2 |
| РЕКОМБИНАНТНЫЕ КЛЕТКИ, ПРОДУЦИРУЮЩИЕ ГИАЛУРОНОВУЮ КИСЛОТУ | 2022 |
|
RU2839983C2 |
| КОНСТРУКЦИИ ДНК-АНТИТЕЛ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ БОЛЕЗНИ ЛАЙМА | 2017 |
|
RU2813829C2 |
| АДЕНОВИРУСЫ И СПОСОБЫ ПРИМЕНЕНИЯ АДЕНОВИРУСОВ | 2019 |
|
RU2782528C1 |
| ВАРИАНТЫ КИСЛОЙ АЛЬФА-ГЛЮКОЗИДАЗЫ И ИХ ИСПОЛЬЗОВАНИЕ | 2017 |
|
RU2780410C2 |
| ПОЛИПЕПТИДНЫЕ КОНСТРУКЦИИ ЛИЗИН-ПРОТИВОМИКРОБНЫЙ ПЕПТИД (AMP), ЛИЗИНЫ, ВЫДЕЛЕННЫЕ ПОЛИНУКЛЕОТИДЫ, КОДИРУЮЩИЕ ИХ, А ТАКЖЕ ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2803121C2 |
| Выделенный рекомбинантный вирус на основе вируса гриппа для индукции специфического иммунитета к вирусу гриппа и/или профилактики заболеваний, вызванных вирусом гриппа | 2021 |
|
RU2813150C2 |


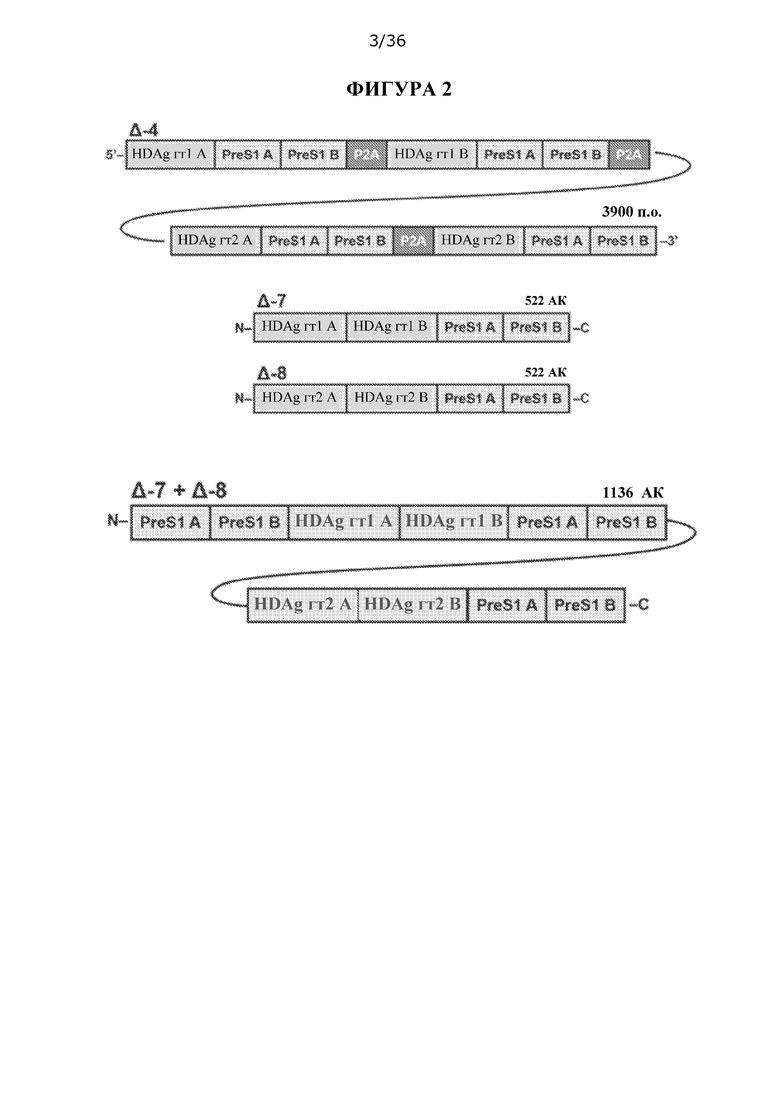
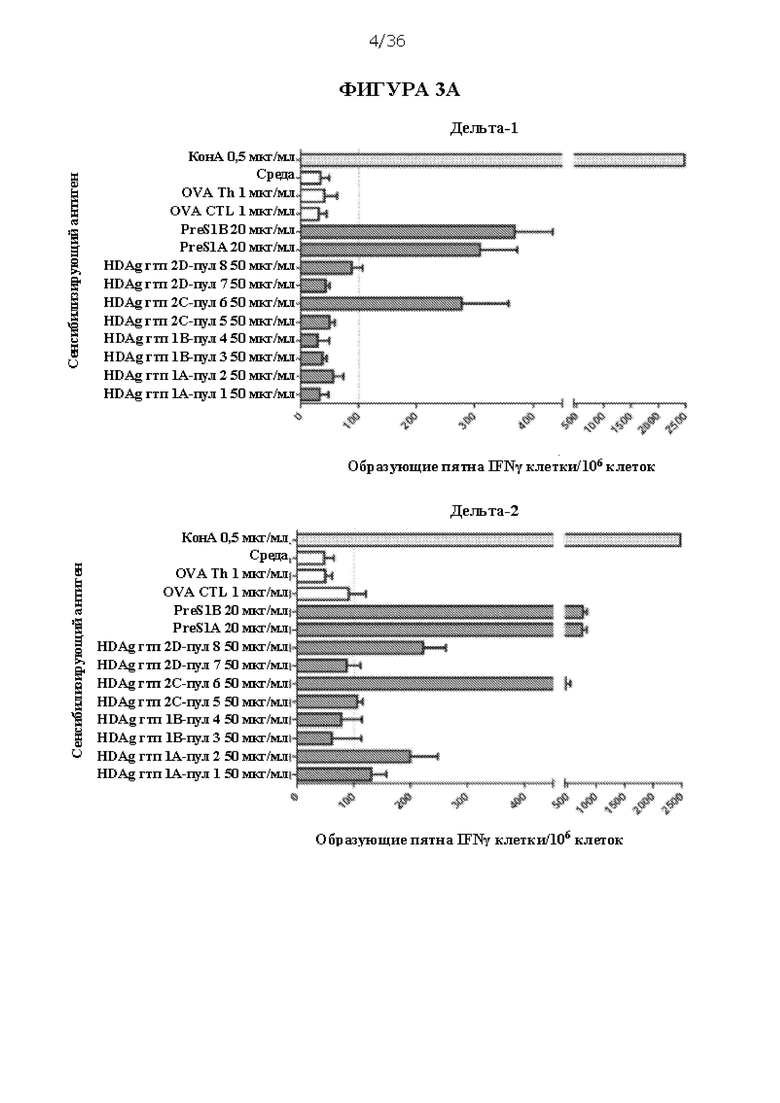
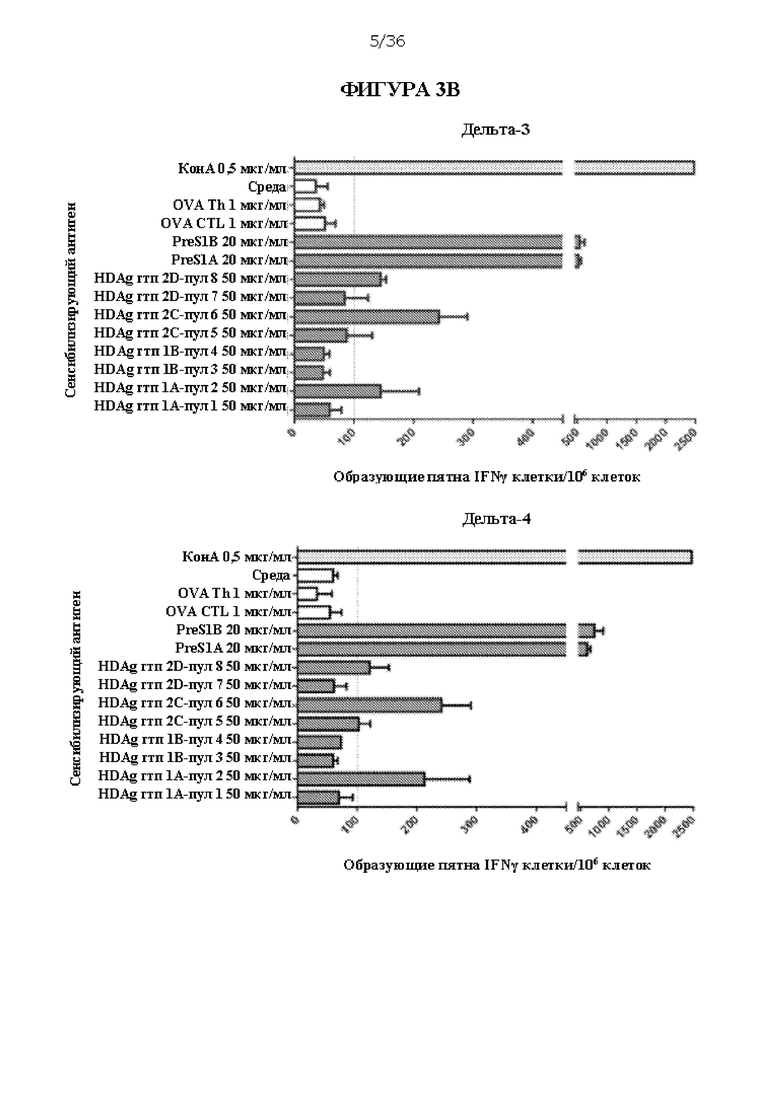
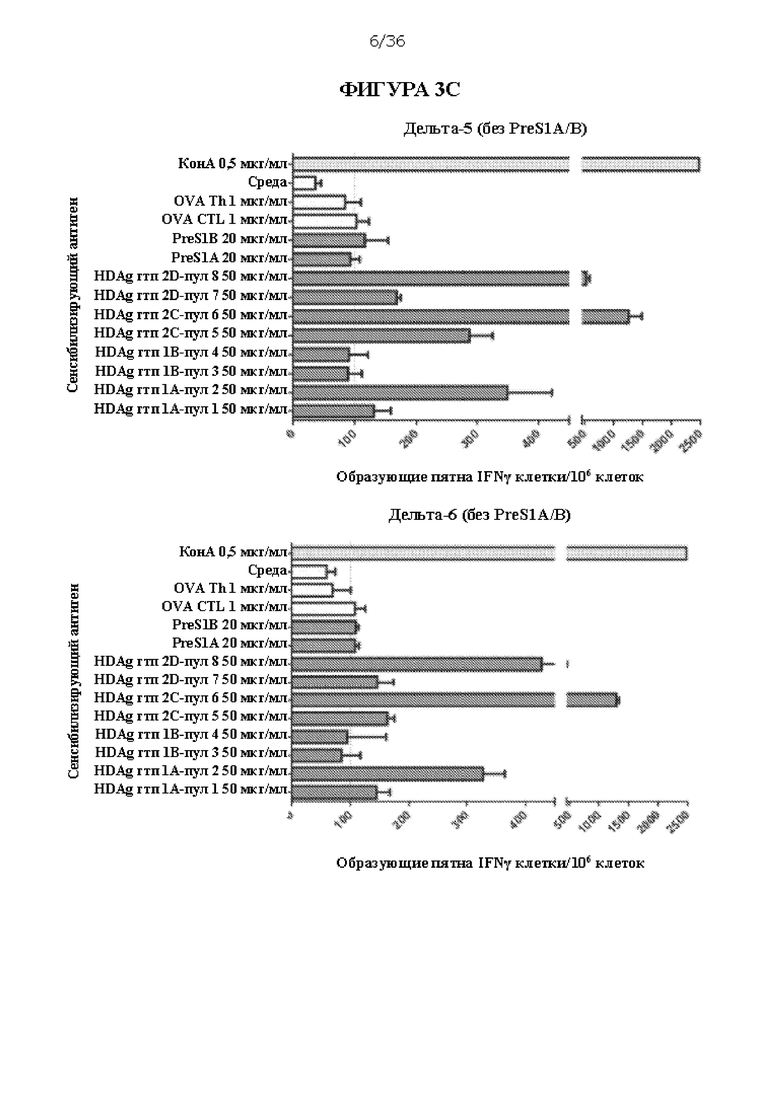
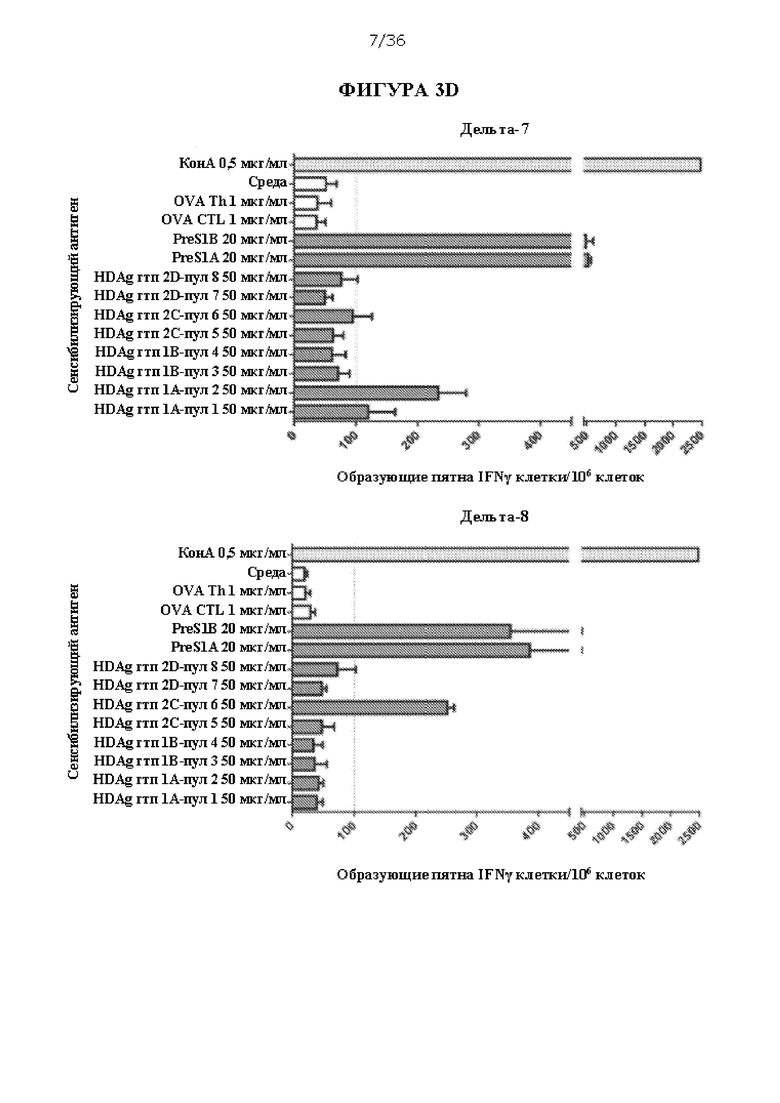
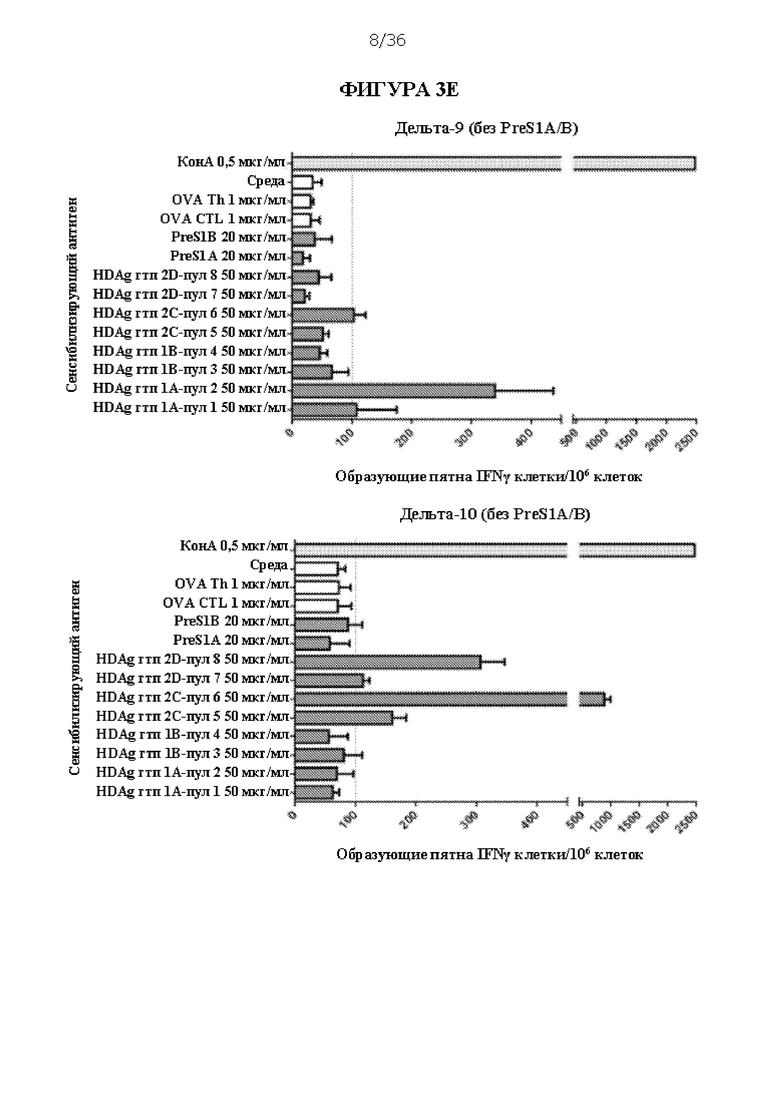
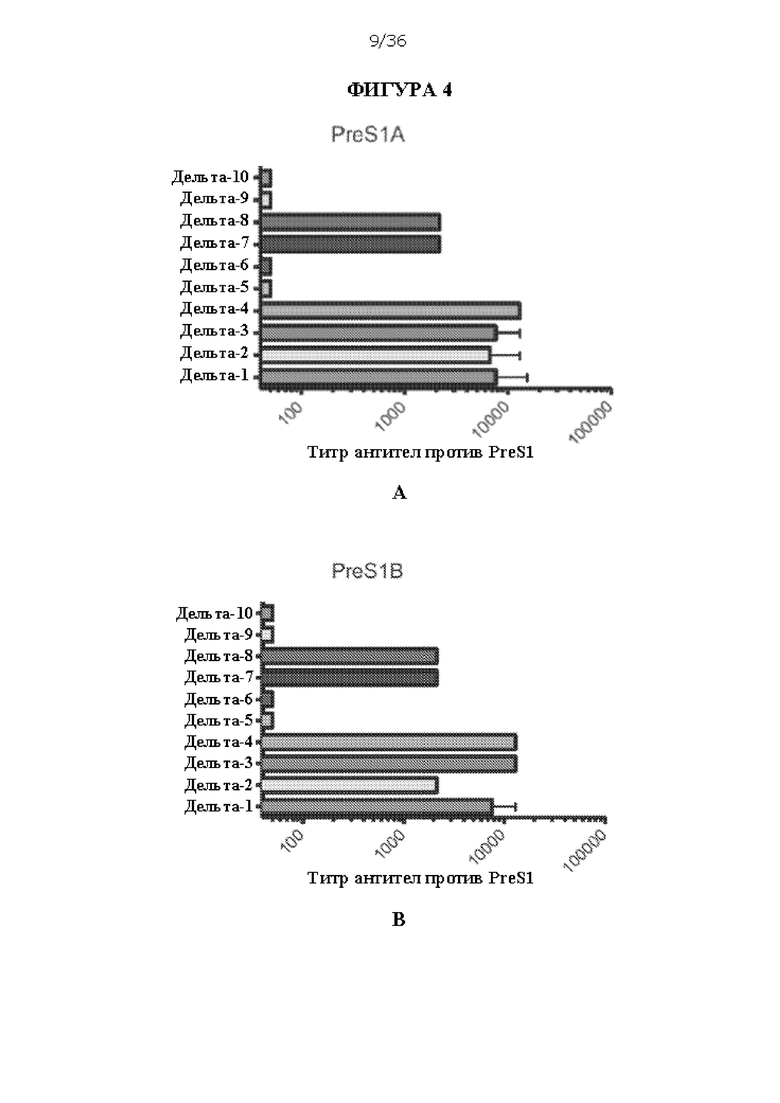
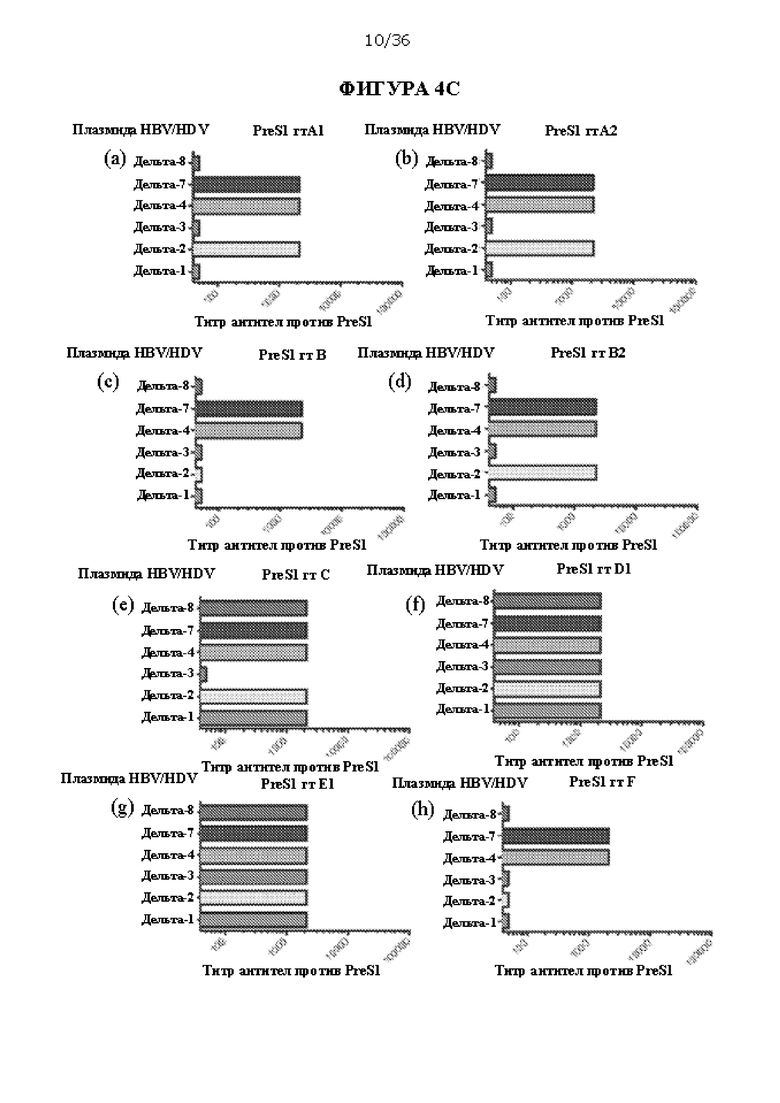
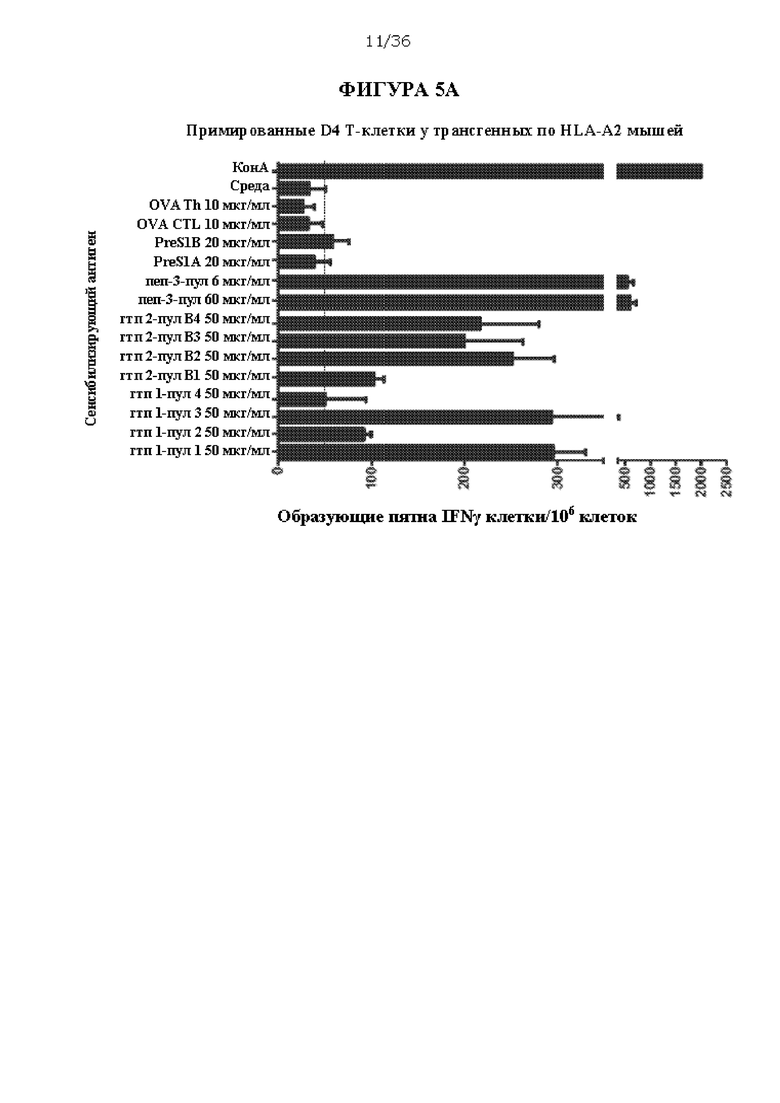
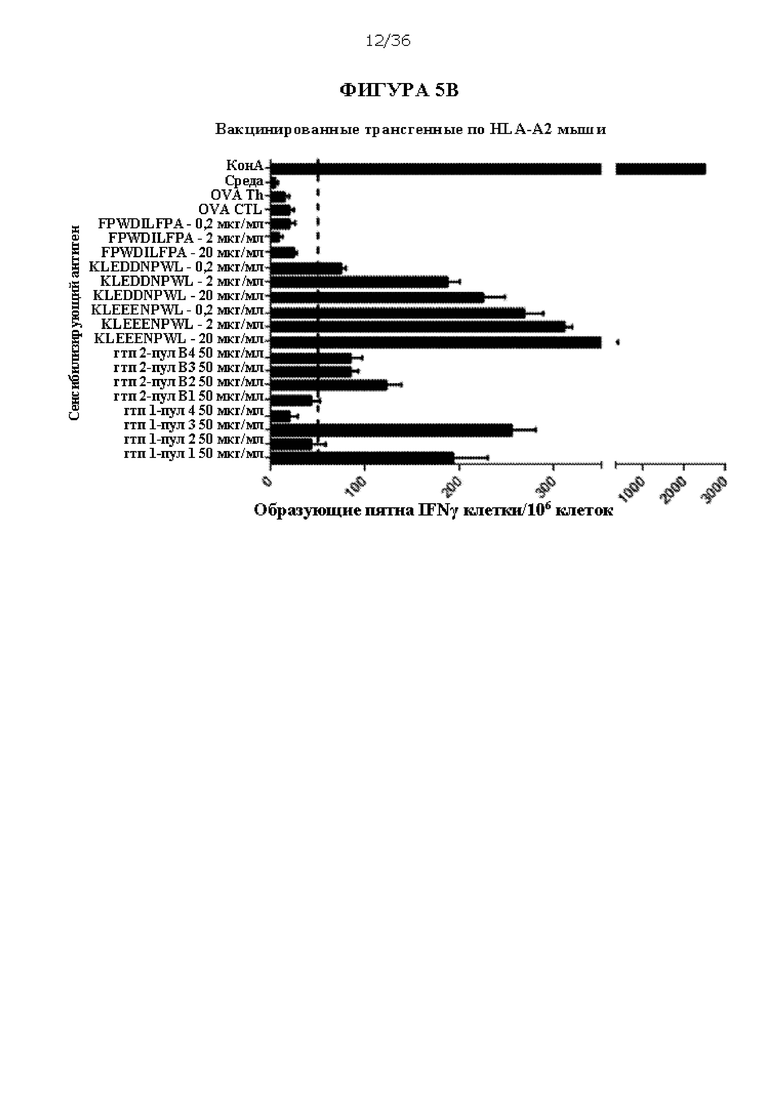

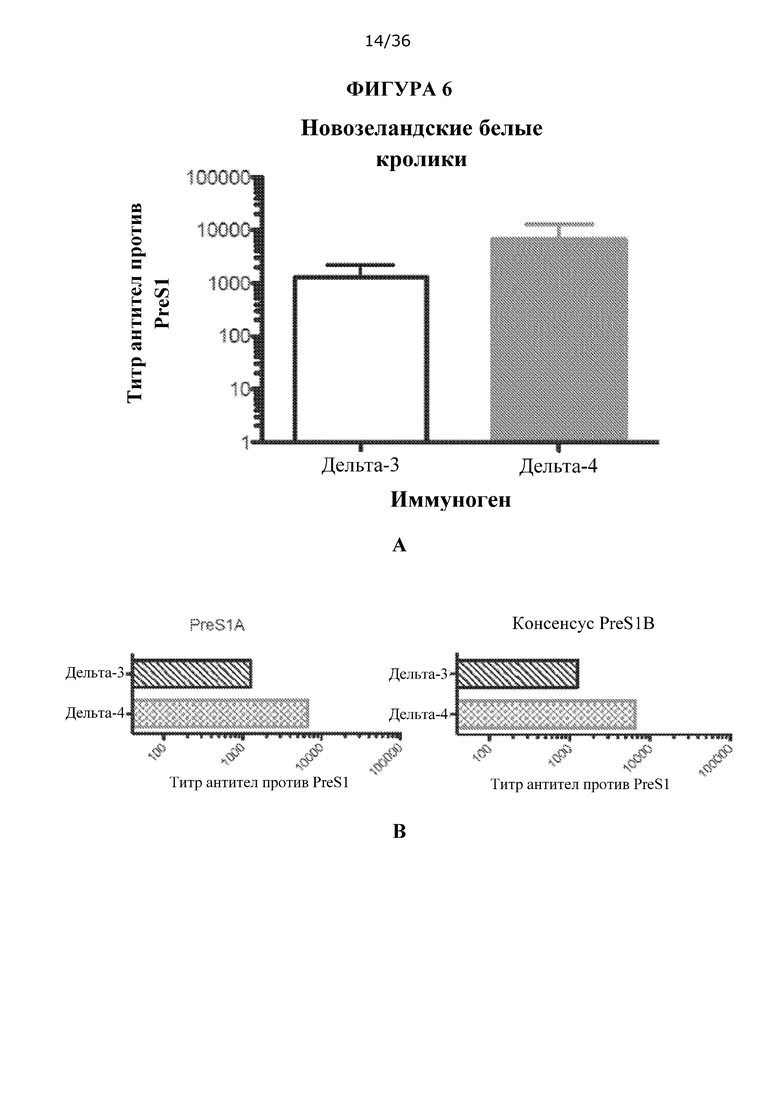
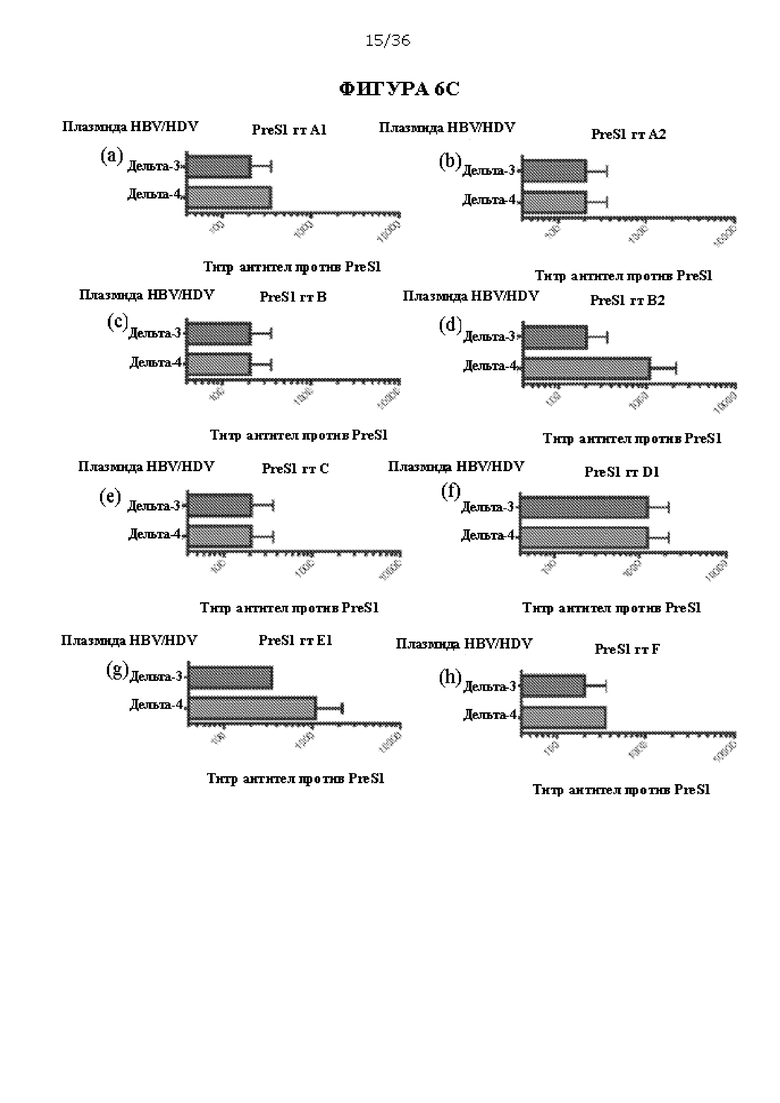
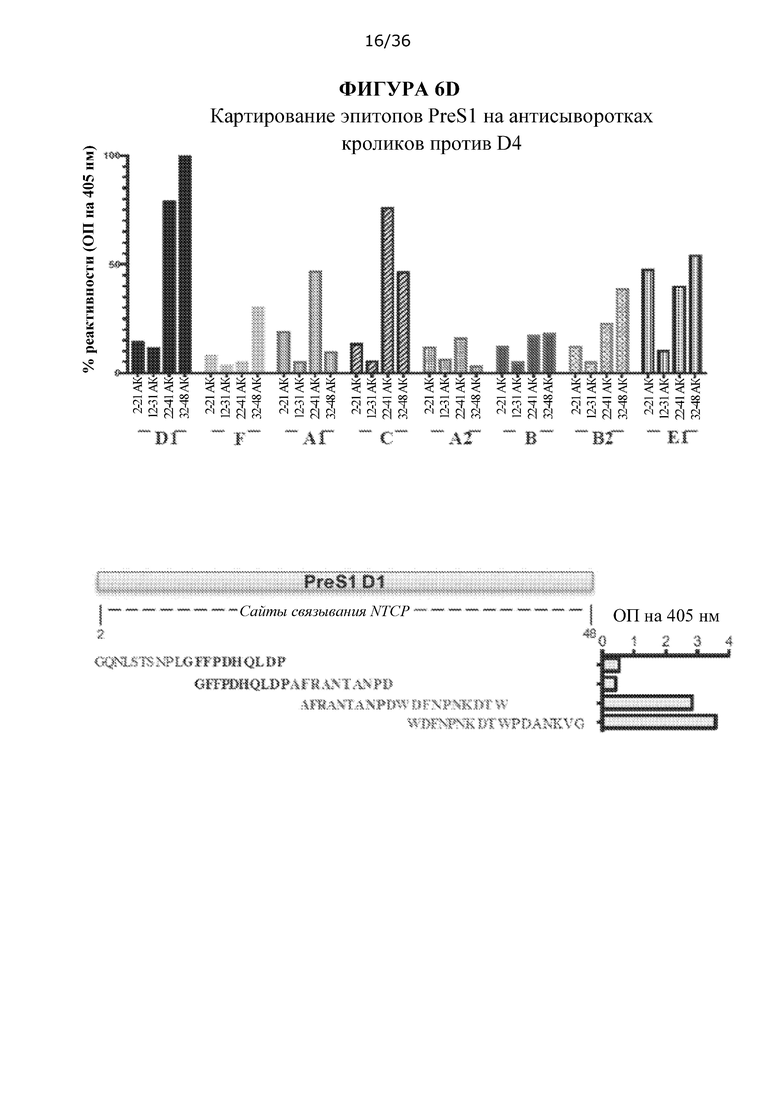
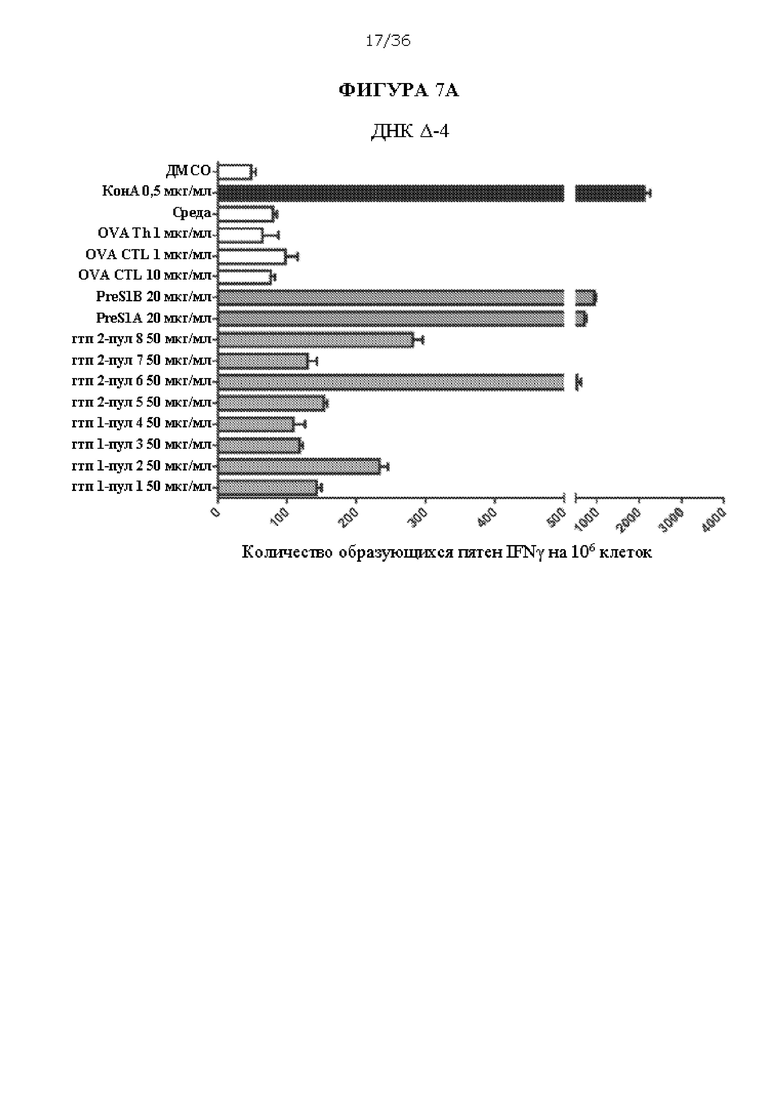
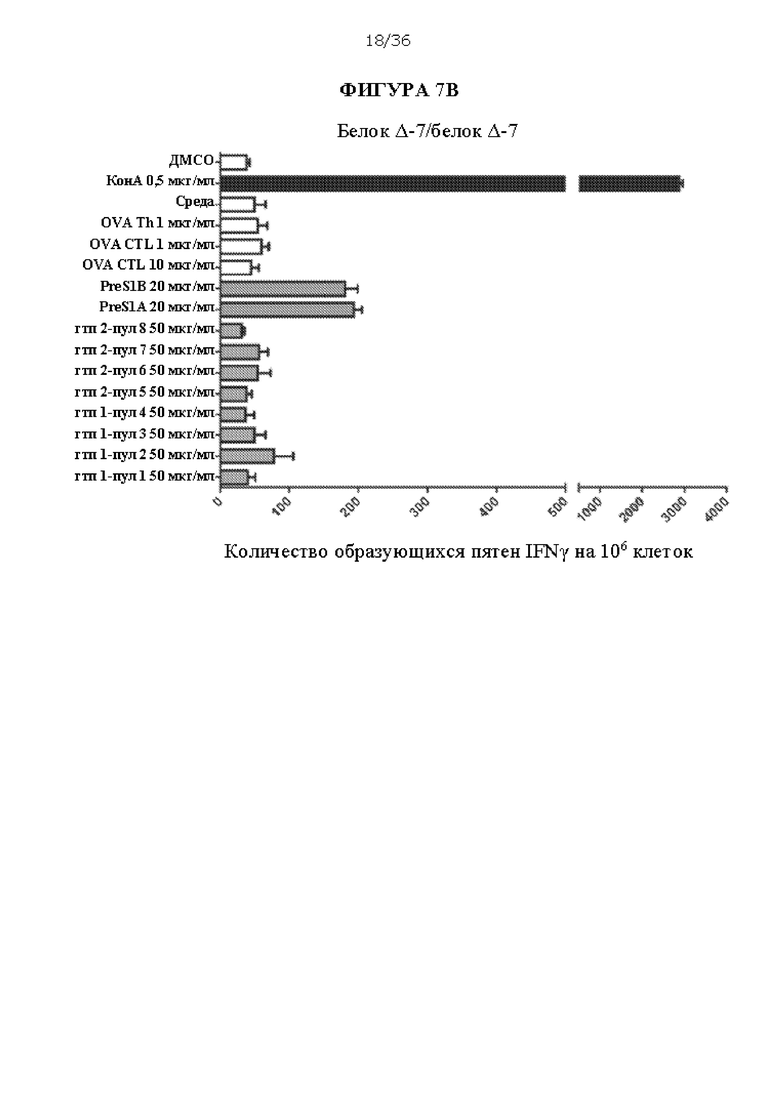
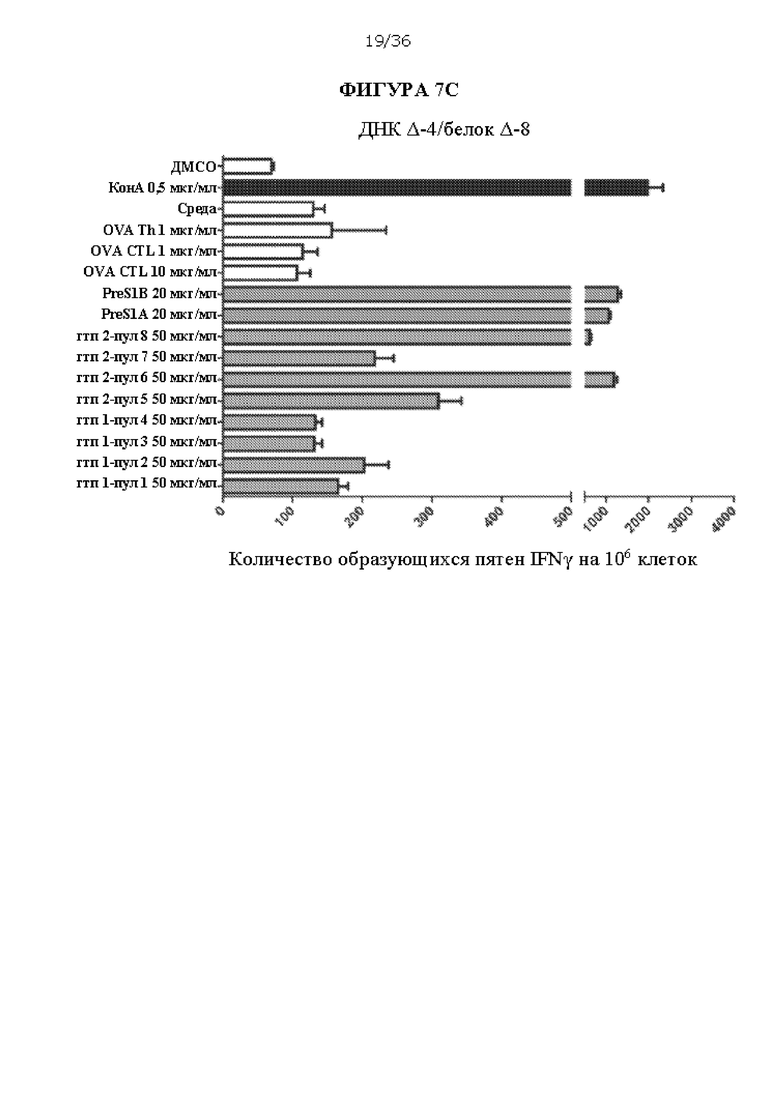
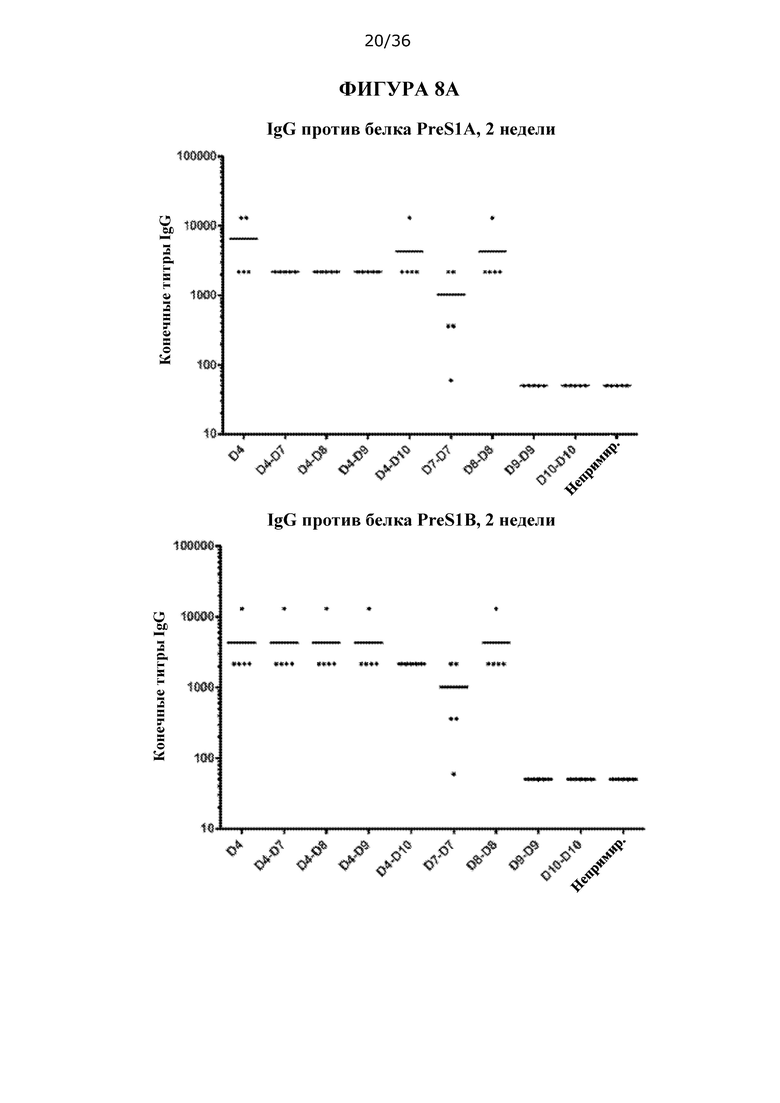
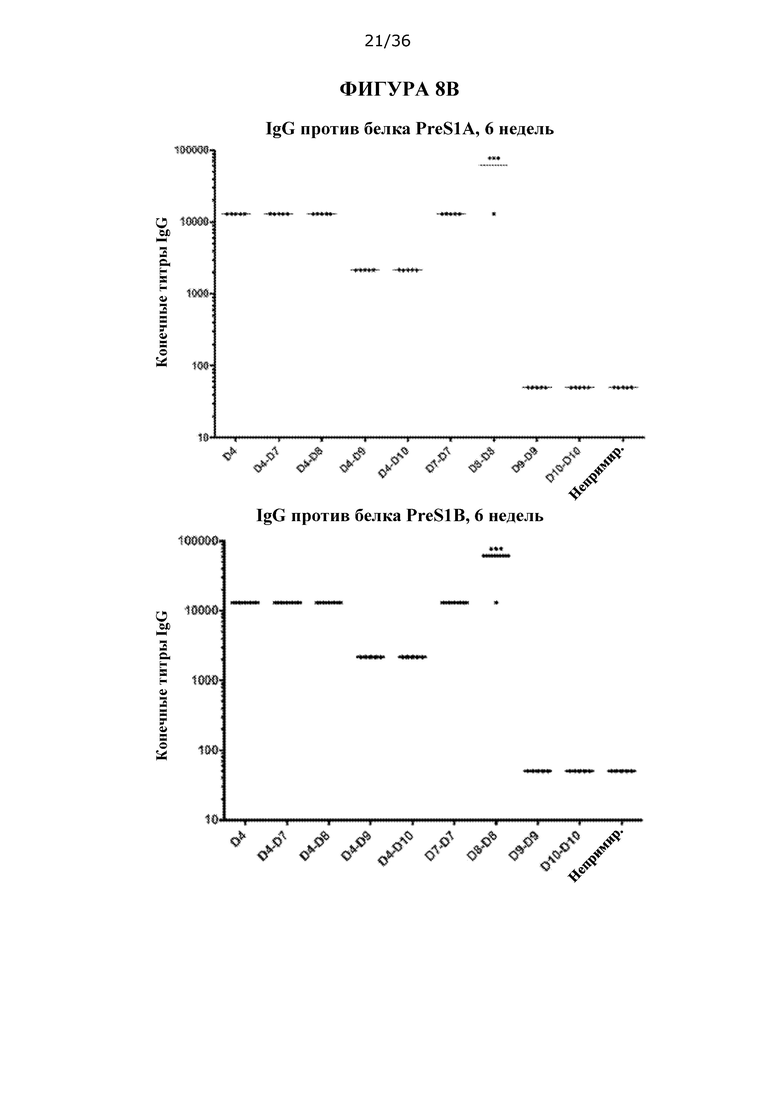
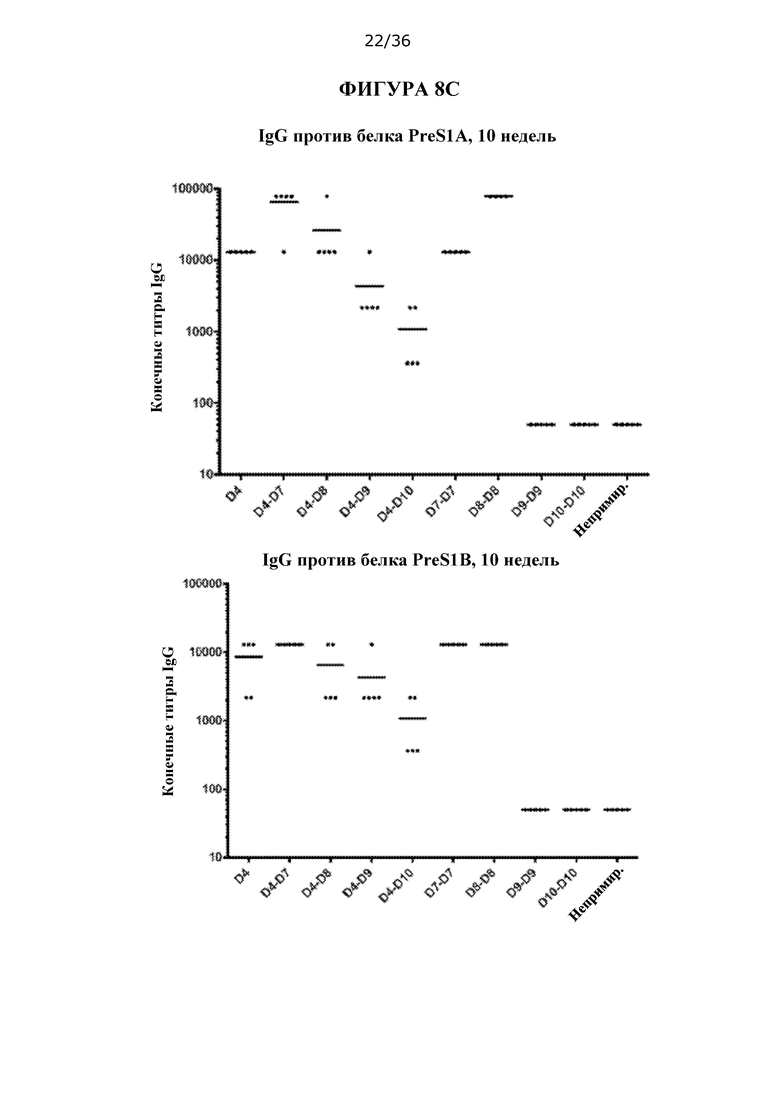
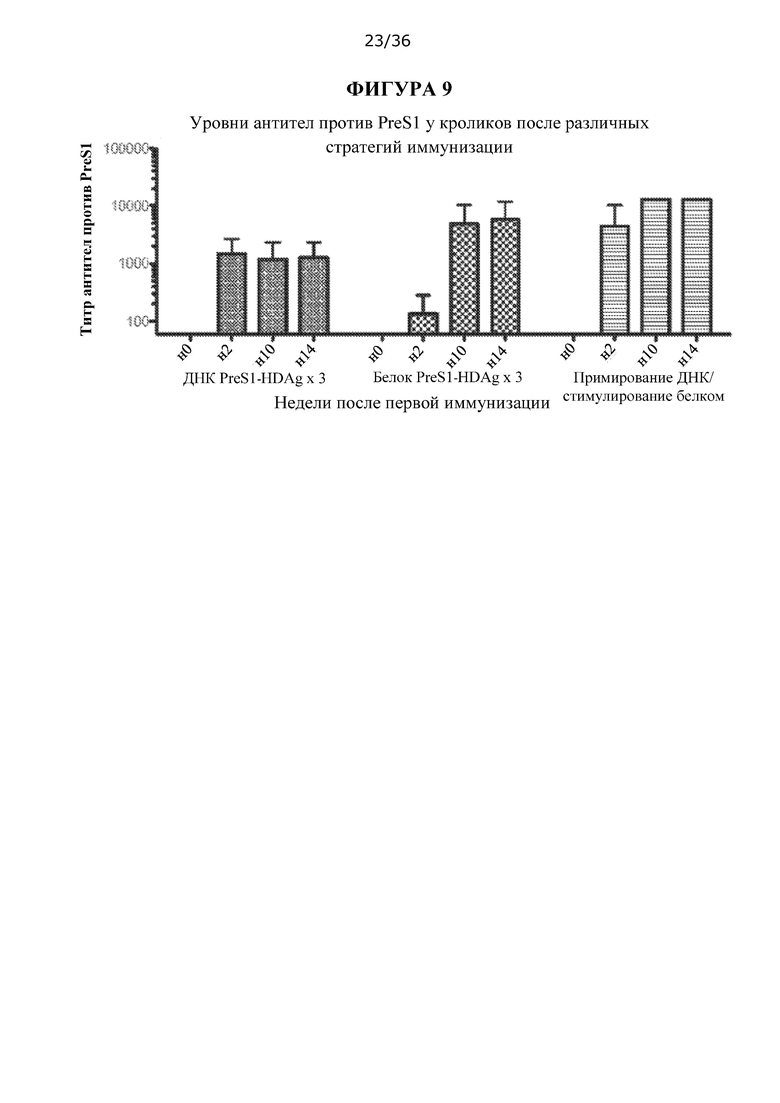


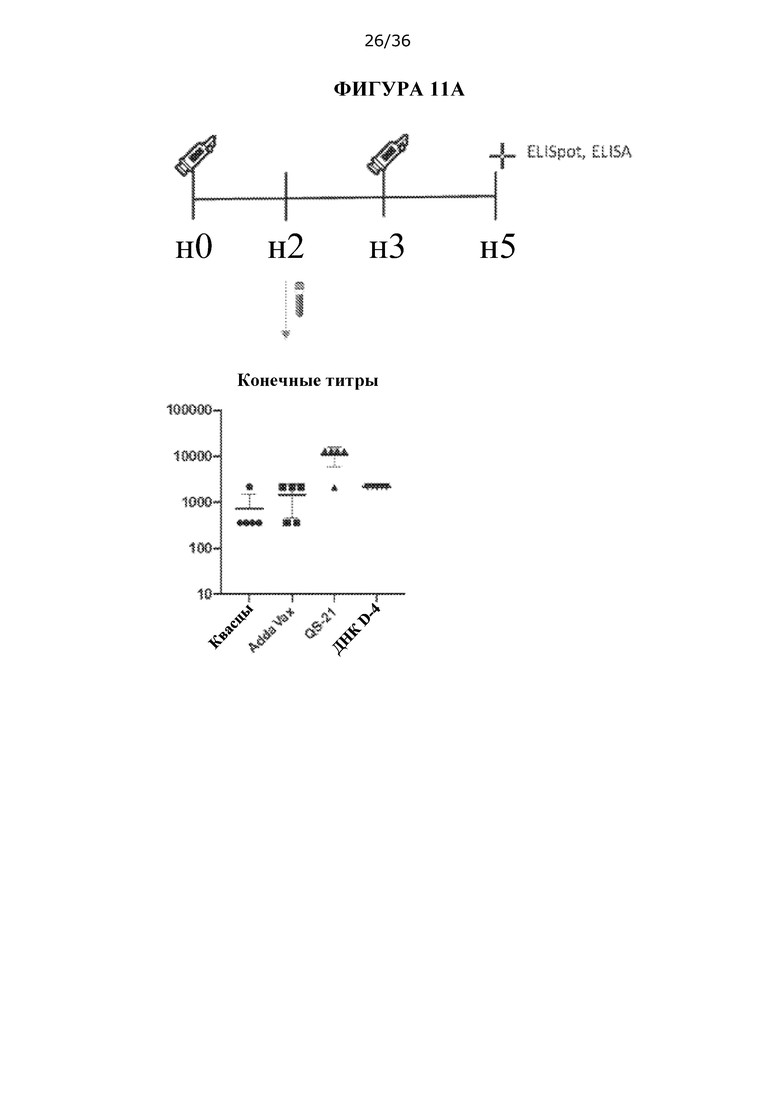
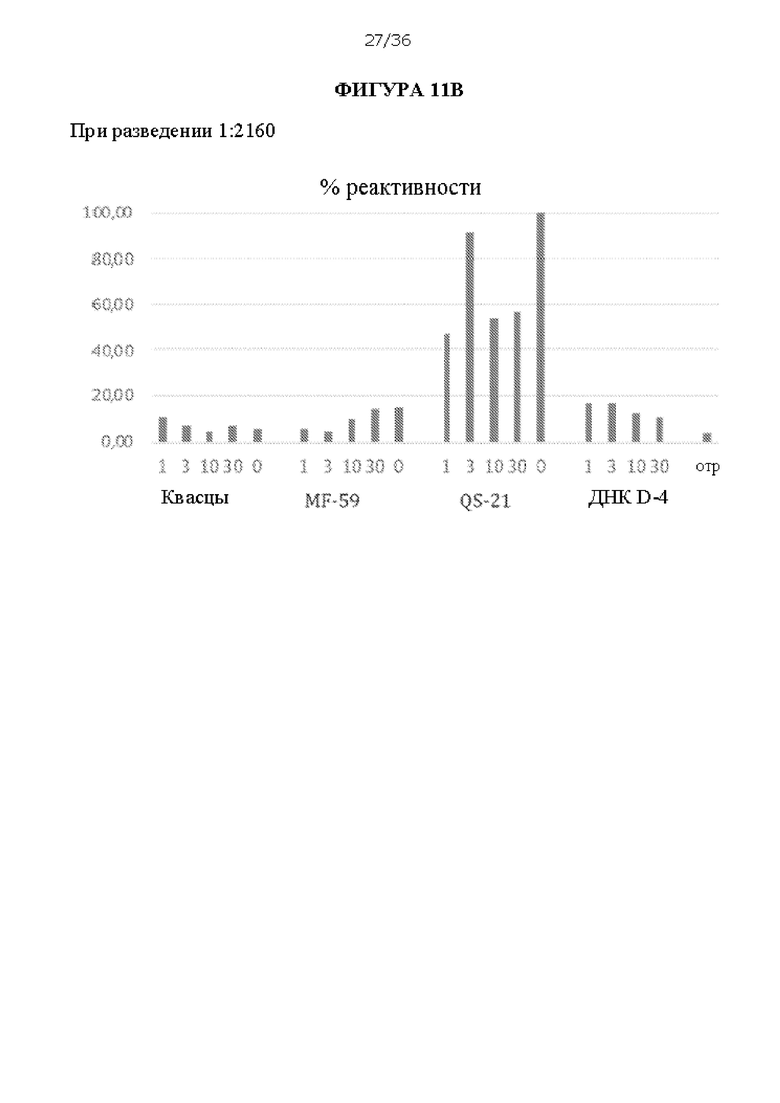
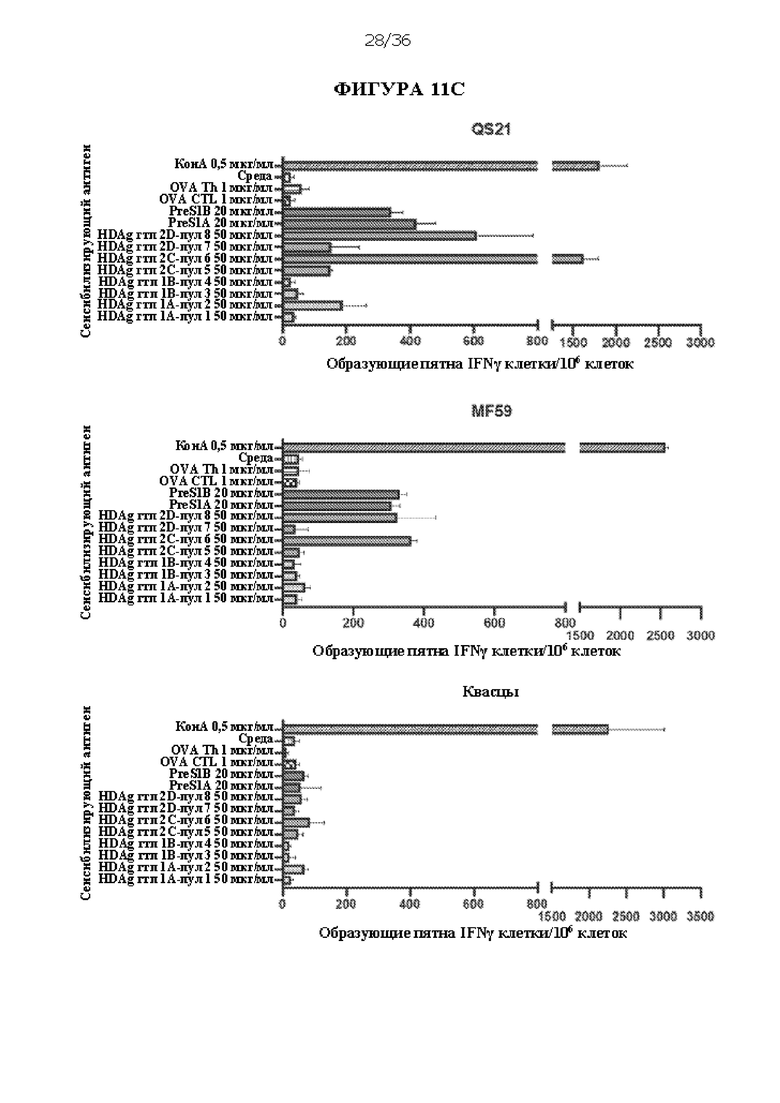
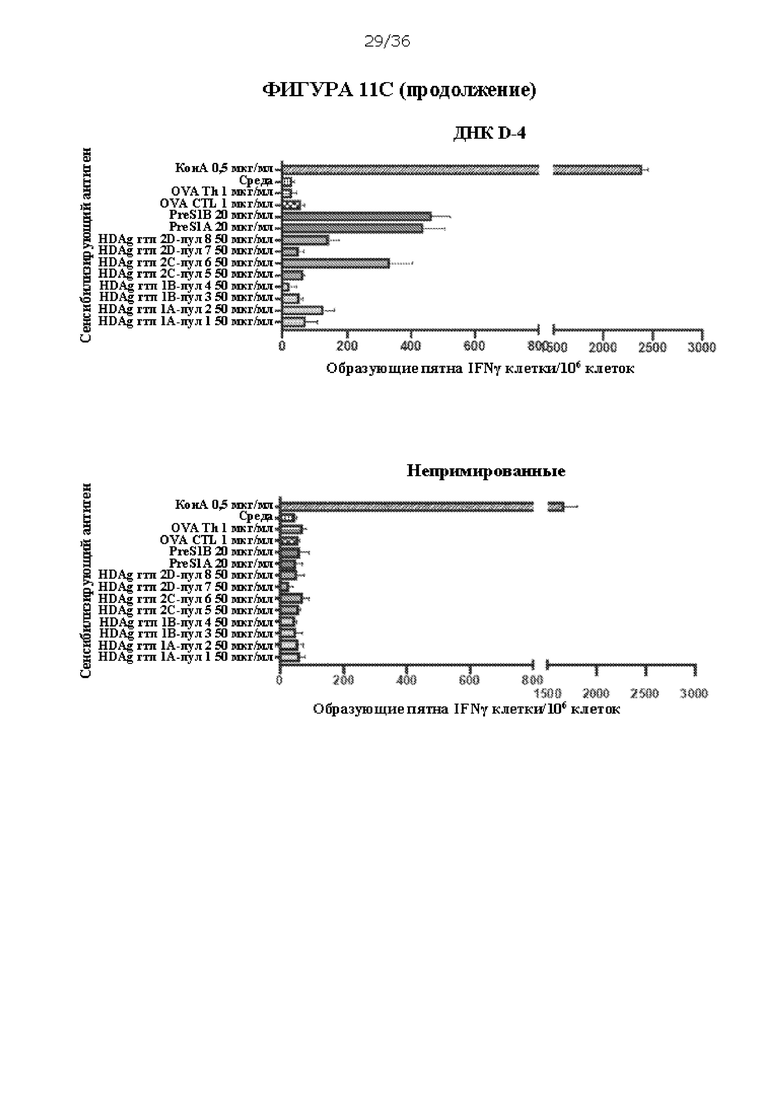
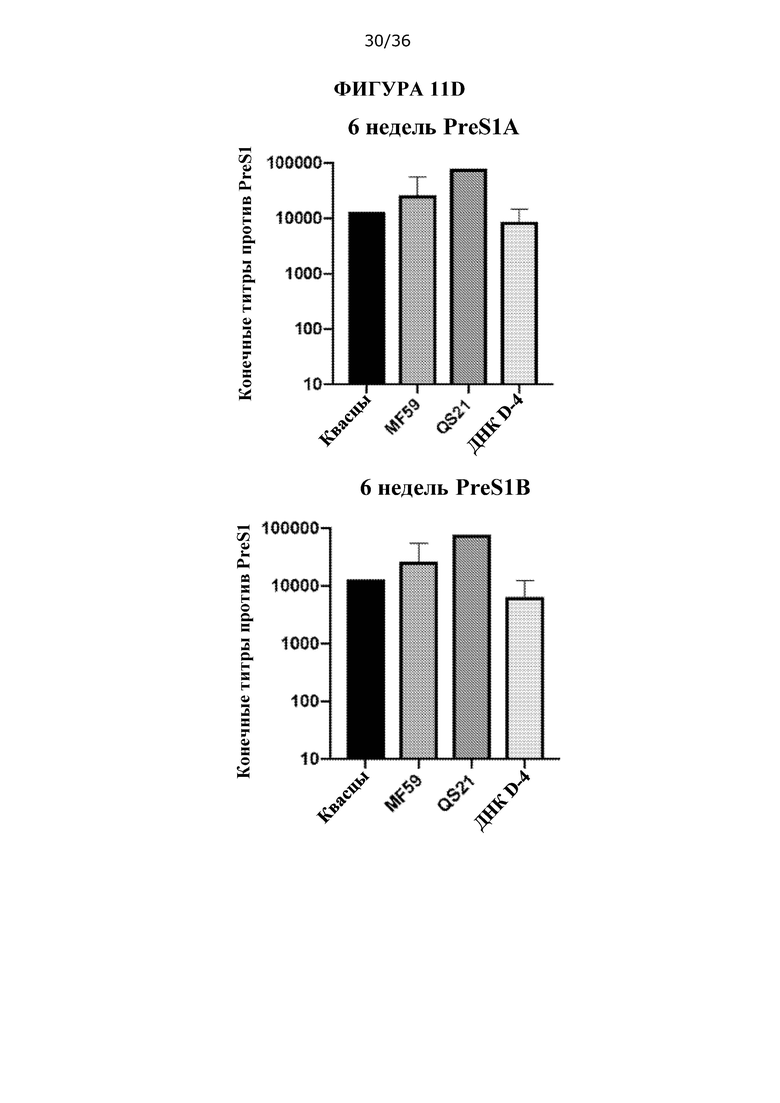
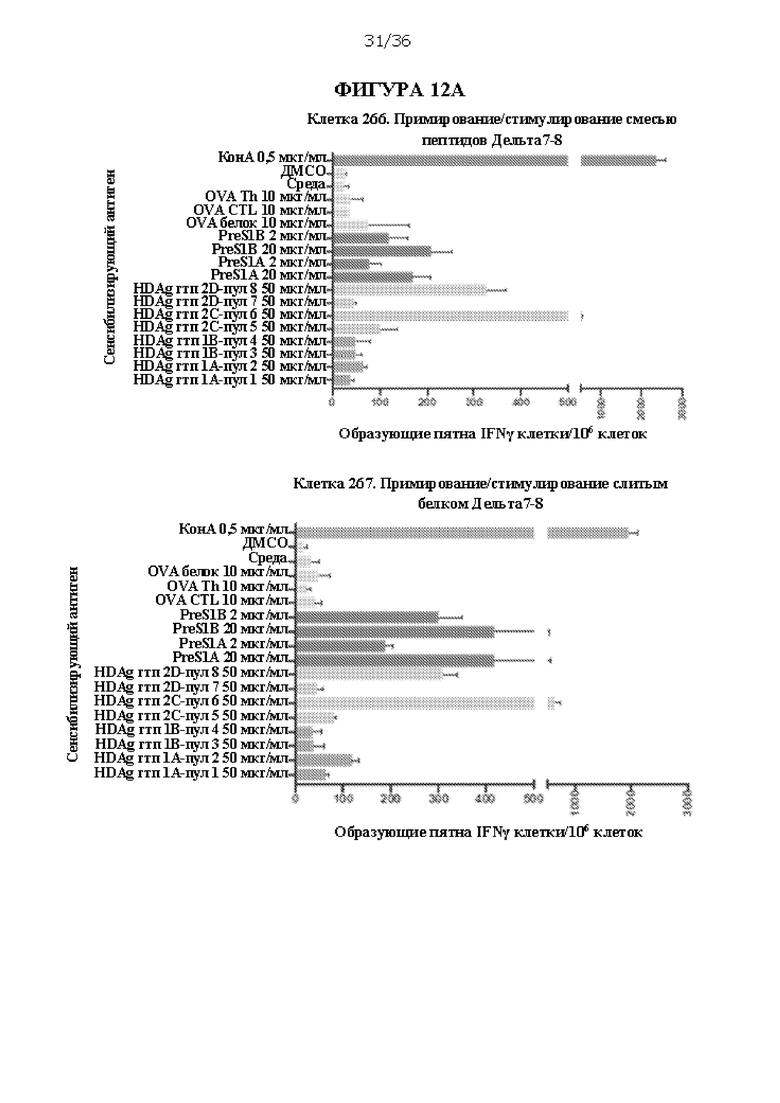
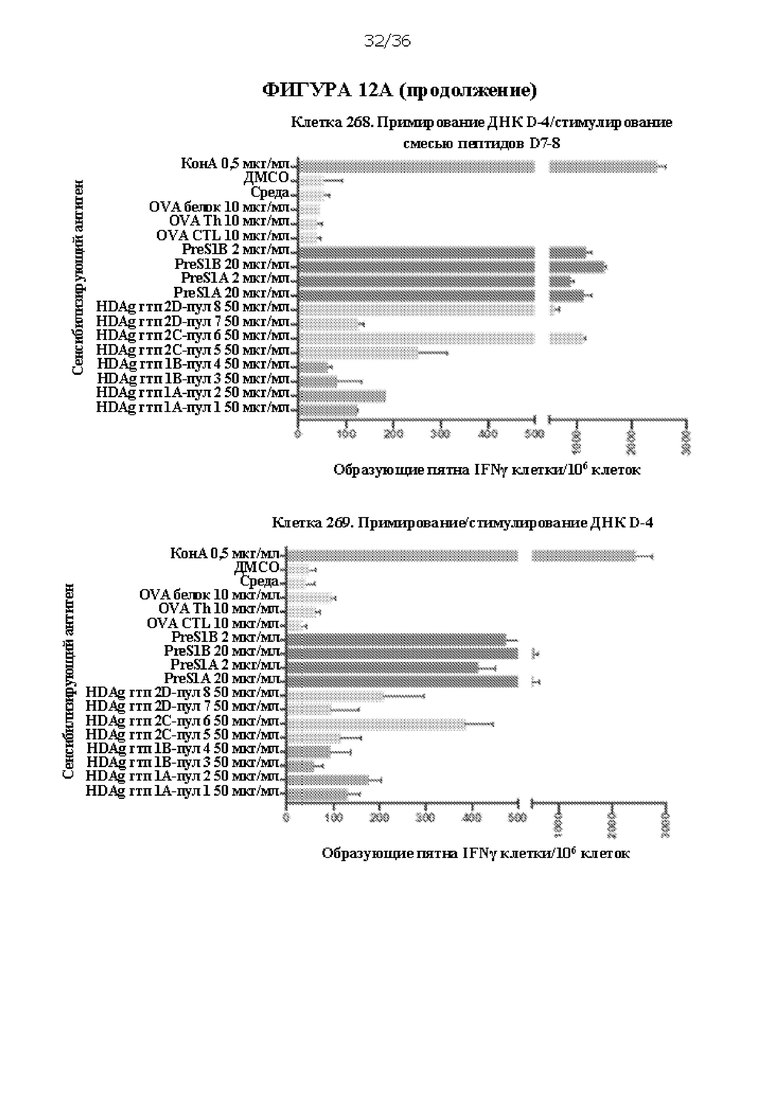
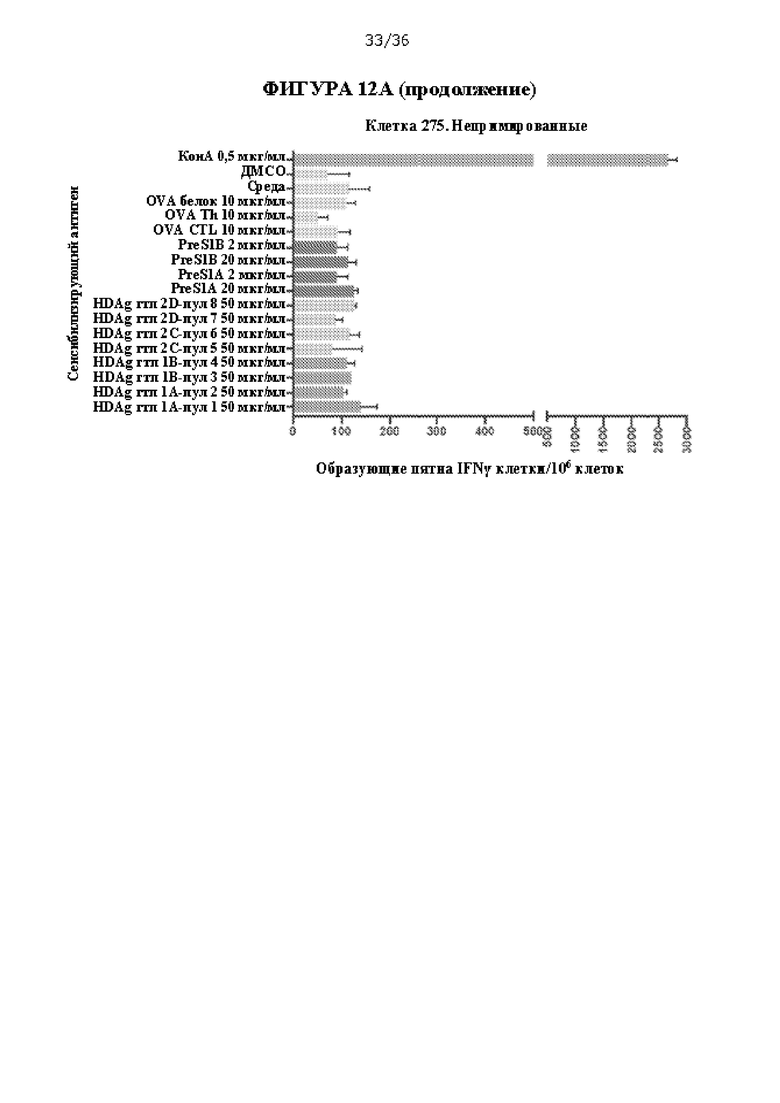
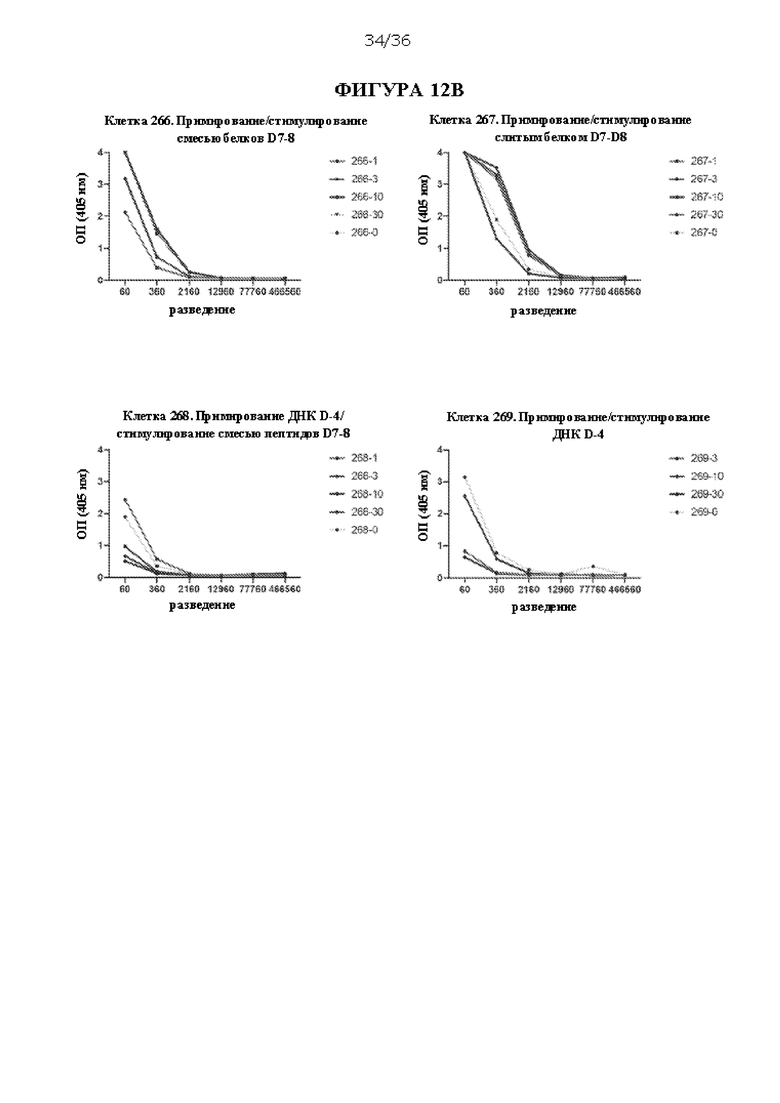
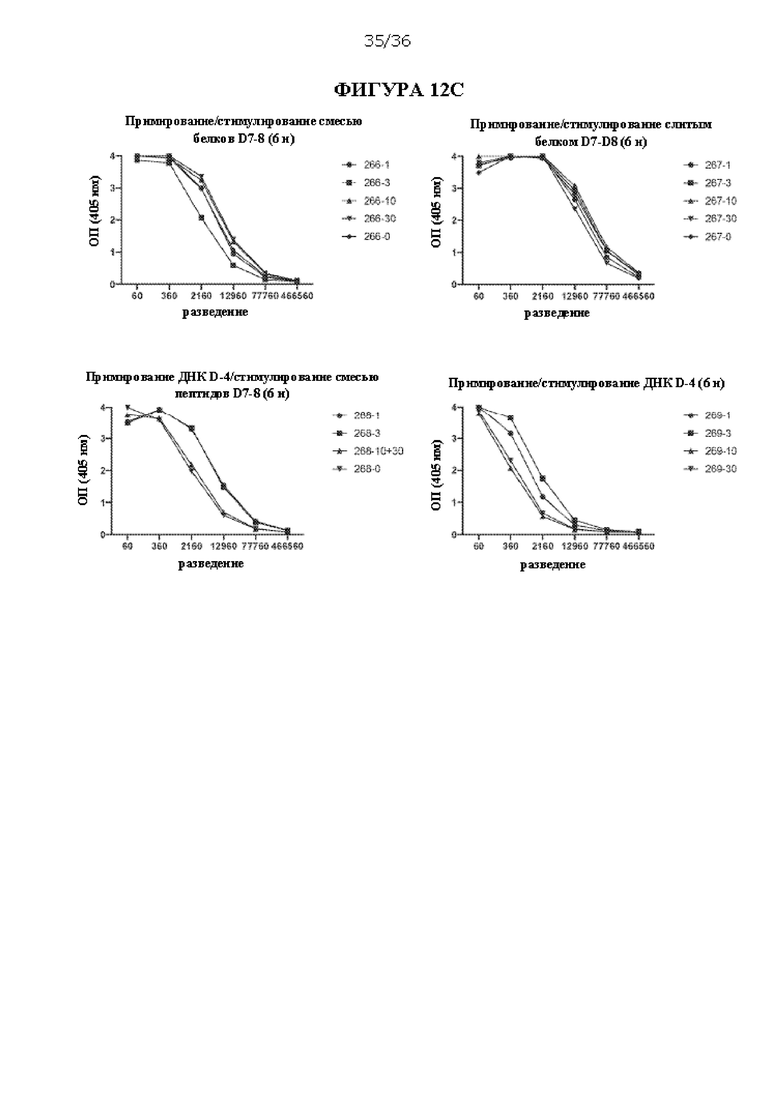
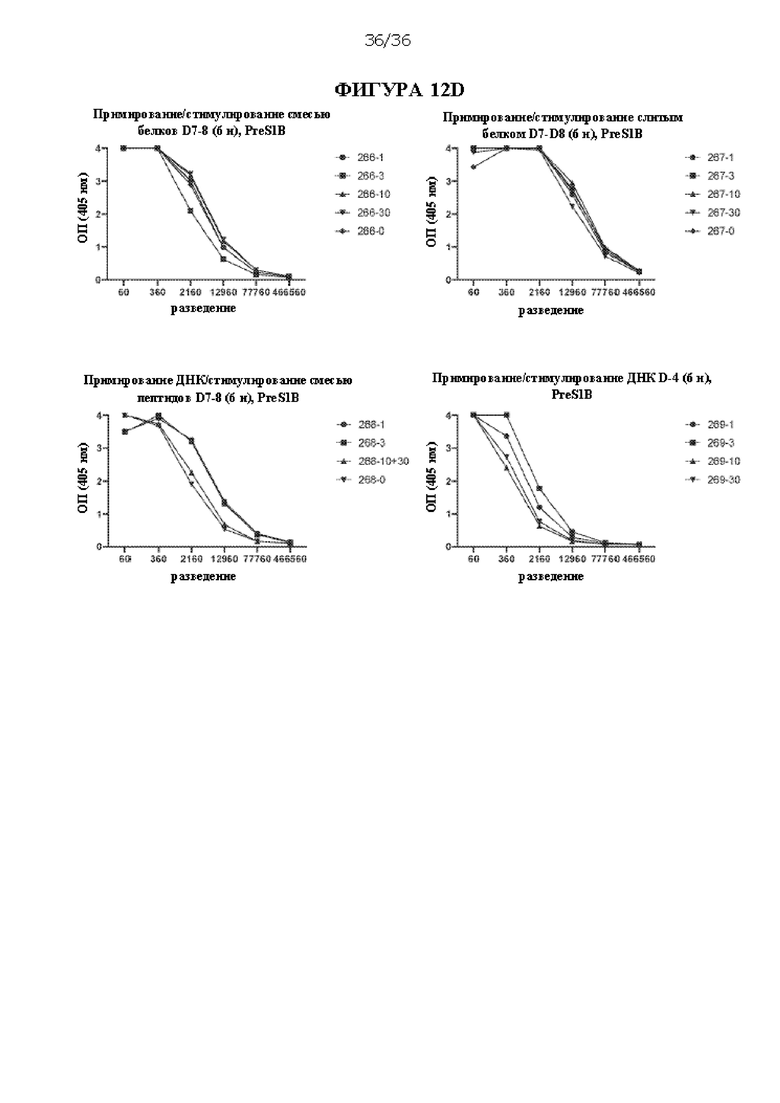
Изобретение относится к области биотехнологии, а именно к комбинации продуктов, содержащей (a) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и (b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1, причем предпочтительно компоненты (a) и (b) указанной комбинации продуктов обеспечены в виде отдельных композиций в составе указанной комбинации продуктов. Изобретение эффективно для индуцирования иммунного ответа на вирус гепатита В и вирус гепатита D у субъекта. 3 н. и 46 з.п. ф-лы, 12 ил., 3 табл., 10 пр.
1. Комбинация продуктов, подходящая для индукции иммунного ответа на вирус гепатита В и вирус гепатита D, которая содержит:
(a) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и
(b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1, причем предпочтительно компоненты (a) и (b) указанной комбинации продуктов обеспечены в виде отдельных композиций в составе указанной комбинации продуктов.
2. Комбинация продуктов по п. 1, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4, или любую их комбинацию.
3. Комбинация продуктов по п. 1 или 2, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе.
4. Комбинация продуктов по любому из пп. 1-3, отличающаяся тем, что указанная нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и при этом указанная последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от последовательности нуклеиновой кислоты HDAg.
5. Комбинация продуктов по п. 4, дополнительно содержащая по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем указанные сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены указанной по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида.
6. Комбинация продуктов по п. 5, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2A тешовируса свиней-1 (P2A), 2A вируса ящура (F2A), 2A вируса ринита лошадей A (ERAV) (E2A) и 2A вируса Thosea asigna (T2A), и при этом каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце.
7. Комбинация продуктов по п. 5 или 6, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ ID NO: 13.
8. Комбинация продуктов по любому из пп. 1-7, отличающаяся тем, что указанная нуклеиновая кислота кодон-оптимизирована для экспрессии у человека.
9. Комбинация продуктов по любому из пп. 1-8, отличающаяся тем, что указанная нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35-36.
10. Комбинация продуктов по любому из пп. 1-9, отличающаяся тем, что указанная нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 18 или SEQ ID NO: 35-36.
11. Комбинация продуктов по любому из пп. 1-10, отличающаяся тем, что указанный по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию.
12. Комбинация продуктов по любому из пп. 1-11, отличающаяся тем, что указанная по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе.
13. Комбинация продуктов по любому из пп. 1-12, отличающаяся тем, что указанная по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от указанной по меньшей мере одной последовательности полипептида HDAg.
14. Комбинация продуктов по любому из пп. 1-13, отличающаяся тем, что указанный полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37.
15. Комбинация продуктов по любому из пп. 1-14, отличающаяся тем, что указанный полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37.
16. Комбинация продуктов по любому из пп. 1-15, отличающаяся тем, что указанный полипептид экспрессирован рекомбинантным образом.
17. Комбинация продуктов по п. 16, отличающаяся тем, что указанный полипептид экспрессирован рекомбинантным образом в системе на основе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе.
18. Комбинация продуктов по любому из пп. 1-17, дополнительно содержащая адъювант.
19. Комбинация продуктов по п. 18, отличающаяся тем, что указанный адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
20. Комбинация продуктов по любому из пп. 1-19, отличающаяся тем, что указанная нуклеиновая кислота включает ДНК.
21. Комбинация продуктов по любому из пп. 1-20, отличающаяся тем, что указанная нуклеиновая кислота обеспечена в рекомбинантном векторе.
22. Способ индуцирования иммунного ответа на вирус гепатита В и вирус гепатита D у субъекта с применением комбинации продуктов согласно любому из пп. 1-21, включающий:
введение указанному субъекту по меньшей мере одной примирующей дозы, содержащей указанную нуклеиновую кислоту; и
введение указанному субъекту по меньшей мере одной стимулирующей дозы, содержащей указанный полипептид.
23. Способ по п. 22, отличающийся тем, что указанная по меньшей мере одна стимулирующая доза дополнительно содержит адъювант.
24. Способ по п. 23, отличающийся тем, что указанный адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
25. Способ по любому из пп. 22-24, отличающийся тем, что указанную по меньшей мере одну стимулирующую дозу вводят по меньшей мере через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 24, 36 или 48 дней или недель после введения указанной по меньшей мере одной примирующей дозы или в пределах диапазона времени, заданного любыми двумя из указанных выше временных точек, например, в пределах 1-48 дней или 1-48 недель.
26. Способ по любому из пп. 22-25, отличающийся тем, что указанное введение обеспечивают энтерально, перорально, интраназально, парентерально, подкожно, внутримышечно, внутрикожно или внутривенно, или любой комбинацией перечисленных путей.
27. Способ по любому из пп. 22-26, отличающийся тем, что указанное введение осуществляют в сочетании с противовирусной терапией.
28. Способ по п. 27, отличающийся тем, что указанная противовирусная терапия включает введение энтекавира, тенофовира, ламивудина, адефовира, телбивудина, эмтрицитабина, интерферона-α, пегилированного интерферона-α или интерферона альфа-2b, или любой их комбинации.
29. Комбинация продуктов для применения при лечении или предотвращении инфекции вирусом гепатита B (HBV) и вирусом гепатита D (HDV), содержащая:
(a) нуклеиновую кислоту, содержащую по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую антиген гепатита D (HDAg), и по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую PreS1; и
(b) полипептид, содержащий по меньшей мере одну последовательность полипептида HDAg и по меньшей мере одну последовательность полипептида PreS1.
30. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 29, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая HDAg, содержит SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3 или SEQ ID NO: 4, или любую их комбинацию.
31. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 29 или 30, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая PreS1, содержит SEQ ID NO: 9 или SEQ ID NO: 10, или обе.
32. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-31, отличающаяся тем, что указанная нуклеиновая кислота сконструирована таким образом, что каждая последовательность нуклеиновой кислоты HDAg сгруппирована с последовательностью нуклеиновой кислоты PreS1, и при этом указанная последовательность нуклеиновой кислоты PreS1 расположена непосредственно по ходу транскрипции от указанной последовательности нуклеиновой кислоты HDAg.
33. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 32, дополнительно содержащая по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую сайт аутокаталитического расщепления пептида, причем указанные сгруппированные последовательности нуклеиновых кислот HDAg и PreS1 разделены указанной по меньшей мере одной последовательностью нуклеиновой кислоты, кодирующей сайт аутокаталитического расщепления пептида.
34. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 33, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит последовательность нуклеиновой кислоты, выбранную из группы, состоящей из нуклеиновых кислот 2A тешовируса свиней-1 (P2A), 2A вируса ящура (F2A), 2A вируса ринита лошадей A (ERAV) (E2A) и 2A вируса Thosea asigna (T2A), и при этом каждый кодируемый сайт аутокаталитического расщепления пептида необязательно может содержать мотив GSG (глицин-серин-глицин) на своем N-конце.
35. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 33 или 34, отличающаяся тем, что указанная по меньшей мере одна последовательность нуклеиновой кислоты, кодирующая сайт аутокаталитического расщепления пептида, содержит SEQ ID NO: 13.
36. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-35, отличающаяся тем, что указанная нуклеиновая кислота кодон-оптимизирована для экспрессии у человека.
37. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-36, отличающаяся тем, что указанная нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 15-24 или 35, 36.
38. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-37, отличающаяся тем, что указанная нуклеиновая кислота содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 18 или SEQ ID NO: 35, 36.
39. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-38, отличающаяся тем, что указанный по меньшей мере один полипептид HDAg содержит SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 или SEQ ID NO: 8, или любую их комбинацию.
40. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-39, отличающаяся тем, что указанная по меньшей мере одна последовательность полипептида PreS1 содержит SEQ ID NO: 11 или SEQ ID NO: 12, или обе.
41. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-40, отличающаяся тем, что указанная по меньшей мере одна последовательность полипептида PreS1 расположена по ходу транскрипции от указанной по меньшей мере одной последовательности полипептида HDAg.
42. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-41, отличающаяся тем, что указанный полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 25-34 или 37.
43. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-42, отличающаяся тем, что указанный полипептид содержит последовательность, по меньшей мере на 80%, 85%, 90%, 95%, 99% или 100% гомологичную последовательности SEQ ID NO: 29, 31, 32 или 37.
44. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-43, отличающаяся тем, что указанный полипептид экспрессирован рекомбинантным образом.
45. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 44, отличающаяся тем, что указанный полипептид экспрессирован рекомбинантным образом в системе на основе млекопитающего, бактерии, дрожжей, насекомого или в бесклеточной системе.
46. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-45, дополнительно содержащая адъювант.
47. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по п. 46, отличающаяся тем, что указанный адъювант представляет собой квасцы, QS-21 или MF59, или любую их комбинацию.
48. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-47, отличающаяся тем, что указанная нуклеиновая кислота включает ДНК.
49. Комбинация продуктов для применения при лечении или предотвращении инфекции HBV и HDV по любому из пп. 29-48, отличающаяся тем, что указанная нуклеиновая кислота обеспечена в рекомбинантном векторе.
| WO 2017132332 A1, 03.08.2017 | |||
| US 5972346 A, 26.10.1999 | |||
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ НЕНАСЫЩЕННЫХY-JIAKTOHOB | 0 |
|
SU251575A1 |
| SINA OGHOLIKHAN AND KATHLEEN B | |||
| SCHWARZ, Hepatitis Vaccines, Vaccines 2016, 4, 6; doi:10.3390/vaccines4010006 | |||
| РЕКОМБИНАНТНАЯ ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ ВИРУСНОГО ГЕПАТИТА В (ВАРИАНТЫ) | 2015 |
|
RU2603729C2 |
Авторы
Даты
2024-02-02—Публикация
2021-01-26—Подача