Изобретение относится к новым физиологическиактивным соединениям, точнее к полимерным гемоглобинам формулы:

где Гб - гемоглобин, Га - глутаровый альдегид с молекулярным весом 6,5·104÷1·106. Изобретение может найти применение в биохимии и медицине в качестве водорастворимой модели переносчика кислорода с сохранением газотранспортной функции (кооперативного взаимодействия между субъединицами) молекул гемоглобина. Ранее получение полимерного гемоглобина с полным сохранением кооперативности не описано.
Известно, что нативный физиологически активный гемоглобин существует в окси- и дезокси-конформациях, обратимый переход между которыми характеризуется кооперативным процессом: в молекуле гемоглобина, состоящей из 4-х субъединиц, существует гем-гемовое взаимодействие, выражающееся в том, что присоединение первой молекулы кислорода к дезоксиформе облегчает присоединение остальных 3-х молекул (кооперативность связывания) E.Antonini, M.Brunori "Hemoglobin and myoglobin in their reaktions with ligands" North Hollahd Publ. Comp.Amsterdam-London, 1971, гл.7, с.153, 367.
В обоих конформациях атом железа в геме двухвалентен. Однако обе конформации нестабильны и при отклонении условий от физиологических атом железа необратимо окисляется до 3-х валентного, давая мет-форму гемоглобина, которая полностью утрачивает кислород-транспортную функцию. (E.Antonini, M.Brunori, (1971 г.) там же, гл.3, с.40).
Дезоксиконформация гемоглобина отличается от оксиконформации тем, что α - концевые аминогруппы блокированы солевыми связями (M.Perutz, Nature, 228, 726, 1970; LaRecherche 14 (2) 677, 1971).
Известны так же другие лигандные формы, например: СО-форма гемоглобина, которая по конформации аналогична окси-форме (E.Antonini, M.Brunori, 1971 г, та же книга "Hemoglobin and myoglobin..." гл.10, с.260).
Известны способы поликонденсации гемоглобина в СО-форме (R.H.Macleod, R.J.Hill, 1970, J.Biol. Chem. 245, №19, 4875) путем взаимодействия с р,р'-дифтор-m,m'-динитродифенилсудьфон-атом. При этом происходит утрата кооперативности, что выражается в полной потере гем-гемового взаимодействия и потере нативной кислород-переносящей функции (константа Хилла П=0,82 вместо 2,5-3,0 для нативного гемоглобина). К потере гем-гемового взаимодействия приводит реакция оксигемоглобина с бифункциональными азокрасителями (H.Fasold, Meyer C., G.Steinkopff (1971), Eur. J.Biochem. 32, №1, 63), константа Хилла в этом случае n=0,7-1,2.
Известен также способ поликонденсации гемоглобина с глутаровым альдегидом (J.W.Payne, 1973, Biochem.J. 135, №4, 867) в фосфатном буфере при нейтральном рН среды при 20°C, в течение 30 мин при перемешивании с последующей инкубацией 48 ч, при 20°C. Целью указанной работы было получение водорастворимых маркеров для электрофореза. При этом использовали дважды перекристаллизованный бычий гемоглобин. Известно, что такой коммерческий продукт содержит 70-80% мет-формы (каталог Serva (1972), Fine biochemical, №24510).
Полученный полимерный мет-гемоглобин не обладал физиологической активностью и не мог переносить кислород.
Целью настоящего изобретения являлось получение полимерного гемоглобина с сохранением нативной конформации и гем-гемового взаимодействия, что выражается в полном сохранении газотранспортной функции нативного белка.
Поставленная цель достигалась тем, что поликонденсацию нативного гемоглобина проводили при 4-6°C в дезоксиконформации, где физиологически важные для газотранспортной функции группы связаны солевыми мостиками. Конкретный пример выполнения изобретения приводится ниже.
К 3 мл 5% раствора гемоглобина в дезоксиформе, предварительно отдиализованного против 0,1М фосфатного буфера рН=7,4, добавляли раствор глутарового альдегида до конечной концентрации 0,2%. Реакцию проводили при 4-6°С с перемешиванием. Избыточные реагенты удаляли диализом против фосфатного буфера. Исследовали молекулярно-массовое распределение полученного полимерного гемоглобина (фиг.1) гель-хроматографией на Sepharose 4B.
Гель-хроматографией полученных образцов полимерного гемоглобина показано широкое молекулярно-весовое распределение от 65000 (10-15%) до 1000000 (30-40%).
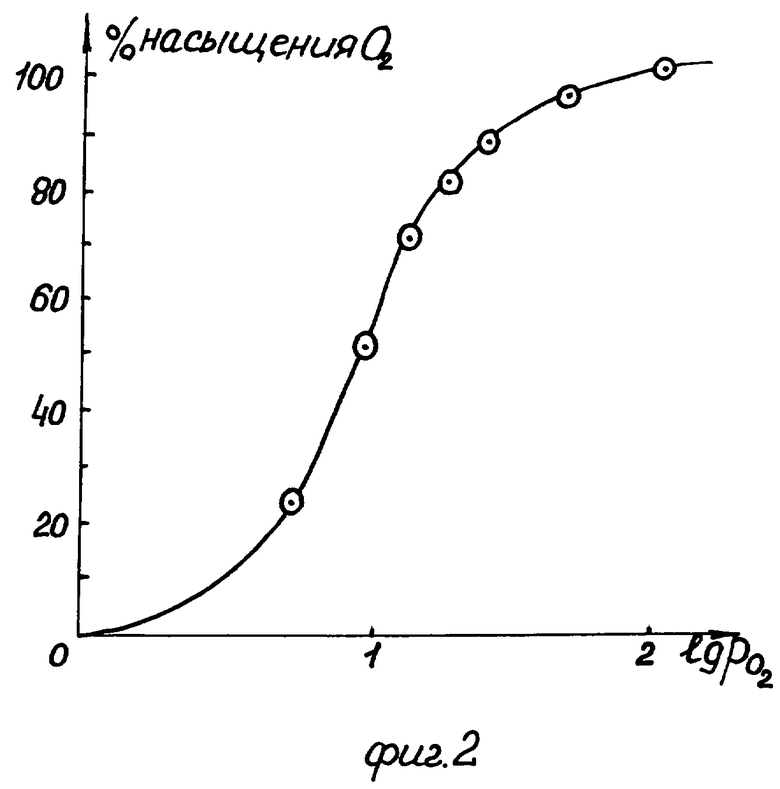
Характеристические параметры газотранспортной функции полимерного гемоглобина, полученные из кривой кислородной диссоциации (фиг.2) практически совпадают с таковыми исходного гемоглобина: сохраняется сигмоидность кривой, сродство к кислороду полимерного гемоглобина (рО2)50≈11 мм Hg, константа Хилла n=2,1; для гемоглобина (pO2)50≈10 мм Hg, n≈2,5-3,0.
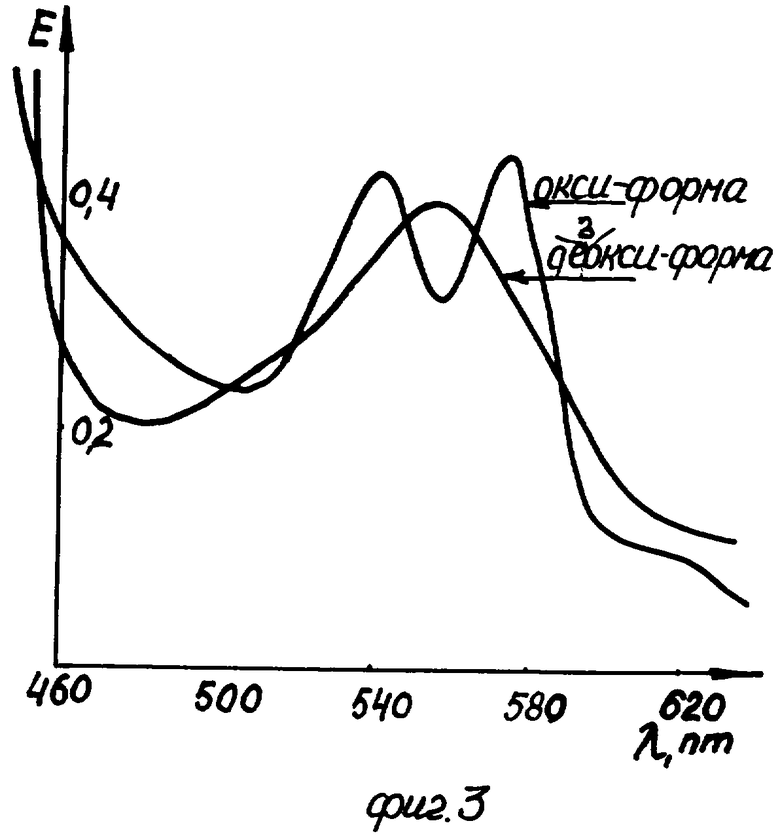
Сохранение нативной конформации гемоглобина после конденсации подтверждено также отсутствием изменений в спектрах окси- и дезокси-форм полимерного гемоглобина по сравнению со спектрами нативного белка (фиг.3).
| название | год | авторы | номер документа |
|---|---|---|---|
| КРОВЕЗАМЕНИТЕЛЬ С ФУНКЦИЕЙ ПЕРЕНОСА КИСЛОРОДА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2008 |
|
RU2361608C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО МОДИФИЦИРОВАННОГО ГЕМОГЛОБИНА | 2012 |
|
RU2504387C2 |
| КРОВЕЗАМЕНИТЕЛЬ - ПЕРЕНОСЧИК КИСЛОРОДА, СОСТАВ ДЛЯ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО МОДИФИЦИРОВАННОГО ГЕМОГЛОБИНА | 1999 |
|
RU2162707C2 |
| ПОЛИФУНКЦИОНАЛЬНЫЙ ПОЛИГЕМОГЛОБИН-ФЕРМЕНТНЫЙ КОМПЛЕКС | 2010 |
|
RU2432172C1 |
| Способ выявления у микроорганизмов протективного действия на молекулу гемоглобина | 2017 |
|
RU2687061C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИГЕМОГЛОБИНА С ПОВЫШЕННОЙ КИСЛОРОДТРАНСПОРТНОЙ ЭФФЕКТИВНОСТЬЮ | 1996 |
|
RU2132687C1 |
| ПРИМЕНЕНИЕ ГЕМОГЛОБИНА ПОЛИМЕРИЗОВАННОГО ДЛЯ МОБИЛИЗАЦИИ КРОВИ ИЗ ДЕПО ПРИ КРОВОПОТЕРЯХ | 2021 |
|
RU2811253C2 |
| КОНЪЮГАТЫ ГЕМОГЛОБИНА С ПОЛИСАХАРИДОМ | 1999 |
|
RU2225222C2 |
| СПОСОБ СВЯЗЫВАНИЯ БЕЛКА | 1974 |
|
SU1840581A1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОЙ СУПЕРОКСИДДИСМУТАЗЫ | 1991 |
|
RU2046143C1 |
Изобретение относится к области химической модификации биополимеров и может быть использовано для создания кровезаменителя - переносчика кислорода. Заявлен полимерный гемоглобин формулы 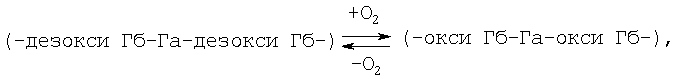
где Гб - гемоглобин, а Га - глутаровый альдегид, с молекулярным весом 6,5·104-1·106, обладающий способностью сохранять газотранспортную функцию гемоглобина. Способ его получения заключается в конденсации нативного гемоглобина в дезоксиконформации с би-функциональными реагентами, например, с глутаровым альдегидом, в буферных растворах, при нейтральных значениях рН и 4-6°С. Полимерный гемоглобин сохраняет нативную конформацию гем-гемового взаимодействия, что выражается в полном сохранении газотранспортной функции молекул гемоглобина. 2 н.п.ф-лы, 3 ил.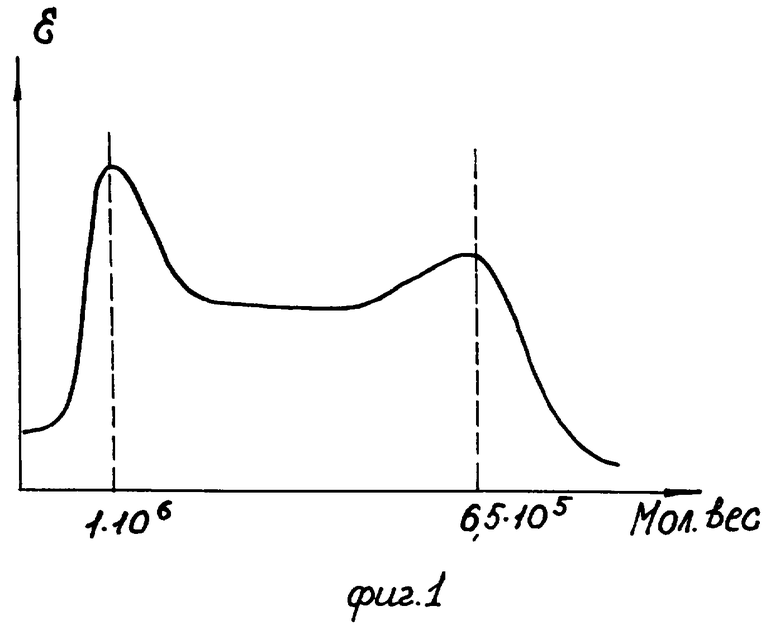
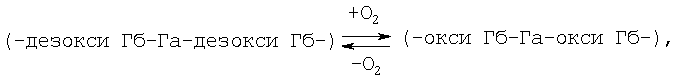 ,
,
где
Гб - гемоглобин, а Га - глутаровый альдегид, с молекулярным весом 6,5·104-1·106, обладающий способностью сохранять газотранспортную функцию гемоглобина.
Авторы
Даты
2007-01-10—Публикация
1976-07-02—Подача