Изобретение относится к области получения новых соединений, которые могут найти применение в фармацевтической промышленности.
Предложен способ получения З-кето-сс-4карбоксамидоалкил-2,3-дигидро-1,4 - бензоксазиноБ общей формулы
Кб
CHRrCO-N/
R,
где RI - атом водорода или низший алкильный радикал, прямой или разветвленный;
Ra, Rg, Ri могут иметь одинаковые или различные значения - атом водорода, низший алкильный радикал, прямой или разветвленный, галоидный атом или низший алкилоксирадикал;
Rs - атом водорода или низший алкильный радикал или группа N-диалкилкарбоксамидо;
Re и Rv могут иметь одинаковые или различные значения - атом водорода, радикал арила или низший алкильный или оксиалкильный радикал, либо Rg и Ry вместе взятые, образуют с атомом азота, с которым они связаны, гетероциклические радикалы с 5 или 6 атомами углерода, которые могут содержать, кроме атома азота, другие гетероатомы, например пирролидил, пинеридил, морфолил или
пиперазинил. Причем низший алкил относится к алкильному радикалу, содержащему от 1 до 6 атомов углерода.
Способ заключается в том, что 3-оксо-2,3-дигидро-1,4-бензоксазин в виде соли щелочного
металла общей формулы
15
где RI, R2, Rs и R4 имеют вышеуказанные значения,
М - щелочной металл, подвергают взаимодействию со сложным эфиром общей формулы
X -CHRs -COOR
где X - галоид, R-низший алкил, Rs имеет; вышеуказанные значения, в среде органического растворителя, преимущественно в среде третичного бутилового спирта. При необ.ходимости для ускорения этой стадии можно добавить небольшое количество йодистого или
бромистого калия или вести эту стадию в смеси растворителей, содержащих приблизительно 50% диметилформамида. Полученный при этом сложный эфир подвергают омылению в водноспиртовой среде при кипении в присутствии гидроокиси щелочного металла, например гидроокиси калия. Получают кислоту, которую обрабатывают сначала взятым в небольщом избытке хлористым тионилом в среде инертного органического растворителя и при необходимости в присутствии катализатора, например пиридина, диметилформамида, при температуре 60-80°С, а затем - избытком аммиака или амина общей формулы
/Ко
HN R,
где Ro и RT имеют выщеуказанные значения, в среде инертного пенолярного органического растворителя, например хлороформа. Продукты выделяют известным способом. Выход 51 - 84%.
Пример 1. Получение З-кето-а-4-диэгиленоксикарбоксамидометил-2,3 - дигидро - 1,4бензоксазина.
В колбе с двумя трубками, снабженной мещалкой, дефлегматором и ампулой с бромом, приготовляют раствор третичного бутилата калия (растворением 6,55 г металлического калия в 250 см третичного бутилового спирта). Раствор, охлажденный до 40°С, интенсивно перемещивают, к нему добавляют 26 г 3-оксо-2,3-дигидро-1,4-бензоксазина,загем
прикапывают 20,5 г этилхлорацетата. Смесь нагревают с флегмой при перемещивании в течение 7 час, растворитель отгоняют в вакууме, и остаток отбирают при помощи приблизительно 200 см воды.
Осадок, частично кристаллический, экстрагируют эфиром, органический раствор промывают водой и сущат (MgSO4), растворитель отгоняют, и остаток кристаллизуют из окиси изопропила. Полученный таким путем 3-oicco4 - карбэтоксиметил - 1,4- дигидробензоксазин плавится при 78°С. Выход 30,8 г (79%).
Вычислено для di-HisNOj, %: С 61,27; Н 5,57; N 5,96.
Найдено, %: С 61,27; Н 5,62; N 6,04.
20 г полученного сложного эфира нагревают 1 час с флегмой с 5,5 г калия в водноспиртовой среде (спирта 200 сМ воды 15 слз), растворитель отгоняют в вакууме, остаток растворяют в воде, раствор, обработанный на животном угле, фильтруют, затем подкисляют 4 Н. соляной кислотой. Осадок сущат, промывают водой и сущат в вакууме над фосфорной кислотой. Выход 16,9 г (92%). З-Оксо-4-карбоксиметил-2,3-дигидро-1,4-бензоксазин, очищенный кристаллизацией в этаноле, плавится при231°С.
Вычислено для CioH9NO4, %: С 57,97; Н 4,38; N 6,76.
го тионила и 0,1 огз безводного пиридина. Смесь нагревают 1 час с флегмой, раствооитель и избыток хлористого тионила отгоняют в вакууме. Твердый остаток растворяют Б 60 СМ - безводного хлороформа, и раствор прикапывают к охлажденному в ледяпой бане и быстро перемещиваемому раствору морфолина (8,7 слгз) в хлороформе (60 слгз). После окончания прикапывания смесь при комнатпой температуре еще перемещивают 2 час, осадок отделяют фильтрованием, затем промывают хлороформом. Соединенные органические растворы промывают отстаиванием, сначала 4 Н. НС1, затем водой, 2 н. NaOn и снова водой. После сущки (MgSOj) растворитель отгоняют, и остаток кристаллизует из бензола. Выход 7,68 г (69,7%).
Для анализа З-кето-а-4-диэтиленоксикарбоксамидометил-2,3-дигидро-1,4-бензоксазин сущат при 110°С 15 мин; т. нл. 155--156°С.
Вычислено для СцП1(;-М2О4, %: С 60,86; Н 5,84; N 10,14.
Найдено, %; С 60,83; Н 6,11; N 10,24. П р и м е р 2. Получение 3-оксо-Н-4-диметилкарбоксамидометил-2,3-дигидро-1,4 - бензоксазина.
Хлорангидрид, выделенный как описано в примере 1, полученный из 8,3 г З-оксо-4-карбоксиметил-2,3-дигидро-1,4-бензоксазина в растворе 60 сжз хлороформа прикапывают к 22 слгз раствора диметнламина в хлороформе, быстро неремещиваемого и охлаждаемого в ледяной бане. По окончании добавления смесь перемешивают 2 час при комнатной темиературе, затем фильтруют и промывают осадок хлороформом, органический раствор последовательно промывают 4 н. ПС1, водой, 2 н. NaOH, затем сущат (MgS04). Растворитель выпаривают, и твердый остаток кристаллизуют из смеси бензола (один объем) и циклогексана (два объема); т. пл. 125-126°С, выход 6,17 г (66%).
Вычислено для Ci2Hi4N203, %: С 61,52; Н 6,02; N 11,96. Найдено, %; С 61,43; Н 6,12; N 11,99.
В таблице приведены константы соединений, полученных по примерам 1 и 2. Соответствующую кислоту получают, как описано в примере 1; конденсацией соли калия З-кето-6-хлор2,3-днгидробензоксазина и этнлхлорацетата получают 3-кето-4-карбэтоксиметил-6-хлор-2,3-дигидро-1,4-бензоксазина, т. нл. 115°С (кристаллизация из смеси циклогексан - эфир).
Вычислено, %: С 53,44; Н 4,49; N 5.19; С1 13,15.
Найдено, %; С 53,29; Н 4,48; N 4,97; С1 13,16.
В результате омыления З-кето-4-карбэтоксиметил-6-хлор-2,3-дигидро-1,4-бензоксазина иолучают 3-кето-4-карбоксиметил-6-хлрр-2,3-дигидро-1,4-бензоксазин; т. пл. 197°С (кристаллизация из этилацетата).
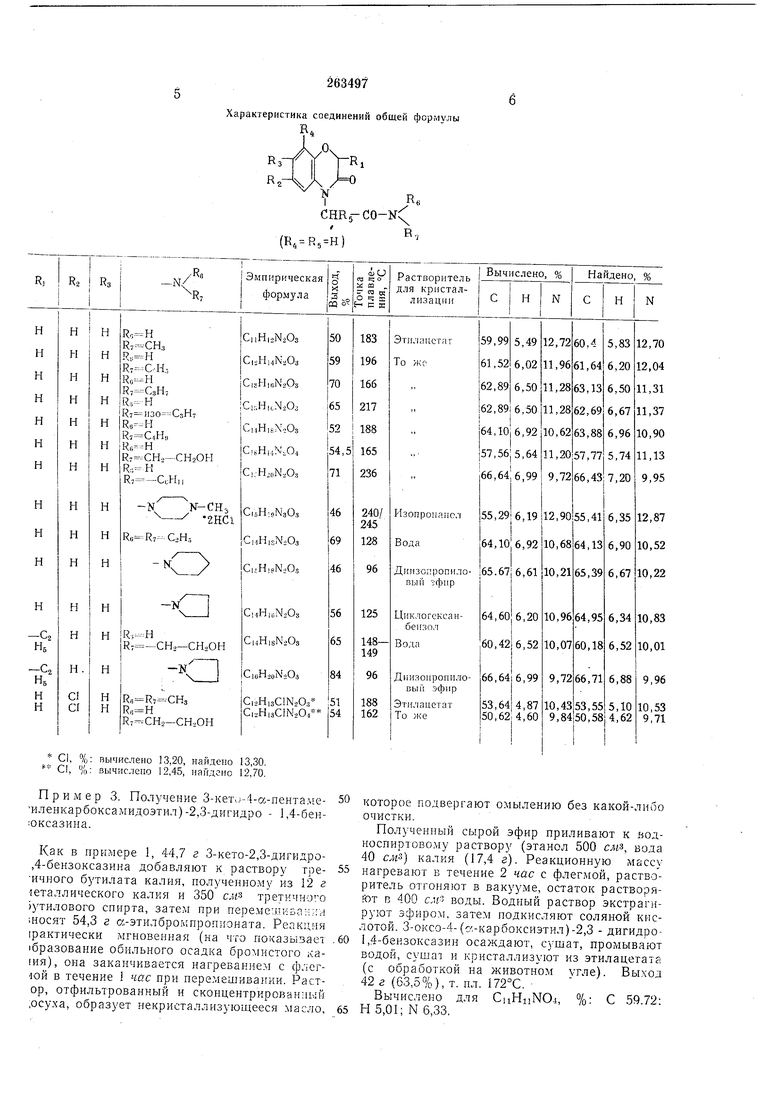
Характеристика соединений общей формулы
R.
CHR.-CO-N
(R, R,H)
/ R,


| название | год | авторы | номер документа |
|---|---|---|---|
| ПАТЕНТНО-ТЕХКл4ЕСНДе| | 1971 |
|
SU309517A1 |
| Способ получения нафтиридинхинолин-или бензоксазинкарбоновых кислот или их фармацевтически допустимых солей присоединения кислоты | 1983 |
|
SU1360584A3 |
| Способ получения 2-замещенных 1,4-бензодиазепинов | 1976 |
|
SU1126209A3 |
| ОПТИЧЕСКИ АКТИВНЫЕ ПРОИЗВОДНЫЕ ПИРИДОБЕНЗОКСАЗИНА ИЛИ ИХ СОЛИ | 1991 |
|
RU2029771C1 |
| Способ получения производных бензодиазепина или их солей | 1973 |
|
SU625607A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-ОКСО-2,3-ДИГИДРОБЕНЗОКСАЗИНА-1,4 | 1971 |
|
SU321004A1 |
| КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИНГИБИТОРЫ СКВАЛЕН-СИНТЕТАЗЫ | 1994 |
|
RU2129547C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОПТИЧЕСКИ АКТИВНЫХ ПРОИЗВОДНЫХ | 1973 |
|
SU373936A1 |
| Способ получения гидразинопири-дАзиНОВ | 1975 |
|
SU799661A3 |
| Способ получения 4-/алкиламиноалкил/-(4н)тиено(3,2-в)( ) бензазепинов | 1973 |
|
SU559648A3 |

С1. %: вычислено 13,20, найдено 13,30. С1, %: вычислено 12,45, найдено 12,70.
Пример 3. Получение 3-ке1..-пента.меиленкарбоксамидозтил)-2,3-дигидро - 1,4-бенюксазина.
Как в примере 1, 44,7 г 3-кето-2,3-дигидро,4-бензоксазина добавляют к раствору треичного бутилата калия, полученному из 12 г 1еталлического калия и 350 слгз третично-о )утилового спирта, затем при перемениБПн;:и 1НОСЯТ 54,3 г с;.-этилбромпроиионата. Реакция |рактически мгновенная (на что показызас |бразование обильного осадка бромистого ), она заканчивается нагреванием с флег10Й в течение i час при перелМешивании. Растор, отфильтрованный и сконцентрированный ,осуха, образует некристаллизуюндееся масло,
которое подвергают омылению без какой-либо очистки.
Полученный сырой эфир приливают к водноспиртовому раствору (этанол 500 слгз, вода 40 слз) калия (17,4 г). Реакционную массу нагревают в течение 2 час с флегмой, растворитель отгоняют в вакууме, остаток растворяют п 400 cj/з воды. Водный раствор экстрагируют эфиром, затем подкисляют соляной кислотой. 3-оксо-4-(с .-карбоксиэтил)-2,3 - дигидро1,4-бензоксазнн осаждают, сушат, промывают водой, сушат и кристаллизуют из этилацетата (с обработкой на животном угле). Выход 42 г (63.5%), т. пл. 172°С.
Авторы
Даты
1970-01-01—Публикация