(54) СПОСОБ ПОЛУЧЕНИЯ 3(-АЛКИЛАМИНОАЦИЛАМИНО)-БЕНЗОДИОКСАНОВ-1,4.:
; . 1
Изобретение касается шособа получения новых замещенных бензодаоксанов - 1,4, а именно 5 - (wалкиламиноациламино) - бензодаоксанов - 1Акоторые Аюгут найти применение в фармзколопш.
Предложенный способ основан на широко известных в органическом оштезе реакциях ацилирования и аминирования гетероциклических соедане НИИ, содержаищх в своем шкле кисло|род, и позволяет получить новые соединения, обладаюцще более ценными свойствами, чём известные ранее акалогичиые соединения.
Предлагается шособ получения 5 - ( агасиламинЬациламцнс4 - бензодиокошов 1,4оацей формулы
КНбО(СНг)МЕ 2 ,25НВ2-Ж Нз)
хлорангвдридом vf - хлорзамещенных кислот в среде органического растворителя, например толуола, с последующим взаимодействием полученного 5 (W хлоращша но ) бензодиоксана с соответствующим амином в среде органического растворителя, например спирта, и вьщелением целевого продукта известными приемами.
Способ прост и позволяет получить выход целевого продукта от 57 до 87 %.
Вследствие введения ц качестве заместителя алкищминоащшаминогрупп полученные новые замещенные беизодиоксань - 1,4 должны обладать рядом новых интересных свойств.
Пример. Раствор 0,11 г моль хлорангидрида соответствующей хлоркислоты в 100 мл безводно5го толуола прибавляют при температуре не выше 15° С к раствору 0,10 г-МО ль 5 - аминобензодиоксана И в 100мл безводного толуола и реакционную смесь кипятят при перемешивании 3 час. Затем смесь охлаждают до 20° С, отфилыровьшают
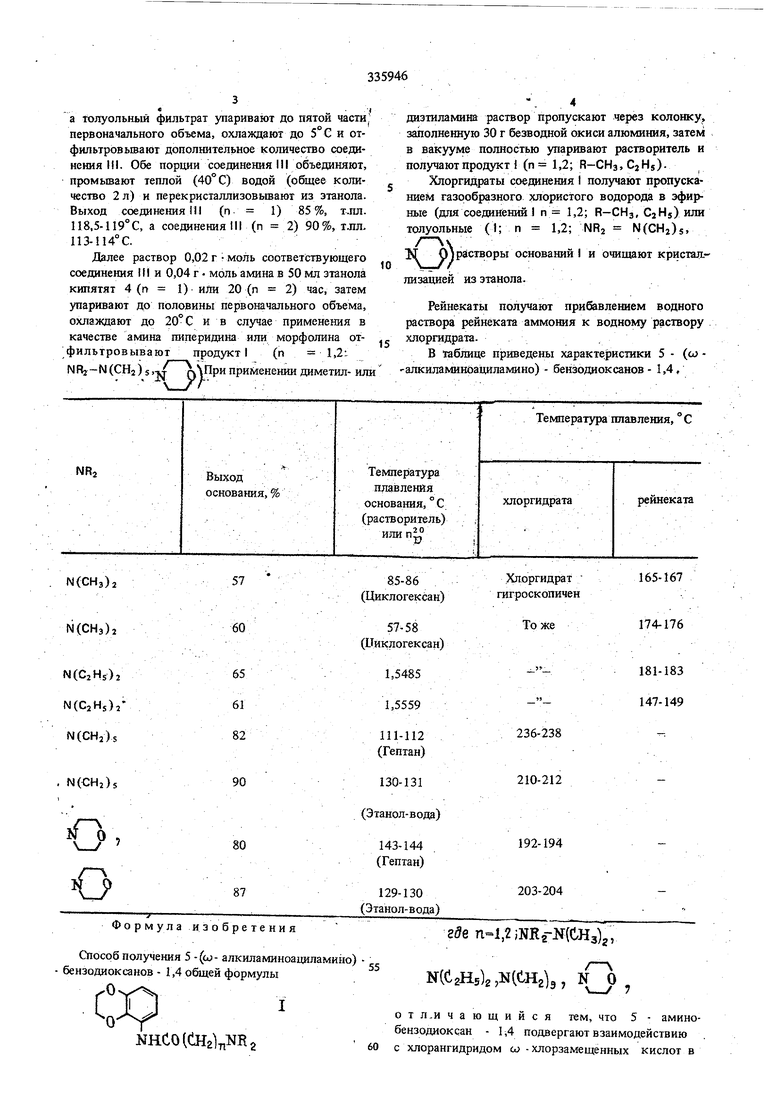
0 соединение а толуольный фильтрат упаривают до пятой части первоначального объема, охлаждают до 5 С и отфильтровывают дополнительное количество соединения III. Обе порции соединения 111 объединяют, промьтают теплой (40° С) водой (общее количество 2л) и перекристаллизовывают из этанола. Выход соединения Ml (п- 1) 85%, т.Ш1. 118,5-119°С, а соеданенияШ (п 2) 90%, тлл, 113-114° С. Далее раствор 0,02 г моль соответствующего соединения III и 0,04 г моль амина в 50 мл этанола кипятят 4 (п 1) или 20 (л 2) час, затем упаривают до половины первоначального объема, охлаждают до 20° С и в случае применения в качестве амина пиперидина или морфолина отфильтровывают продукт I (п 1,2; NRj-N(CHj)5,j МПРИ I применении диметил- или диэтиламина раствор пропускают через колонку, заполненную 30 г безводной окиси алюминия, затем в вакууме полностью упаривают растворитель и получают продукт i (п 1,2; R-CH3,CjHs)Хлорпщраты соединения получают пропусканием газообразного хлористого водорода в эфирные (для соедин1ений 1 п 1,2; R-СНз, С2Н5) или толуольные (1; п 1,2; NRj N(€N2)5. К PJ растворы оснований I и очищают кристаллизацией из этанола. Рейнекаты получают прибавлением водного раствора рейнеката аммония к водному раствору хлоргидрата. В таблице приведены характеристики 5 - (w алкиламинбациламино) - бензодиок санов - 1,4,
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 6-алкил-7-( -алкиламиноациламино)-бензодиоксанов-1,4 | 1971 |
|
SU388551A1 |
| Способ получения производных дифениламина | 1976 |
|
SU628811A3 |
| ТРИЦИКЛИЧЕСКИЕ ПРОИЗВОДНЫЕ ПИРРОЛА, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1994 |
|
RU2128649C1 |
| Способ получения производных 1,4-диазепина или их солей | 1975 |
|
SU583758A3 |
| Способ получения 6-амино-1,2-дигидро-1-окси-2-имино-4-пиперидинопиримидина | 1987 |
|
SU1498390A3 |
| АМИДЫ АМИНОКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2134683C1 |
| Способ получения замещенных - 2-(фурил-2)-этил -пропиниламина или их солей,или их оптических изомеров | 1976 |
|
SU741796A3 |
| 5-( ω - АМИНОАЦИЛ)-5,10-ДИГИДРО-11H-ДИБЕНЗО[B, E] [1,4]-ДИАЗЕПИН-11-ОНЫ ИЛИ ИХ СОЛИ, ОБЛАДАЮЩИЕ ПРОТИВОАРИТМИЧЕСКОЙ АКТИВНОСТЬЮ | 1989 |
|
RU2026862C1 |
| Способ получения сложных эфиров аповинкаминовой кислоты | 1981 |
|
SU1114336A3 |
| Способ получения соединенийиМидАзО (1,5-A)(1,4)диАзЕпиНАили иХ фАРМАцЕВТичЕСКи пРиМЕНи-МыХ СОлЕй | 1975 |
|
SU814278A3 |

Формула изобретения г5е ,2 iNRf-WHa) .5, , среде opraHHMetKoro растворителя, например толуола, с последующим взаимодействием полученного 5 - (со - хлорациламино) - беизодиоксана с ., . соответствующим амином в среде органического растворителя, например спирта, и выделением целевого продукта известными приемами.

Авторы
Даты
1977-04-05—Публикация
1971-01-06—Подача