Изобретение относид-ся к способам получения производных 2,4-дихлорфеноксиуксуспой кислоты (2,4-Д}, а именно сложных эфиров Р-ОКСИЭТИЛОВОГО эфира 2,4-Д, которые могут оыть использованы в сельском хозяйстве в качестве гербицидов.
Известен способ получения эфиров 2,4-Д, например бутилового эфира, путем взаимодействия бутилового спирта с 2,4-Д в присутствии фосфористой кислоты и растворителя при пагревапии. Однако бутиловый эфир 2,4-Д обладает высокой летучестью, пары его способны повреждать посевы культурных растений.
Бутиловый эфир 2,4-Д отличается резким пеириятным запахом. Эфиры высокомолекулярных спиртов, обладая меньшей летучестью, чем Эфиры бутилового спирта, но гербин,идной активности уступают им.
С целью получеппя нового эфира 2,4-Д, обладающего малой летучестью и достаточно высокой гербицидной активностью, предлагается способ получения сложных эфиров Р-ОКСИЭТИЛОВОГО эфира 2,4-Д, основанный на взаимодействии р-хлорэтилового эфира 2,4-Д с солями карбоновых кислот при нагревании до 130-150°С. Целевые продукты выделяют известными способами.
активность по мере увеличения молекулярного веса не только не уменьшается, как у эфиров одноатомных спиртов, а увеличивается, что является неожиданным.
Гербицидная активность каприлоксиэтилового эфира 2,4-Д п сравнению с бутиловым эфиром значительно выше. Капрйлоксиэтиловый эфир является более высококипяш.им эфиром и обладает резко выраженной селективностью.
Новый класс эфиров обладает свойствами гербицидов системного действия с резко выраженной селективностью.
При М е р. Получение ацетоксиэтилового эфира 2,4-дихлорфеноксиуксуспой кислоты.
Смесь 28,3 г р-хлорэтилового эфира 2,4-Д, 9,5 г свежеирокаленного уксуснокислого калия и 70 мл м-ксилола перемешивают 10 час при 130-140°С. По окончании реакции в колбу добавляют воду, после чего делают бензольную вытяжку. Продукт сушат над сернокислым натрием. После отгонки растворителя вакуумной разгонкой выделяют 10 г ацетоксиэтилового эфира 2,4-Д, т. кип. 199-
200°С; По L5320; df 1,3782, выход 45%. Реакцию можно вести и без растворителя при нагревании до 140-150°С.
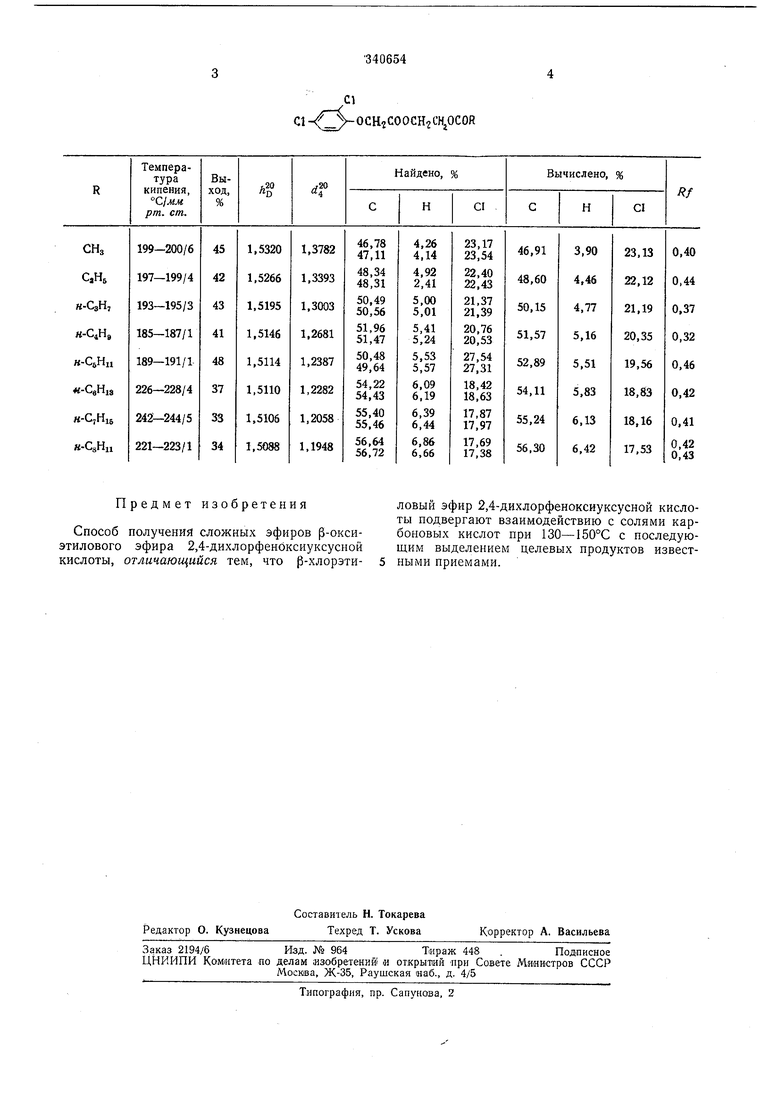
Cl Ct- OCH COOGH CH OCOR
| название | год | авторы | номер документа |
|---|---|---|---|
| Ацилоксиэтиловые эфиры /2,4-дихлорфенокси/-масляной кислоты | 1974 |
|
SU504756A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННЫХ СЛОЖНЫХ ЭФИРОВ ГЛИКОЛЯ | 1970 |
|
SU278672A1 |
| СПОСОБ ПОЛУЧЕНИЯ СМЕШАННЫХ СЛОЖНЫХ ЭФИРОВ | 1973 |
|
SU386917A1 |
| Способ получения 2,4-дихлорфеноксиуксусного эфира 2-оксиэтиловых эфиров синтетических жирных кислот фракции с @ -с @ | 1978 |
|
SU889657A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ КАРБОНОВЫХКИСЛОТ | 1971 |
|
SU292957A1 |
| ГЕРБИЦИД | 1972 |
|
SU426637A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНО- ИЛИ ДИПОЛИФТОР- АЛКИЛОВЫХ ЭФИРОВ ГЛИКОЛЕЙ | 1972 |
|
SU424855A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ЭФИРОВ ЭТИЛЕНГЛИКОЛЯ и 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ И ЖИРНЫХкислот С5~Сб | 1973 |
|
SU389078A1 |
| Способ получения сложных эфиров 1,4-дигидропиридинкарбоновой кислоты или их солей | 1974 |
|
SU515452A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ о-АМИДОФЕНИЛ- ФОСФОРИСТОЙ КИСЛОТЫ | 1969 |
|
SU245101A1 |

Предмет изобретения Способ получения сложных эфиров |3-оксиэтилового эфира 2,4-дихлорфенбксиуксусной кислоты, отличающийся тем, что р-хлорэти- 5 ловый эфир 2,4-дихлорфеноксиуксусной кислоты подвергают взаимодействию с солями карбоновых кислот при 130-150°С с последующим выделением целевых продуктов известными приемами.
Авторы
Даты
1972-01-01—Публикация