1
Изобретение относится к способу получения N-замещенных эфиров или тиоэфиров Nхлорметилкарбаминовых кислот общей формулы
C1-CH,-N-CO-X-RS(I)
I R
где R и R - алкил, алкенил, алкинил, галоидалкил, галоидалкенил, галоидалкинил, циклоалкил, циклоалкенил, замещенный арил или замещенный аралкил, X - кислород или сера.
Известен способ получения N-замещенных эфиров N-хлорметилкарбаминавых кислот взаимодействием монозамещеиных эфиров карбаминовых кислот с параформальдегидом и хлористым водородом.
Предлагаемый способ основан на известном химическом методе. Однако применение в качестве исходных соединений других монозамещенных эфиров и тиоэфиров карбаминовых кислот позволяет получить новые соединения, которые можно использовать в качестве специальных продуктов, применяемых в текстильной промыщленности.
Предлагаемый способ состоит в том, что монозамещенные эфиры или тиоэфиры карбаминовых кислот формулы
H-N- CO-X-R,
(II) I R
где R, R и X имеют указанные значения, подвергают взаимодействию с параформальдегидом и хлористым тиони.п:ом.
Применяемые в качестве исходных продуктов N - монозамещенные эфиры и тиоэфиры
карбаминовых кислот определены общей формулой (И), в которой R и R2 предпочтительно означают неразветвленный или разветвленный алкил с Ci-€20, в частности с , неразветвленный или разветвленный алкенил,
предпочтительно с Сз-Се, в частности с Сз- -€4, неразветвлеиный или разветвленный алкинил, предпочтительно с Сз-Се, в частности с Сз-С4. Кроме того, R и R означают галоидалкил, предпочтительно с С2-Се, в частности с С2-С4 в алкильной части и с 1 - 4 атомами галоида, причем пригодны, прежде всего фтор или хлор. R и R означают также галоидалкенил и галоидалкинил, .причем алкенильная или алкинильная часть содержит
Сз-Сб, предпочтительно Сз-С4, и в качестве галоида можно использовать предпочтительно 1-4 атома галоида, в частности фтора или хлора. Кроме того, R и R .представляют собой циклоалкил и циклоалкенил с Сз-Cs,
предпочтительно с Сз-С, замещенный ъ случае необходимости арил, предпочтительно с Сб-Сю и замещенный в случае необходимости аралкил, предпочтительно с Се-Сю в арильной и с Ci-Cz в алкильной части.
В качестве заместителей арильного или аралкильного радикала пригодны: арильные радикалы с Се-Сю, разветвленные или перазветвленные алкильные радикалы, предпочтительно с Ci-С4, разветвленные или неразветвлениые галоидалкильные радикалы, предпочтительно с Ci-С2 и 1-5 атомами фтора или хлора в качестве галоида, в частности трихлорметил или трифторметил, разветвленные или неразветвленные алкоксигруппы, предпочтительно с Ci-С4, арилоксигруппы, предпочтительно с Се-Сю, циклоалкил и циклоалкенил, предпочтительно с СБ-Су, в частности с Cs. Кроме того, арильный или а-ралкильный радикал может быть замещен нитрогруппами или галоидом, предпочтительно фтором, хлором или бромом.
В качестве исходных соединений используют N-монозамещенные эфиры или тиоэфиры карбаминовых кислот.
В качестве разбавителей при предлагаемом взаимодействии можно использовать все инертные органические растворители, например, предпочтительно такие углеводороды, как бензол или толуол, такие галоидированные углеводороды, как хлорбензол или 1,2-дихлорбензол, такие нитроароматические соединения, например нитробензол и любые смеси из этих растворителей; особенно пригодными являются бензол или толуол.
Температуру реакпии можно изменять в широких пределах, обычно работают в пределах 10-120°С, предпочтительно 15-70°С.
Обычно реакцию проводят при нормальном давлении. При проведении реакции ino предлагаемому способу обычно применяют эквимолярные количества N-монозамещенных эфиров или тиоэфиров карбаминовых кислот, параформальдегида и хлористого тионила. В случае необходимости можно применять небольшой избыток (1-5%) параформальдегида. Компоненты реакции смешивают с четырехкратным количеством разбавителя и перемешивают при комнатной температуре. Смесь
при этом нагревается до 30-60°С, и после достижения максимальной температуры реакция завершается. Разбавитель отгоняют и остаток перегоняют в вакууме.
Пример 1. 356 г (4 моля) метилового эфира N-метилкарбаминовой кислоты растворяют в 2 л безводного бензола. При сильном перемешивании добавляют 120 г (4 моля) параформальдегида и 476 г (4 моля) хлористого тионила. Эту смесь нагревают до 45°С в течение 2 ч. Спустя 30 мин растворитель отгопяют при нормальном давлении и остаток перегоняют в вакууме. Получают 616 г (95% теории) метилового эфира Ы-метил-М-хлорметилкарбаминовой кислоты; т. кип. 68-69°С при 10 мм рт. ст. и показателе.м преломления rf° 1,4535.
Пример 2. В течение 4 ч при сильном
пере.мешивании смешивают 610 г (3,03 моля) а-нафтилового эфира N-метилкарбаминовой кислоты, 90,1 г (3,0i3 моля) параформальдегида и 360,5 г (3,03 моля) хлористого тионила и 3 л бензола. После отгонки растворителя в
вакууме получают 746 г (99% теории) а-нафтилового эфира N-мeтил-N-xлopмeтилкapбaминовой кислоты в виде бесцветного масла с показателем преломления « 1,6013.
Пример 3. 332 г (2,1 моля) S-изопропилового эфира N-н-пропилтиокарбаминовой кислоты растворяют в 1 л бензола, добавляют 68 т (2,3 моля) параформальдегида и 245 г (2,1 моля) хлористого тионила и перемешивают в течение 1,5 ч. Затем растворитель отгоняют и остаток перегоняют в вакууме.
Получают 389 г (90% теории) тиоизопропилового эфира М-н-Пропил-Ь1-хлорметилкарбаминовой кислоты с т. кип. 90-92°С/0,2 мм рт. ст.
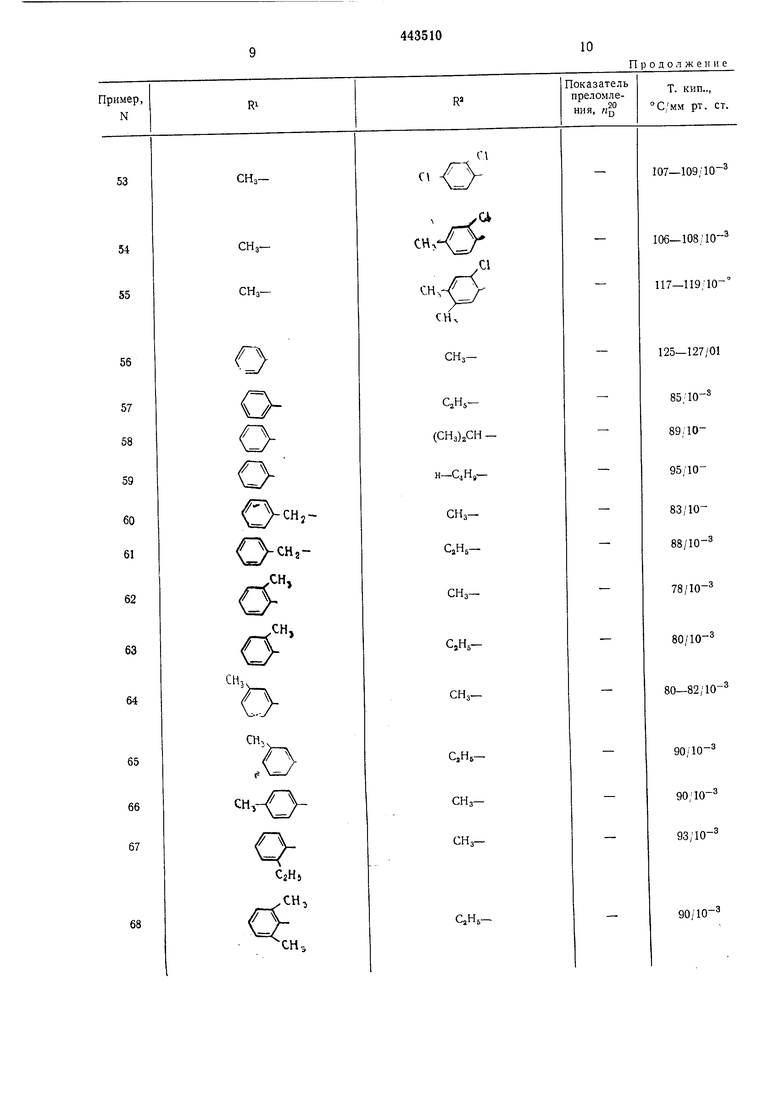
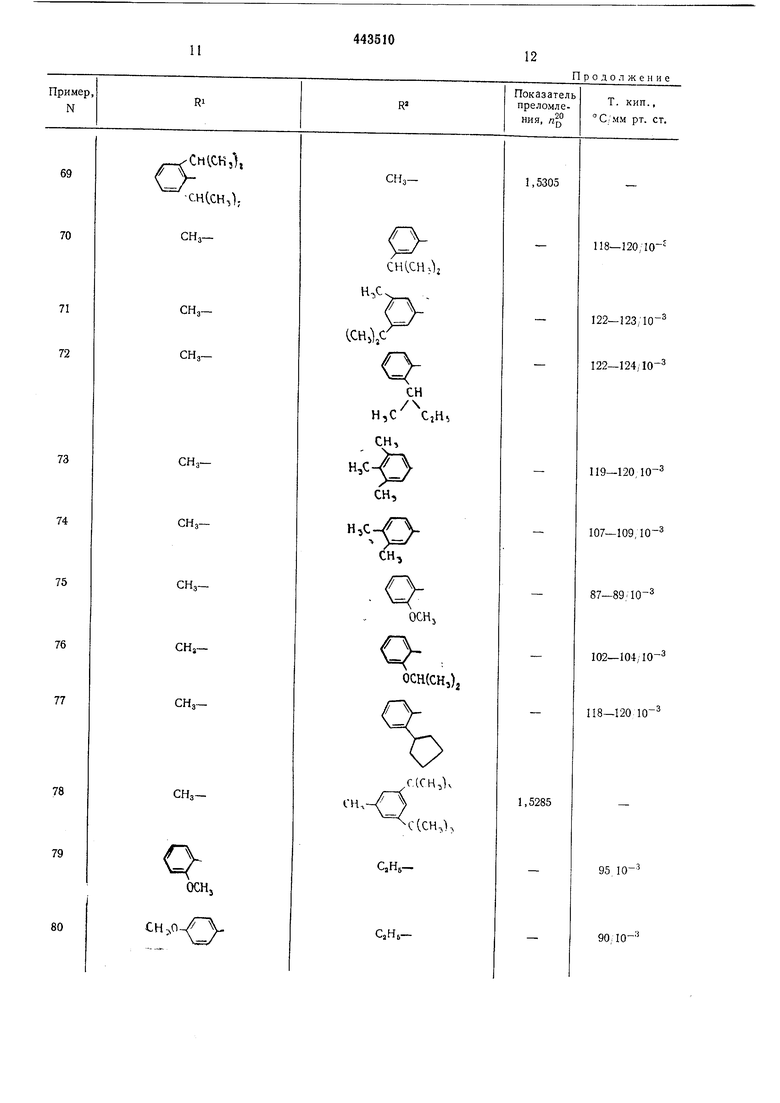
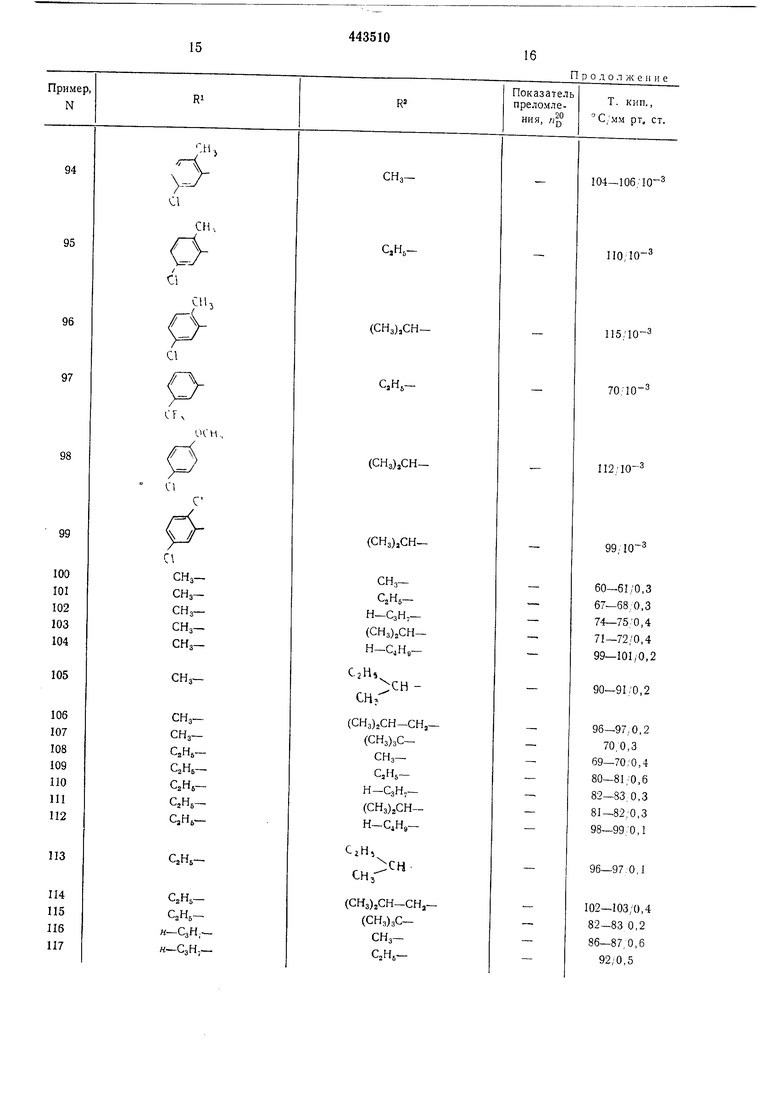
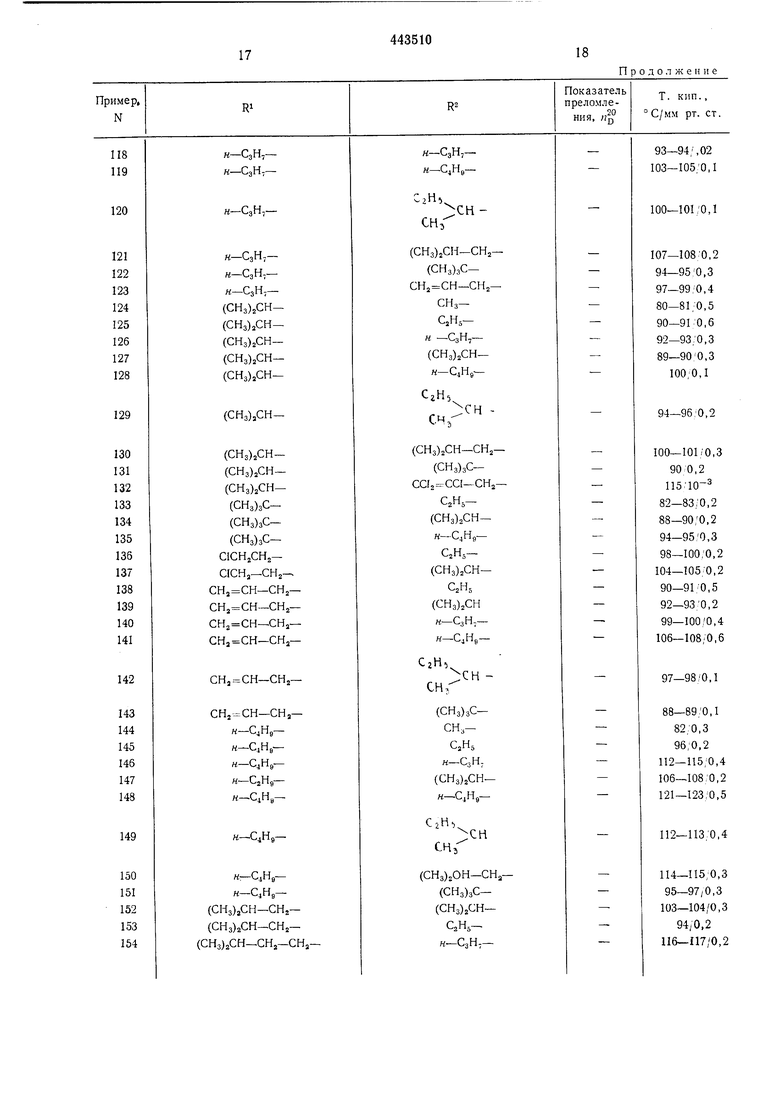
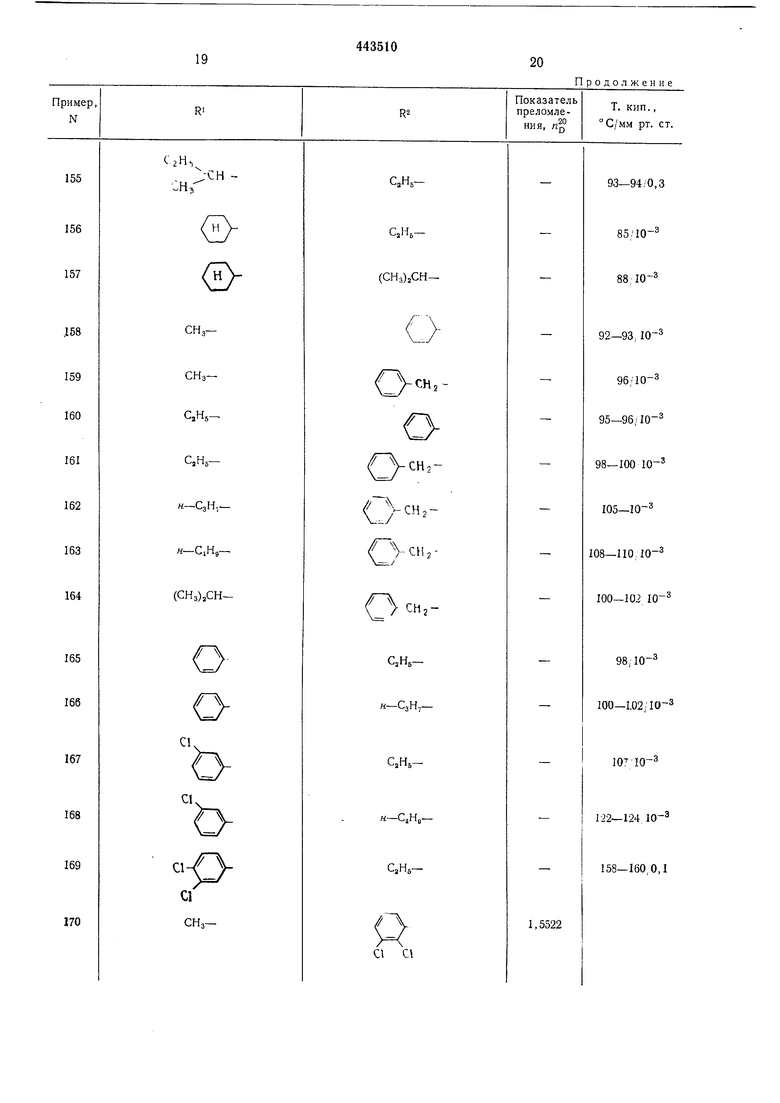
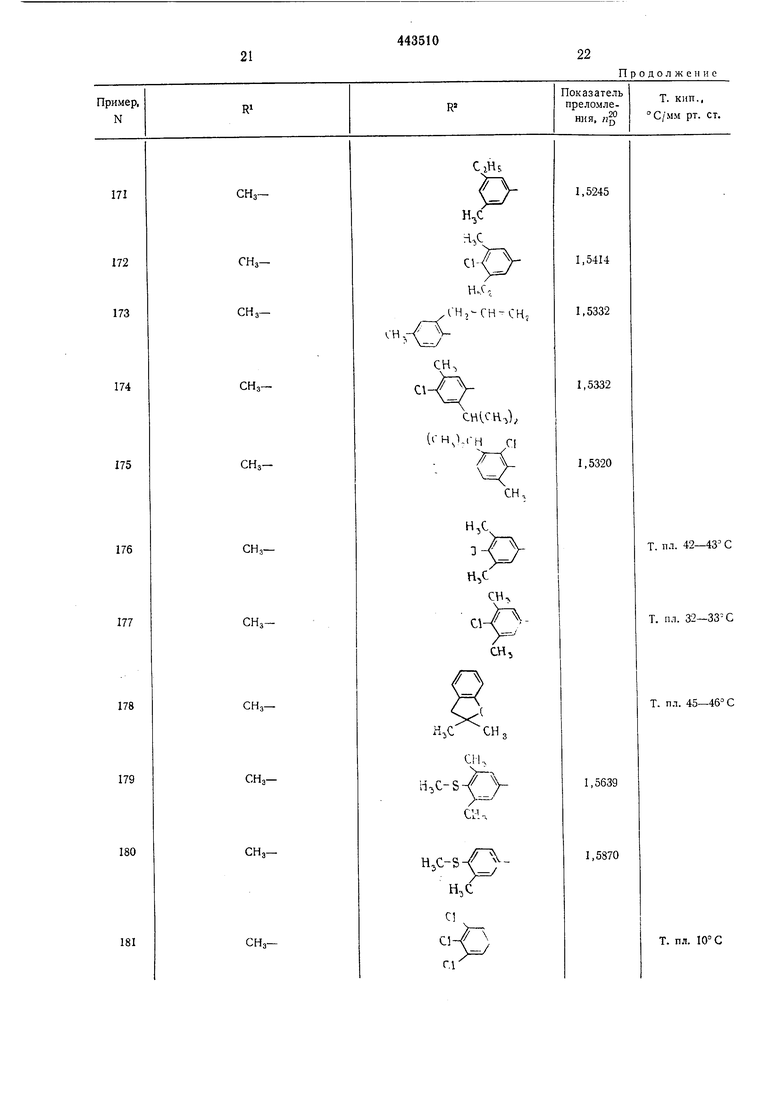
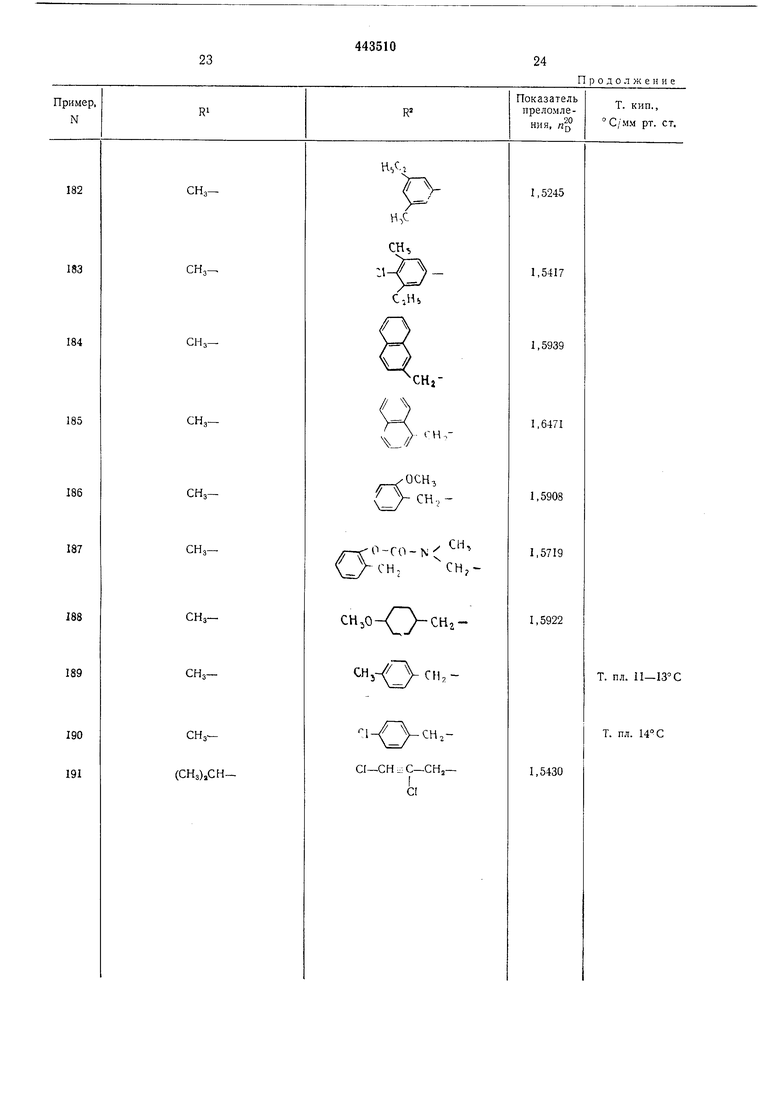
Приведенные в таблице соединения получают аналогичным способом. В примерах 4- 99 и 170-183 X-кислород; в примерах 100- 169 и 184-191 X-сера. При дистилляции Nарил-, 0-арил-, N-аралкил- и 0-аралкилпроизводных следует работать при давлениях менее мм рт. ст., при температуре бани менее 140°С и с возможно большими скоростями дистилляции (молекулярная перегонка), чтобы избежать уменьшения выхода из-за термического разложения.
CI-CH,-N -СО -X-R
Таблица I R
П р о д о л /к е я и е
Продолжение
Продолжение
13
14
Продолжение
Продолжение
17
18
Продолжение
19
20
Продолжение
21
22
Продолжение
23
Пример,
R1
N
СН,-
182
сн,
183
24
Продолжение
Т. кип., С/мм рт. с т.
1,5245
и,е СНг
1,5417
сн,184
1,5939
сн, сн, сн,(СНз),СНO-CO-NН,.-,V/ CH,CI-СН:;;С-СНа-С . пл. И-ISС Т. пл. 14С 25 Предмет изобретения Способ получения N-замещенных эфироз или тиоэфиров N-хлорметилкарбаминовых кислот, отличающийся тем, что N-моноза-5 мещенные эфиры или тиоэфиры карбаминовой кислоты формулы (QX-R (П I р/Ш где R1 и R2 - алкил, алкенил, алкинил, галоидалкил, галоидалкенил, галоидалкинил, 26 циклоалкил, циклоалкенил, замещенный арил или замещенный аралкнл, X - кислород или сера, подвергают взаимодействию с параформальдетдом и хлористым тионилом при 10-120°С и целевой продукт выделяют или переводят в соль известным приемом. Способ по п. 1, отличающийся тем, что процесс осуществляют при 15-70°С. 3. Способ по п. 1, отличающийся тем, что процесс ведут в среде растворителя, например бензоле, толуоле, 





| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ БОРЬБЫ С ВРЕДНЫМИ РАСТЕНИЯМИ В КУЛЬТУРАХ ПОЛЕЗНЫХ РАСТЕНИЙ | 2002 |
|
RU2420065C2 |
| Способ получения 1,3,4-тиадиазолил-5-мочевины | 1969 |
|
SU458127A3 |
| КОМБИНАЦИЯ ИЗ ГЕРБИЦИДОВ И ЗАЩИТНЫХ СРЕДСТВ | 2002 |
|
RU2291616C2 |
| Способ получения изоцианатов | 1974 |
|
SU567400A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-БЕНЗОДНАЗЕПИНОНА-2 ИЛИ ИХ СОЛЕЙ | 1970 |
|
SU417948A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИУРЕТАНОВ ХИНАЗОЛОНА | 1973 |
|
SU406356A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОЗАМЕЩЕННЫХ АЛКИЛОВЫХ ЭФИРОВ ТИОЛКАРБАМИНОВОЙ КИСЛОТЫ | 1971 |
|
SU419025A3 |
| Способ получения основнозамещенных алкиловых эфиров тиолкарбаминовой кислоты | 1971 |
|
SU450402A3 |
| Способ получения аминокетонов | 1970 |
|
SU470108A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БУТИРОФЕНОНА | 1973 |
|
SU404242A1 |


Авторы
Даты
1974-09-15—Публикация
1972-04-14—Подача