Изобретение относится к способу получения новых 4-амино-6,7,8-триалкоксихиназолинов, которые могут найти применение в фармацевтической промышленности. Известны 4-амино- и 4-аминоалкиламинохиназолины, содержащие алкоксигруппы в бензольном кольце, полученные взаимодей- i ствием замещенных 4-галоидхиназолинов с I соответствующими аминами. Предлагаемый способ предусматривает с использованием известного метода получение новых 4-амино-6,7,8-триалкоксихиназолинов, содержащих в алкиламиноостатке дополнительно оксигруппу. Способ заключается во I взаимодействии 6,7,8-триалкоксихиназолинов, содержащих в положении 4 галоид, или заменяемую группу - алкокси-, феноксиг. бензилокси-, -или соответствующую серу- i содержащую группировку, с аминами формулы И N KR, где J, а также 1. означают каждый | водород, алкил с 1-4 атомами углерюда или группы:, а)-СН (-CH), б)-СН (-СН ) -ОН или в) -СН„ ( -СН„)- N i Z, ( причем R означает водород или остаток - (СН) - СНд или - (СН) - ОН, п -1-6, преимущественно 3-5, т -О-4, У 1-4 и 35в1-4, но где присутствуют минимально одна и максимально две оксигруппы;один из заместителей R и R означает водород или алкио. если другой представляет собой указанную в п. б) rpyroiyj в одной из присутствующих в соответст венном случае групп, указанного в п. б) f вида, заместитель имеет другое зна чение чем водород; сумма не более 6; сумма П.-у не более 7, или где Я и Ц вместе с атомом азота образуют ост ток формулы --/ Л-СН2{(Н2)г-ОН , причем Z имеет вышеуказанное значение. Реакцию ведут преимущественно в среде органических растворителей, таких как бензол, диоксан, изопропанол при температуре 20-150° С преимущественно 50-10О в присутствии связывающего кислоту средства, например карбоната натрия. Целевой продукт выделяют известными приемами. Получение исходных соединений описано в примерах. Пример. Получение 4- 3-бис(2-оксиэтил )а минопропил мино-6,7,8-триметоксихиназолина. 1. Смесь 39 г 2-нитро-3,4,5-триметоксиметилбензоата, ЮО мл уксусной кислоты и 2,5 г 5%-ного палладия на угле встряхивают в течение 25 час с водородом при температуре 6О°С и под давлением 3,5 кг/см. Затем отфильтровывают и кон центрируют в вакууме. Полученный остаток растворяют в хлористом метилене и промывают избытком раствора карбоната натрия. I аствор хлористого метилена высушивают и концентрируют в вакууме и после перегонки полученного при этом масла (1О5°С, vSxlO мм.-рт.ст) получают масло 2-амин ;, 4,5-триметоксиметилбензоата. И. f acTBop 24,2 г 2-амино-3,4,5грнметоксиметилбензоата в ВО мл 99%лого формамида нагревают 1,25 час с обратным холодильником. Реакционную смесь охла 1шают, прибавляют 2 СО мл очень холо ной воды,, твердое вещество отфильтровывают, промывают водой и высушивают, полу чаю г 6,7,8-триметоксихиназолин-4 (ЗН )-он, т, нл. 220-22 20С. III. Смесь 11,6 г в,7,8-триметоксихииа;1ал11н-4/ЗН/-она и 40 мл хлорокиси фос фира нагревают 20 мин с обратным холодильником. Реакционную смесь охлаждают и при прибавляют к избытку разбавленного раствора аммиака. Полученную смесь встряхивают при 0° с 350 мл хлорог. форма, органическую фазу высушивают и затем пропускают через силикагель. После удаления в вакууме растворителя получают 4-хло{ 6,7.8-триметоксихнназолин, т.пл. . 1У. Смесь 6 г 4-хлор-6,7,8-триметокси, хиназолина, 4,2 г 3-бис (2-оксиэтил)аминопропиламина и 3,5 г карбоната натрия нагревают с обратным холодильником 35 мин в 50 мл изопропанола. Реакционную смесь отфильтровывают, растворитель удаляют в вакууме. Кристаллический остаток перекристаллизовывают из этилацетата. Получают 4 |3-бис (2-оксиэтил)аминопропил амино-6,7,8- триметоксихиназолин, т.пл. 142-144°С. Аналогично, применяя соответствующие исходные продукты в подходящих количествах, получают следующие соединения: 4(б-Оксигексш1) 1амино-6,7, Ei-триметоксихиназолин, т.пл. 143-144°С (кристаллизация из этилацетата). 4-{ 5-Оксипентил) амино-6,7,8-триметоксихиназолин, т.пл. 143-144°С (кристаллизация из этилацетата) 4-( 4-JOкjcибyтшI)aминo-6,7,8-триметокси- хиназолин, т.пл. 174-175,5°С (кристаллизация из этилацетата) 4- 4-(2-Оксиэтил)-1-пиперазино -6,7,8триэтоксихиназолин, т.пл. 1ОО-1О2°С 4-(5-Оксицентил) амино-6,7,8-триэгоксихиназолин, т.пл. 1О9-110,5°С 4- | 3-Бис (2-оксиэтил )аминопроиил| -&мино 6,7,8-триэтоксихиназолин, т.пл. 9З-В °С 4- 3-Eiic (3-оксипропил)аминопропил| -амино6,7,8-триметоксихиназолин, т.пл. 117-118°С 4-| 4-Бис (2-оксиэтил)аминобутил -амино6р7,8-триметоксихиназолин, т.пл. 15S -16O°C 4- (4-оксиметил-5-окси )пентил -амино-6, 7,8-триметоксихиназолин, т. пл. 15 5-16О°С 4-| Ь|-/Летил- М - З-бис(2-оксиэтил)аминопропил -амино -6,7,8-триметоксихиназолин, .пл. 89-9 € 4-Д (2-оксиэтил )амино-6,7,8-триметоксихиназолин, Т.ПЛ.11О-113°С
4-(2,3 1иоксипрошот)амино-6,7.8-триме-, вместе с атомом азота образуют остаток токсихгаазолинГт.Ж 185-186 0 .,.. , Г2-Бис (2-.оксиэтип)аминоэтип| амино-6,7,
,- . - -л
в-триметоксихиназопин. т. пл. - 153-1 54 С 5
Предмет изобретения . где Z имеет вышеуказанное значение,
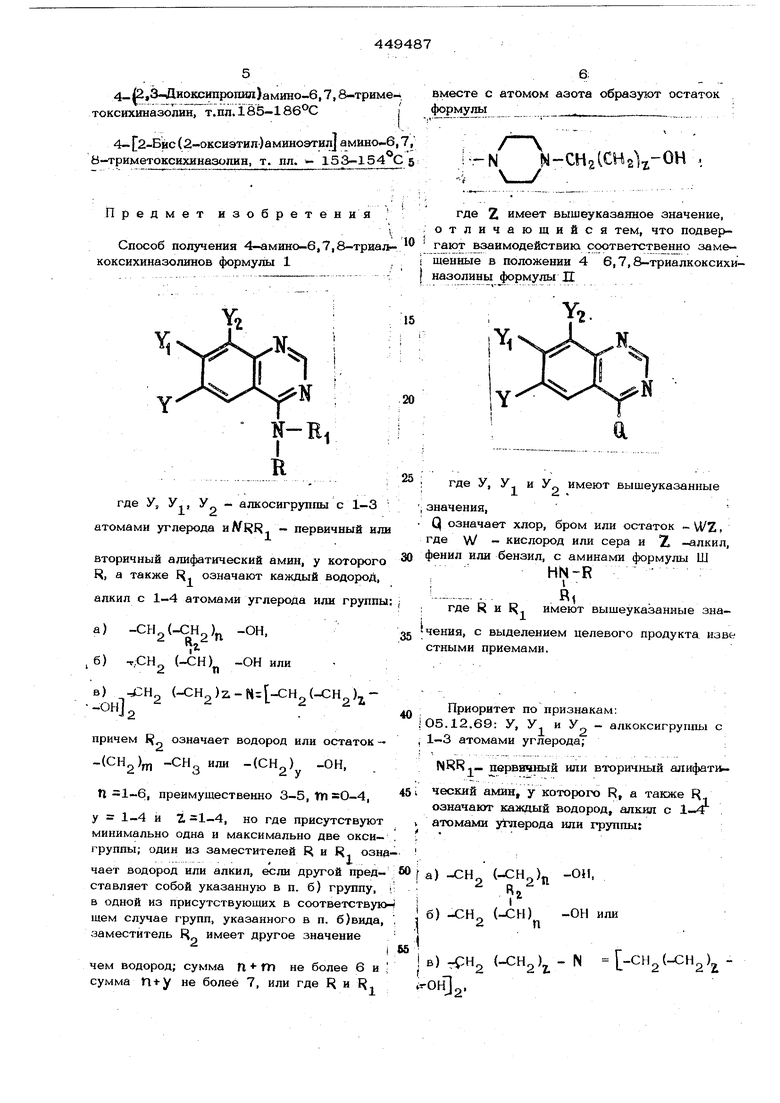
Способ получения 4-амино-6,7,8-триал- гаютвзаимодействик соответственно замекоксихиназолинов формулы 1,, Гшенные в положении 4 6,7,8-триалкоксихи- j назолины формулы Д где YS У, У - алкосигруппы с 1-3 атомами углерода - первичный или вторичный алифатический амин, у которого R, а также R означают каждый водород, алкил с 1-4 атомами углерода или группы а) -ОН, г .6) гСН (-СН) -он или в) Н (-СН ) (-СН„),-OHJsпричем 1 означает водород или остаток - -(СН) -СНд или -(СН) -ОН, П 1-6, преимущественно 3-5, m , у 1-4 и Z -1-4, но где присутствуют минимально одна и максимально две окси- группы; один из заместителей R и R озна чает водород или алкил, если другой представляет собой указанную в п. б) группу, в одной из присутствующих в соответствую тем случае групп, указанного в н. б)вида, заместитель R имеет другое значение чем водород; сумма П « Ш не более 6 и сумма не более 7, или где R и 1
,-он .
h-N N-СНг f Nil .У
; о т л и ч а ю щ и и с я тем, что подвергде У, У и У„ имеют вышеуказанные Л. « , значения, Q означает хлор, бром или остаток - U/Z, где VV - кислород или сера и °JL -алкил, фенил или бензил, с аминами формулы Ш HN-R -R, ; где R и 1 имеют вышеуказанные зна|чения, с выделением целевого продукта изве стными приемами. Приоритет по признакам: .12.69: У, У. и У :О5.12.69: У, У и У - алкоксигруппы с , 1-3 атомами углерода; первичный или вторичный алифати ческий амин, у которого R, а также R означают каждый водород, алкил с 1-4 атомами углерода или группы: , Га) -СН (-СН L -ОН, j б) -СН () -он или I в) -рн (-CH) - N ) ,
„р,„ем R, означает -водород или остаток8.«месте с атомом
-(СН,)„ -ОН, или ,. (СН,) - ОН,. - tePH& - -- --
,, преимущественно 3-5 m SO-4. (CH2)™OH
у 1-4 и г 1-4. но где присутствуютV /
минимально одна и максимально две окси-- : -/
группы; один из заместителей R и R.j озна-,где X имеет вышеуказанное значение;:
ает водород или алкил. если другой пред-., ц -алоид (хлор или бром), преимушестставляет собой указанную в п. 6) группу; .. „
в одной из присутствующих в соответствуют
щем случае групп, указанного в п.б)вида,
заместитель R другое значение26.08.70: Q - остаток WZ. где W
чем водород; сумма П+Ш не более 6 и- кислород или сера и 21 - алкил, фенил
сумма П + у не более 7, или где R и 15. или бензил.
8
OOnnw AJiUtJ




Авторы
Даты
1974-11-05—Публикация
1970-12-04—Подача