(54) СПОСОБ ПОЛУЧЕНИЯ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
3
Предпочтительно подвергают соединения формулы II реакции обмена с этилендиамином в присутствии кислоты, по меньшей мере один из реакционных компонентов всегда должен быть в форме свободного основания.
Молярное соотношение между солью соединений структуры (II) и этилендиамином составляет примерно I : 2 - 1:6. Проводят реакцию обмена предпочтительно в инертном при реакционных условиях полярном растворителе, например в низшем алканоле, как этанол, изопропанол, в амиде органической карбоновой кислоты, как диметилформамид, в простом эфире с открытой цепью или циклическом простом эфире, как диоксан и т. д., или в смеси последних с водой. Употребляемый в избытке этилендиамин может также служить растворителем. Проводят реакцию обмена при повышенной температуре, предпочтительно при температуре кипения реакционной смеси. Реакция длится примерно 2- 10 час.
Полученные по описанному способу соединения имидазолина структуры I можно выделять как свободные основания или в форме их кислотно-аддитивных солей и очищать их.
Необходимые как исходный продукт соединения структуры II также новы.
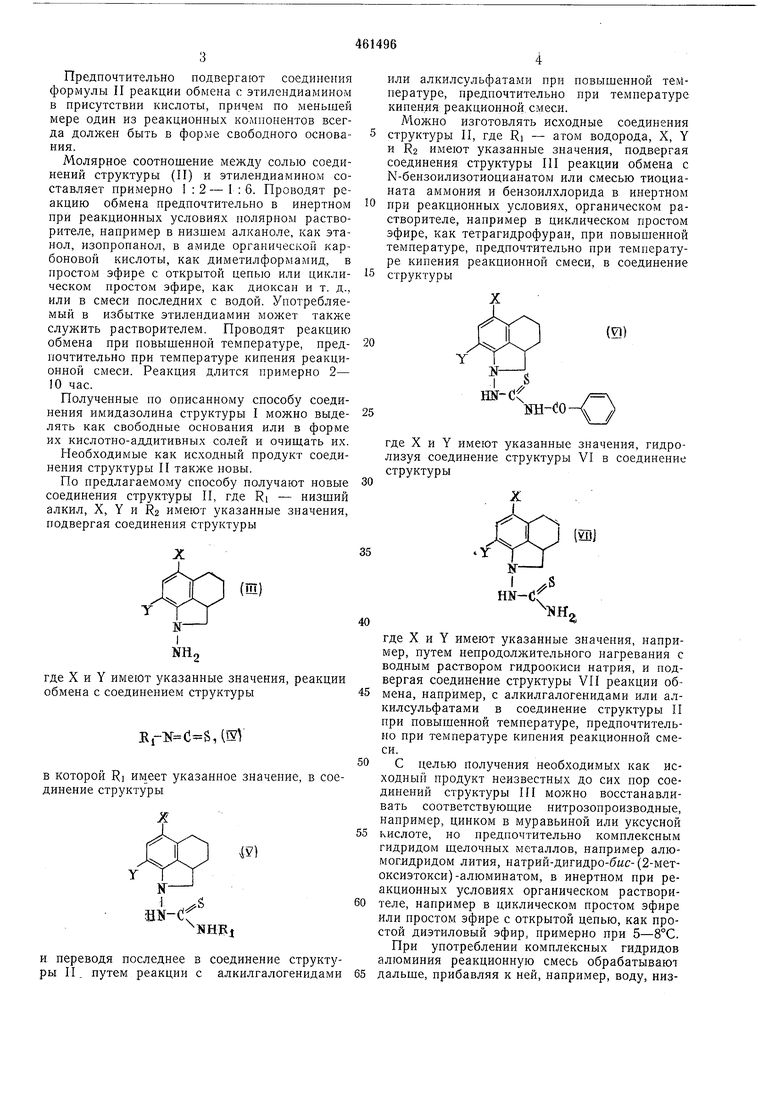
По предлагаемому способу получают новые соединения структуры II, где Ri - низший алкил, X, Y и Кз имеют указанные значения, подвергая соединения структуры
(Ш)
где X и У имеют указанные значения, реакции обмена с соединением структуры
ji-X(,(5V
в которой RI имеет указанное значение, в соединение структуры
4)
m-(i
NHlRj
И переводя последнее в соединение структуры II. путем реакции с алкилгалогенидами
или алкилсульфатами при повышенной температуре, предпочтительно при температуре кипения реакционной, смеси.
Можно изготовлять исходные соединения структуры II, где Ri - атом водорода, X, У и R2 имеют указанные значения, подвергая соединения структуры III реакции обмена с N-бензоилизотиоцианатом или смесью тиоцианата аммония и бензоилхлорида в инертном при реакционных условиях, органическом растворителе, например в циклическом простом эфире, как тетрагидрофуран, при повышенной температуре, предпочтительно при температуре кипения реакционной смеси, в соединение структуры
О)
1Шш- о
где X и Y имеют указанные значения, гидролизуя соединение структуры VI в соединение структуры
К
где X и Y имеют указанные значения, например, путем непродолжительного нагревания с водным раствором гидроокиси натрия, и подвергая соединение структуры VII реакции обмена, например, с алкилгалогенидами или алкилсульфатами в соединение структуры II при повышенной температуре, предпочтительно при температуре кипения реакционной смеси.
С целью получения необходимых как исходный продукт неизвестных до сих пор соединений структуры III можно восстанавливать соответствующие нитрозопроизводные, например, цинком в муравьиной или уксусной кислоте, но предпочтительно комплексным гидридом щелочных металлов, например алюмогидридом лития, натрий-дигидрО5«с- (2-метоксиэтокси)-алюминатом, в инертном при реакционных условиях органическом растворителе, например в циклическом простом эфире или простом эфире с открытой цепью, как простой диэтиловый эфир, примерно при 5-8°С.
При употреблении комплексных гидридов алюминия реакционную смесь обрабатывают дальше, прибавляя к ней, например, воду, низший спирт и т. д., отделяя органическую фазу, отфильтровывая осадок и промывая его инертным в данных условиях органическим растворителем, например простым эфиром с открытой цепью или циклическим простым эфиром, как простой диэтиловый эфир, тетрагидрофуран и т. д. При выпаривании соединенных высушенных органических фаз в качестве остатка остаются соединения структуры III. Нитрозосоединения также новы; можпо изготовлять их известным образом из соединений структуры
где X и Y имеют указанные значения.
Практически поступают, например, так, что к раствору соединений структуры VIII в избыточной разбавленной соляной кислоте прибавляют нитрит натрия.
Пример 1. 1,2,2а,3,4,5-Гексагидро-1-(2имидазолин-2-иламино) -бенз d индол.
25 г гидройодида 1-(1,2,2а,3,4,5-гексагидробенз сй индол - 1-ил)-2 - метил - изотиомочевины и 12,8 мл этилендиамина нагревают 2,5 часа в 65 мл этанола до кипения. Выпаривают раствор досуха и взбалтыванием извлекают остаток с помощью метиленхлорида и в присутствии концентрированного раствора гидроокиси натрия. Высушенный над сульфатом магния раствор метиленхлорида выпаривают досуха и переводят полученный как остаток от выпаривания 1,2,2а,3,4,5-гексагидро1-(2-имидазолин-2-иламино)-бенз cd индол в его гидрохлорид.
Т. пл. 258-260°С из смеси этанол/простой эфир.
Необходимый как исходный продукт гидройодид 1 - (1,2,2а,3,4,5 - гексагидробенз cd -индол- 1 -ил) -2-метилизотиомочевины получают следующим образом.
При комнатной температуре нитрозируют 1,2,2а,3,4,5-гексагидробенз сс индол в солянокислом растворе нитритом натрия в 1,2,2а,3,4, 5-гексагидро - 1 - нитрозобенз с / индол (бесцветные кристаллы из простого эфира/петролейного эфира с т. пл. 70-71°С). Восстановлением алюмогидридом лития в простом эфире получают из него при 1-амино-1,2, 2а,3,4,5-гексагидробенз с индол (т. пл. 59- 61°С из простого эфира/петролейного эфира). Реакцией обмена аминосоедипения с бензоилизотиоцианатом в кипящем тетрагидрофуране и последующим омылением разбавленным раствором гидроокиси натрия с флегмой в течение 10 мин получают 1-(1,2,2а,3,4,5-гексагидр.обенз erf индол-1-ил)-тиомочевину с т. пл. 182-184°С (и глетнленхлорпда/петролейног;
эфира). Последние соединения после 4-час кипячения с метилйодидом в метаноле дает гидройодид 1-(1,2,2а,3,4,5-гексагидробенз erf индол-1-ил) -2 - метилизотиомочевины, который кристаллизуется из метанола/простого эфира. Т. пл. 198-201°С.
Пример 2. 6-Хлор-1,2,2а,3,4,5-гексагидро1-(2-имидазолин-2-иламино)-бенз cd индол. Получают аналогично примеру 1, употребляя гилройодид 1-(6-хлор-1,2,2а,3,4,5-гексагидробенз сй индол - 1-ил)-2-метилизотиомочевины. Полученный 6-хлор-1,2,2а,3,4,5-гексагидро -(2-имидазолин - 2 - иламино)-бенз erf индол выкристаллизовывают из метиленхлорида/петролейного эфира с т. нл. 212-214°С.
Употребляемый как исходный продукт гидройодид 1-(6-хлор-1,2,2а,3,4,5-гексагидробенз erf индол-1-ил)-2-метилизотиомочевины получают следующим образом.
При комнатной температуре хлорируют 1-ацетил-1,2,2а,3,4,5 - гексагидробенз erf индол в тетрахлорметане вычисленным количеством хлора. Полученный 1-ацетил-6-хлор-1,2,2а,3,4,5гексагидробенз erf индол (т. пл. 141 - 143°С,
из метиленхлорида/петролейного эфира) омыляют кипячением в концентрированной соляной кислоте/ледяной уксусной кислоте в течение 90 мин в 6-хлор-1,2,2а,3,4,5-гексагидробенз erf индол (т. пл. 109-111°С, из простого эфира/петролейного эфира). При 5°С нитрозируют последний в солянокислом растворе нитритом натрия в 6-хлор-1,2,2а,3,4,5-гексагидро-1-нитробенз erf индол (т. пл. 123-125°С, из простого эфира). Восстанавливая последний алюмогидридом лития в простом эфире при 5-8°С, получают 1-амино-6-хлор-1,2,2а.З,4,5-гексагидробенз erf индол (т. пл. 74-76°С, из простого эфира/петролейного эфира). Реакцией обмена аминосоединения с бензоилизотиоцианатом в
кипящем тетрагидрофуране и последующим омылением разбавленным раствором гидроокиси натрия с флегмой в течение 10 мин получают 1-(6-хлор-1,2,2а,3,4,5-гексагидробекз erf индол-1-ил)-тиомочевину (т. пл. 226-
228°С, из метанола/простого эфира). Последнее соединение после кипячения в течение 4 час с метилйодидом в метаноле дает гидройодид 1 - (6-хлор-1,2,2а,3,4,5-гексагидробенз erf индол-1 -ил) -2-метилизотиомочевины, который
выкристаллизовывается из метанола/простого эфира.
Т. нл. 174-177°С.
Пример 3. 6,8-Дихлор-1,2,2а,3,4,5-гексагидро - 1-(2-имидазолип-2-иЛамино) -
индол. ..--12 г гидройодида 1-(6,8-дихлор-Г,2,2а,3.4,5гeкcaгидpoбeнз erf индoл-l-ил)-2 - метилизотиомочевины и 18 мл этилендиамина нагревают в течение 10 час в 36 мл этанола до кипеиия. Выпаривают раствор досуха и взбалтыванием извлекают остаток с помощью метиленхлорида и Б присутствии концентрированного раствора гидроокиси натрия. Выпаривают высушенный над сульфатом магния растпор метиленхлорида досуха. Полученный как
остаток от выпаривания б,8-дихлор-1,2,2а,3,4, 5-гексагидро - 1-(2-имидазолин-2 - иламино)бенз ccf индол выкристаллизовывается из метиленхлорида/простого эфира с т. пл. 200- 202°С.
Необходимый как исходный продукт гидройодид I - (6,8-дихлор-1,2,2а,3,4,5-гексагидробенз cd индол-1 -ил) -2-метилизот11Омечевины получают следующим образом.
Хлорируют 1-ацетил-б-хлор-1,2,2а,3,4,5-гексагидробенз сй индол (т. пл. 141 - 143°С, из метиленхлорида/петролейного эфира) в кипящем тетрахлорметане в присутствии хлорида железа в 1-ацетил-6,8-дихлор-1,2,2а,3,4,5-гексагидробенз сй индол (т. пл. 170-172°, из метиленхлорида/простого эфира). Кипятят последний 2 час в концентрированной соляной кислоте/ледяной уксусной кислоте, получают 6,8-дихлор-1,2,2а,3,4,5 - гексагидробенз сй1 индол (т. пл. 103-105°С, из простого эфира/петролейного эфира). При 5°С нитрозируют последний в солянокислом растворе нитритом натрия в 6,8-дихлор-1,2,2а,3,4,5-гексагидро-1-нитрозобенз erf индол (т. пл. 179-181°С, из метиленхлорида/петролейного эфира). Восстановлением алюмогидридом лития в простом эфире при 5-8°С получают 1-амино-6.8-дихлор - 1,2,2а,3,4,5 - гексагидробенз сй индол (т. пл. 101-103°С, из метиленхлорида/петролейного эфира). Реакцией обмена аминосоединения с бензоилизотиоцианатом в кипящем тетрагидрофуране и последующим омылением разбавленным раствором гидроокиси натрия с флегмой в течение 10 мин получают I-(6,8дихлор-1,2,2а,3,4,5 - гексагидробензГсй индол1-ил)-тиомочевину (т. пл. 230-232°С, из метанола/метиленхлорида/простого эфира), который после часового кипячения с метилйодидом в метаноле дает гидройодид 1-(6,8-дихлор-1,2,2а,3,4,5 - гексагидробенз индол -1ил)-2-метилизотиомочевины, который кристаллизуется из метанола/простого эфира. Т. пл. 210-212°С.
Пример 4. 1,2,2а,3,4,5-Гексагидро-1 - (2имидазолин-2 - иламино)-6 - метилтиобензГс( индол.
Гидройодид 1 - (1,2,2а,3,4.5-гексагидро-6-метилтиобенз сй индол-1-ил)-2 - метилизотиомочевины и этилендиамин кипятят в течение 2 час и обрабатывают аналогично примеру 1. Полученный 1,2,2а,3,4,5-гексагидро-1-(2-имидазолин - 2-иламино)-б - метилтиобенз ее индол переводят в гидромалеинат. Последний кристаллизуется из метанола/простого эфира и плавится при 191-192°С.
Необходимый как исходный продукт гидройодид I - (1,2,2а,3,4,5-гексагидро-6-метилтиобенз сй индол - 1-ил)-2-метилизотиомочевины получают следующим образом.
При 10°С нитрируют I-ацетил-1,2,2а,3,4,5гексагидробенз сй индол в ледяной уксусной кислоте дымящей азотной кислотой. При 50- 60С восстанавливают полученный I-ацетил-1, 2,2а,3,4,5 - гексагидро-6 - нитробенз erf индол (т. пл. 174-175°С, из метиленхлорида/простого эфира) в тетрагидрофуране/метаноле гидразингидратом в присутствии никеля Ренея в I-ацетил - 6-амино-,2,2а,3,4,5-гексагидробенз сй индол (т. пл. 147-149°С, из метиленхлорида/петролейного эфира). При О-5°С диазотируют аминосоединение в сернокислом растворе нитритом натрия и при помощи метилмеркаптана в присутствии медного порощка переводят полученную диазониевую соль по
Зандмейеру при 0°С в 1-яцетил-1,2,2а,3,4,5гексагидро-6 - метилтиобенз сй индол (т. пл. 127-129°С, из метиленхлорида/простого эфира). Кипячением последнего в течение 30 мин в этаноле с разбавленным раствором гидроокиси натрия получают 1,2,2а,3,4,5-гексагидро 6-метилтиобенз сс индол (гидромалеинат с т. пл. 121 - 123°С, из метанола/простого эфи ра). При 0°С нитрозируют последний в разбавленной соляной кислоте/ледяной уксусной
кислоте нитритом натрия в 1,2,2а,3,4,5-гексагидро - б - метилтио - - нитрозобепз сй индол (т. пл. 94-97°С, из метиленхлорида/простого эфира). Восстанавливая последний алюмогидридом лития в простом з(Ьире при 5-10°С, получают 1-амино-1.2.2а.3.4,5-гексагидро-6-метилтиобенз erf индол (как гидромалеинат из метанола/простого яфира. т. пл. 108-109°С). Реакцией обмена аминосоединения с бензоилизотиоцианатом в кипящем тетрагидрофуране
с последующим омылением разбавленным раствором гидроокиси натрия с Ллегмой в течение 10 мин получают 1-(1,2.2а.З,4.5-гексагидро-6 - метилтиобенз erf индол-1 - ил)-тиомочевину (т. пл. 205-207 С, из метиленхлорида/метанола/простого эфира). Кипячением последней в течение 2 час с метилйопилом в метаноле получают гидройодид 1-(1,2.2а.3.4.5гексагидро - 6-мeтилтиoбeнзГerflинтoл - 1-ил)2-мети тазотиомочевины, который выкристаллизовывается из метанола/сложного эЛира уксусной кислоты, т. пл. .
Пример 5. 1,2,2а,3,4,5-Гексагиаро-1-(2имидазолин-2 - иламино)-8 - метилбенз erf индол.
Подвергают гидройолид 1-(1.2,2а,3.4,5-гексагидро-8 - метилбенз erf индол-1-ил)-2 - метилизотиомочевины реакции обмена с этилендиамином и перерабатывают аналогично примеру 1. Затем переводят полученный 1.2,2а.3.4.5гексагидро-1-(2-имидазолин-2-нлачно)-8 - нетилбeнзГerfl индол в гидрохлорид. Т. пл. 240- 242С, из метанола/простого эфира.
Необходимый как исходный продукт гидро7°одид 1 - (1,2,2а,3,4,5-гексагидро-8-метилбенз
erf индол-1-ил)-2-метилизотиомочевины получают следующим образом.
7-Метилграмин переводят с метилйодидом в его йодметилат. Реакцией обмена последнего со сложным диэтиловым эфиром малоновой кислоты в присутствии гидрида натрия в кипящем ксилоле, последующим омылением путем кипячения в разбавленном растворе гидроокиси натрия в течение 7 час и последующим лекарбоксилированием при IBOC получают 7-метилиндол-З-цропионовую кислоту (т. пл. 117-119°С, из простого эфира/петролейного эфира). Эту кислоту восстанавливают в разбавленной соляной кислоте/ледяной уксусной кислоте нри 95°С цинковой пылью в присутствии хлорида ртути в 7-метилиндолин3-пропионовую кислоту (т. пл. 165-167°С, из метиленхлорида). Из последней получают при помощи пентахлорида фосфора в метиленхлориде при 5-10°С хлорангидрид кислоты и затем получают по реакции Фриделя-Крафтса с хлоридом алюминия в кипящем метиленхлориде 1-бензоил- 1,2,2а,3-тетрагидро-8-метилбенз ссг -индол-5(4Н)-он (т. пл. 169-171°С, из смеси метиленхлорид/метанол/простой эфир). При одновременном отщеплении бензоильной группы получают по реакции Huang- Minlon 1,2,2а,3,4,5-гексагидро-8-метилбенз сй индол (т. пл. 81-82°С, из петролейного эфира). Последний нитрозируют в соляном растворе при О-5°С нитритом натрия в 1,2,2а,3,4,5 - гексагидро-8-метил -1 - нитробенз cuf индол (т. пл. 83-85°С, из простого эфира/петролейного эфира). Восстановлением алюмогидридом лития в простом эфире при 5°С получают 1-амино-1,2,2а,3,4,5-гексагидро-8метилбенз с( индол (т. пл. 162-164°С, из метанола/простого эфира) как гидрохлорид. Реакцией обмена аминосоединениями с бензоилизотиоцианатом в кипящем тетрагидрофуране и последующим омылением разбавленным раствором гидроокиси натрия с флегмой в течение 10 мин получают 1-(1,2,2а,3,4,5-гексагидро-8-метилбензГс индол-1 - ил)-тиомочевину (т. пл. 214-215°С, из метиленхлорида/метанола/простого эфира). Кипячением последнего соединения в течение 2 час с метилйолилом в метаноле получают гидройодид 1-(1,2,2а,3.4, 5-гексагидро-8 - метилбенз сс индол-1-ил)-2метилизотиомочевины, который кристаллизуется из метанола/простого эфира. Т. пл. 200- 202°С. Пример 6. 1,2,2а,3,4,5-Гексагидро-1-(2имидазолин - 2-иламино)-6-метилбенз erf индол. 12 г гидройодида 1-(1,2,2а.З,4,5-гексагидро6-метилбензГсс индол - 1-ил)-2 - метилизотиомочевины и 12 мл этилендиамина в 60 мл этанола кипятят в течение 2 час и перерабатывают аналогично примеру 1. Полученный 1,2,2а, 3,4,5-гексагилро - 1-(2-имидазолин-2-иламино)6-метилбенз erf индол переводят в гидрохлорид. Т. пл. 238-239°С, из метанола/простого эфира. Необходимый как исходный продукт гидройодид 1 - (1,2,2а,3,4,5-гексагидро-6-метилбенз erf индол-1 -ил) -2-метилизотиомочевины получают следующим образом. При 10°С нитрируют 1-ацетил-1,2.2а,3,4,5гексагидробенз erf индол в ледяной уксусной кислоте дымящей азотной кислотой. При 50-- 60°С восстанавливают полученный при этом 1-ацетил - 1,2,2а,3,4,5 - гексагидро-6-нитробенз erf индол (т. пл. 174-175°С, из метиленхлорида/простого эфира) в метаноле гидразинидратом в присутствии никеля Ренея в 1-ацеил-6 - амино-1,2,2а,3,4,5 - гексагидробенз ес ндол (т. пл. 147-149°С, из метиленхлорида/ етролейного эфира). При диазотирут аминосоединение в сернокислом растворе нитритом натрия и при 60°С переводят полученную диазониевую соль по Зандмейеру цианидом меди в 1-ацетил-6-циан-1,2,2а,3,4,5-гексагидробенз erf индол (т. пл. 169-171°С, из метиленхлорида/петролейного эфира). Перемешивая последний 20 час с гипофосфитом натрия и никелем Ренея в смеси из ледяной уксусной кислоты/пиридина/воды при комнатной температуре, получают 1-ацетил-6-формил - 1,2,2а,3,4,5 - гексагидробенз erf индол (т. пл. 145-147°С, из метиленхлорида/петролейного эфира), который переводят по реакции Huang-Minion при одновременном отщеплении ацетильной группы в 1,2,2а,3,4,5гексагидро-6-метилбенз erf индол (т. пл. 86- 88°С, из метанола/воды. При 5°С нитрозируют последний в солянокислом растворе нитритом натрия в 1,2,2а,3,4,5-гексагидро-6-метил1-нитрозобенз erf индол (т. пл. 103-105°С, из простого эфира). Восстановлением алюмогидридом лития в простом эфире при 5-8° получают 1-амино-1,2,2а,3,4,5-гексагидро-6-метилбенз erf индол (как гидрохлорид из метанола/ простого эфира, т. пл. 185-187°С). Реакцией обмена аминосоединения с N-бензоилизотиоцианатом в кипящем тетрагидрофуране с последующим омылением разбавленным раствором гидроокиси натрия с флегмой в течение 10 мин получают 1-(1,2,2а,3,4,5-гексагидро-6А1етилбенз erf индол-1-ил)-тиомочевину (т. пл. 209-211°С, из метиленхлорида/метанола). Кипячением последнего соединения в течение 2 час с метилйодидом в метаноле получают гидройодид 1 - (1,2,2а,3,4,5-гексагидро-6-метилбенз erf индол-1-ил)-2 - метилизотиомочевины, который кристаллизуется из метанола/простого эфира. Т. пл. 167-169°С. Предмет изобретения 1. Способ получения гетероциклических соединений общей фюрмулы X - атом водорода, галоид, метил- или метилтиогруппа; Y - атом водорода, или X - атом водорода, Y - метилгруппа, или X и Y-
11
атомы хлора, отличающийся тем, что соединение общей формулы
(П)
:N-E,
т-с
S-Ko
где X и Y имеют указанные значения;
RI - атом водорода или низший алкилрадикал;
Ro - низший алкйЛрадикал, или его соль подвергают реакции обмена с этилендиамином в присутствии растворителя с последующим выделением целевого продук12
та в свободном состоянии или в виде соли известными способами.
2. Способ по п. 1, о т л и ч а ю щ и и с я тем, что в качестве растворителя применяют низшие спирты, как этанол, изопропанол, амиды органической карбоновой кислоты, как диметилформамид, простые эфиры с открытой цепью или циклические, как диоксан, или смеси последних с водой.
3. Способ по пп. I и 2, отличающийся тем, что процесс ведут в избытке этилендиамина.
4. Способ по п. 1, от ли ч а ю щ и и с я тел1. что процесс ведут при нагревании, например
при температуре кипения реакционной смеси.
Приоритет по признакам 24.10.69 при X -
атом водорода, галогена, метилгруппа; Y-
атом водорода.
06.07.70 при X - атом водорода; Y - метилгруппа; X - метилтиогруппа; Т -водород; X и Y - атомы хЛора.






Авторы
Даты
1975-02-25—Публикация
1970-10-15—Подача