3
выделением целевого продутста известными способами.
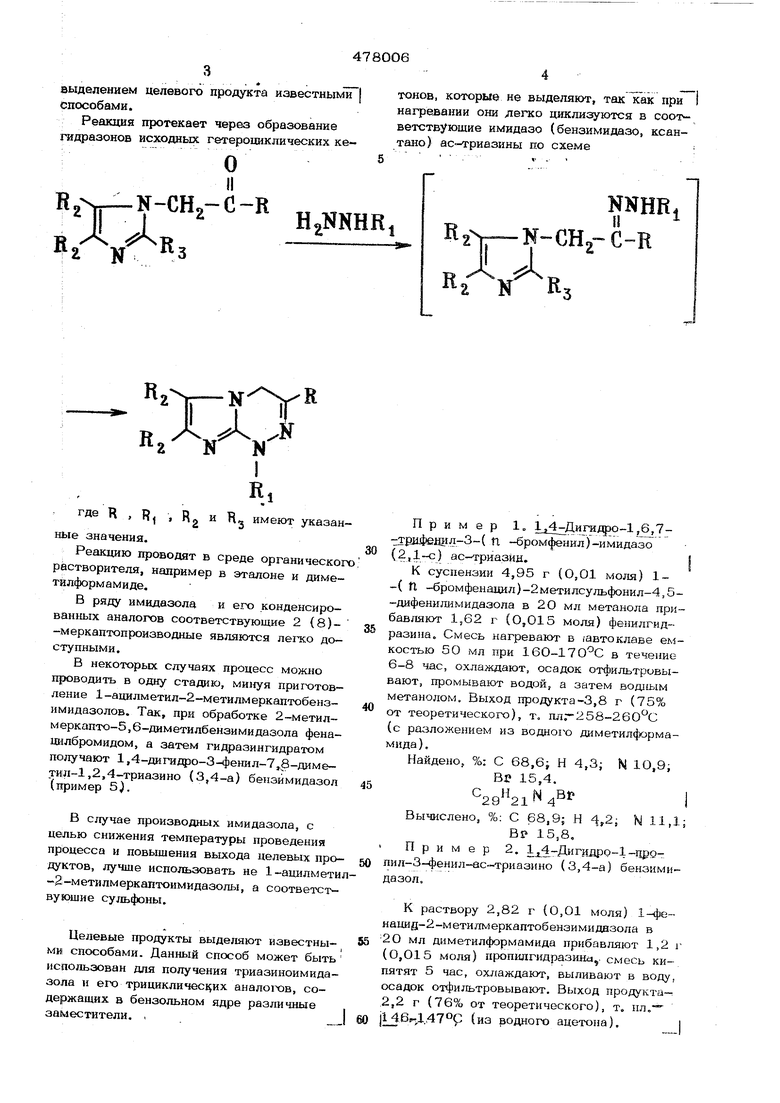
Реакция протекает через образование гидразонов исходных гетероциклических кеО
II
C-R
H NNHRi
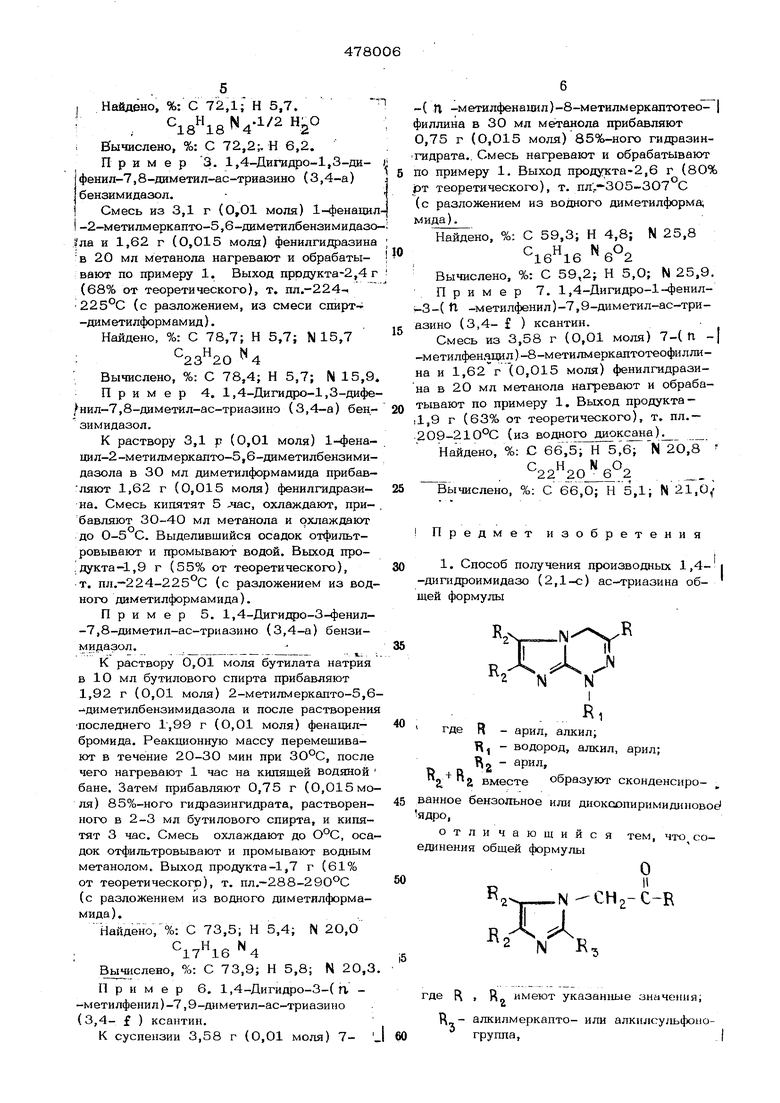
тонов, которые не выделяют, так как при нагревании они легко диклизуются в соответствующие имидазо (бензимидазо, ксантано) ас триазины по схеме:
NNHRi
и 

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1,2,3,4тетрагидроимидазе (2,1-с) ас-триазина | 1973 |
|
SU555098A1 |
| Способ получения производных имидазо (2,1-с) ас-триазинона-4 | 1974 |
|
SU502888A1 |
| Способ получения производных 1,4-дигидроимидазо(2,1-с)ас-триазина | 1974 |
|
SU507571A1 |
| Способ получения пиримидинонов или их кислотно-аддитивных солей | 1981 |
|
SU1056900A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1,4-ДИГИДРОПРОИЗВОДНЫХ ИМИДАЗО- | 1973 |
|
SU374308A1 |
| Способ получения 2,5-дигидро-1,2-тиазино (5,6-в) индол-3-карбоксамид-1,1-диоксидов или их солей | 1978 |
|
SU654173A3 |
| Способ получения производных имидазола | 1973 |
|
SU477158A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,4-ДИГНДРОНАФТ-(!,2-d)-ИMИДAЗO- | 1973 |
|
SU362017A1 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СМЕСИ ИХ ИЗОМЕРОВ И ИХ СОЛИ | 1992 |
|
RU2017740C1 |
| Способ получения производных триазолазепина | 1973 |
|
SU475777A3 |

где R
R« и R,
f « «2 ° указанные значения.
Реакцию проводят в среде органическог растворителя, например в эталоне и диметилформамиде.
В ряду имидазола и его конденсированных аналогов соответствующие 2(8)-меркаятопроизводные являются легко доступными.
В некоторых случаях процесс можно проводить в одну стадию, минуя приготовление 1-аинлметил-2-метилмеркапто6ензимидазолов. Так, при обработке 2-метилмеркапто-5,6-диметилбензимидазола фенашшбромидом, а затем гидразиигидратом получают 1,4-диги/фо-3-фенил-7,8-димети1Л-1,2,4-триазино (3,4-а) бензймидазол (пример 5.
В случае производных имидазола, с целью снижения температуры проведения процесса и повышения выхода целевых продуктов, лучше использовать не 1-ацилмети-2-метилмеркаптоимидазояы, а соответст- вуюшие сульфоны.
Целевые продукты выделяют известными способами. Данный способ может быть использован для получения триазиноимидазола и его трицикличес1 их анало1Х)в, содержащих в бензольном ядре различные заместители. ,
Пример 1. 1 4--Дига/дк)-1,7- 5|й14 дал-3-( П -бромфенил)-имидазо (2,1-с) ас-триазин.
К суспензии 4,95 г (О,01 моля) 1-( П -бромфенацил)-2метилсульфонил-4,5-дифенилимидазола в 2О мл метанола прибавляют 1,62 г (0,015 моля) феиилгидразина. Смесь нагревают в (автоклаве емкостью 5 О мл при 160-17О С в течение 6-8 час, охлаждают, осадок отфильтровывают, промывают водой, а затем метанолом. Выход продукта-3,8 г (75% от теоретического), То плг 258-26О С (с разложением из водного диметилформамида).
Найдено, %: С 68,6; Н 4,3; N 1О,9, Вг 15,4.
Вычислено, %: С 68,9; Н 2, N 11,1
Bs 15,8,
Пример 2. lJ,4-Дигш po-l- IpOпил-3-фенил-вс-триазино (3,4-а) бензимидазол
К раствору 2,82 г (0,01 моля) 1-фенaIШQ-2-мeтия iepкaптoбeнзимиднзoлa в 2О мл даметилформамида прибавляют 1,2 (О,О15 Mojra) пропилгидразина, смесь кипятят 5 час, охлаждают, выливают в воду осадок отфильтровывают. Выход продукта2,2 г (76% от теоретического), т. пл, .47°Р (из родного ацетона). Найдено, %: С 72,1; Н 5,7. N 4.1/2 Вычислено, %: С 72,2;, Н 6,2. Пример 3. 1,4-Дигидро-1,3-дифенип-7,8-диметил-ас-триазино (3,4-а) бензимидазол. Смесь из 3,1 г (0,01 моля) 1-фенаци i -2-метилм еркапто-5,6 -диметилбензимидазо ла и 1,62 г (0,015 моля) фенилги;фазина в 20 мл метанола нагревают и обрабатывают по примеру 1. Выход продукта-2,4 г (68% от теоретического), т. пл.-224-i 225°С (с разложением, из смеси спирт-диметилформамид). Найдено, %: С 78,7; Н 5,7; N15,7 4 Вычислено, %: С 78,4; Н 5,7; N 15,9 Пример 4. 1,4-Дигидро-1,3-дифе /нил-7,8-диметил-ас-триазино (3,4-а) бензимидазол. К раствору 3,1 р (0,01 моля) 1-фенацил-2-метилмеркапто-5,6-диметилбензимидазола в ЗО мл диметилформамида прибав- ляют 1,62 г (0,015 моля) фенилгидразина. Смесь кипятят 5 -час, охлаждают, прибавляют ЗО-4О мл метанола и охлаждают до 0-5 С. Выделившийся осадок отфильтровьшают и промывают водой. Выход про,дукта-1,9 г (55% от теоретического), т. пл.-224-225°С (с разложением из вод ного диметилформамида). Пример 5. 1,4-Дигищ)о-3-4|енил-7,8-диметил-ас-тр11азино (3,4-а) бензимидазол. К раствору 0,01 моля бутилата натрия в 1О мл бутилового спирта прибавляют 1,92 г (0,01 моля) 2-метилмеркапто-5,6 -диметилбензимидазола и после растворени последнего 1,99 г (0,01 моля) фенацилбромида. Реакционную массу перемешивают в течение 20-30 мин при ЗО-С, после чего нагревают 1 час на кипящей водяной бане. Затем прибавляют 0,75 г (0,015мо ля) 85%-ного гидразингидрата, растворенного в 2-3 мл бутилового спирта, и кипятят 3 час. Смесь охлаждают до О°С, оса док отфильтровывают и промывают водным метанолом. Выход продукта-1,7 г (61% от теоретического), т. пл.-288-290°С (с разложением из водного диметилформамида). Найдено,%: С 73,5; Н 5,4; N 2О,О 4 Вь1числено, %: С 73,9; Н 5,8; N 20,3 Пример 6. 1,4-Дигидро-3-( а -метилфенил)-7,9-диметил-ас-триазино (3,4- f ) ксантин, К суспензии 3,58 г (0,01 моля) 7- J -( П -метилфенаш1л)-8-метилмеркаптотеоиллина в 30 мл метанола прибавляют 0,75 г (0,О15 моля) 85%-ного гидразинГидрата.. Смесь нагревают и обрабатывают по примеру 1. Выход продукта-2,6 г (8О% DT теоретического), т. пл;-ЗО5 ЗО7 С (с разложением из водного диметилформа; мида). , %: С 59,3; Н 4,8; N 25,8 Вычислено, %: С 59,2; Н 5,0; N 25,9. Пример 7. 1,4-Дигидро-1-фенил; 3-( П -метилфенил)-7,9-диметил-ас-триазино (3,4- ) ксантин. Смесь из 3,58 г (0,О1 моля) 7-( П -} -метилфенядал)-8-метилмеркаптотеофиллина и 1,62г (О,015 моля) фенилгидразина в 2О мл метанола нагревают и обрабатывают по примеру 1. Выход продукта,1,9 г (63% от теоретического), т. пл.- .2О9-210°С (из водного диоксина). Найдено, %: С Н N 20,8 . 2«2о1б°2. ., Вычислено, %: С 66,0; Н 5,1; N 21,0, Предмет изобретения 1. Способ получения производных 1,4-дигидроимидазо (2,1-е) ас-триазина общей формулы N N . HI где R - арил, алкил; R, - водород, алкил, арил; Q 2 вместе образуют сконденсированное бензольное или диоксопиримидиново ядро, отличающийся тем, что соединения общей формулы N-CH -C-R Д.. 2 N R, где R , R имеют указанные значения, 1 - алкилмеркапто- или алкилсульфоногрупна. обрабатывают при нагревании гидрази-ном обшей формулы . ; Н NNHR 1 :9л где Я, имеет указанное значение, в среде органического растворителя с последующим выделением целевого цродук У известными способами.
Авторы
Даты
1975-07-25—Публикация
1973-05-18—Подача