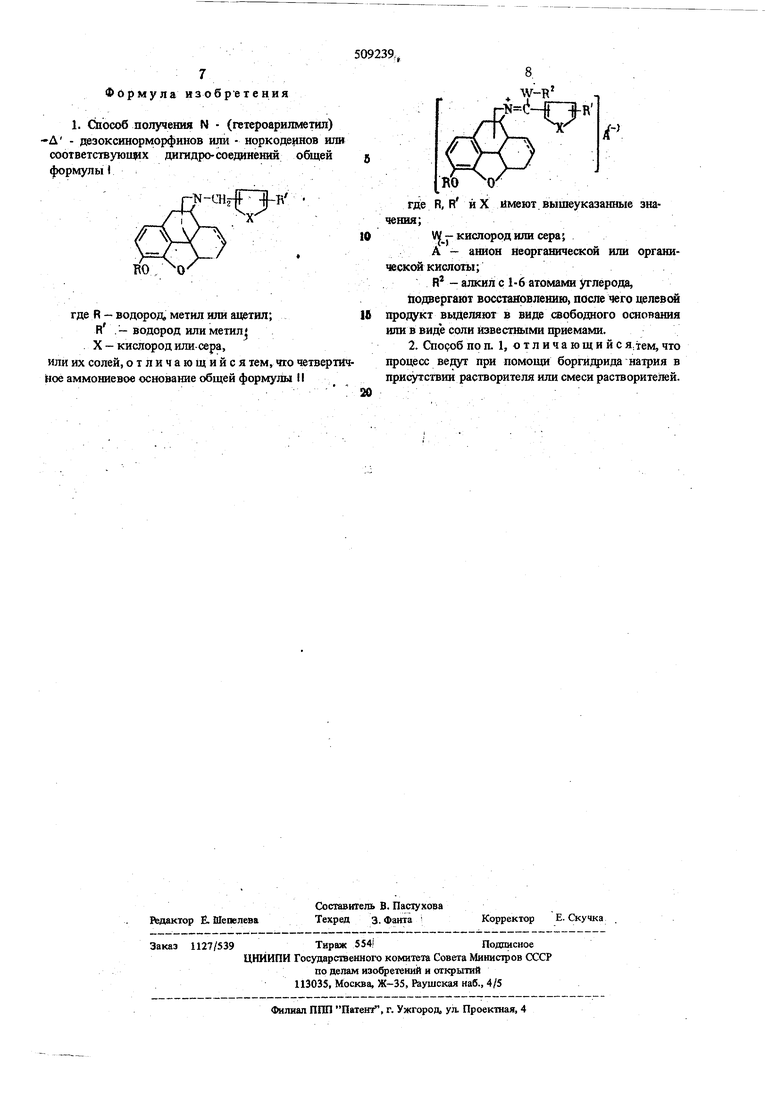
(S4) СПОСОБ ПОЛУЧЕНИЯ Ы- ГЕТЕЮАРИЛМЕТИЛ) - Д - ДЕЗОКСИ НОРМОРФИНОВ ИЛИ - НОРКОДЕИНОВ в присутствии катализатора гидрирования, например скелетного никелевого катализатора, причем в случае применения последнего получают дигидросоединение. Возможные .побочные реакщш предотвращают тем, что работают JB инертных pacrsov рителях. Продукты реакции вьщеляют известными методами, очища от, кристаллизуют и при желании переводят в соответствующие соли. Получение исходных соединений описано в примерах. . Соединения общей формулы I, согласно изобретению, представляют собой основания и могут обычным способом быть переведены в физиологически переносимые соли. Пригодными для солеобразования кислотами являются минеральные кислоты, например соляная, фосфорная, или органические кислоты, например уксусная, салициловая, аскорбиновая и др. Пример. Хлоргидрат N - фурфурилдигидродезоксиноркодеина, получаемьш восстановлением; иодметилата N - (2 - тиофуроил) - дигидродезоксиноркодеина:а)N - (2 - фуроил) - дигидродезоксиноркодеин. 6,16 г (0,02 моля) хлоргидрата дигидродезоксиноркодеина растворяют в 150 мл метанола, добавляют раствор 5,2 г карбоната калИя в 8 мл воды и при перемешивании при 20° С в тече1ше 10 мин прикапывают 2,6 г (0,022 моля) хлорангидрида фуран - 2 - карбоновой кислоты. Размещивают дополнительно в течение 30 мин при комнатной температуре, а потом раствор концентрируют в вакууме. Остаток встряхивают с 150 мл хлороформа и 100 мл воды. Органическую фазу отделяют, зкстрагируют путем последовательного встряхивания в 50 мл 2 н. раствора соляной кислоты и два раза в воде, каждый раз в количестве 70 мл, и после сушки над сульфатом натрия концентрируют в вакууме. При этом получают продукт реакида (8,2 г), который используют в стадии б. б)N - (2 - тиофуроил) - дигидродезокси кодеин. Полученный на предыдущей ступени реакции продукт растворяют в 100 мл абсолютного пиридина и этот раствор кипятят 3 час с обратным холодильником после добавления к нему 5 г пятисернистого фосфата. Растворитель выпаривают в вакууме и остаток поглощают 200 мл хлороформа и Нг О . Водную фазу извлекают еще два раза. хлороформом, каждий раз в количестве 5Q мд. Соединенные хлороформные растворы экстрагируют в присутствии льда встряхиванием с 100 мл 2 н. раствора соляной кислоты и затем промывают несколько раз водой. После сущки над сульфатом натрия концентрируют в вакууме в ротационном выпарном аппарате. Выход; 8,95 г. в)иодметилат N - (2 - тиофуроил) - дигидродезоксиноркодеина. Раствор 6, - (2 - тиофуроил) - дигидродезоксинррйодеиша в 100 мл абсолютного ацетона смешивают с 14,2 г (0,1 моля) йодистого метила и нагревают с обратным холодильником. Приблизительно через 2 час продукт реакции начинает выделяться в виде кристаллов. Реакционую смесь охлаждают, прибавляют 250 мл эфира и отсасывают кристаллизат. Выход сырого продукта 4,8 г; т.пл. 146-150°С (высушен над Pj QS ). г)Хлоргидрат N - фурфурилдигидродезоксиноркодеина. Полученный по пункту а иодметилат подают порциями в раствор 1,85 г борводорода натрия в смеси 36мл этанола и 18мл воды. При этом температура поднимается до 45° С. Для завершения реакции дополнительно перемешивают в течение часа. За темпо каплям осторожно подают 45 мл 2 н. раствора соляной кислоты и кипятят 15 мин с обратным холодильником. Реакционной смеси дают остыть, затем ее делают аммиачной и экстрагируют трехкратным встряхиванием хлороформом, каждый раз 100 мл. Органическую фазу промьшают 100 мл , сушат над сульфатом натрия и концентрируют в вакууме. Остаток (3,2 г) очищают аналогично примеру с хроматографией на колонне и переводят в хлоргидрат. Выход 2,6 г; т.пл. 233-235°С. Описанным выше способом получают и следующие соединения; Фбрмула изобретения 1. Способ получения N (гетероарилметил) Д - дезоксинорморфинов или - норкодеинов или соответствую1щх дигидро-соединений общей формулы Г ,N-CHef |-B где R - водород, метил или ацетил; R . - водород или метил . X - кислород или-сера, или их солей, отличающийся тем, что четверти ное аммониевое основание общей формулы 11 -- -СТв т О где R, R и X имеют вышеуказанные значения;VV -кислород или сера; А - анион неорганической или органической кислоты; R - алкилс 1-6 атомами углерода, Подвергают восстановлению, после чего целевой продукт выделяют в виде свободного основания шш в виде соли известными приемами. 2. Спороб по п. 1, отличающийс я, тем, что процесс Bejoyr при помощи боргидрида натрия в присутствии растворителя или смеси растворителей.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-тетрагидрофурил-6,7-бензоморфанов или их солей | 1975 |
|
SU588916A3 |
| АМИДЫ АМИНОКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2134683C1 |
| Способ получения -(гетероарил-метил) бензоморфанов или = морфинанов | 1974 |
|
SU543347A3 |
| Способ получения (гетероарилметил)- дезокси-норморфинов или их дигидросоединений или их солей | 1974 |
|
SU520049A3 |
| Способ получения -(гетероарилметил)- -дезокси-нормофинов или -норкодеинов | 1974 |
|
SU503523A3 |
| Способ получения пептидов | 1977 |
|
SU753358A3 |
| Способ получения 5,9- -дизамещенных-2-тетрагидрофурфурил-6,7бензоморфанов или их солей | 1976 |
|
SU587858A3 |
| Способ получения производных 4-амино-2-пиперидинхиназолина или их солей | 1980 |
|
SU953982A3 |
| Способ получения гидразин- -фенилпропионовой кислоты | 1972 |
|
SU539522A3 |
| 8-ЗАМЕЩЕННЫЕ-2-АМИНОТЕТРАЛИНОВЫЕ ПРОИЗВОДНЫЕ И СПОСОБЫ ИЗ ПОЛУЧЕНИЯ | 1990 |
|
RU2093507C1 |

Авторы
Даты
1976-03-30—Публикация
1974-09-30—Подача