ние простого эфира с применением гкцрохлорида пиридина. Также возможно расщепление в щелочной среде, например, с помощью VaOH и КОН в диэтипенгликопе. Продукты реакции выделяют известными методами, очищают, кристаллизуют и при желании переводят в соответствующие солг. Производные формулы П получают путем взаимодействия соответствующего норсоеди- нения с гетероарилметилгалогенидом или тозилатом. Соединения общей формулы 1, согласно изобретению, могут обычным способом п&реводиться в физисшогически переносимые соли. Пригодными для с оле образования кис-т лотами являются минеральные например соляная, азотная или органические, наприн мер уксусная, салициловая, аскорбиновая. 8-хлортеофиллин, метансульфоновая, бензолсульфоновая, этанфосфоновая кислоты и т.п Пример 1. Гидрохлорид Ы -(3-тиенилметил)-нордезоморфина. 3,6 г гидрохлорида N -(3-тиенилметил) -дигидродезоксиноркодеина нагревают в 150 мл концентрированной бромистоводород ной кислоты с обратным холодильником в течение 3 час. После удаления избыточной кислоты путем упаривания под вакуумом подщелачивают натровым щелоком и экстра гируют хлористым метиленом. Органическую фазу перерабатывают обычным образом, npi чем получают 1,83 г основания, которое переводят в гидрохлорид, Пример 2. JV -фурфурилнордезоморфин. 4,5 г гидрохлорида И -фурфурилдигидр дезокси-норкодеина и 25 г гидроокиси нагревают в 150 мл диэтиленгликопя в масл5шой ванне в течение 5 час. Затем разбавляют, добавляя 86 О мл воды, подгкисляют концентрированной соляной кислотой и делают аммиачным. Экстрагируют хлороформом, промывают хлороформовые экстрак- ты водой, сушат их над сульфатом натрия и упаривают в вакууме. После перекристаллизации из уксусного эфира получают 2,3 г продукта с точкой плавления 166-167 4::, Пример 3. - 2-метш1фурилм&тил- (ЗД -нордезоморфин, 3,2 г N - 2-метш1фурШ1метил(33-0-ацетилнордезоморфина растворяют в 150 мл абсолютного тетрагидрофурана и к раствору, охлаждая, каплями добавляют суспензшо из 2 г алюмогищ)ида лития в 50 мл абсогаот ного тетрагидрофурана. По истечении 2 час нагревают до кипения, охлаждают и осторожно смешивают с водой. Добавляют 20О Мл насыщенного раствора тетрата диаммония, размещивают в течение двух часов и отделяют тетрагидрофурановьдй слой. Растворитель отсасывают в вакууме и остаток пер&ч кристаллизовывают из уксусного эфира. Выход 2,78 г; т, пл, 166-167°С, Пример 4.N -{2-метил-фурилметил- (3)J -нордезоморфин. 3,5 г гидрохлорида М -У2-метилфурил- метил-(3)-0 ацетилнордезоморфина нагревают в 100 МП концентрированной ссщяной кислоты с обратным холодильником в течение 2 час. Затем избыточную кислоту удаляют в вакууме и остаток подщелачивают аммиаком. Аммиачный раствор экстрагируют хлороформом, органическую фазу упаривают досуха над сульфатом натрия и остаток пер&кристаллизовывают из уксусного эфира. Выход 2,06 г; т, пл, 165-166 °С, Пример 5, Гидрохлорид Ц -(3-триенилметил) -нордезоморфина., 3,6 г (0,009 моль) гидрохлорида N-(3-тиенилметил)-дигидродезоксиноркодеина нагревают 30 мин вместе с 17,5 г гидрохлорида пиридина на масляной ванне, разогретой до 190 С. После охлаждения раоплав растворяют в воде, примещивают 20 г карбоната натрия, а пиридин удаляют перегонкой с водяным паром. Затем охлаждают, остаток поглощают в хлористом метилене и раствор хлористого метилена после сущкиего над сульфатом натрия выпаривают. Выход 1,9 г (62% от теории). Получаемый обычным способом гидрохлорид перекристаллизовывают сначала из спирта-ацетона, а потом из воды. Получаемый моноги;фат разагается при температуре выще 190°С, Описанным Bbmie способом получают содинения, приведенные в таблице.
А, ДЕГЕиц)Одезокс№-вроизводш 1е
520049

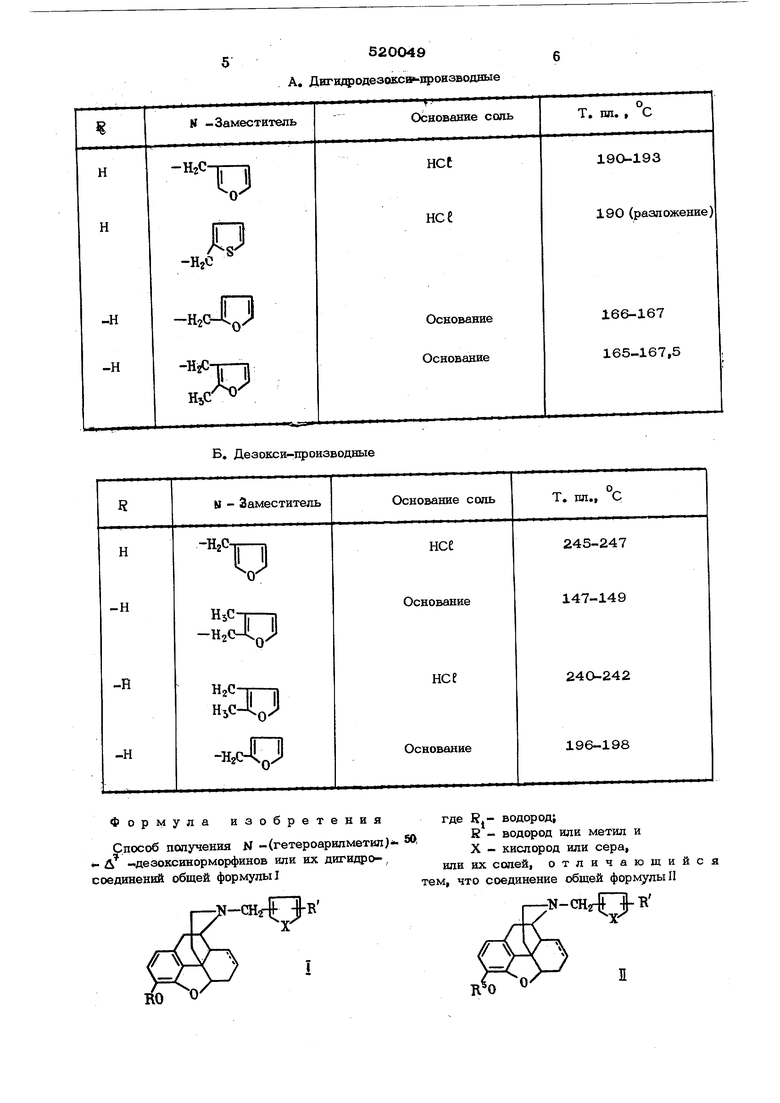


Б. Дезокси-производные Формула изобретения Способ получения N -(гетероарипметип)«- Л -«дезоксинорморфинов или их дигидро-, соединений общей формулы где водород; 50,К - водород или метил и X - кислород или сера, или их сапей, отличающийся тем, что соединение общей формулы П r-N-CHrg i ie R и X имеют вышеуказанные значения алкилированию, с последующим выделением ий- аиильная, алкильная или аралкильнаяцелевого продукта в виде свободнсяго осногруппа, подвергают деацилированию или де-вания или в виде соли.
520049
Авторы
Даты
1976-06-30—Публикация
1974-09-30—Подача