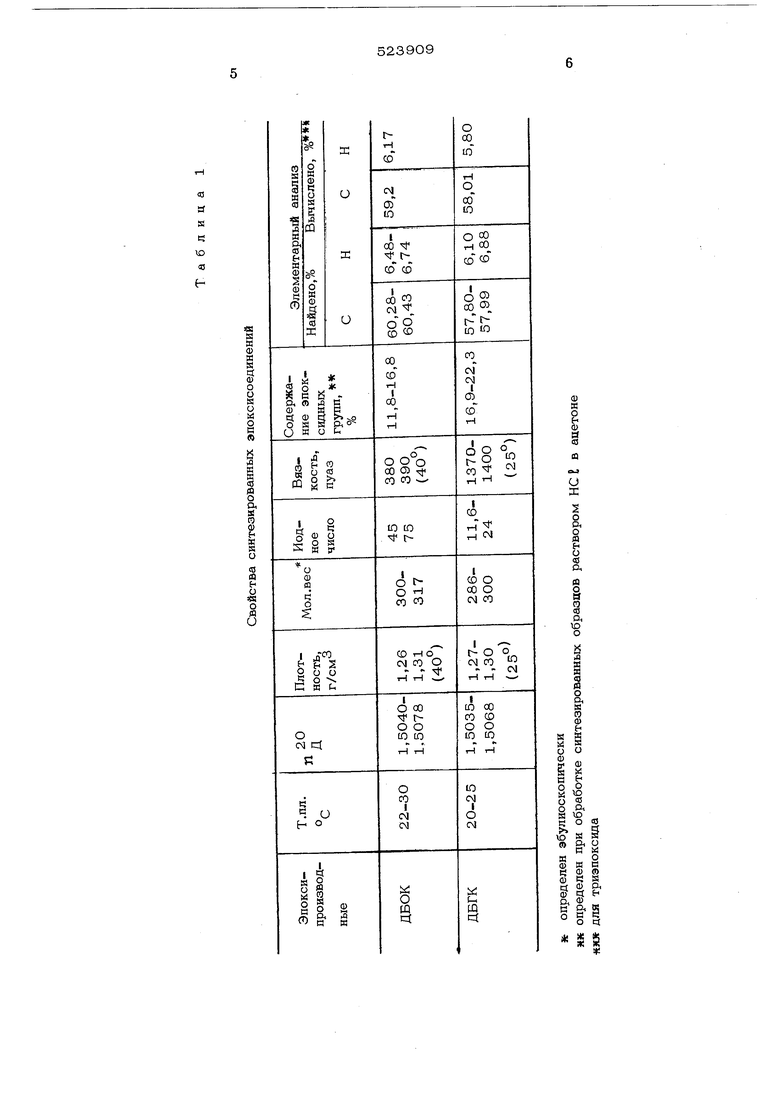
Изобретение относится к новым химическим соединениям, в частности к эпоксипроиз водным диаллиповых эфиров бицикло (2.2.1) гептен-5-дикарбоновой-2,3-кислоты и бицик ло (2.2.2) октен-5-дикарбоновой-2,3-кисло ты общей формулы СООСНзСН-СНг COOCHnCH-tiHn где А - атом кислорода или С-С связь, п 1 или 2. Известны диглицидиловые эфиры бицикло (2.2.1)гепт-5-ен-2,3-дикарбоновых кислот LI,2,Известные соединения содержат двойную связь в цикле, а эпоксидные группы В боковых цепях. Известен способ получения эфидрв эпокси замещенных поликарбоновых кислот и эпоксизамешенных спиртов, в частности эпоксипроизводных аллиловых эфиров эйкозандиендикарбоновой кислоты, димеризованной линолевой кислоты и 4-циклогексекдикарбо; овой кислоты и их отверждение в присутствии полиглицидилового полиэфира бисфеноиа и 2,4,6- -ггри (диметиламинометил) фенола 3J - Предлагаемые диглицидиловые эфиры отличаются от известных структурной формулой. Целью изобретения является синтез циклоалифатических эпоксисоединений бициклической структуры, содержащих не менее двух эпоксидных групп, которые могли бы быть использованы для изготовления коррозионнои водостойких покрытий. Эпоксисоединения указанной общей формулы получают эпоксидиоованием диаллиловых эфиров бицикло (2.2.2) октен-5-дикарбоновой-2,3-кислоты (ДБОК) и бицикло ( 2.2.1) гептен-5-дикарбоновой-2,3-кислоты (ДБГК) в среде органического растворителя при использовании в качестве эпоксидирующего агента 5О-80%-ной надуксусной кислоты. Реакцию эпоксидирования целесообразно проводить при 25-50%-ном избытке надуксусной кислоты в среде этилацетата или хлороформа при использовании в качестве буфера безводного сульфата натрия или ацетата натрия при температуре 30-40 С. Ход реакции контролируют, следя за изменением концентрации надуксусной кислоты. Продукты представл5цот собой смесь дии триэпоксипроизводных диаллиловых эфиров. Эти эпоксидные смолы далее могут быть отверждены: а) в присутствии 0,5-5% катионного катализатора (например, ) с последующей термообработкой при 18020О ; б) ангидридами кислот (например, ангидридом изометилтетрагидрофталевой кислоты при эквимолекулярном соотнощении эпоксидных и кислотных групп) с последующей термообработкой при 70-180 С; в) сло ными ненасыщенными полиэфирами с последующей термообработкой при 12О-150°С; г) ненасыщенными жирными кислотами (ла- пример, льняного масла при избытке эпоксидных групп по отношению к карбоксиль- ным) с последующей термообработкой при 14О-170°С. Небольшое количество свободных аллильных связей обеспечивает дополнительную сщивку отверждаемых продуктов и, следовательно, улучшение физико-механических свойств. Синтезированные эпоксидные смолы были использованы для получения покрытий по металлу и стеклу. Для лучшего понимания данного изобрете ния приводятся следующие примеры получения эпоксипроизводных диаллиловых эфиров бициклических дикарбоновых кислот .и покрытий на их основе. Синтез эпоксисоединений В раствор 0,1 моля диаллилового эфира бициклической кислоты в 100 мл хлороформа вводят 5% (от веса надкислоты) безводного Nuj. затем при 20 С добавляют О,35-О,4 моля 50-80%-ной надуксусной кислоты. Реакционную смесь выдержива ют при 30-35 С в течение 5-7 дней до. практически полного прекращения изменения концентрации надкислоты в растворе (концентрацию надкислоты определяли иодометрически). Реакционную смесь обрабатьтают холодной водой, раствором соды, вновь водой и отделяли органический слой, который сушили с помощью свежепрокаленного затем удаляют в вакууме при 20 С раство- ритель. В остатке получают бесцветную вяз кую жидкость (выход 75-85% из расчета на триэпоксид), которая при охлаждении застывает с белую пастообразную массу. Свой ства синтезированных продуктов приведены в табл. 1. Получение покрытий Пример 1. 5,5 эпоксидированного ДБОК, синтезированного по методике, описанной выше, содержащего 6,2 5% эпоксидного кислорода и имеющего йодное число 45, помещают в ампулу в атмосфере аргона, вводят при 20 С с помощью щприца 1 мл Sn С1д в виде бензольного раствора, со- держащего 0,16 г $7гС1д(3% от веса эпоксипроизводного), при этом мгновенно образуется форполимер, который затем растворяют в 5 мл ацетона, полученный вязкий раствор наносят на стеклянные пластинки, которые выдерживают при 200 С в течение 1 час, получают блестящие желтоватого цвета покрытия, результаты испытаний свойств которых приведены в табл. 2. Пример 2. В раствор форполимера, полученного по методике, описанной в примере 1, вводят 2% перекиси бензоила, наносят на стеклянные пластинки и вьщер- живают 7 час при 60°С и 14 час при15О С и получают покрытие желтоватого цвета. Свойства приведены в табл, 2. Пример 3. Смесь 58,5% эпоксидированного ДБОК с содержанием эпоксидных групп 11% и 41,5% жидкого изометилтетрагидрофталевого ангидрида наносят на стеклянную пластинку и отверждают при нагревании до 140 С в течение 15 час и 3 час при 200 С; получают прочные прозрачные покрытия, свойства которых приведены в табл. 2. При отверждении этой композиции в форме, в предложенных условиях получают прозрачные отливки, нерастворимые в органических растворителях и не разрушающиеся при действии 10%-ного раствора NaOHи 5-1О%-ного раствора NaCt свыше 6 месяцев. Пример 4. Смесь 1,2 г эпоксидированного ДБГК с содержанием эпоксвдного кислорода 7% и 8 г ненасыщенного сложного полиэфира, имеющего кислотное число 35, синтезированного взаимодействием при 19О С эквимолекулярных количеств малеинового ангидрида с диэтйленгликолем, растворяют при нагревании в 10 мл диметилформамида, полученный раствор наносят на стеклянные и медные пластинки, выдерживают 6 час при 120 С и 6 час при 14015О С, получают прозрачные эластичные покрытия, свойства которых приведены в табл. 2. Пример 5. Смесь 20,2 г эпоксидированного ДБГК (содержание эпоксидното кислорода 6%) и 6,0 г жирных кислот льняного масла (кислотное число 183) нагревают 2 час при 160 С, продукт реакции. имеющий кислотное число 16,5 растворяют в 15 мл толуола, вводят раствор 0,66 г S-nCl в 5 мл толуола, нагревают 2 час при 100 С, добавляют 1,2 г нафтената Со
в а
S
« ю яз t



| название | год | авторы | номер документа |
|---|---|---|---|
| Эпоксипроизводные дициклогексениловых эфиров для повышения адгезии резины к полиэфирным волокнам | 1977 |
|
SU704954A1 |
| Способ получения модифицированного полиакрилонитрила | 1976 |
|
SU651008A1 |
| СПОСОБ ОТВЕРЖДЕНИЯ ДИЕНОВЫХ ПОЛИМЕРОВ С ФУНКЦИОНАЛЬНЫМИ ГРУППАМИ И ОТВЕРЖДЕННЫЙ ДИЕНОВЫЙ ПОЛИМЕР | 1993 |
|
RU2120449C1 |
| ИЗДЕЛИЯ ИЗ ТЕРМОПЛАСТОВ С ВЫСОКОЙ СТЕПЕНЬЮ СТРУКТУРООБРАЗОВАНИЯ | 2002 |
|
RU2289597C2 |
| Способ получения модифицированного полиэтилентерефталата | 1979 |
|
SU891699A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИДИРОВАННЫХ ПЛАСТИФИКАТОРОВ | 1969 |
|
SU245760A1 |
| Способ получения термореактивных полимеров | 1973 |
|
SU459966A1 |
| ФОТОРЕЗИСТНАЯ КОМПОЗИЦИЯ | 1998 |
|
RU2199773C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭПОКСИДИРОВАННЫХ РАСТИТЕЛЬНЫХ МАСЕЛ | 1999 |
|
RU2161172C1 |
| КОМПОЗИЦИЯ ДЛЯ ПОКРЫТИЯ, ВКЛЮЧАЮЩАЯ БИЦИКЛО-ИЛИ СПИРО-ОРТО-СЛОЖНОЭФИРНОЕ ФУНКЦИОНАЛЬНОЕ СОЕДИНЕНИЕ | 1997 |
|
RU2180674C2 |

«:
S
а
о
о
л
о а
g
IS
о ffl
OQ
ш I
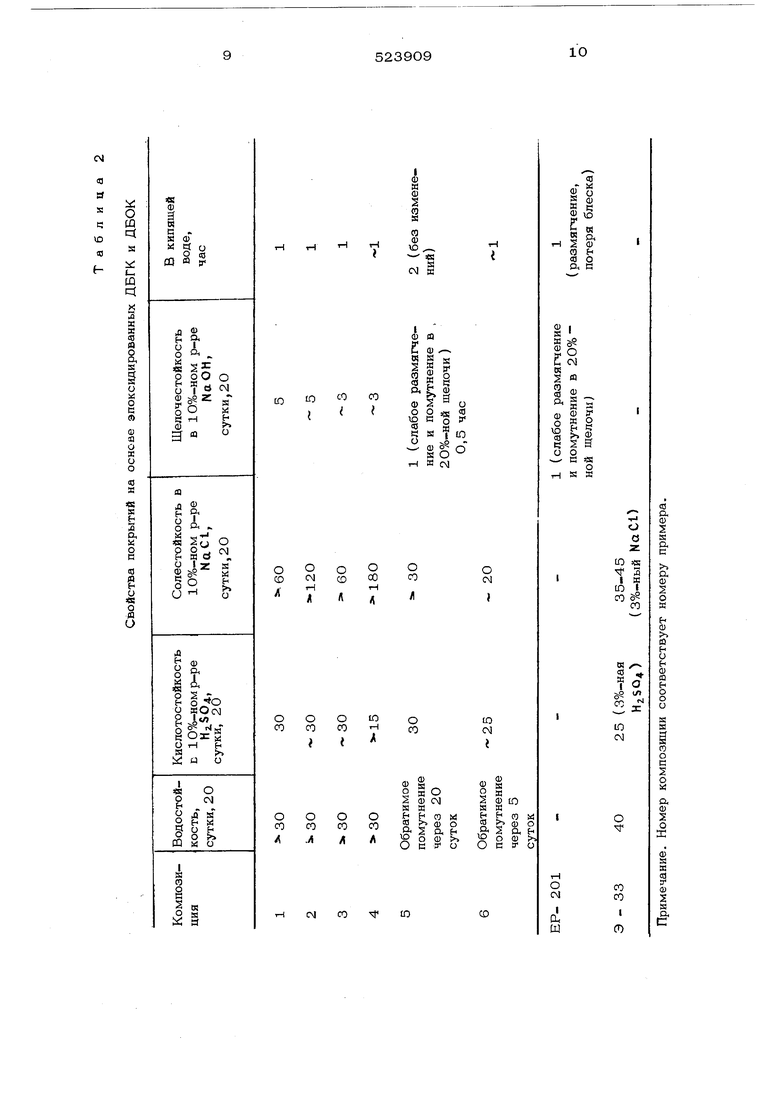
0) 52 и наносят полученную композицию на стеклянные и медные пластинки, вьщерживают 2 час при 140-150°С и 3 час при17О°С, получают прозрачные очень эластичные покрытия, свойства которых приведены в табл. 2. Пример 6. Композицию, приготовленную по примеру 5, сушат 15 час при 1ОО-12 О С и получают прозрачные эластичные покрытия, свойства которых приведены в табл. 2. Таким образом, синтезированные зпоксипроизводные пригодны для получения покрытий горгсчей сушки, обладающих улучшенной ВОДО-, КИСЛОТО-, исолестойкостью. При использовании в качестве отвердителей ненасыщенных сложных полиэфиров и жирных кислот масел получают покрытия по металлу повышенной эластичности, которые могут вьщерживать обработку металла, например щтамповку. Все приведенные составы лаков отличаются высокой жизнестойкостью при хранении их при кокшатной температуре.
я я
s
с:
VD
а
(tS D, 0)
О С5
S
а
Ю«
:
л
а
IЯ
0)
ЮI
2
со ss
о
со
§
f о 6 С,
со .
Ю см
о ф
ф s
а
ф 2 11 Формула изобретения Эпоксипроизводные диаллиловых эфиров бициклических дикарбоновых кислот общей формулы : tx COOCHjCH-CHi ft lttHlT и Ц21п1 CUWtrll24 / 2 10 где А - эпоксидный кислород или С-С связь, 5239О 9 12 71-1,2 для получения химстойких покрытий. Источники информации, принятые во внимание при экспертизе: 1- Патент США № 3764584,кл. СО8 д. ЗО/12, 1974, - прототип, 2, Патент Англии № 132О944,1сл.СО8 9-30/12, 1974. 3. Патент США № 287017О,КЛ.СО8д.ЗО/12, 1959 г.
Авторы
Даты
1976-08-05—Публикация
1975-01-10—Подача