где R, Ri, R2, Rs и X имеют указаЁное значение и Halo означает атомы хлора или брома. Реакцию проводят в среде безводного, инертного в условиях реакции, органического растворителя, например бензола, при 150- 160°С.
Применяемые ацетидины получают описанным способом. Производные галогенэтил имидазола формулы И получают циклизацией 2-(2-фёниламинэтил)-аминоспирта в присутствии фосгена с последующим щелочным гидролизом полученного продукта и замещением оксиостатка атомом галогена с помощью тионилгалогенида.
Полученные соединения являются твердыми веществами, которые умеренно растворимы в воде и сильно растворимы в разбавленных кислотах или в обычных органических растворителях.
Пример 1. 1-(л4-Хлорфенил)-4-метил-3 2-(3,3-дипропилацетидин - 1 ил) - 1 - метилэтил -2-имидазолидинон.
Смесь 7 г 3-(2-хлор-1-метилэтил)-1-(и лорфенил)-4-метил - 2 - имидазолидинопа и 10 г 3,3-дипропилацетидина в 100 мл безводного бензола нагревают в течение 8 час при 150-160°С в бомбе. Растворитель упаривают в вакууме и остаток растворяют в воде, доводят до щелочпой реакции при помощи водного карбоната натрия и экстрагируют диэтиловым эфиром. Полученный остаток очищают после концентрирования органического слоя колоночной хроматографией на силикагеле при применении хлороформа, содержащего 8% метанола, в качестве элюента.
Выход 8,6 г, т. кии. 220°С/0,5 мм рт. ст.
Пример 2. 1-(/г-Хлорфенил)-4-метил-3- 2(3,3-дипропилацетидин - 1-ил) - 1-метилэтил 2-имидазолидинон.
При применении 3-(2-хлор-1-метилэтил)-1(п-ХЛ9рфенил)-4 - метил - 2-имидазолидинона вместо 3-(2-хлор-1-метилэтил) - 1-(ж-хлорфенил),-4-метил - 2-имидазолидинона в способе примера 1 получают названное соединение, т. кип. 160°С/0,6 мм рт. ст.
Пример 3. 1-(ж-Хлорфенил)-4-метил-3- 2(3,3-диметилацетидин-1-ил) - 1 -метилэтил -2ИМИД.ЗЗОЛИДИНОН.
Получают согласно описаиному в примере 4 способу из 3,3-диметилацетидина и 3- (2хлор-1-метилэтил) - 1-(ж-хлорфепил)-4-метил2-имидазолидинона, т. кип. 200°С/0,6 мм рт. ст.
Соответствующий гидрохлорид плавится при 162-164°С.
Пример 4. (п-Хлорфенил)-амино-1метилэтил -амино-1-пропанол.
К суспензии 38 г литийалюминийгидрида в 2000 мл диэтилового эфира, охлажденной до 0°С, прибавляют по порциям при перемешивании 95 г сложного этилового эфира (лхлорфепилкарбамил)-этиламино - пропионовой кислоты, растворенного в 1200 мл безводного диэтилового эфира.
После этого нагревают в течение 2 час при перемешивании с обратным холодильником.
Прибавлением воды разлагают полученный комплекс при 0°С. Смесь перемещивают в течение 30 мин при комнатной температуре и неорганические твердые вещества удаляют
фильтрацией. Эфирный раствор сушат и упаривают. Полученный остаток дает после дистилляции в колбе 76 г упомянутого в заголовке соединения, т. кип. 170°С/04 мм рт. ст., выход 98,5%.
Полученный обработкой ацетилхлоридом в уксусной кислоте ацетат кипятят при 160°С/0,5 мм рт. ст.
Таким же путем получают л-хлорфенилзамещенное производное, т. кип. 170°С/0,5 мм
рт. ст.
Соответствующий ацетат кипятят при 160°С/0,5 мм рт. ст.
Пример 5. 1 - (n-Xлopфeнил)-3-(l-oкcимeтилэтил)-4-мeтил-2-имидaзoлидинoн.
К смеси 36 г (п-хлорфенил)-амино-1метилэтил -амино-1-иропанола в 75 мл толуола и 29 г КОН в 250 мл воды, охлажденной до 0°С, прибавляют раствор 22 г фосгена в 75 мл безводного толуола. Смесь перемешивают в течение 90 мип и прибавлением раствора КОН поддерживают щелочную реакцию. Толуол отделяют и водную фазу экстрагируют диэтиловым эфиром. Органические растворы собирают, сушат и коицептрируют.
остаток растворяют в 500 мл метанола и обрабатывают 2,5 г КОН.
Смесь оставляют стоять в течение 2 час и после упаривания метанола в вакууме ее растворяют в воде и подкисляют разбавленной
соляной кислотой. После экстракции эфиром очищают полученный после упаривания растворителя остаток колоночной хроматографией на силикагеле при элюировании хлороформом, содержащим 1% метанола. Фракции,
содержащие продукт, собирают и концентрируют. Остаток промывают небольшим количеством изопропилового эфира, фильтруют и после этого промывают петролейным эфиром. Выход 15,2 г (38%); т. пл. 108-110°С.
Так же получают ж-хлорзамещенный ана-, лог, выход 63%; т. пл. 75-77°С.
Пример 6. 1-(п-Хлорфенил)-3-(2-хлор-1метилэтил)-4-метил-2-имидазолидинон.
К раствору 16 г 1-(п-хлорфенил)-3-(1-оксиметилэтил)-4 - метил - 2 - имидазолидинона в 400 мл безводного хлороформа прибавляют по каплям при перемещивании 14,5 г SOCb и смесь выдерживают при 0°С. Смесь нагревают в течение 45 мин с обратным холодильником,
концентрируют в вакууме и растворяют в бензоле и опять концентрируют досуха. Выход 15,1 г (94%) упомянутого в заголовке соединения, т. пл. 70-72°С (из диизопропилового эфира).
Соответствующее ж-хлорфенилзамещенное соединение получают так же. Выход 97%, т. кип. 200°С/0,5 мм рт. ст.
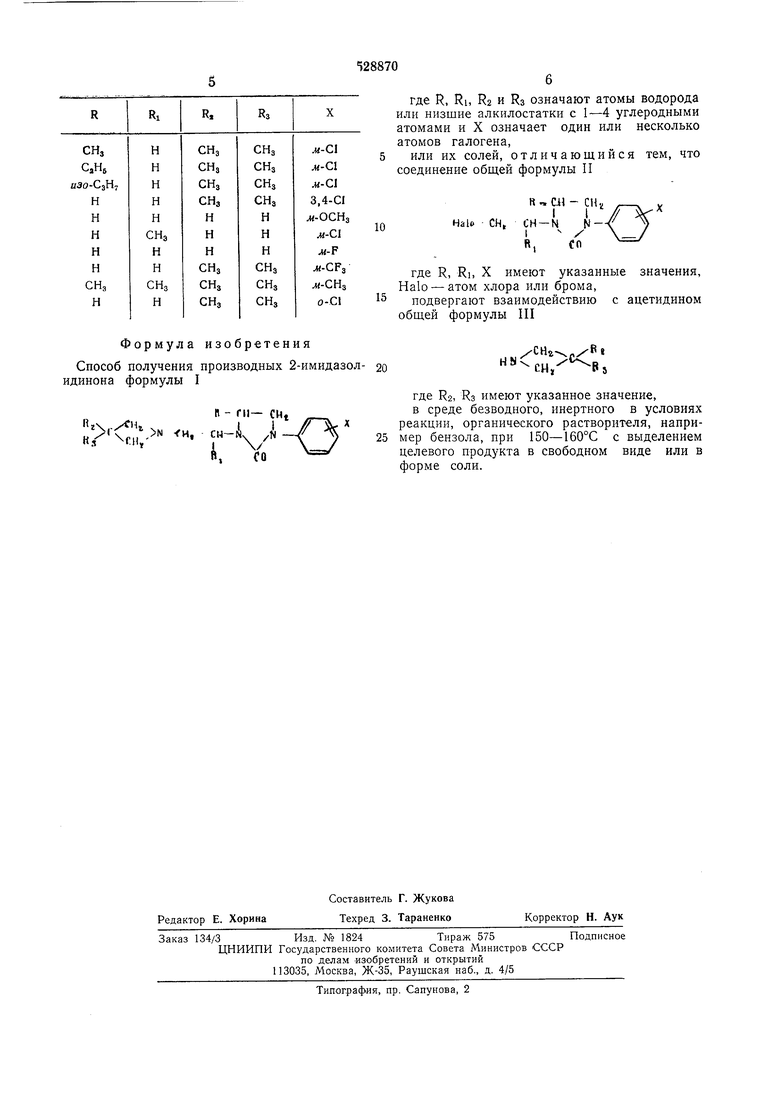
Согласно описанному способу получают соединения формулы I, значения R, Ri, Rj, Rs и
X которых приведены в таблице.
Формула изобретения
Способ получения производных 2-имидазолидинона формулы I
R - ГЦ- CMt
-СИ,
СН-N4 ,N
./
СО
где R, Rb R2 и Rs означают атомы водорода или низшие алкилостатки с 1-4 углеродными атомами и X означает один или несколько атомов галогена,
или их солей, отличающийся тем, что соединение общей формулы II
- cHj,
I
СИ,
СИ -N
NI
СП
где R, Ri, X имеют указанные значения. Halo - атом хлора или брома,
подвергают взаимодействию с ацетидином общей формулы III
/снг /RI
НЫ
сн.
где Rg, Ra имеют указанное значение, в среде безводного, инертного в условиях реакции, органического растворителя, например бензола, при 150-160°С с выделением
целевого продукта в свободном
виде или в форме соли.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ 0-АНИЛИНО- ФЕНИЛЭТИЛОВЫХ СПИРТОВ | 1973 |
|
SU381217A1 |
| Способ получения производных бутирофенонпирролидина или их солей | 1973 |
|
SU548206A3 |
| Способ получения производных имидазолидинона | 1971 |
|
SU448645A1 |
| ПРОИЗВОДНЫЕ 1-АМИНО-2-ЗАМЕЩЕННОГО ФЕНИЛЭТАНОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) | 1992 |
|
RU2095344C1 |
| Способ получения 1,1-дигалоид3-арилпропена-1 | 1972 |
|
SU444357A1 |
| Способ получения производных аминопиррола или его солей | 1974 |
|
SU843738A3 |
| ПРОИЗВОДНЫЕ 1-(АРИЛАЛКИЛАМИНОАЛКИЛ) ИМИДАЗОЛА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1992 |
|
RU2118957C1 |
| Способ получения производных изоксазолидина | 1973 |
|
SU481157A3 |
| ПРОИЗВОДНЫЕ ОКСАЗОЛИДИНА, ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, ИЛИ СЛОЖНЫЕ ЭФИРЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1993 |
|
RU2090564C1 |
| ПЛТЕИТНО- ПХНЙЧЕСКАЯ БИБ.1ИОТЕКА | 1969 |
|
SU241320A1 |


Авторы
Даты
1976-09-15—Публикация
1975-02-27—Подача