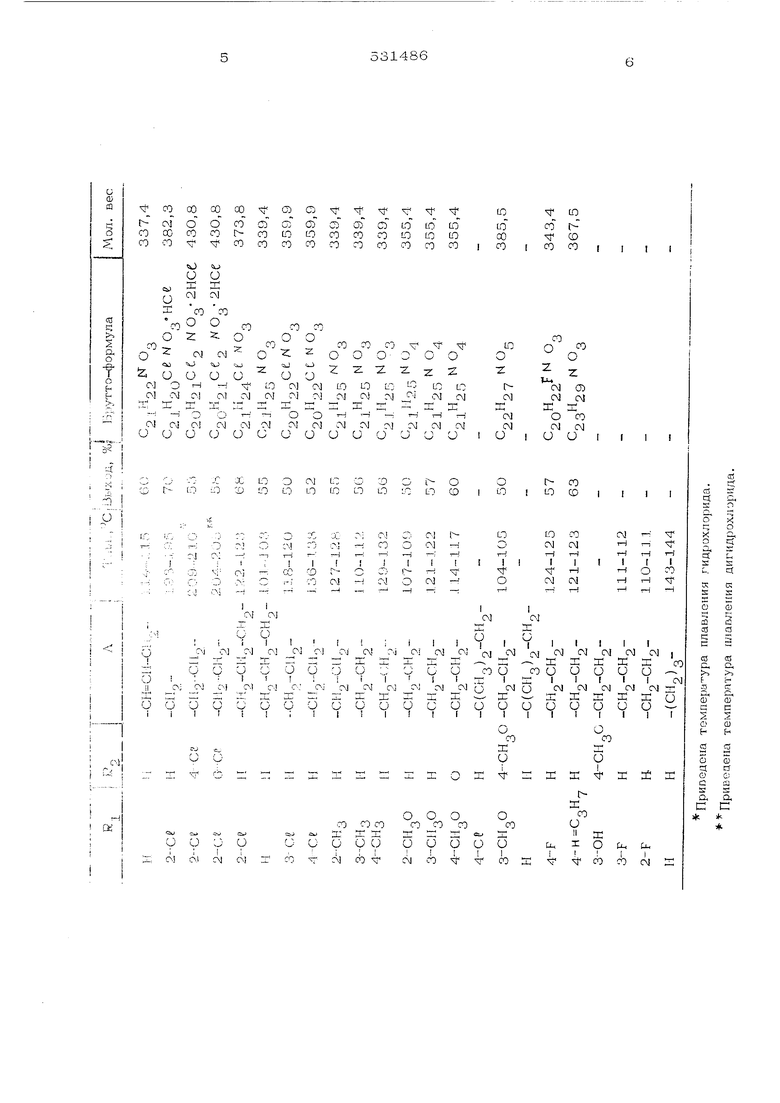
де Органического растворителя, реакционную смесь гидролизуют и целевой продукт выделяют в виде основания или соли. В целевых соединениях - низшие алкил или алкокси обычно содержат 1-4 атома углерода, чаще всего R, и R представляют собой метил или метоксил. Когда R и Rj - галоид, то это фтор, хлор, бром или йод, предпочтительно хлор, находящиеся в 0-положении. В качестве органического растворителя MOJifflo использовать эфиры, например диэтийовый эфир или тетрагидрофуран (ТГФ),аооматические углеводороды, напримео бензол. Температура .реакции (-20) - 8О С, предпочтительно 20 - 55 С. Гидролиз проводят известным способом, например в присутствии водного раствора хлористого аммония, Исходные производные пиперидина можно получить при взаимодействии соответствующих фенилалкиламинов с 2 моль эфира акриловой кислоты, последующей циклизации по Дикману, омылении образовавшегося кетоэфи ра и декарбоксилировании кетокислоты. Для получения солей целевых соединений применяют органические и неорганические кислоты, например малеиновую, фумаровую, щавелевую, соляную и бромистоводородную. Необходимо особенно отметить целевые соединения, в которых R, и R 2 - хлор или :ОДОрОД, R, - водород,П - 1 ИЛИ 2. П р и м е р 1. 1-фенилэтил 4-окси-4-(3 ,4- стилендкоксифенил)-пиперидин. Суслензшо 12,2 г метилендиоксибензола и 17,8 г N -бромсукцинимида в 120 мл хлорс:.;0рма кипятят 3 час с обратным холо дильником, получая через 20 мин прозрачный красно-коричнезый раствор, а через 1,5 час - желтый раствор. По окончании ки пячения промывают прозрачный раствор воцой, сушат сульфатом натрия и отгоняют 3,4 ибромбензол, т.кип. 105-108 -метил ендног /11- мм рт.ст. В колбу с мешалкой, капельной воронкой термометром и обратным холодильником, сна женным осушительной трубкой с едким каля загружают в атмосфере азота 1,35 г магн 2О мл ТГФ, нагревают до евой стоужки я 50-80 С и добавляют несколько капельбро илендиоксибромбензола в ТГФ добавляют по каплям в течение 10 мин, выдерживают 1 час лри 5О-60 С и получают раствор 3,4-метилендиоксифенилмагнийбромида, который охлаждают и в течение 45 мин добавляют к раствору 10,15 г 1-фенилэтилпиперидона-4 в 35 мл ТГФ, поддерживая температуру не выще 40 С. По окончании добавления выпадает осадок. Затем смесь выдерживают 2 час при 38-40 С, упариваЮ1Т в вакууме, добавляют к остатку 150 мл эфира при 10-15 С, по каплям в течение 15 мин вводят 100 мл концентрированного водного раствора хлористого аммония, промывают эфирный слой два раза водой, сушат сульфатом натрия, упаривают досуха на роторном испарителе и получают 1-фенилэтил-4-окси-4- (3,4-метилендиоксифенил)-пиперидин, т.пл. 123-125 С, (изопропанол), с выходом 70%. Аналогичным образом получают соединения, перечисленные в таблице. Пример 2. 1-{2-Хлорфенилэтил)-4-ОКСИ-4- (3,4-метилендиоксифенил)-пиперидин. 1,31 г магниевой стружки в 30 мл абсолютного ТГФ активируют добавлением следов иода и йодистого метила при нагревании К этой смеси в атмосфере азота добавляют по каплям раствор 1О,О7 г метилового эф1Дра 4-бромпирокатехина в 60 мл абсолютного ТГФ, нагревают до 50-55 С, по окончании взаимодействия нагревают еще 45 мин; при 55 С, охлаждают до 30 С и при этой температуре при перемещивании добавляют по каплям раствор 10,7 г 1-(2-хлорфенил.этил)-4-пиаеридона в 30 мл абсолютного ТГФ, наблюдая повышение темпеоатуры до 45 С, нагревают 1 час при 55 С, наблю дая выделение белого осадка в прозрачном желтоватом растворе, отгоняют ТГФ в вакууме, добавляют к остатку 2О%-ный раствор хлористого аммония и эфир. Эфирный слой промывают один раз 20%-ным водным раствором хлористого аммония и два раза водой, сушат сульфатом натрия, упаривают досуха, растворяют остаток Б ацетоне, обрабатывают углем, перекристаллизовывают из смеси эфир-петролейный эфир и получают 1-(хлорфенилэтил )-4-окси-4- {3,4-метилендиоксифенил)-пиперидин, бесцветные кристаллы, т.пл. 105-106°С, с выходом .
Ф .... р м у л а и 3 о б р С т е н и я
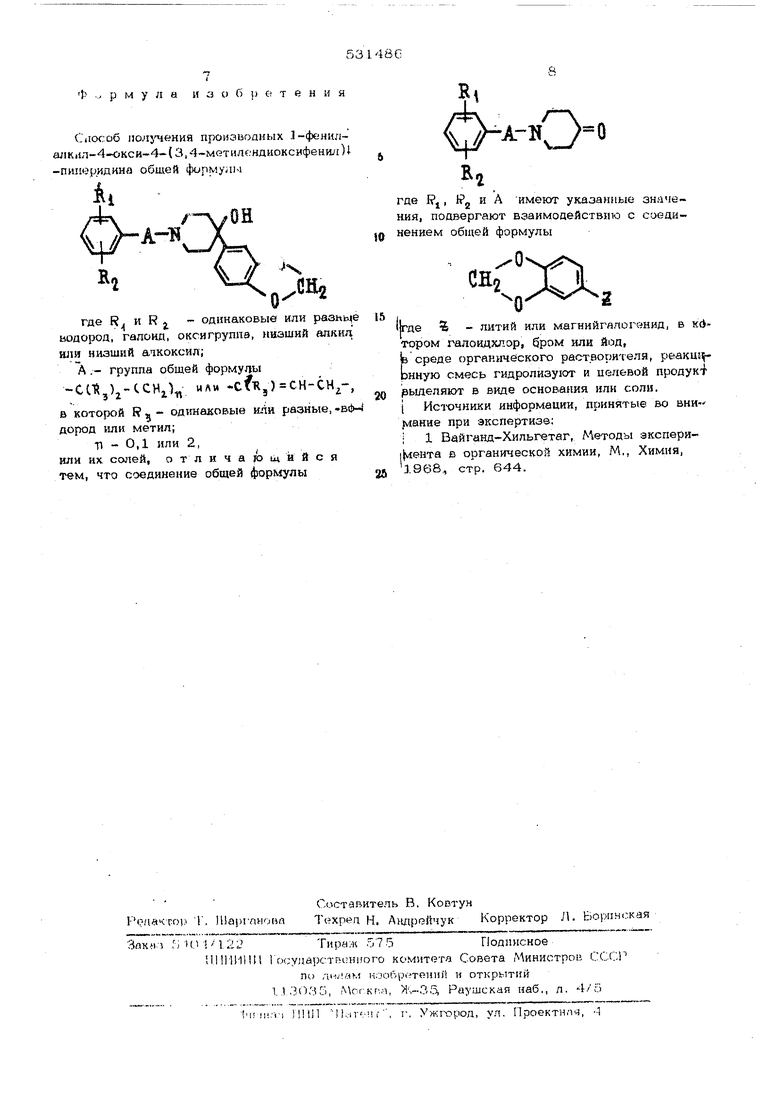
CiiOf.:D6 11ОЛ1чения П юиэводиых 1-фенилШ1кал-4-окси-4-{3,4-метилендиоксифенил)1 -пиперидина общей формулы
Jx CHj
где R и R
- одинаковые или разные водород, галоид, оксигруппа, ннэший алкил шш низший ачкоксил;
А.- группа общей фopмyJlы CU,)j-tCHiV -cfK5)CH-CH -, в которой R а - одинаковые или разные, -вфдород или метил;
Т1 - 0,1 или 2,
или их солей, отличак 1цИЙся тем, что соединение общей
где PJ , и А имеют указаняьге значе ния, подвергают взаимодействию с соеди}0 неннем общей формулы
СН2
XQX-- - 2
(где % - литий или магнийгялогенид, в кйтором галоид хлор, бром или йод, fe среде оргакического растворителя, реакш) рнную смесь гидролизуют и игааевой продук рыделяют в виде основания или сопн. t Источники информации, пг)инятые во вни jviaHHe при экспертизе;
1 Вайганд-Хильгетаг, Методы эксперив органической химии, М,, Химия,
iJvieHTa 1968, стр. 644.



Авторы
Даты
1976-10-05—Публикация
1974-09-25—Подача