(54) СПОСОБ ПОЛУЧЕНИЯ ВИНИЛОВУХ ПРОИЗВОДНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
гетероциклического соединения определяют методом газожидкостной хроматографии; целевые виниловые производные выделяют методом препаративной газовой хроматографии.
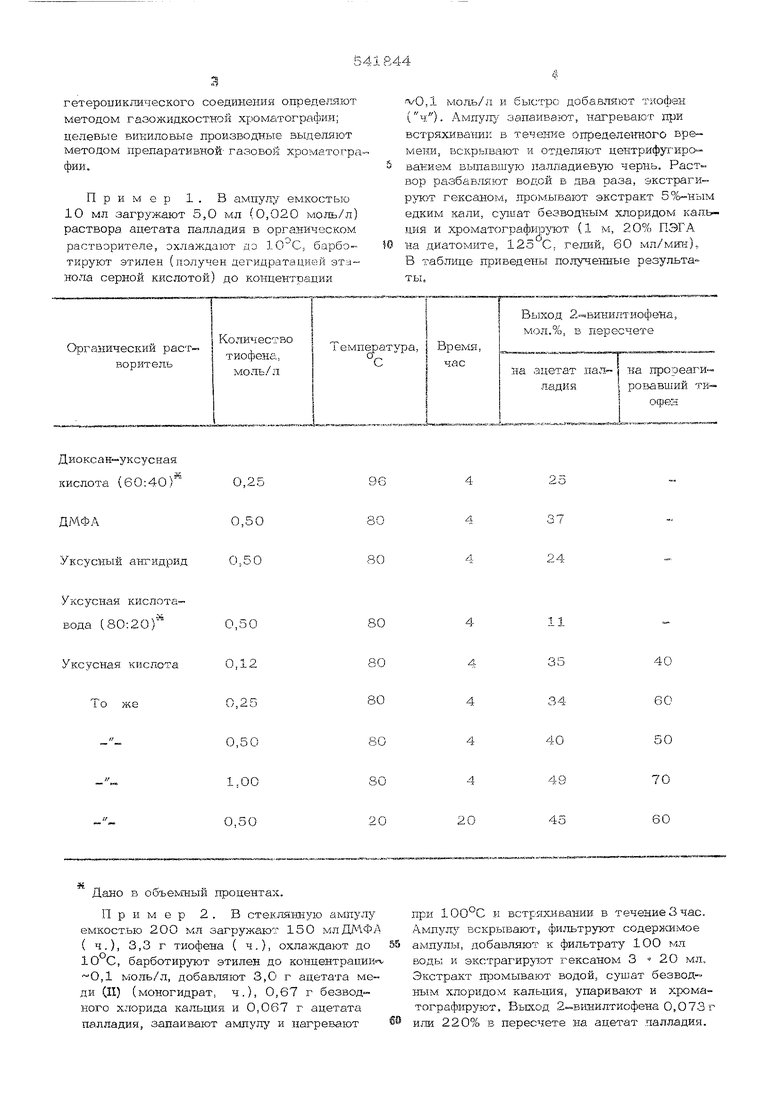
Пример 1. В ампул;; емкостью 10 мл загружают 5,0 мл (0,020 моль/л) раствора ацетата палладия в органическом растворителе, охлаждают ДЭ , барботируют этилен (получен дегидратацией этанола серной кислотой) до концентрации Количество Температура Органический расттиофена, воритель МОль/л
Диоксан-уксусная кислота (60:40)
ДМФА0,50
Уксусный ангидридО ЬО
Уксусная кислотавода (80:20)
V
0,12
ксусная кислота
О о с
i о же
, ui t
0,50
1.00
0.50
vO, мояь/л и быстро добавляют тхюфен (ч). Ампулу запаивают, нагревают щ.)И встряхиваник в течение определенного времени, вскрывают и отдепяют центрифугиро-
ванием выпавшую иалладиев то чернь. Раствор разбав.юют водой в два раза, экстрагируют гексаном, промывают экстракт 5°ь-ным едким кали, сушат безводным хлоридом кальция и хроматограф1;тутот (1 м, 20% ПЭГ А
на диатомите, 123 С, геШШ, 60 мл/мигн), В таблипе приведены полученные результаты.
80
24 80
11
4
40
4 60
34 50 40 49 7 О
60
45
20 2 винилтиофена, мол.%, в пересчете а ацетат пал- на прореагиладия ровавший ти- I офен

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,2 -дифурила и 2,3 -дифурила | 1974 |
|
SU482084A1 |
| 13-Е-(2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОПИРИМИДИН-5-ИЛ) ЭВДЕСМАНОЛИДЫ, ОБЛАДАЮЩИЕ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ | 2013 |
|
RU2536870C1 |
| (3aR,4aS,8aR,9aR,E)-3-АРИЛИДЕН-8a-МЕТИЛ-5-МЕТИЛЕН-ДЕКАГИДРОНАФТО[2,3-b]ФУРАН-2(3Н)-ОНЫ, ОБЛАДАЮЩИЕ ПРОТИВОЯЗВЕННОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2413724C1 |
| Способ получения 2,2-диалкил-2Н-имидазол-1-оксидов | 1988 |
|
SU1770321A1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТИЛОВОГО ЭФИРА 5-АЦЕТИЛПИРРОЛ-2-КАРБОНОВОЙ КИСЛОТЫ | 2008 |
|
RU2404162C2 |
| 2,2-Диалкил-2Н-имидазол-1-оксиды как промежуточные соединения для получения стабильных радикалов имидазолина и способ их получения | 1988 |
|
SU1770322A1 |
| Способ получения кремнийорганических соединений | 1978 |
|
SU765272A1 |
| Метил-2-О-бензоил-3-фтор-3-дезокси-Д-рибофуранозиды в качестве промежуточных продуктов в синтезе биологически активных 3 @ -фтор-3 @ -дезоксирибонуклеозидов | 1987 |
|
SU1521738A1 |
| 6-N-Бензоил-9-(2 @ -0-ацетил-3- @ дезокси-3 @ -хлор- @ - @ -ксилофуранозил)аденин в качестве промежуточного соединения в синтезе динатриевой соли аденилил-(2 @ -5 @ )аденилил(2 @ -5 @ )-9-(2 @ ,3 @ -ангидро- @ - @ -рибофуранозил)аденина, обладающей фиторостостимулирующей активностью | 1988 |
|
SU1573833A1 |
| 1-О-Ацетил-2,5-ди-О-бензоил-3-фтор-3-дезокси-Д-рибофураноза в качестве промежуточного продукта в синтезе биологически активных 3 @ -фтор-3 @ -дезоксирибонуклеозидов | 1987 |
|
SU1507764A1 |

«
Дано в объемный процентах.
Пример 2 . В стекля:нную ампулу емкостью 2СО мл загружают 150 млДД ФД ( ч.), 3,3 г тиофена ( ч.), охлаждают до 10°С, барботируют этилен до концентрации О,1 моль/л, добавляют 3,0 г ацетата меди (И) (моногидрат, ч,), 0,67 г безводного хлорида кальция и 0,067 г ацетата палладия, запаивают ампулу и нагревают
при 100°С и встряхивании в течеыиеЗчас. Ампулу вскрывают, фильтруют содержимое ампулы, добавляют к фильтрату 1ОО мл водь; и экстрагирутот гексаном 3 «20 мл. Экстракт зтромывают водой, сушат безводным хлоридом кальция, упаривают и хроматографируют. Выход 2«.винилтиофена 0,073г или 220% в пересчете на ацетат палладия.
ИК- и УФ-спектры продукта соответствуют литературным данным.
Пример 3. Проводят реакцию, как в примере 1, при 80°С в течение 2 час используя 0,27 моль/п свежеперегнанного фурана, полученного декарбоксилированием пирослизевой кислоты. При проведении реакции в ДМФА или уксусной кислоте выход 2-винилфурана в пересчете на ацетат naj ладия и прореагировавший фуран составляет 42 и 70 или 32 и 50 моп,% соответственно.
Пример 4. Проводят опыт, как в примере 2, используя 3,1 г свежеперег- нанного фурана и 3,0 г активированного угля. Выход 2-винилфурана 0,14 г или 510% в пересчете на ацетат палладия.
ИК- и УФ-спектрь продукта соответст- BJTOT литературным данным.
Пример 5. В ампулу емкостью 2ОО мл загружают 0,70 г ацетата палладия и 100 мл уксусной кислоты ( хн. } при 10°С барботируют 1 л этилена, добавляют 15,0 мл свежеперегнанного фурфурола, запаивают ампулу и нагревают 4 час при 100°С и встряхива,. Ампулу вскрывают, содержимое фильтруют, отгоняют в вакууме растворит е.ль и хроматографируют (1 м, 25% S Е-30 на хромосорбе В, 90°С, гелий, 90 мл/мин). Выход 2-винил-5-формилфурана 0,084 г или 22% в пересчете на ацетат палладия.
ИК-спектр (.четыреххлористый углерод), см 929с.,, 989 с., 1030 с,, 1160 ср., 1205 с., 1269 ср., 1291 ср., 1399 с., 1411 с., 15iil с., 1582 ср., 1708 с. УФ-спектр (изооктан), А С )j нм; 299 (1790О), 310 (146ОО).
Формула изобретения
1, Способ пол5 ения виниловых производных гетероциклических соединений общей формулы I
К .
где R - водород ИЛ1 альдегидная группа; X - кислород или сера, из гетероциклических соединений, например фуранового ряда, в среде органического растворителя, отличающийся тем, что, с целью упрощения процесса и повышения выхода целевого продукта, гетероциклическое соединение общей формулы II
I
R
где R и X имеют выше казанные значения, подвергают взаимодействию с этиленом в присутствии соли палладия (П)2Q 2, Способ по п, 1, отличающийся тем, что процесс проводят в присутствии соли палладия (II) концентрации 0,0001-0,1 мэль/л ,
36
о
I а ю
щ и и с я
тем, что гфоцесс проводят при 20-100°С.
Источник информации. прш1ятый во вни40мание при экспертизе:
46 3531.
Авторы
Даты
1977-01-05—Публикация
1975-10-22—Подача