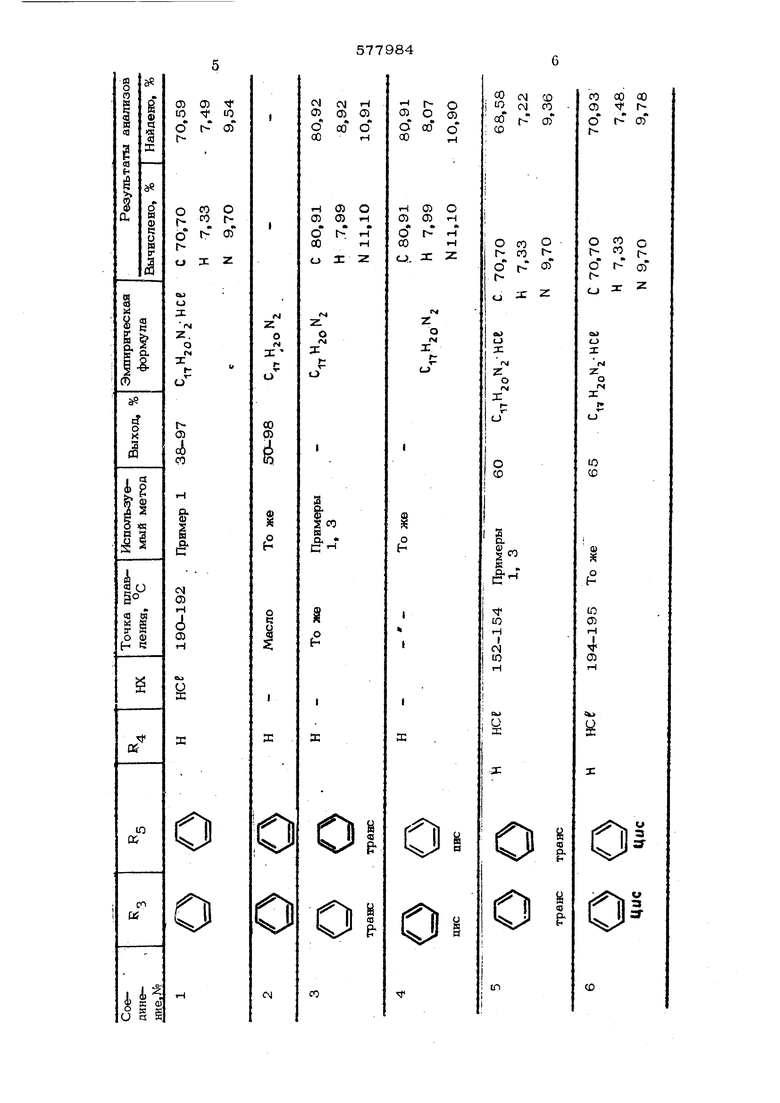
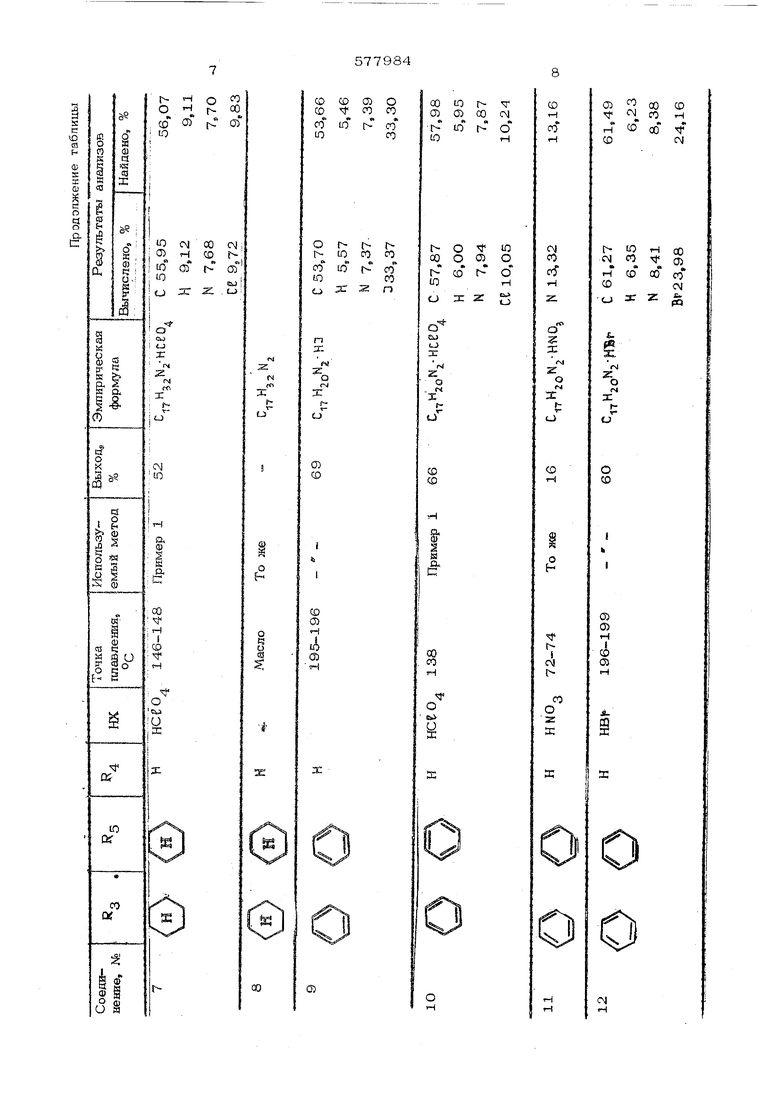
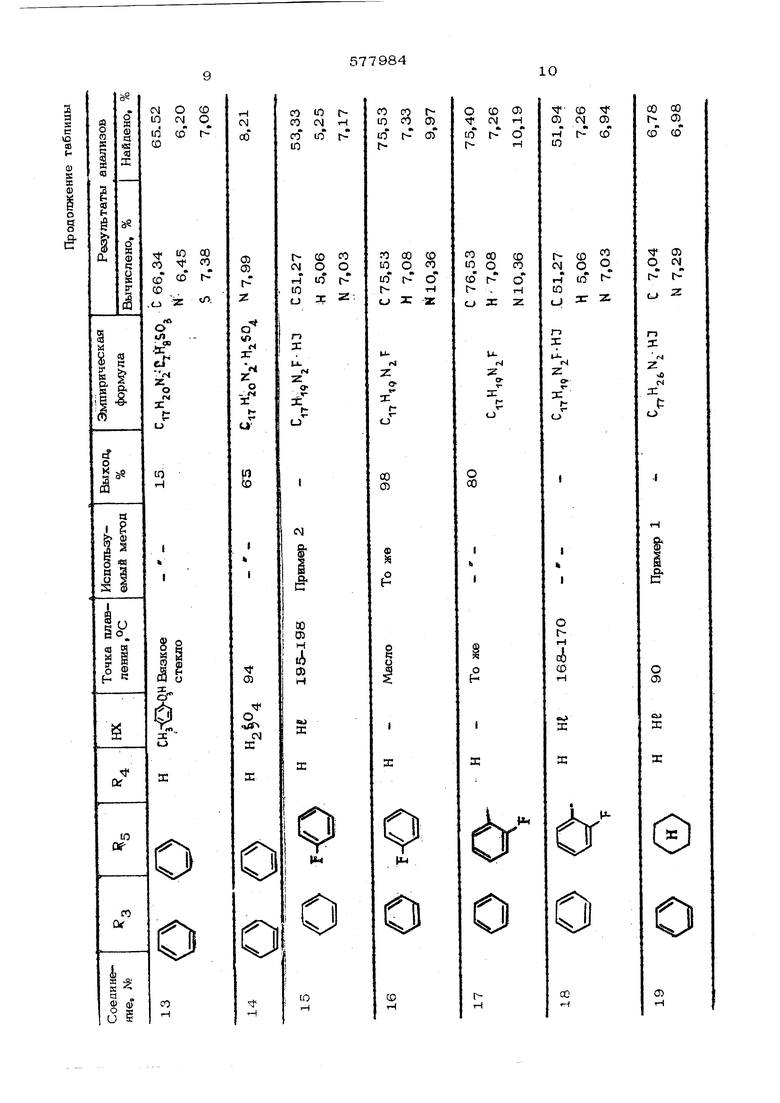
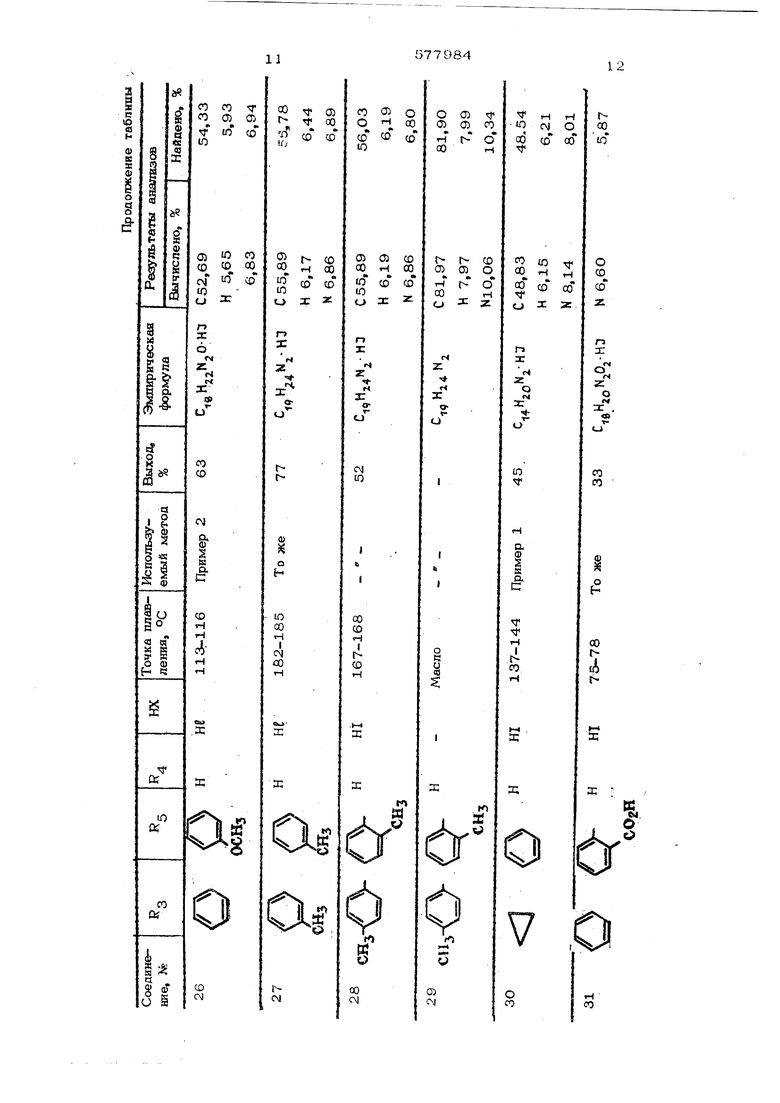
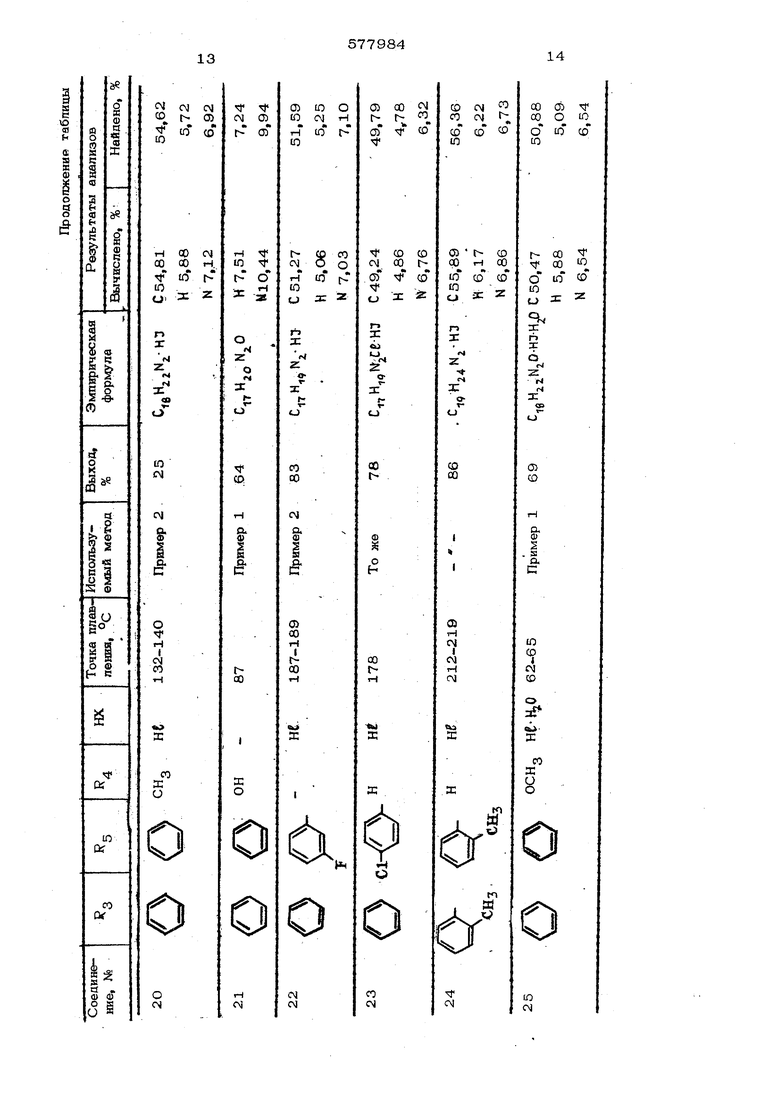
Rj-C IjT-Bg R4-C-C-BS (b) RO 4 e имеют укаэаныые (хачения; А ® - ион, восстанавпивают с помощью боргищэида ватрия в наопропанопе при 2O-SO°C я выдепшот целевой продукт в свободном виде или в виде солей с неорганическими кислотами. Пример 1. Получение 1,2-диметш1-3,&-дифенвлшфаа(;лидина. 19, г (0,5 моль) борпшрида натрия пороками добавляют к 1 л раствора 1,2 двмети -3,5 днфенилшфазолинметвпсульфата в 4О г (0,25 мота) изопропанопа. Реакция протекаетпри комнатной тек nepatype в течение 3 дней, затем добавляют дополнительно 9 г (0,25 моль) баргнаркаа натрия н нагревают оо темп атуры кипения с перемеипшахшем, ТакЕю услсюия подд жнвают в течение 7 ч, РеакЕшонаую смесь охлаждают до комнатной температуры и через каждые 1,5 ч добавляют lOO мл воды. После перемевшванья в течешсе 2 ч изопропанод извлекают на вращающемся испарителе и получающуюся в результате мозсу, разбавпенцую водой, извлекают с помощью диэтилового эфира. При испарении эфирного слоя получают 48,3 г (72% от теоретического) пиразолишсна в виде вязкого маслообразного вещества. Найдено, %: С 7О,59{ Н 7,49j N9,44 2 . Шдчислено, %: С 7О,7О{ Н 7t73| N 9,7О Ряд соединений, указанных в таблице, получают методом, аналогичным описанному в примере 1, из соли четвертичного основания пиразолина и боргидркда натрия. Пример 2. Получение 1,2-диметил- 3,1- (метафтор фенил) - 5-феннлпиразо лиди лгидройодида. 76 г (0,02 моль) боргидрида натрия добавляют к 4 г (0,01 моль) 1,2-диметил-З-(метафторфешш)-5-фенилпнразолилйодида в 125 мл изопропанола. После того как реакционная смесь станет однородной, перемешивание продолжают в течение 24 ч. Затем очень медленно добавляют 1О мл воды. Изопропанол извлекают на вращающемся испарителе и получающийся в результате остаток разбавляют в 50 мл воды и извлекают с по мощью хлороформа. При испарении органического слоя получают маслообразную жидкость, которую разбавляют водой. Затем добавляют 5 мл (46-50%-ного ) водного раствора йодистоводородной кислоты. После перемещивания в течение 1 ч получающееся в результате -геердое вещество отфильтровывают, сущат и Получают 3,3 г (83% от теоретического); т. пл. 187-189°С. Найдено, %: С 51,59; Н 5,25; N7,10. Вычислено, %: С 51,27;Н 5,О6; М7,ОЗ. Пиразолидиновые соединения формулы ( f-СНз «4 в 3 где нх - неорганическая кислота
Соедиие1ше 31 приготавливают модификацией метода из примера 1. Исходным пнразо линовым соединением является 3-(о-карбоксифенил)1,2-9иметил-5-фенилпиразолинйодид сложный метиловый эфир, который пос пе восстановления боргкдрида натрия в изопропаноле дает пиразопидин, но как смесь метилового и каогфопилового сложных эфиров с карбоксильной функцией. Эту смесь гидролизуют при (югревании вместе с 25%ным раствором гидроокиси натрия в метаноле, и продукт выделяют из смеси при обработке водным раствором йодистого водорода и получают пнразолидингидройодид.
Ф 0:ip мула изобретения
СК-, карбоалкокси-, карбоксамнцс: - или цианогруппа;
R . - водород, С io ® коксИ-. или алкилтиогруппа при условии, что, когда RX - водород или метил, по крайней мере, один из R, и R, не является фенилом,
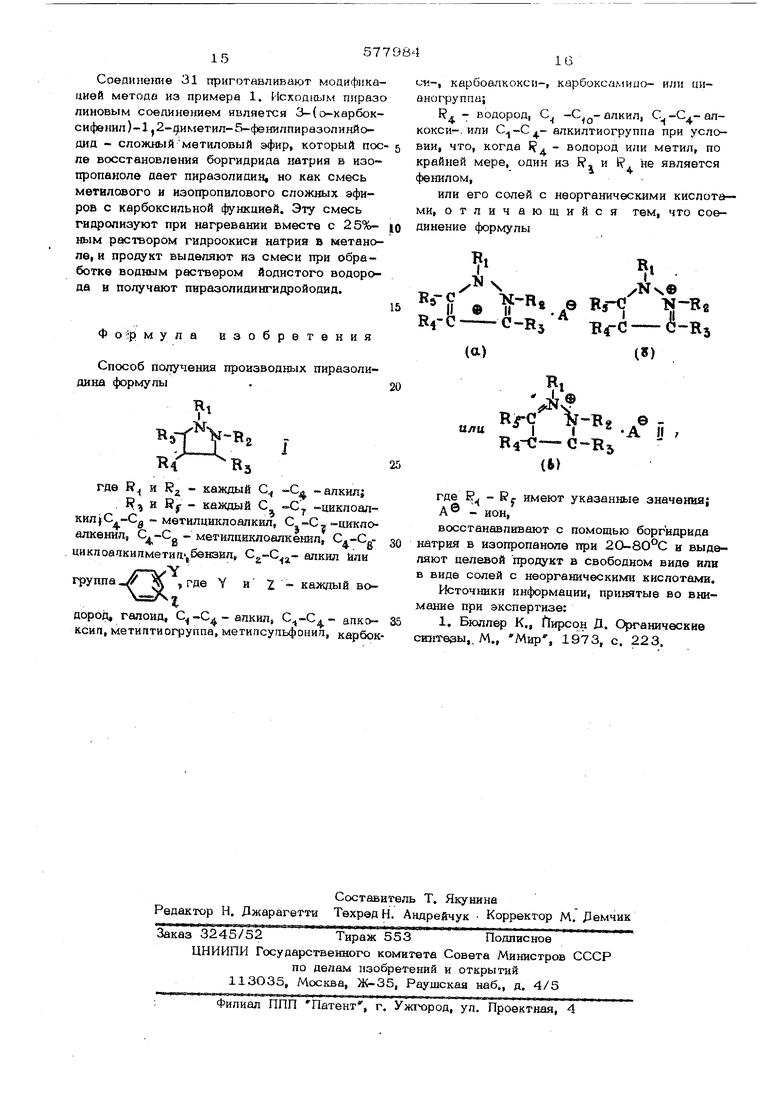
или его солей с неорганическими кислотами, отлич ающкйся тем, что соединение формулы
/NN®
В5-0 IJ-Ra БгСС-Нз
(«)
(а)
Способ получения производных пиразолидина формулы
., ,
KI
R
5
где R и R - каждый С -С -алкил|
. R и RJ- - каждый С С -цикпоалкил С -Сд - мегилциклоалкил, С -С,аиклоалкенил, - метилциклоалкенил, Сд-С.циклоапкилметиа- бензил, ,- алкил или
группа. Л У и 2 - каждый воI
дород, галоид, С -С -алкил, апкоксип, метипти огруппа, метипсупьфонип, карбок
Д
Rrc К-В2
А ii
R4-C-C-BS
(fr)
где i - Rj. имеют указанные значения;
А® - ион,
восстанавливают с помощью боргидрида натрия в изопропаноле при 20-80°С и выделяют целевой продукт в свободном виде или в виде солей с неорганическими кислотами.
Источники информации, принятые во внимание при экспертизе:
1. Бюллер К., Лирсон Д. С анические сшгтезы,, М., Мир, 1973, с. 223.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1-алкил-1( -алкоксикарбонилэтил)1,2,3,4,6,7,12,12в-октагидроиндоло (2,3-а) хинолизина или его солей | 1976 |
|
SU619107A3 |
| Способ получения гидразидов индазол-3-карбоновой кислоты или их солей | 1974 |
|
SU703019A3 |
| Способ получения (1,2)-анеллированных 1,4-бензодиазепинов или их оптических изомеров или кислотно-аддитивных солей | 1982 |
|
SU1331431A3 |
| Способ получения замещенных пиразолов | 1974 |
|
SU577985A3 |
| Способ получения аминоспиртов или их солей | 1970 |
|
SU578860A3 |
| Способ получения производных нафтиридина или их стереоизомеров или их солей | 1977 |
|
SU655314A3 |
| Способ получения производных карбоксамида оксобензотиазин-1,1-диоксида | 1975 |
|
SU664563A3 |
| Способ получения простых пиридин-2-эфиров или пиридин-2-тиоэфиров, или их кислотно-аддитивных солей, или пиридин-N-оксидов (его варианты) | 1984 |
|
SU1417796A3 |
| Способ получения тиено-/2,3-с/-или /3,2-с/пиридинов или их солей | 1977 |
|
SU668605A3 |
| Способ получения замещенных ненасыщенных алифатических эфиров | 1972 |
|
SU500751A3 |


Авторы
Даты
1977-10-25—Публикация
1975-11-21—Подача