Изобретение относится к инсектицидным средствам, содержащим в качестве активного компонента фосфорилированиые замещенные сукцинимиды. Известно средство, действующим началом которого является 0,0-диалкил -S - 12 - галоид-1 - (К - сукцинимид) эти |-тиoфocфaт l , но оно недостаточно активно в качестве инсектицида. Известно также средство, действующим началом которого является оксимидтиофосфата-0,0-дизтилянтарной кислоты 2j. Это средство также облагает инсектицидньол, действием. Целью изобретения является инсектицидное средство на основе соединений данного тийа, отличающееся более высокой инсектицидной активностью по сравнению с известным. Это может быть достигнуто введением заместителя в jкoльцq соединения, входящего в средс в6 2. Предлагают инсектицидное средство, содержащее в качестве активно действу щего вещества фосфорилированный сукцинимид общей формулы /р-о-эс где X - сера или кислород низший алкил низший алкоксил, низший ёшкил или арил; алкил, циклоалкил, алке.нил, циклоалкенил, арил, бензил; U R - одинаковые или различные и означают водород, низший алкил, фенил или R о R вместе - многочленное углеводородное к.ольцо. Активно-действующее вещество находится в средстве в количестве от 0,1 дс, 95 вес.%, ост сильное добавки; наполнитель, растворитель, диспергатор в зависимости от формы применения средства. Предлагаемые соединения получают взаимодействием фосфорилирующих средств общей формулы Р и HOI гдеР., R uX имеют приведенные значения, а НаЕ- атом галоида (хлор, бром), с замещенными оксимидалш янтарной кислоты общей -структурной формулы н4 V глей, R , . имеют приведенн значения, в виде их солеР щелочных металлов или же в присутствии со св зующими кислоту средствами. Замещенные оксимидн янтарной кислоты или их натриевые соли получают взаимодействием замещенных сложных диэфиров янтарной кислоты с гидроксиламином в чистом виде или/ в соответствующем случае, с помощью с ответствующих агентов, например мет лата натрия, согласно схеме SY «-HjlfCfH +11оОСЯз -гнон -CHjOH R R, R , R u R имеют приведенны значения, Я - низший алкил. Путем добавления кислоты к солям натрия можно выделить замещенные ок симиды янтарной кислоты. Для их получения можноисходить также из соо ветствующим образом замещенных анги ридов янтарной кислоты. Необходимые для синтеза замещенны оксимидов янтарной кислоты замещенн сложные диэфиры янтарной кислоты ил ангидриды янтарной кислоты и янтарн кислоты описаны в литературе. Действующие начала , предпочтитель получают в присутствии кислотных ак цепторов. В качестве последних применимы в первую очередь карбонаты, алкоголяты, гидроокиси щелочных металлов или органические основания, например пиридин или триалкиламины. Можно также подвергать взаимодейств соли щелочных металлов приведенных замещенных оксимидов янтарной кисло ты с приведенными галогенангидридам фосфорной кислоты. 5fy реакцию, пре пс1Тительно, проводят в инертном ор ганическом растворителе при темпера туре от О до , предпочтительно 30-130 С. В качес±ве растворителей пригодны, в частности, кетоиы, бензол, толуол, ксилолы,диоксан, нитрилы, как ацетронитрил или пропионитрил, затем диметилформамид, ди -етилсульфоксид или сложные эфиры органических кислот Требующиеся в качестве исходных соединений компоненты фосфорилирования известны. Новые сложные эфиры фосфорной кислоты.- либо кристаллические вещества, либо масла окраски от бес.цветной до красноватой, трудно растворимые в во де и плохо поддающиеся перегонке даже при сильно пониженном давлении. Соединения ртличаются хорошим инсектицидным действием вследствие чего приведенные соединения целесообразны; для применения в качестве борьбы с вредителями, поражающими растения, П. р и м е р 1. Раствор гидроксйламина в СГЮН. 9 частей по весу гидроксиламингидрохлорида смешивают со 100 частями CHgOH. Размешивая, в атмосфере азота по каплям добавляют 180 частей по весу 30%-ного по весу технического раствора NoOCH,/CHj ОН при охлаждении извне. После этого еще 1ч. перемешивают при . Хлористый натрий отделяют. Натриевая соль оксимида 3,3-диметилянтарной кислоты. 174 части диметилов.ого сложного эфира 2,2-диметИлянтарной кислоты раствгряют в 100 частях CHjOH, затем размешивая, добавляют полученный выШ1еописанный раствор гидроксиламина, после чего по каплям в течение 0,5 ч добавляют 180 частей по весу 30%-аого , по весу раствора No OCHj/eH ОН ,1ч нагревают с обратным холодильником, дефлегматор заменяют короткой колонной и холодильником нисходящего типа, метанол отгоняют, заменяя отгоняемое количество добавлением по каплям ксилола. Вскоре начинает выпадать студнеобразная соль. Внутреннюю температуру повышают до , при этом отгоняется чистый ксилол. Взвесь натриевой соли можно применять затем для фосфолирования или же соль отделяют. Образуется 165 частей по весу (100% от теории) натриевой, соли оксимида 3,3-диметилянтар;1ой кислоты.. Оксимидотионофосфат 0,0-диэтилг-О(3,3-диметилянтарной кислоты. Полученную взвесь 165 чаотей по весу натриевой соли оксимида 3,3диметилянтарной кислоты в ксилоле нагревают до , затем по каплям добавляют, тщательно размешивая, 188 частей по весу длэтокситиофосфррилхлорида, 4 ч размешивают при этой
температуре, дают охладиться/ отсасы вают выделившийся хлористый натрий, ксилольный раствор сложного эфира фосфорной кислоты промывают 10%-ным по весу раствором бикарбоната натрия (200 чартей по весу)/ затем водой (200 частей по весу) , высушивают над сульфатом натрия, растворитель отгоняют.
Образуется масло бледно-желтого цвета.
Выход 245 частей по весу (83 % от теории).
Вычислено, %: С 40,7; Н 6,1; М 4,7; Р 10,5,- S 10,8.
Найдено,%: С 41,0; Н 6,7;К4,3; Р 10,2; S 10,6. Пд 1,48.
пГ
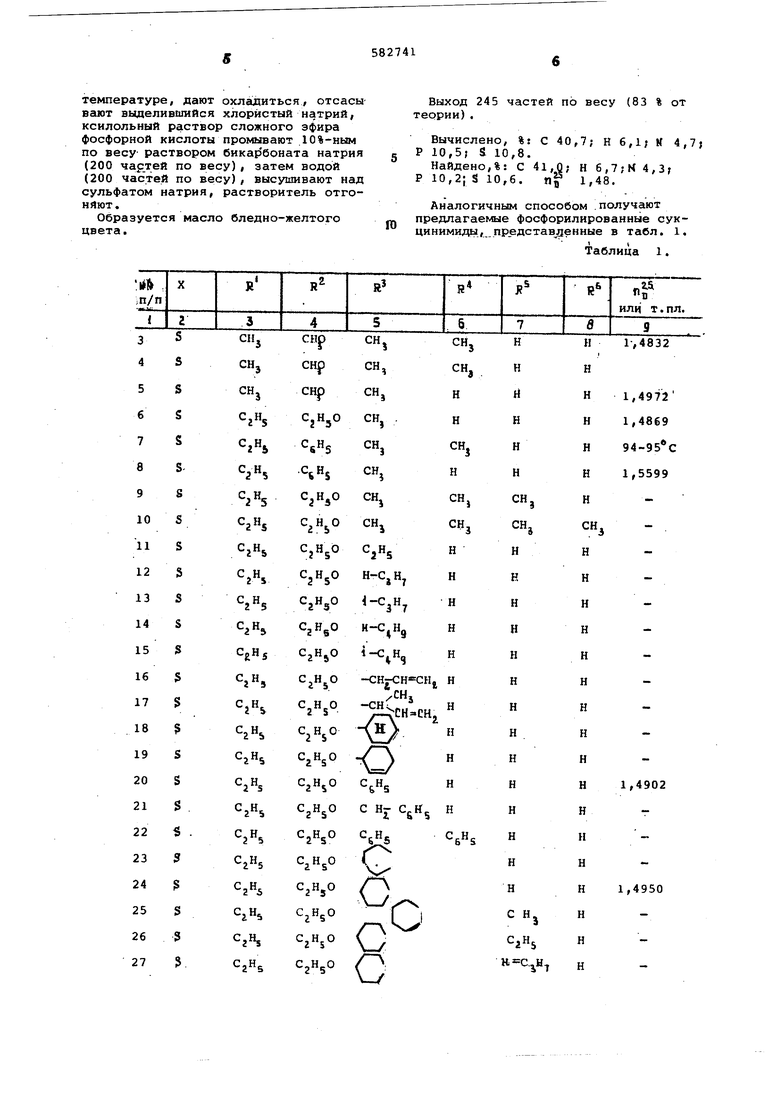
Аналогичным способом .получают предлагаемые фосфорилированные сукцинимиды.,.пр едстав ениые в табл. 1.
Таблица 1.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных простых арилфениловых эфиров или их кислотно-аддитивных солей,или их металлических комплексов | 1982 |
|
SU1148564A3 |
| Инсектицидное средство | 1975 |
|
SU619086A3 |
| Средство борьбы с насекомыми и клещами | 1972 |
|
SU680613A3 |
| Способ борьбы с насекомыми | 1973 |
|
SU668563A3 |
| Средство для борьбы с насекомыми и клещами | 1973 |
|
SU673141A3 |
| Инсектицидное средство | 1977 |
|
SU841570A3 |
| Инсектицидное средство | 1977 |
|
SU650479A3 |
| Инсекто-акарицидное средство | 1976 |
|
SU849977A3 |
| Инсектоакарицидное средство | 1975 |
|
SU615833A3 |
| Способ получения 2,6-диаминопиридинового азокрасителя | 1973 |
|
SU521848A3 |

S
снр
CH.
S снр
CH,
S 5 S S S S S 3 S S S S S снр
CH,
CjHj
S«s
C2«5
C. S«5 b°
sv
CzHj
CjHjO
л
S«5
Сг«5° C,H,
CjHjO
CjH,
i«v
S«5°
S S
CjHj
CjH.O CjH,
$
C,H,
S
C.HjO C,H,
3
Ca«sO
C.HS
A
S 3 3
CjH
C2«S°
CjHs
CjHs
l-,4832
H H
H
CH,
I
H
CHj
rt
1,4972
H
H 1,4869
H H H CH,
H
H 94-95 C
CH,
H 1,5599
H
H
H
CH,
снз
CHj
CH,
«5 H
H
H H H -C,H,
H H H H H H H H H H H H H
H
H
H H
H
-c,H,
H
H
CH;-CH CHj H /CHj
H
CH-CHj. H
H
H
H H
1,4902
H
H- c.rt
H
H
H
H
r
1,4950
H
с H.
H
CaHs
H
,H,
H
Продолжение таблицы
Пример 3. Действие против ilOt (kphie {oboe).
Посаженные в вегетационные сосуды растения бобов с большими колониями
Действующее начало
Концентрация действующего
5 б 3
1 20
1 I
Пример 4. Действие против долгоносика амбарного (SitophiCu еаnafHuf).
Вредителей помещали на 4 ч на обра ботанные действующими началами стекТаблица 2.
тлей обрабатывали в камере для опрыс кивания водными дисперсиями действую,цих начал. Летальность определяли через 24 ч.
Результаты приведены в табл. 3.
Таблица 3.
Летальность, % начала, вес. %
98
95
100
80
80 80 30
лённые подставки (чашка Петри диаметром 10 см) .
Летальность определяли через сутки. Результаты приведены таОл. 4.
Таблица 4.
Количество действукнцего начала на чашку Петри,
ДеЯств)поцее начало
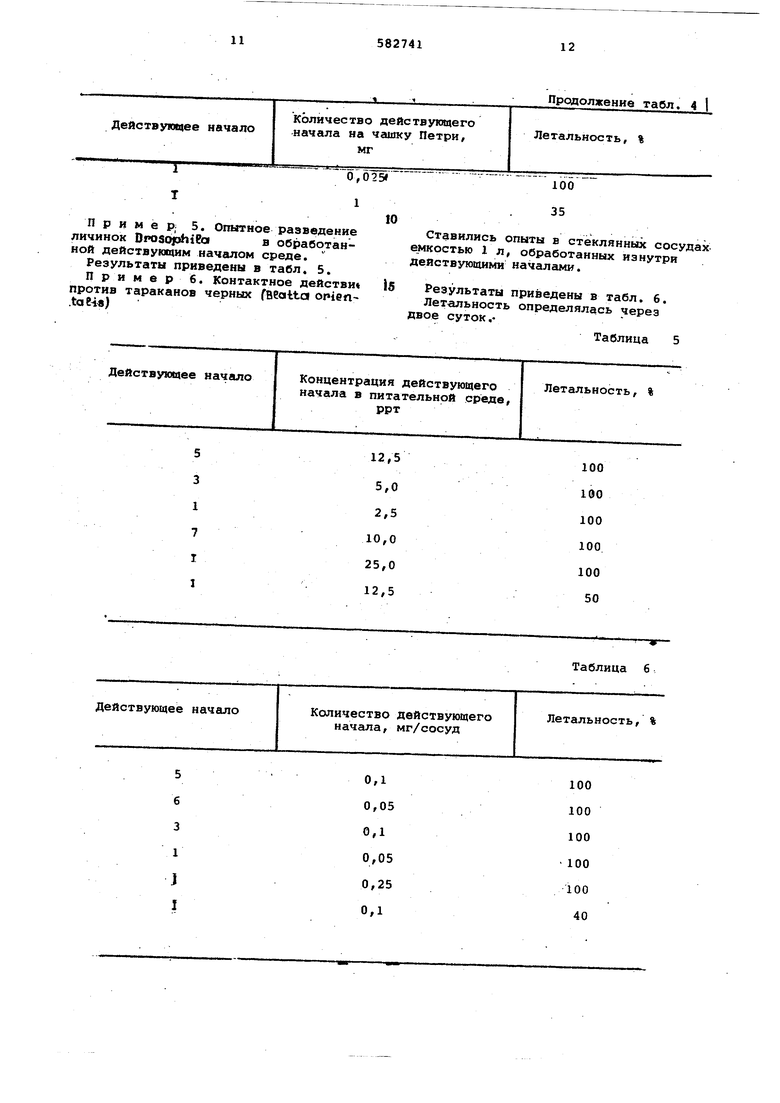
Пример; 5. Опытное разведение личинок OroscqahiCaв обработанной действующим началом среде.
Результаты приведены в табл. 5.
П р и м е р 6. Контактное действи против тараканов черных fBCattc onien.tae4«)
Концентрация действующего
Действующее начгшо начала в питательной среде, Количество Действующее начало
Прсэдолжение табл. 4 |
Летальность, %
0,025
100
Ставились опыты в стеклянных сосудах емкостью 1 л, обработанных изнутри де1Яствуюшими началами.
Результаты приведены в табл. 6. Лет-альность определялась через двое суток,Таблица 5
Летальность, % ррт
100 100 100 100 100 50
Таблица 6 начала, Летальность, % действующего мг/сосуд тти-тд - - - , 
Авторы
Даты
1977-11-30—Публикация
1974-12-03—Подача