(54)СПОСОБ ПОЛУЧЕНИЯ ДИУРЕТАНОВ




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диуретанов | 1976 |
|
SU691084A3 |
| Способ получения диуретанов | 1975 |
|
SU625602A3 |
| Способ получения диуретанов | 1975 |
|
SU592352A3 |
| Способ получения @ -арилсульфонил- @ -аргининамида или его солей | 1978 |
|
SU1181539A3 |
| Способ получения карбоксиалкенамидоцефалоспоринов, или их сложных эфиров, или их солей с щелочными металлами | 1984 |
|
SU1500163A3 |
| Способ получения фениловых сложных эфиров карбаминовой кислоты | 1979 |
|
SU1083906A3 |
| Способ получения производных 1,2,4-оксадиазола (его вариант) | 1979 |
|
SU969162A3 |
| Способ получения замещенных сложных эфиров карбаниловой кислоты | 1980 |
|
SU1048983A3 |
| Способ получения N -арилсульфонил-L-аргининамидов или их солей | 1979 |
|
SU938739A3 |
| МОНО- ИЛИ ДИАЦИЛФОСФИНОКСИДЫ | 1992 |
|
RU2057759C1 |

, I , .-.
Изобретение относится к HOBJM хими4еским соеДйненлем- k диуретанам общей формулы:Б R
t
О-СО-Н
Ш-СО-О-Вз
где аллил, нвзамегцённый или замещенный галогеном алкнл ,, ;
Rg незамещенный или замещенный галогеном алкил С| -С , или ал|синил С,-к; , циклогексил, ;фенйл } i фёнэтил, алкрксифенил , галоид. фенил или бензил;
- незг1мещенНЕЛ или зам эденный галогеном алкил Cj-С .. :
Диуретаны общей формулыТявляютс:Ч гербицидами избирательного действия , содержащими эти соединения в качестве действующего начала.
Предложенный способ основан на известной реакции получения уретанов, т,,ё.эфиров карбё1миновой кислоты, которые получают из| слд а1нгидрида кар баминовой кислоты и спирта 11. -,
Использование в качестве исходньос соединений карбама тов общей формулы карбамонлхлорида общей . Щ., позволяет подучить новые соедкненкя фбщей J , обладающие селективным гербициднам дейсвтием.
Диуретаны формулы j цолуча ют путем взаимодействия соедииения общей формулы п -
II
ТШ-бО-О R:
где из имеет вышеуказанное эн чеиив, йлн его соли щешочйого метгшла с карбамоилхлрридом общей формулы
R
Н-СО-С1 Ш
R.
где R и Rj, имеют выаеуказанные значения, в присутствии третичногЧ). органического основания, предпочтительно
триэтиламина или пиридина, при температуре 20-70С.
Пример 1. К- Пропил -N (К,Н -ди-&«по| -бутилкарбги« ОилоксиГфенил| -карбамат.
Натриевую соль, полученную из 19,5.г (0,1 моль) W-пропиловбго сложного эфира 3 оксикарбамильной клслоты и мети- лата натрия (из 2,3 г натрия) в абсолютном метаноле, суспендируют после основательного удаления метанола в вакууме в 100 мл сухого мeтилизoбyтиJ кетона. пербинешяванин закапывают раствор вз 1,1 г (0,1 моль) днбутилкарбсшоилхлорида в 50 мл метили- эббутилкетона причем температураповьюаётся приблизительно на , За.тем в течение 1 час дополнительно перемёишвают при 70°С. После охлаждения разбавляют приблизительно 200 мл уксус ного эфира и. при промывают разбавленньтнатровымЬвлоком и водой, сушат на сульфате магния и выпаривают при пониженном давлении.Выход 30,6 (87% от теории); п 1,4925
П р и м в- р 2. Изопропил -м -/3Я-этйл-К- (2-хлорэтил)-карбамоиллокси фенил -карбанат.
К суспензии 19,5 г (0,1 моль) изопропилового эфира З-оксикарбаниловоО кислоты в смеси с 10,1 г (0,1 моль) триэтиламина и 50 мл уксусного зфира при комнатной температуре и при пере мешивакми медленно прикапывают 17,0 г (0,1 моль) К-этил-М-(2-хлорэтил)карбамоилхлорида, растворенного .в 40 мл уксусного эфира. Затем Гродолжашт перемешивать приблизительно 1час
W при . После охлаждения до комнатной температуры реакционную смесь разбавляют 50 мп уксусного эфира, промывают разбавленной натриевой щелочью разбавленной соляной, кислотой и водой
IS высушивают над сульфатом магния и испаряют при пониженном да1влении. Выход 22/2 г (68% от теория); т.пл. 105- JP7 с.
SO Такие же реэулых ал ы можно получить, если вместо триэтилс1мина использовать в качестве третичного органического .рснозания пиридия.
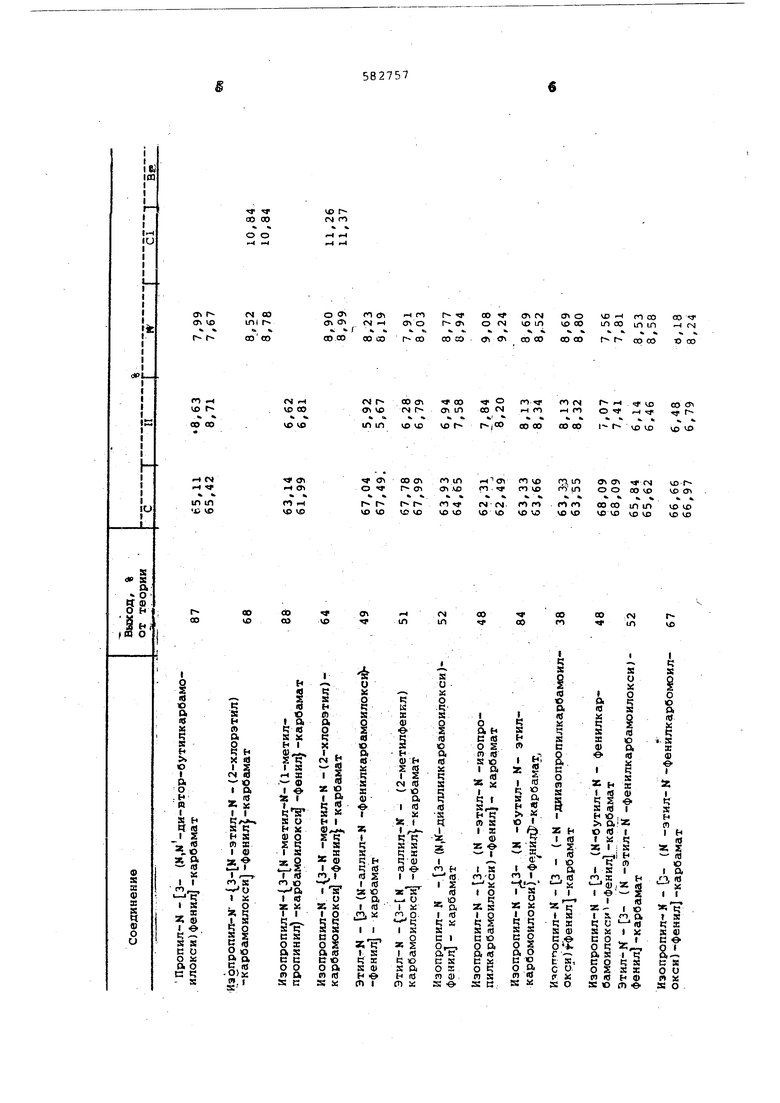
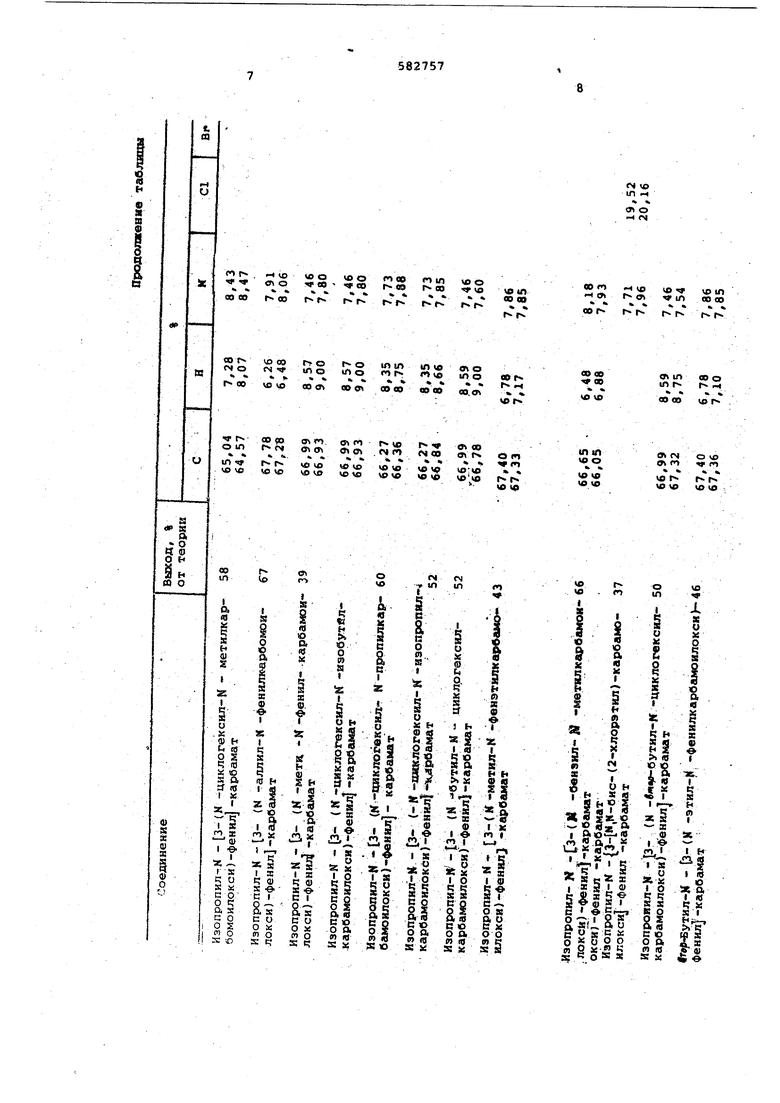
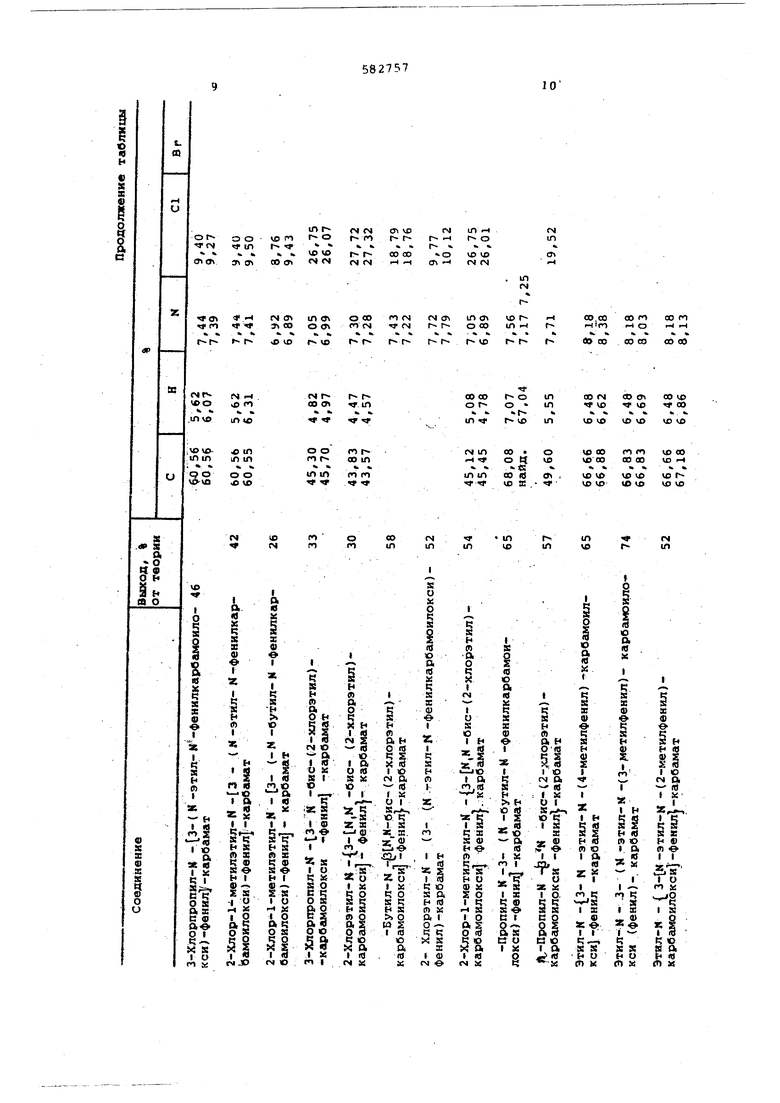
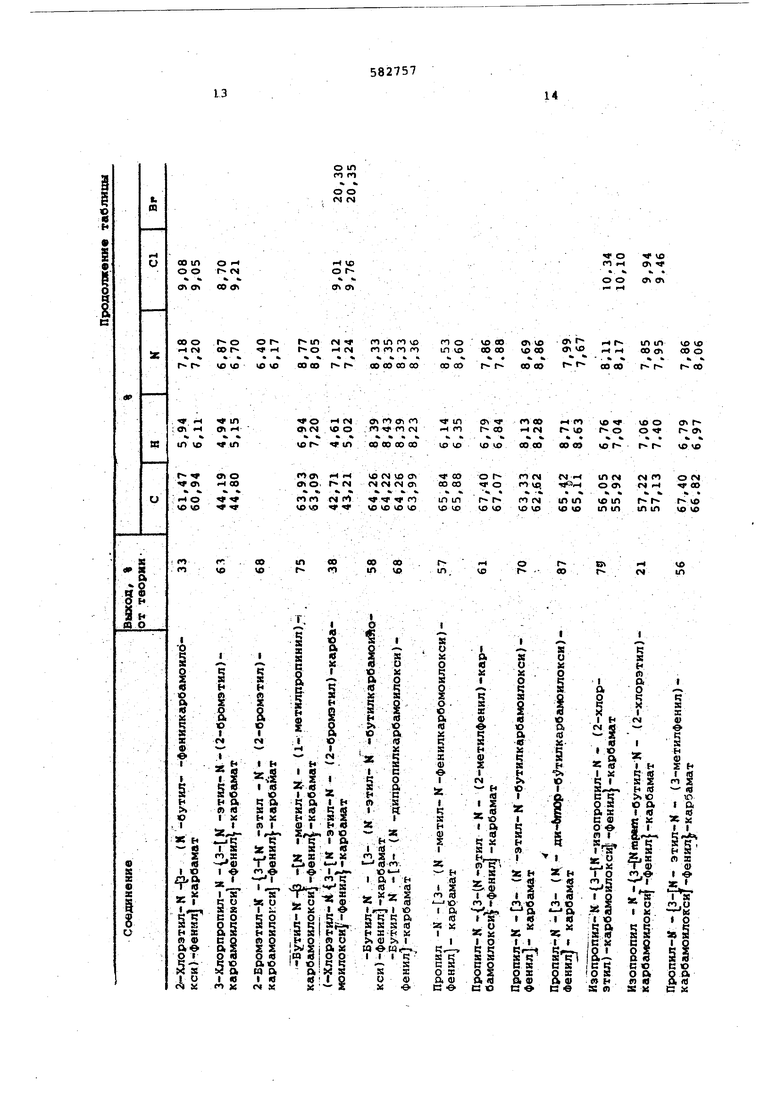
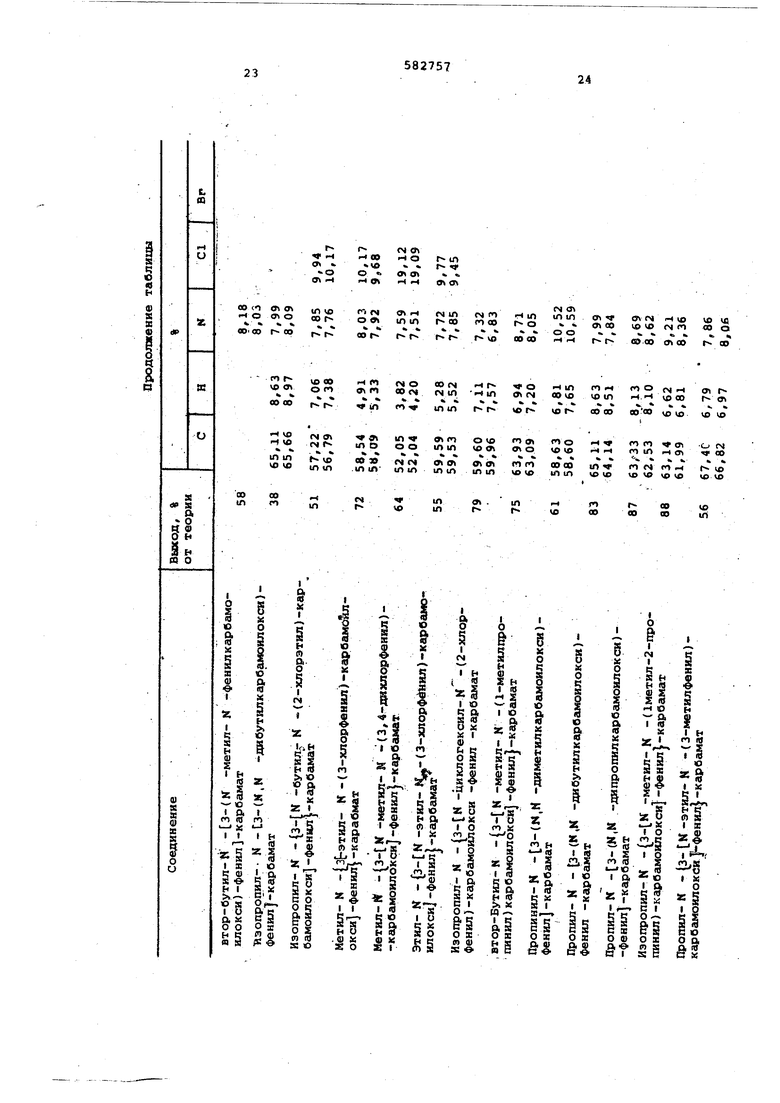
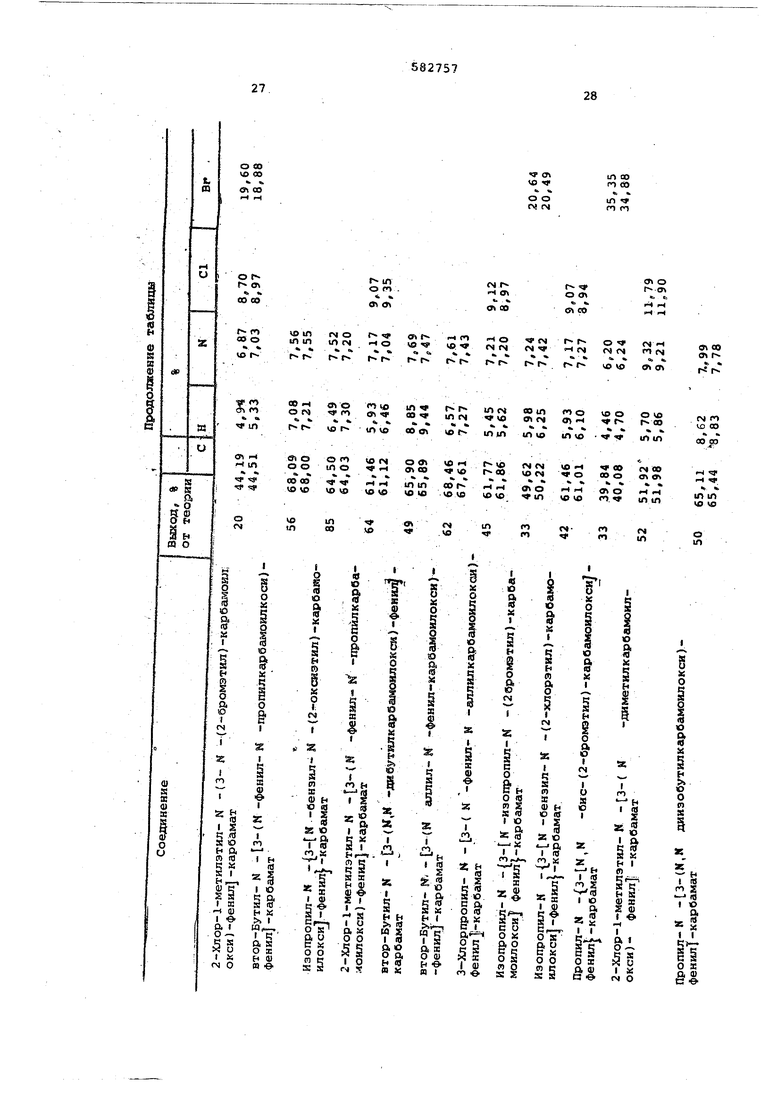
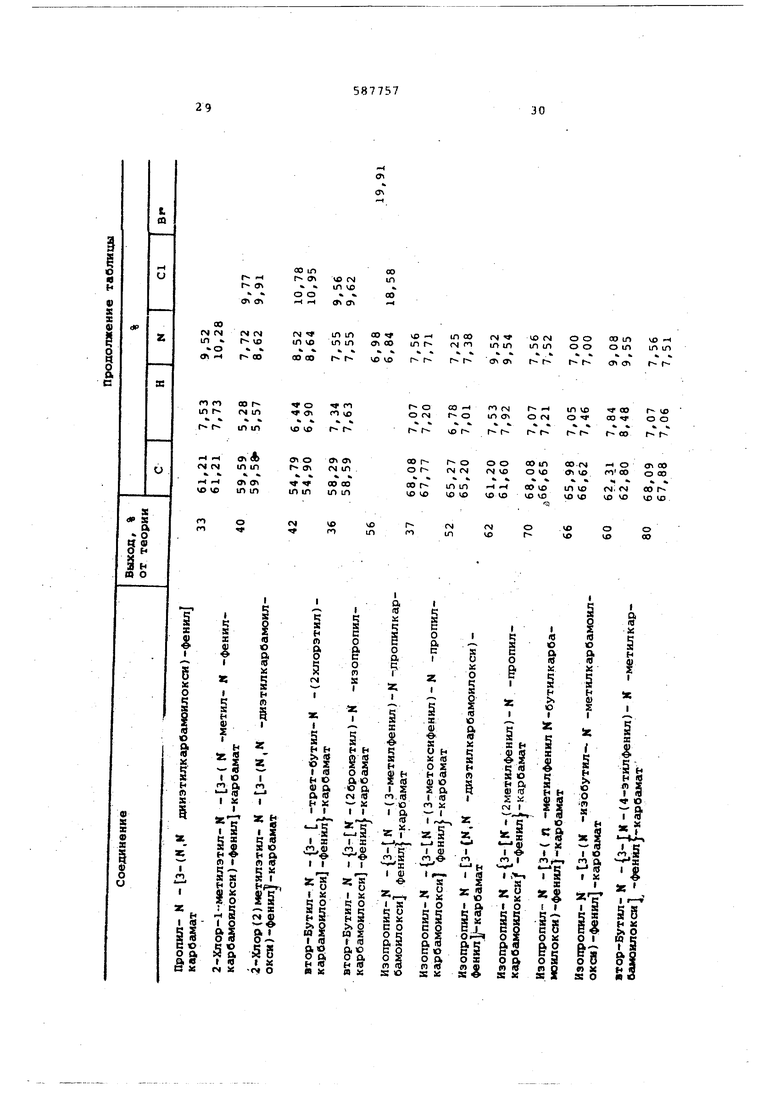
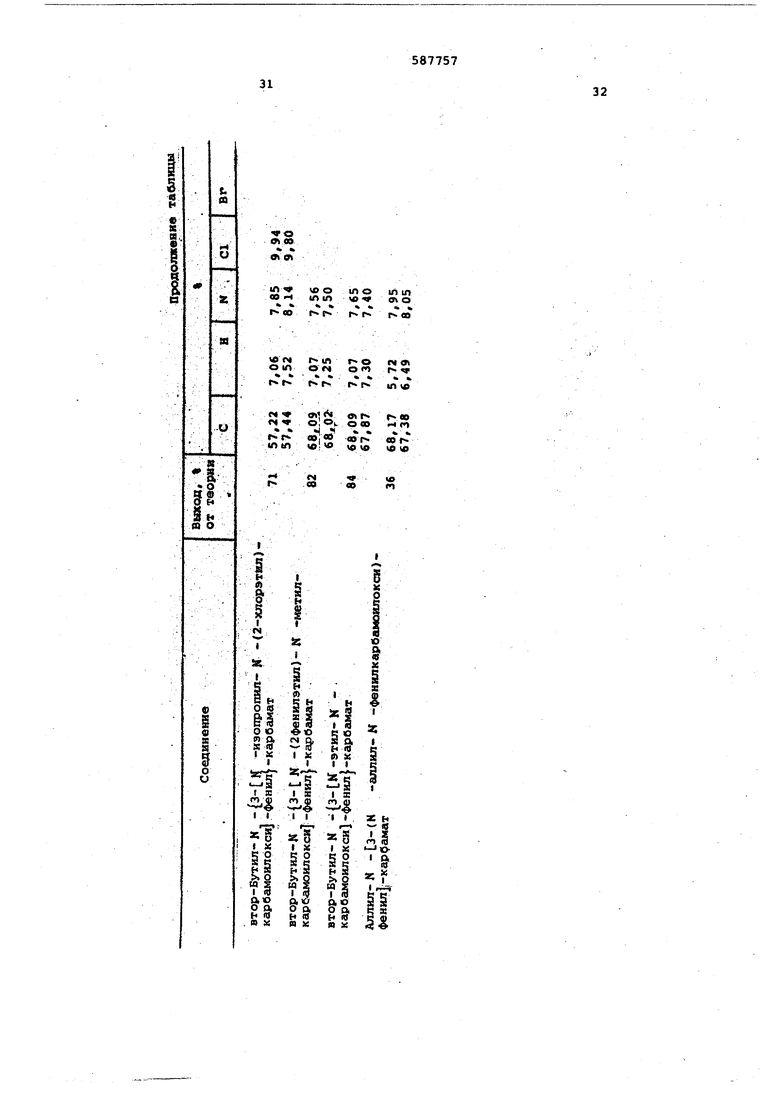
В таблице приведены выходы и данные элементарных анализов полученных соединений.
-н ю
ч
ф 1Л г в
V 1Л
00 Г Гг Г« . Г
ох tn
оо о in t
Г -4
оо оо VO 1
Л0 VO
ел (N
о о ох П
г («1
О f
Г 1
Ф «о «о VO
13
14
19
20
21
22
г
V -Н
ел «.
-о
а .4
Г in
1 Ч
«
в« at
оо о в л
1Л te
и о Г1 о 00 Г
СО ОО Г со
Г--
т т
VO 00 г-1 сч о л о ел м
ift ro intn Of «or OOOO COOO (DkO. VO VO
00 ОС
VO (M да
О
n in
- VO
VO VO
CD
CO
in
n
0)
s to
X
о и
РЧ Л
гч
( Г4гЧ (ОШ
ГЧ f Н 1Л
(Ч m
1Л Ш(Л го 00 г о
г 00
л 00
te V0Г4 (
1Л
о о-
W ъо
69-00да
оосо
н -«г г
гг- VO
««)-1 «) даг
во (М
-- г о Ч л VO 1Л -ч. - в 00 f да -11Л да (N 00ш (Ч Ш
e iO спда (ПО Н -о CM то ОО1П1Л «ода да о о«о
rr| Г4 r i-i r VO
00 «4 r« дада дада м го оооо . .
1Л
.tni/t tnininin inin «ОЮ tnm VOU VOVO
ro
oo eo
да .
rin
VO
in in r
00
Г00
in
VO i g
25
г со
О
ОЧ
Г4
«
г
г
S
26
tr
OS
N
0 «л
27
28
о со о f
%. rs ггч го
VD 00 00 |Р
Ж
ТЙ
го 2
- я) I в
.1
I I
29
30
31
32
33
Формула изобретения.
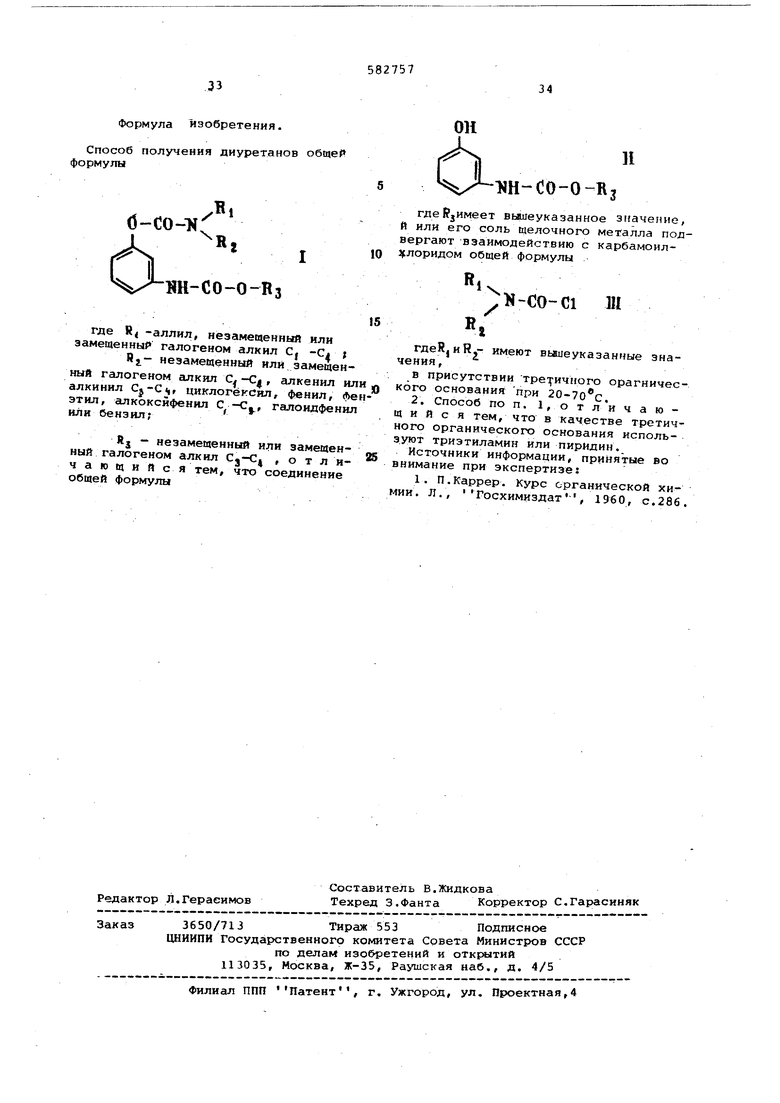
Способ получения диуретанов общей формулы б-со-т ЙН-СО-О-Нз где Rj -аллил, незамещенный илн замещенный галогеном алкил С| -С ; fij- незамещенный или замещенный галогеном алкил С. -С|, алкенил ил алкинил циклогёксил, фенил. Ле этил, алкоксйфенил С -Cj, галоидфенил или бензил; Йд незамешенный или замещенный галогеном алкил Cj-Cj , о т л ич а го щ и и с я тем, что соединение общей формулы
34
1
Ж-СО-0-Rj гдеЙ имеет вьшеуказаиное зг{ачение, И или его соль щелочного металла подвергают -взаимодействию с карбамоилхлоридом общей формулы J-co-ci ш гдеН|ИН,- имеют вьшеуказанные значения, в присутствии тре ичного орагнического основания при 20-70 с, 2. Способ по п. 1,отл ичающ и и с я тем, что в качестве третичного органического основания испольЗУют триэтиламин или пиридин. Источники информации, принятые во нимание при экспертизе: 1. П.Каррер. Курс органической хиии. Л., Госхимиздат, 1960, с.286,
Авторы
Даты
1977-11-30—Публикация
1976-01-07—Подача