Цель изобретения - расширение арсенала средств воздействия на живой организм.
Это достигается получением новых производных дигидро-4,1-бензоксазепинона: 2-фенацилйден-2,5-дигидро-4,1-бензоксазепионами-З формулы 1 и применением их в качестве вещест проявляющих противомикробную активность.
Способ получения 2-фенацилиден-2,5-дигидро-4,1-бензоксазепинов-З заключается в том, что соответствующую ароилпировиноградную кислоту-подвергают взаимодействию с о-аминобензиловым спиртом при кипячении в среде толуола в качестве рас творителя.
Схема реакции
СОСН„СОСООЯ+
It
.
,
/
CH-CQгде R имеет указанные значения.
Целевые продукты представляют собой желто-оранжевые кристаллические вещества, устойчивые при комнатной температуре, растворимые в спирте, толуоле, диоксане и других органических растворителях.
В ИК-спектре полученных соединений отсутствуют линии гидроксила и свободной аминогруппы, но присутствуют полосы 1735-1720 см , соответствующие валентным колебаниям сложноэфирного карбонила.
Доказательство неаминной. структуры 2-фенацилиден-2, 5-ДИГИДРО-4,1-бензоксазепинов-3 получают с помощью спектров ПМР, определенных, для растворов в ССе4 В спектре ПМР присутствует сигнал при 5,08 м.д., соответствующий двум протонам метиленовой группы. При 6,52 м.д. появл ется синглет,. соответствующий протону метиновой группы. В области 7,0-8,15 м.д, имеется мультиплет, соответствующий девяти протонам ароматических циклов, Сигнал при 13,1 м.д. обусловлен протоном гру пы NH.
В УФ-области длинноволновый максимум полученных соединений нахо датся около 380 им, что.близко к положению длинноволнового максимума в эфирах о х-ариламинобензоилакриловых кислот (377-380 нм), имеющих аналогичную хромофорную систему.
Пример 1. Получение 2-фенацилиден-2,5 дигидро-4,1-бензоксазепинона-3 .
Смесь 1,54 г (0,008 моль) бензо гшпировиноградной кислоты в 130 мл
fcyxoro толуола и 1 г (0,008 моль) о-аминобензилового спирта в 30 мл сухого толуола кипятят в течение 2 ч. После охлаждения реакционной массы выделяют 1,54 г (70%) кристаллического продукта ярко-желтого цвета с т.пл-. 153-154°С (из спирта) .
Найдено, %: С 73,28 Н 4,51; N 5,24.
С,, H.NO,,
Вычислено, %: С ,11 Н 4,65 N 5,00.
Пример 2. Получение 2-(п-хлорфенацилиден)-2,5-дигидро-4,1-бензоксазепинона-3.
СмесЫ, г (0,005 моль) п-хлорбензоилпировиноградной кислоты в 70 мл сухого толуола и 0,62 г (0,005 моль) о-аминобензилового спирта в 25 мл сухого толуола кипятят в
0 течение 3 ч. После охлаждения реакционной массы выделяют 1,2 г (76%) кристаллического продукта оранжевого цвета с т.пл. 162-163С (из изопропилового спирта),
5 Найдено, %: С 65 ,07 Н 3,71 N 4,39; се 11,19.
, NOjCe.
Вычислено,%: С 64,96; Н 3,82; N 4,49; C;f. 11,32.
0 Противомикробную активность 2-фенацилиден-2,5-дигидро-4,1-бензоксазепинонов-3 изучают методом двухкратных серийных разведений в жидкой питательной среде на спектре,включающем
5 два штамма: грамм-положительные бактерии Staphygococcus aureus и грамм-отрицательные бактерии B.CoEi- . Для культивирования бактерий используют мясопептонный бульон. МикробнаяQ нагрузка 2,5-10 клеток в 1 мл среды.
Активность оценивают по минимальной бЬктериостатической (МБсК) концен Трации химических соединений,выраженных в мкг/мл.
В качестве растворителя используют
спирт.
Наибольшую активность в отношении кишечной палочки проявляет 2-(п-хлорфёнацилиден)-2,5-дигидро-4,1-бензоксазепинон-3 (ЬР Государственной регистрации 971577), МБсК которого соС
тавляет 500 мкг/мл, что вдвое превышает активность сулемы.
2-Фенацилиден-2,5-дигидро-4,1-бензоксазепинон-3 (№ Государственной 5 регистрации 971477) показывает меньшую активность - 1000мкг/мл, равную активности сулемы.
В отношении золотистого стафило кокка -наиболее высокую активность. 60 проявляет 2-(п-хлорфенацилиден)-2,5-дигидро-4., 1-бензоксазепинон-З, МБсК 250 мкг/мл, что в четыре раза выше по сравнению с сулемой (1000 мкг/мл).
2-фенацилиден-2,5-дигидро-4,165 -бензоксазепинон-3 показывает активность 1000 мкг/мл, равную активности рулеты.
Формула
изобретения
1. 2-фенацилиден-2,5-дигидро-4,1-бенэоксазепиноны-3 общей формулы
, ИН-С
сн-со
где R - водород или хлор,
проявляющие противомикробную .активность.
2. Способ получения соединений по П.1, отличающийся тем,, что соответствующую ароилпировиноградную кислоту подвергают взаимодействию с о-аминобензиловым спиртом при кипячении в среде толуола в качестве растворителя.
Источники информации, принятые во внимание при экспертизе
1.Патент Великобритании
№ 1090611, кл. С 2 С, опублик. 1967.
2.Машковский М..Д, Лекарственные средства, ч. П, М., Медицина,
1972, с. 436-449.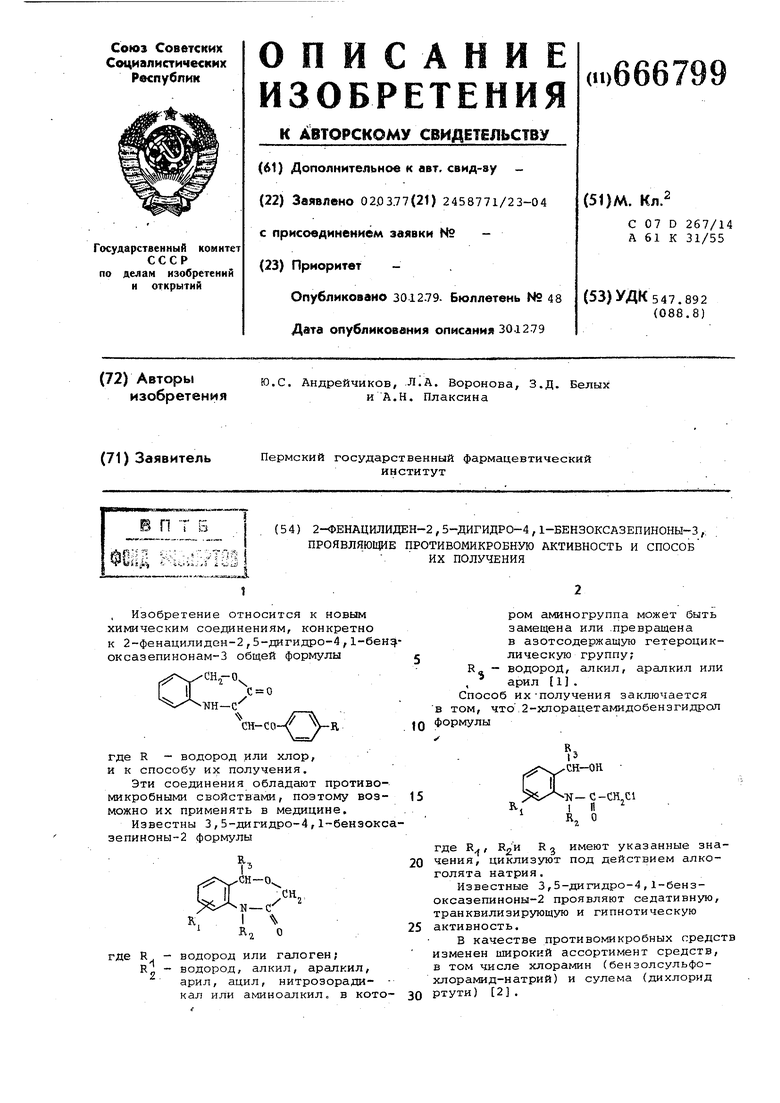


| название | год | авторы | номер документа |
|---|---|---|---|
| 2-Метил-2,6-диарил-1,3-диоксен-4-оны,пРОяВляющиЕ пРОТиВОМиКРОбНую АКТиВНОСТь,и СпОСОб иХ пОлучЕНия | 1977 |
|
SU677328A1 |
| Способ получения 3-фенацилиден 5,6 дигидро -1,4-оксазионов | 1976 |
|
SU621676A1 |
| Способ получения 2-фенацилиден-5,6-дигидро-1,4-оксазин-3-онов | 1980 |
|
SU910627A1 |
| СУКЦИНАТ N-(2,4,6-ТРИМЕТИЛФЕНИЛ)АМИДА 2-(БЕТА-N, N-ДИЭТИЛАМИНОЭТИЛАМИНО)-4-ОКСО-4-(4-МЕТИЛФЕНИЛ)-2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩУЮ И ПРОТИВОМИКРОБНУЮ АКТИВНОСТЬ | 2009 |
|
RU2428412C2 |
| N-ЗАМЕЩЕННЫЕ АМИДЫ 2-ГИДРОКСИ-4-ОКСО-4-(4-ХЛОРФЕНИЛ)2-БУТЕНОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОМИКРОБНУЮ АКТИВНОСТЬ | 2009 |
|
RU2429225C2 |
| 4-N-(4-АРИЛ-2,4-ДИОКСОБУТИРИЛ)АМИНОБЕНЗОЛСУЛЬФАМИДЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОВОСПАЛИТЕЛЬНУЮ, АНАЛЬГЕТИЧЕСКУЮ И АНТИМИКРОБНУЮ АКТИВНОСТИ | 2008 |
|
RU2367651C1 |
| 2-Карбометокси-2- бромфенацил диоксен оны,пРОяВляющиЕ пРОТиВОМиКРОбНую АКТиВНОСТь | 1978 |
|
SU707199A1 |
| Способ получения 5-арил-2-гидрокси-2-метоксикарбонилметил-2,3-дигидрофуран-3-онов | 1989 |
|
SU1606510A1 |
| N-замещенные амиды ароилпировиноградных кисло,проявляющие противосудорожную активность | 1979 |
|
SU769992A1 |
| Бис-(этоксалилдиазометил) ртуть, проявляющая антимикробную активность | 1987 |
|
SU1559679A1 |


Авторы
Даты
1979-12-30—Публикация
1977-03-02—Подача