Окисление предпочтительно ведут при 50-200°С в присутствии 0,001-20 вес. % серной кислоты или ее соли, в расчете на одноатомный фенол и при мольном соотношении перекись водорода - одноатомный фенол, равном 0,01-0,50 : 1. Отличительным признаком способа является использование при окислении добавок МОНО-, ди- или циклокетона Сз-С2о, который может содержать атом галогена, гидроксил или аминогруппу, при мольном соотношении кетон-нерекись водорода 0,005- 20: 1. Изобретение позволяет увеличить выход производных двухатомного фенола, в расчете на фенол, и несколько упростить технологию выделения целевых продуктов за счет легкости их отделения от использованных реагентов, так как используемая в процессе перекись водорода по окончании реакции превращается в воду. В качестве одноатомных фенолов используют, например, орто-, мета- и паракрезол, орто-, мета- или параэтилфенол, ортопропилфенол, параизопропилфенол, метабутилфенол, пара-йтор-бутилфенол, пара-третбутилфенол, метаизобутилфенол, паранентилфенол, парагексилфенол, 2,3-диметилфенол, 2,5-диметилфенол, 3,4-диметилфенол, 2,4-диметилфенол, 2,6-диметилфенол, 3,5диметилфенол, 2,3,4-триметилфенол, 2,3,6триметилфенол, 2,4,5-триметилфенол, 2,3,5триметилфенол, 3,4,5-триметилфенол, 2,3,4,5тетраметилфенол, 2,3,5,6-тетраметилфенол, 2-этил-З-метилфенол, 3-т/7ег-бутил-4-метилфенол, 2-изопропил-5-метилфенол, 2-пентил-6-метилфенол, З-гексил-5-метилфенол и т. п. Радикал R в формуле I может быть нормальным или разветвленным алкильным радикалом, например метилом, этилом,пропилом, изонропилом, бутилом, бтор-бутилом, изобутилом, грег-бутилом, пентилом, гексилом и др. В качестве моно-, ди- или циклокетона используют следующие соединения, выбранные из группы Сз-2020: кетон R,(II) где радикалы JRi и могут иметь одинаковое или различное значение и каждый из них представляет собой прямую или разветвленную алкильную группу из Ci-dg или фенильную группу, атом водорода алкильной группы обычно замещен атомом галогена, гидроксильной группой, аминогруппой или фенильной группой, а символами RI и/или Кг может быть обозначена алифатическая группа, содержащая двойную связь; дикетон, имеющий основную формулу 1,(СНг), оо где п - целое число от О до 16 включительно;RI и Rj имеют те же значения, что и указанные выше; циклокетон, имеющий основную формулу где п - целое число от 4 до 11 включительно;i+m представляют собой целое число от 3 до 10 включительно; RI имеет то же значение, что и приведенное выше. В алифатических кетонах вышеуказанной общей формулы II алкильные группы Ri и R2 могут содержать от 1 до 18 атомов С, быть нормального или разветвленного строения. Примерами алкильных групп могут служить следующие группы: метильная, этильная, пропильная, 1-метилэтильная, бутильная, 1-метилпропильная, 1,1-диметилэтильная, 2-метилпронильная, пентильная, 1-метилбугильная, 2-метилбутильная, 3-метилбутильная, 1,2-диметилпропильная, гексильная, 1-метилпентильная, октильная, децильная, ундецильная, 2-додецильная, тридецильная, тетрадецнльная, пентадецильная, октадецильная и т. п. В качестве кетонов используют соединения: ацетон, метилэтилкетон, 2-пентанон, 3-пентанон, З-метил-2-бутанон, 2-гексанон, 3-гексанон, З-метил-2-пентанон, 4-метил-2пентанон, 3,3-диметил-2-бутанон, 2-гептанон, 3-гептанон, 4-гептанон, 2,4-диметил-З-пентанон, 2-октанон, 6-метил-2-гептанон, 2-нонанон, 2,6-диметил-4-гептанон, 2,2,4,4-тетраметил-3-гептанон, 3-деканон, 6-ундеканон, 2-тридеканон, 7-тридеканон, 2-тетрадеканон, 2-пентадеканон, 2-гексадеканон, 2-гептадеканон, 3-октадеканон, 4-нонадеканон, 5-эйкозанон, З-бутен-2-он, З-пентен-2-он, 5-гексен-2-он, 4-метил-3-пентен-2-он, 6-метил-5-гептен-2-он, 5-октен-2-он, 7-нонадецен-2-он, 1-хлор-2-пропанон, 1-хлор-З-гептанон, З-гидрокси-2-бутанон, 1-бром-З-гептанон, 1-гидрокси-2-пропанон, 4-амино-4метил-2-пентанон, метилфенилкетон, бензофенон, 1-фенил-2-пропанон, 1-фенил-1-бутанон, 1-фенил-З-бутанон, 1-фенил-З-пентанон, 1,3-дифенил-2-пропанон и т. п. В алифатических кетонах выщеуказанной общей формулы II алкильные группы Ri и R2 могут содержать от 1 до 18 атомов С, быть нормального или разветвленного строения. Примерами алкильных групп могут служить следующие группы: метильная, этильная, пропильная, 1-метилэтильная, бутильная, 1-метилпропильная, 1,1-диметилэтильная, 2-метилпропильная, пентильная, 1-метилбутильная, 2-метилбутильная, 3-метилбутильная, 1,2-диметилпропильная, гексильная, 1-метилпентильная, октильная, децильная, ундецнльная, 2-додецильная, тридецильная, тетрадецильная, пентадецильная, октадецильная и т. п.
В качестве дикетонов используют соединения 2,3-бутаднон, 2,4-пентандион, 2,5-гександиоп и др.
В качестве циклокетонов используют соединения циклопентанон, циклогексанон, 2-этил-1-циклопентанон, 2 - метил-1-циклогексанон, циклододеканон и т. п.
Концентрация используемой перекиси водорода не является определяющим фактором, но предпочтительно использование 30-60%-ной перекиси водорода, применяемой в промышленности.
Предпочтительное молярное соотношение кетона к перекиси водорода составляет 0,005-20:1. Молярное соотношение используемой перекиси водорода к одноатомным фенолам не является критическим фактором, но оно составляет величину 0,005- 1,0:1, предпочтительно 0,01-0,50:1.
Реакцию можно проводить при температуре от О до 250°С, предпочтительно 45- 200°С. Если реакцию необходимо проводить при температуре, лежащей ниже температуры плавления фенольного производного, используемого в качестве исходного материала, то в качестве растворителя применяют метилацетат, этилацетат, этилендиацетат, метилбензоат, диметилфталат, диэтилфталат и т. п., которые не препятствуют протеканию реакции окисления. В большом количестве кетон может служить растворителем.
Время реакции может меняться в зависимости от температуры реакции, количества кетона и наличия и количества катализатора. Время реакции не является определяющей величиной. Реакцию можно проводить при атмосферном давлении, но она может протекать при пониженном давлении п под давлением. Для достижения улучшенных выходов двухатомного фенола, желательно, чтобы количество воды in situ в реакции было как можно меньше.
Реакцию можно проводить без использования катализатора, но предпочтительно в присутствии его. В качестве катализаторов согласно изобретению используют серную
кислоту или ее соли или сульфоновую кислоту или ее соли.
В качестве солей серной кислоты могут быть использованы соли: сульфат аммония, бисульфат лития, сульфат натрия, бисульфат натрия, сульфат магния, сульфат алюминия, бисульфат калия, сульфат меди, сульфат цинка, сульфат титана, сульфат хрома, сульфат марганца, сульфат н елеза,
сульфат аммоний железа, сульфат кобальта, сульфат никеля, сульфат калий алюмииия, сульфат серебра, сульфат кадмия, сульфат индия, сульфат циркония, сульфат олова, сульфат сурьмы, сульфат молибдена,
сульфат рутения, сульфат бария, сульфат ртути, сульфат таллия, сульфат свинца, сульфат церия, сульфат гидроксиламина, сульфат дибутиламина, сульфат анилина, сульфат пиридина, сульфат пиперидина
и т. п.
В качестве сульфоновых кислот используют кислоты алифатические сульфоновые, такие как метансульфоновая, этансульфоновая кислоты и др., бензолсульфоновая кислота, паратолуолсульфоновая кислота, парафенолсульфоновая кислота, парааминосульфоновая кислота, нафталин-а-сульфоновая кислота и т. п. наряду со смолами сульфокислотного типа, такими как сильнокислотные ионообменные смолы. В качестве солей сульфоновых кислот используют различные соли, например металлов или органических оснований, аналогичные вышеприведенным сульфатам.
Производные двухатомного фенола общей формулы I могут быть иолучены в основном одного типа или в виде смеси нескольких типов, в зависимости от структуры исходного одноатомиого фенола.
Папример, если в качестве исходного материала используется фенол, то образуется смесь катехина и гидрохинона. При использовании в качестве исходного соединения о-алкилфенола получают смесь 3-алкилкатехина и 2-алкилгидрохинона. Если в качестве исходного соединения взят jit-алкилфенол, то образуется смесь 3-алкилкатехола, 4 - алкилкатехина и 2 - алкилгидрохинона. Если в качестве исходного материала взят
п-алкилфенол, то образуется в основном 4-алкилкатехин. Если в качестве исходного соединения исиользованы диалкилфенол или другие полиалкилфеиолы, то образуются смеси производных двухатомного фенола, как указано ниже.
Исходные
Продукты реакции полиалкилфенолы
3,4-Диметилкатехин, 2,3-диметилгидрохинон
3,5-Диметилкатехин
3,6-Диметилкатехин, 2,5-диметилгидрохинон
2,6-Диметилгидрохинон
3,4-Диметилкатехин, 4,5-Диметилкатехин
3,5-Диметилкатехин, 2,6-диметилгидрохинон
2-Изопропил-5-метилгидрохинон, З-изопропил-6-метилкатехол
3,4,5-Триметилкатехин
3,4,6-Триметилкатехин, 2,3,5- Триметилгидрохинон
2.,3,6-Триметилгидрохинон
3,4,5-Триметилкатехин 3,4,6-Триметилкатехин
2,3,5,6-Тетраметилгидрохинон
3,4,5,6-Тетраметилкатехин
Изобретение иллюстрируется следующими примерами конкретного выполнения способа получения производных двухатомных фенолов.
Пример 1. В плоскодонную колбу емкостью 50 мл, снабженную обратным холодильником, термометром, мешалкой и выходным отверстием для жидкости, загружают 10 г (106 ммоль) фенола, 8,20 ммоль 4-метил-2-пентанона и 0,300 г (5,29 ммоль) 60%-ного раствора перекиси водорода, и колбу помещают в масляную баню, нагретую до 170°С, реакционную смесь перемешивают в течение 120 мин. Реакционную смесь анализируют методом газовой хроматографии. Выходы катехина и гидрохинона, рассчитанные по количеству перекиси водорода, как показано ниже.
количество, ммоль, полученного катехина
ХШО
ыход катехина.
количество, ммоль, загруженной перекиси водорода
количество, ммоль, полученного гидрохинона
Х100
ыход гидрохинона, %
количество, ммоль, загруженной перекиси водорода
Примеры 2-5. Реакции проводят таким же образом, как и в примере 1, за исключением того, что используют кетоны. Заказанные в табл. 1. Выход целевых продуктов приведены в табл. 1.
Таблица I








Пример 6. Реакцию проводят так же, как и в примере 1, за исключением того, что не добавляют кетон. Результаты опыта приведены в табл. 1.
Пример 7. 10 г фенола (106 ммоль), 0,476 г ацетона (8,20 ммоль), 0,601 г (5,29 ммоль) 30%-ной перекиси водорода и 0,070 г бисульфата натрия (NaHSO4 ПзО) смешивают и нагревают при 50°С в течение 30 мин так же, как и в примере 1, в
результате образуется 0,292 г катехина и 0,216 г гидрохинона. Общий выход катехина и гидрохинона составляет 87,4%.
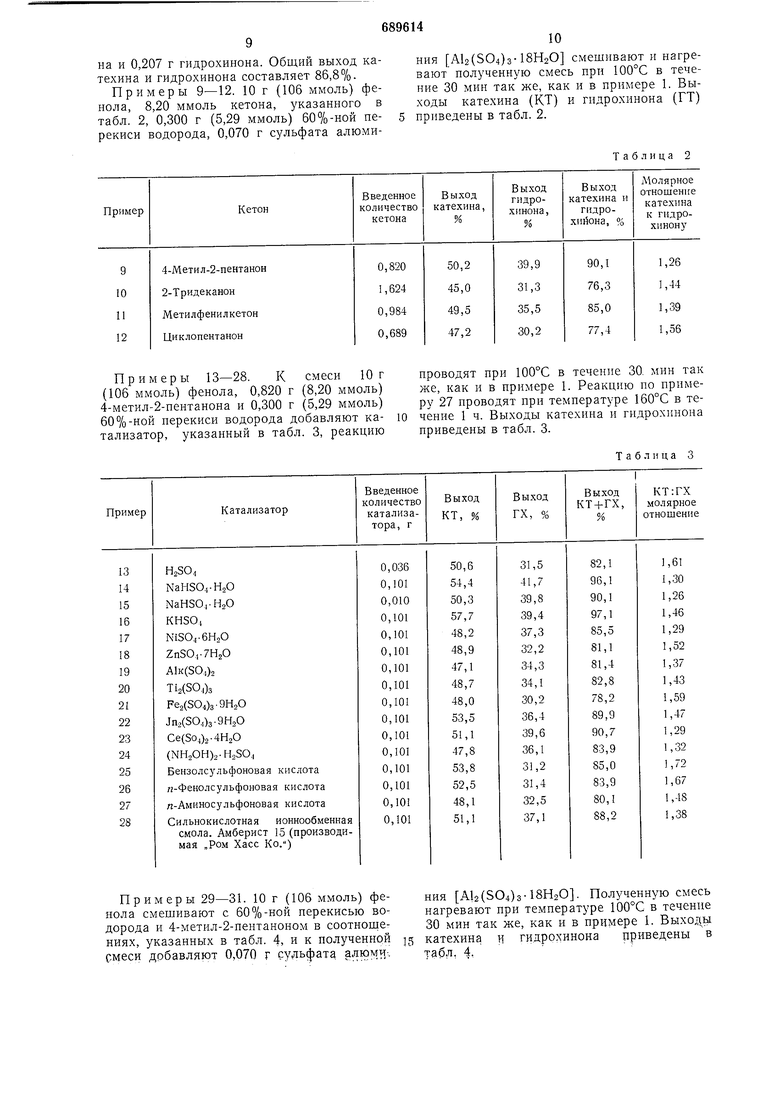
Пример 8. 10 г (106 ммоль) фенола, 0,5904 г (8,20 ммоль) метилэтилкетона, 0,601 г (5,29 ммоль) 30%-ной перекиси водорода и 0,375 г сульфата индия 1п2(ЗО4)з-9Н2О смешивают и нагревают при 70°С в течение 30 мин, как и в примере 1, в результате получают 0,298 г катехина и 0,207 г гидрохинона. Общий выход катехина и гидрохинона составляет 86,8%. Примеры 9-12. 10 г (106 ммоль) фенола, 8,20 ммоль кетона, указанного в табл. 2, 0,300 г (5,29 ммоль) 60%-ной перекиси водорода, 0,070 г сульфата алюмиПримеры 13-28. К смеси 10 г (106 ммоль) фенола, 0,820 г (8,20 ммоль) 4-метил-2-нентанона и 0,300 г (5,29 ммоль) 60%-ной перекиси водорода добавляют катализатор, указанный в табл. 3, реакцию
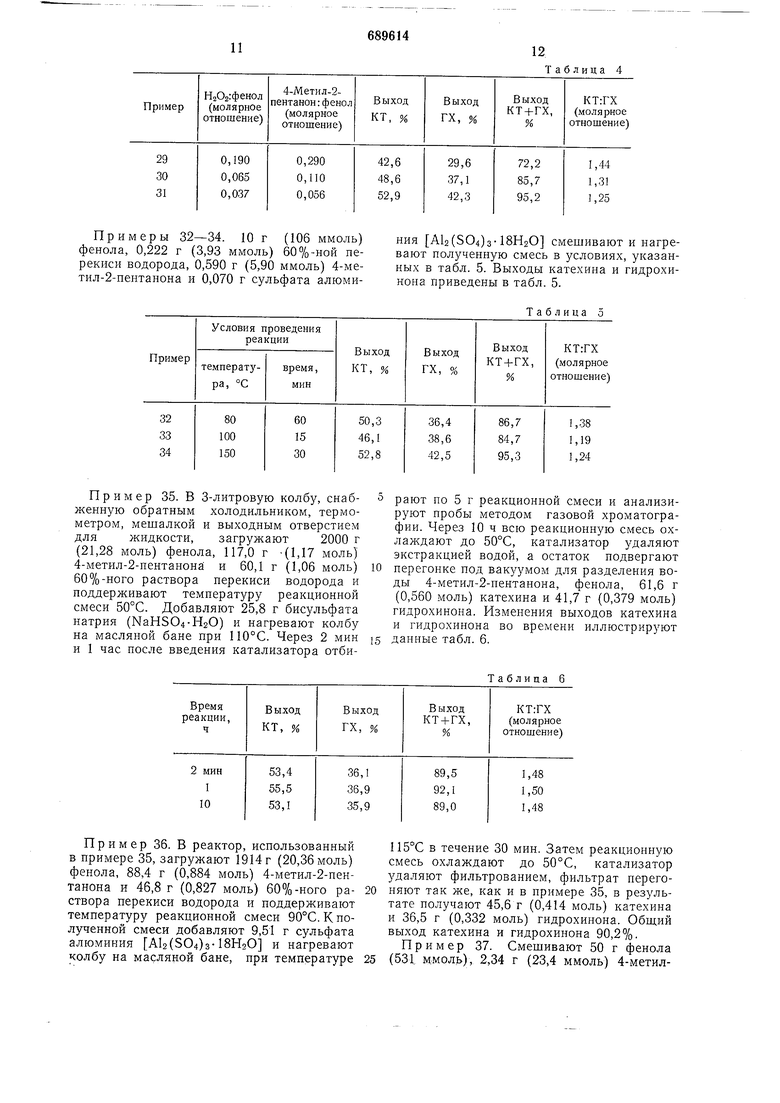
Примеры 29-31. 10 г (106 ммоль) фенола смешивают с 60%-ной перекисью водорода и 4-метил-2-пентаноном в соотношениях, указанных в табл. 4, и к полученной смеси добавляют 0,070 г сульфата алюмич
Таблица 2
проводят при 100°С в течение 30. мин так же, как и в примере 1. Реакцию по примеру 27 проводят при температуре 160°С в течение 1 ч. Выходы катехина и гидрохинона приведены в табл. 3.
Таблица 3
ния А12(5О4)з-18Н2О. Полученную смесь нагревают при температуре 100°С в течение 30 мин так же, как и в примере 1. Выходы катехина и гидрохинона приведены в табл. 4, ния А12(504)з-18Н2О смешивают и нагревают полученную смесь при 100°С в течение 30 мин так же, как и в примере 1. Выходы катехина (КТ) и гидрохинона (ГТ) приведены в табл. 2.
Примеры 32-34. 10 г (106 ммоль) фенола, 0,222 г (3,93 ммоль) 60%-ной перекиси водорода, 0,590 г (5,90 ммоль) 4-метил-2-иентанона и 0,070 г сульфата алюмиПример 35. В 3-литровую колбу, снабженную обратным холодильником, термометром, мешалкой и выходным отверстием для жидкости, загружают 2000 г (21,28 моль) фенола, 117,0 г -(1,17 моль) 4-метил-2-пентанона и 60,1 г (l,OQ моль) 60%-него раствора перекиси водорода и поддерживают температуру реакционной смеси 50°С. Добавляют 25,8 г бисульфата натрия (NaHSO4-H2O) и нагревают колбу на масляной бане нри 110°С. Через 2 мин и I час носле введения катализатора отбиПример 36. В реактор, использованный в примере 35, загружают 1914 г (20,36 моль) фенола, 88,4 г (0,884 моль) 4-метил-2-пентанона и 46,8 г (0,827 моль) 60%-ного ра- 20 створа перекиси водорода и поддерживают температуру реакционной смеси 90°С. К полученной смеси добавляют 9,51 г сульфата алюминия АЬ(504)3-ISHgO и нагревают колбу на масляной бане, при температуре 25
Таблица 4
ния А12(504)з-ISHsO смешивают и нагревают полученную смесь в условиях, указанных в табл. 5. Выходы катехина и гидрохинона приведены в табл. 5.
Таблица 5
рают по 5 г реакционной смеси и анализируют пробы методом газовой хроматографии. Через 10 ч всю реакционную смесь охлаждают до 50°С, катализатор удаляют экстракцией водой, а остаток подвергают перегонке нод вакуумом для разделения воды 4-метил-2-пентанона, фенола, 61,6 г (0,560 моль) катехина и 41,7 г (0,379 моль) гидрохинона. Изменения выходов катехина и гидрохинона во времени иллюстрируют данные табл. 6.
Таблица 6
15°С в течение 30 мин. Затем реакционную смесь охлаждают до 50°С, катализатор удаляют фильтрованием, фильтрат перегоняют так же, как и в примере 35, в результате получают 45,6 г (0,414 моль) катехина и 36,5 г (0,332 моль) гидрохинона. Общий выход катехина и гидрохинона 90,2%.
Пример 37. Смешивают 50 г фенола (531 ммоль), 2,34 г (23,4 ммоль) 4-метил2-пентаноиа, 1,31 г (23,2 ммоль) 60%-ной перекиси водорода и 0,4 мг серной кислоты и нагревают реакционную смесь в течение 15 мин нри 50°С. Получают 1,23 г катехина и 0,93 г гидрохинона. Общий выход катехина и гидрохинона составляет 84,7%. Пример 38. В тот же реактор, что li в примере 35, помещают 1852 г фенола (19,68 моль), 4,6 г (0,046 моль) 4-мстпл2-пентанона, 55,8 г (0,985 моль) 60%-но:; перекиси водорода и 0,10 г концентрированной серной кислоты и нагревают реакционную смесь на масляной бане при 50°С з течение 10 мин при перемещивании. После нейтрализации серной кислоты (добавлением 0,16 г 50%-ного водного раствора гидроокиси натрия) смесь перегоняют при пониженном давлении. Получают 3,7 г 4-метил-2-пентанона, 1762г фенола (18,72моль), Таблица 7 56,8 г катех; ;1а (0,516 моль) и 38,5 г гидрохинона (0,350 моль). Общий БЫ.чод двухатомных фенолов в расчете на перекись водорода составляет 88,0%, а в расчете на прореагировавший фенол 90,2%. В табл. 7 приведены результаты для дв -хатол1ны : фенолов полученных его окислением фенола. П р н м ер 39. В четырехгорлую колбу емкостью 300 мл, снабжепную обратным холодпльннком, термометром, мешалкой и выходным отверстием для жидкости, загружают 150 г (1390,0 ммоль) ..н-крезола, 6,09 г (60,9 ммоль) 4-метил-2-пентанона и 2,56 г (45,2 ммоль) 60%-ного раствора перекиси водорода и нагревают реакционную смесь на масляной бане при 120°С в течение 90 мин. Реакционную смесь анализируют методом газовой хроматографии. Получают 1,22 г (9,8 ммоль) 3-ме.тилкатехииа, 1,57 г (12,7 ммоль) 4-метилкатехина и 1,00 г (8,1 ммоль) 2-метилгидрохинона. Общий выход двухатомных алкилфенолов составляет 67,7% в расчете на перекись водорода. Пример 40. Реакцию проводят как и в примере 39 за исключением того, что вместо 4-метил-2-пентанона используют 7,20 г (60,0 ммоль) метилфенилкетопа. В результате чего получают 1,10 г (8,9 ммоль) 3-мет лкатехина, 1,00 г (8,1 ммоль) 4-метплкатехина и 1,23 г (9,9 ммоль) 2-метилгидрохннона. Общий выход двухатомных алкнлфенолов составляет 59,5% в расчете на перекись водорода. Пример 41. Реакцию проводят так же, как и в примере 39, за исключением того, что не добавляют 4-метил-2-пентанон, в результате получают 0,68 г (5,5 ммоль) 3-метилкатехина,о,80 г (6,4 ммоль) 4-метилкатехина и 0,94 г (7,6 ммоль) 2-метилгидрохинона. Общий выход двухатомных алкилфенолов 43,1 %. Пример 42. В реакционный сосуд, использованный в примере 39, загружают 150 г (1390 ммоль) о-крезола, 6,09 г (60,9 ммоль) 4-метил-2-нентанона, 2,56 г (45,2 ммоль) 60%-ного раствора перекиси водорода и 0,40 г серной кислоты и нагревают реакционную смесь в течение 30 мин при 100°С, в результате получают 2,68 г (21,6 ммоль) 3-метилкатехина и 1,36 г (10,9 ммоль) 2-метилгидрохинона. Общий выход двухатомных алкилфенолов 72,1%. Пример 43. Реакцию проводят как в примере 42, за исключением того, что вместо о-крезола используют150 г (1390 ммоль) лг-крезола, в результате получают 1.31 г (10.5 ммоль) 3-метилкатехина, 2,29 г (18,5 ммоль) 4-метнлкатехина и 1,74 г (14,0 ммоль) 2-метплгидрохинона. Общий выход двзхатомных алкилфенолов 95,4%. Примеры 44-49. Все опыты проведены как и в примере 42, за исключением
того, что вместо о-крезола использ пот я-крезол и широко варьируют условия реакции, тии кетона и катализатора. Условия проведения реакций и результаты опытов представлены в табл. 8.
Пример 50. Реакцию проводят как и в примере 42, за исключением того, что вместо о-крезола используют 170 г (1390,0 ммоль) л-этилфенола, в результате получают 3,84 г (27,8 ммоль) 4-этилкатехина. Выход 4-этилкатехина 61,6%.
Пример 51. В реактор, использованный в примере 42, загружают 150 г (1000,0 ммоль) л-грггт-бутилфенола, 12,5 г (125,0 ммоль) 4-метил-2-пептанона, 4,72 г (83,3 ммоль) 60%-ного раствора перекиси водорода и 1,00 г бисульфата иатрия (NaHSO4-H2O) и нагревают реакционную смесь в течение 10 мин при температуре 120°С, в результате получают 7,72 г (46,5 ммоль) 4-г/ ег-бутилкатехина. Выход 4-7рет-бутилкатехина составляет 55,8%.
Пример 52. 150 г (1000,0 ммоль) п-грег-бутилфенола, 5,00 г (50,0 ммоль) 4-метил-2-пентанона, 1,89 г (33,3 ммоль) 60%-ного раствора перекиси водорода и 0,40 г серной кислоты загружают в реактор, использованный в примере 42, и нагревают реакционную смесь при 110°С в течение 30 мин, в результате получают 3,31 г (20,0 моль) 4-трег-бутилкатехина. Выход двухатомного алкилфенола 60,0%.
Пример 53. В 3-литровую колбу, спабженнзЮ обратным холодильником, термометром, мешалкой и выходом для жидкости, помещают 2160 г (20,00 моль) л-креЗрла 90,0 г (0,90 мо,чь) 4.ддртил-2-лентанп
Таблица 8
на и 37,4 г (0,66 моль) 60%-ного раствора перекиси водорода и поддерживают температуру реакционной смеси 50°С. К полученной смеси добавляют 1,5 г серной кислоты и нагревают колбу в течение 20 мин при . После охлаждения реакционной смеси серную кислоту экстрагируют водой, а смесь перегоняют под вакуумом, в результате получают 49,9 г (0,403 моль) 4-метилкатехина. Выход двухатомного алкилфенола составляет 61,0%.
Пример 54. В реакционный сосуд, снабженный обратным холодильником, имеющим водяную ловушку, термометр, мешалку и выход для жидкости, помещают 100 г (819 ммоль) 3,5-диметилфенола, 4,1 г (41 ммоль) 4-метил-2-пентанона, и 2,32 г (41,0 ммоль) 60%-ной перекиси водорода.
Реакционную смесь нагревают на масляной бане при 150°С при перемешивании в течение 2 ч. В течение этого времени вода непрерывно собирается в водяной ловушке. Реакционную смесь анализирзют методом
газовой хроматографии. В качестве продуктов реакции получают 1,59 г (11,5 ммоль) 3,5-диметилкатехина и 0,69 г (5,0 ммоль) 2,6-диметилгидрохинона. Общий выход двухатомных алкилфенолов составляет
40,3% в расчете на перекись водорода.
Пример 55. Реакцию проводят как и в примере 54, за исключением того, что не добавляют 4-метил-2-пентанон. В результате реакции получают 1,02 г (7,4 ммоль)
3,5-диметилкатехина и 0,55 г (4,0 ммоль) 2,6-диметилгидрохинона. Общий выход двухатомных алкилфенолов 27,9%,
17
Пример 56. В реактор, использованный в примере 54, помещают 100 г (819 ммоль) 3,5-диметилфенола, 3,61 г (36,1 ммоль) 4-метил-2-пентанона, 2,88 г (50,8 ммоль) 60%-ной перекиси водорода п 0,01 г серной кислоты и реакционная смесь в течение 20 мин нагрета при 110°С, так же, как и в примере 54. Реакционную смесь анализируют методом газовой хроматографии. Продуктами реакции являются 3,19 г (23,1 ммоль) 3,5-диметилкатехина и 2,24 г (16,2 ммоль) 2,6-диметилгидрохинона. Общий выход двухатомных алкилфенолов составляет 77,4%.
Пример 57. В реактор, исиользованиый в примере 52, помещают 100 г (819 ммоль) 3,5-диметилфенола, 2,97 г (29,7 ммоль) 4-метил-2-иентанона, 2,52 г (44,5 ммоль) 60%-ной перекиси водорода и 0,01 г бисульфата натрия (NaHS04-n2O) и нагревают реакциоиную смесь ири 110°С в течение 20 мин как и в примере 54. В качестве продуктов реакции получают 2,19 г (15,9 ммоль) 3,5 - диметилкатехина и 1,25 г (9,08 ммоль) 2,6 - диметилгидрохинона. Общий выход двухатомных алкилфенолов составляет 56,1 %.
Пример 58. Реакцию проводят как описано в примере 56, за исключением того, что вместо серной кислоты используют 1,10 г сильнокислотной ионообменной смолы типа Амберист-15 (производства «Ром Хаас Ко.). Получают 2,88 г (20,9 ммоль) 3,5-диметилкатехина и 1,74 г (12,6 ммоль) 2,6-диметилгидрохиноиа. Общий выход двухатомных алкилфенолов составляет 65,9%.
Пример 59. В реактор, использованный в примере 54, помещают 100 г (819 ммоль) 3,5-диметилфенола, 2,64 г (22,0 ммоль) метилфенилкетона, 1,81 г (31,9 ммоль) 60%-ной перекиси водорода и 0,01 г серной кислоты и нагревают реакционную смесь ири 110°С в течение 20 мин так же, как и в примере 54. Получают 2,10 г (15,2 ммоль) 3,5-диметилкатехина и 1,04 г (7,5 ммоль) 2,6-диметилгидрохиноиа. Общий выход двухатомных алкилфенолов 70,9%.
Пример 60. Реакцию цроводят так же, как в примере 56, за исключением того, что вместо 3,61 г (36,1 ммоль) 4-метил-2-иентанона используют 0,25 г (2,5 ммоль). Получают 3,09 г (22,4 ммоль) 3,5-диметилкатехина и 2,07 г (15 ммоль) 2,6-диметилгидрохинона. Общий выход двухатомных фенолов составляет 73,6%.
Пример 61. Реакцию проводят так же, как в примере 56, за исключением того, что количество серной кислоты сокращают с 0,01 до 0,001 г и время реакции составляет 30 мин. Получают 3,16 г (22,9 ммоль) 3,5-диметилкатехина и 2,13 г (15,4 ммоль) 2,6-диметилгидрохинона. Общий выход двухатомных алкилфенолов 75,4%.
18
Пример 62. Реакцию проводят так же, как в примере 56, за исключением того, что количество 60%-)шй перекиси водорода увеличивают с 2,88 г (50,7 ммоль) до 4,50 г (7Э,4 ммоль). Получают 4,69 г (34,0 ммоль) 3,5-диметилкатехина и 2,75 г (19,9 ммоль) 2,6 - диметплгидрохинопа. Общий выход двухатомиых алкилфенолов 67,9%.
Пример 63. Реакцию проводят так же, как в примере 56, за исключением того, что вместо 3,5-диметплфенола используют 100 г (819 ммоль) 2,4-диметилфенола. Получают 2,50 г (18,1 ммоль) 3,5-дпметплкатехпна. Выход двухатомного алкилфенола составляет 35,6%.
Пример 64. Реакцию проводят так же, как в примере 56, за исключением того, что вместо 3,5-диметилфенола используют 100 г (819 ммоль) 2,5-диметилфенола. Получают 1,45 г (10,5 ммоль) 3,6-дпметилкатехина и 1,85 г (13,4 ммоль) 2,5-диметилгидрохинона. Общий выход двухатомных алкилфенолов составляет 46,9%.
П р и м е р 65. Реакцию ироводят так же,
как в примере 56, за исключением того, что
вместо 3,5-диметплфенола используют 100 г
(819 ммоль) 2,6-дпметилфенола. Получают
1,04 г (7,5 ммоль) 2,6-диметилгидрохинона.
Выход двухатомного алкилфенола составляет 14,7%.
Пример 66. В реактор, исиользованный в нримере 54, помещают 100 г (735 ммоль) 2,3,5-триметилфеиола, 2,31 г (23,1 ммоль) 4-метил-2-пентанопа, 2,61 г (46,0 ммоль) 60%-ной перекпси водорода и 1,0 г сульфата индия 1п2(504) и нагревают реакционную смесь при температуре 100°С в теченпе 60 мин. Получают 2,16 г (14,2 ммоль) 3,4,6-триметилкатехина и 0,64 г (4,2 ммоль) 2,3,5-триметилгидрохинона. Общий выход двухатомных алкилфенолов 40,0%.
При м е р 67. Реакцию проводят в уело-. ВИЯХ примера 66, за исключением того, что вместо 2,3,5-триметилфенола используют 100 г (735 ммоль) 2,3,6-триметилфенола. Получают 2,05 г (1365 ммоль) 2,3,6-триметилгидрохинона. Выход двухатомного алкилфенола 29,4%.
Пример 68. В использованный в примере 54 реакционный сосуд помещают 100 г (666 ммоль) 2,3,4,5-тетраметилфенола, 3,0 г (30 ммоль) 4 - метил-2-иентанона, 2,1 г (37,0 ммоль) 60%-ной перекиси водорода и 0,01 г 98%-ной серной кислоты и обрабатывают при 120°С в течение 20 мин таким же образом, как и в иримере 52. Получают 3,43 г (20,8 ммоль) 3,4,5,6-тетраметилиирокатехола. Выход двухатомного фенола 56%., Пример 69. В исиользованный в иримере 54 реакционный сосуд помещают 10 г (61 ммоль) 4-(1-этилпропил)-фенола, 0,3 г (3 ммоль) 4-метил-2 - пентанона, 0,20 г (3,5 ммоль) 60%-ной иерекиси водорода и 0,001 г 98%-ной серной кислоты и обрабатывают при 120°С в течение 20 мин таким же образом, как и в примере 52. Получают 0,28 г (1,58 ммоль) 4-(Ьэтилироиллу-катсхола. Выход двухатомиого фенола 45,1%. Пример 70. В использованный в иримере 54 реакционный сосуд помещают 10 г (56 ммоль) 4-(этилбутил) - фенола, 0,3 г (3,0 ммоль) 4-метил-2-пентанона, 0,20 г (3,5 ммоль) 60%-ной перекиси водорода и 0,001 г 98%-ной серной кислоты и обрабатывают при 120°С в течение 20 мин таким же образом, как и в примере 52. Получают 0,30 г (1,55 ммоль) 4-(1-этилбутил)-катехола. Выход двухатомного фенола 44,3%. Формула изобретения 1. Снособ получения производных двухатомного фенпла общей формулы где R - низщий алкил, содержащий 1-6 углеродных атомов, каждое значение R может быть одинаковым или различным; п - целое число от О до 4, и если л 3 или 4, то все 2-, 4- и 6-положения не могут быть заняты алкильными радикалами одновременно. окислением соответствующего производиого одноатомного фенола 30-60%-ной персмсисью водорода в присутствии катализатора кислого характера при новыщениой температуре, отличающийся тем, что, с целью увсличеиия выхода целевого продукта, окисление ведут в присутствии мо110-, ди- или циклокетопа Сз-С2о, который может содержать атом галогена, гидроксил 1Л1 аминогруппу, причем мольные соотношения кетон - перекись водорода составляют 0,005-20: 1. 2.Способ по п. 1, отличающийся тем, что окисление ведут при 50-200°С в присутствии 0,001-20 вес. % серной кислоты или ее соли в расчете иа одноатомный фенол. 3.Способ по пп. 1 и 2, отличающийс я тем, что окисление ведут при мольном соотношении иерекиеь водорода - фенол, равном 0,01-0,50: 1. Приоритет по признакам: 04.04.74 при л 0; 07.05.74 при . Источники информации, принятые во внимание при экспертизе 1.А. Chwala, М. Pailer. ОЬег die Oxydation von Phenol mit HjOs bei Anwesenheit von FeSO,i. J. «Pract. Chem., 1939, v. 152, p. 45. 2.Патент Великобритании o 1347625, КЛ. С 2C, опубл. 20.02.74 (прототип).
Авторы
Даты
1979-09-30—Публикация
1975-04-04—Подача