достато но высокой для инициирования и поддержания реакции взаимодействия сложного эфира фосфорной кислоты с триазином в целях получения желаемых продуктов. Хотя для проведения.предлагаемого процесса растворитель не требуется, в некоторых случаях рекомендуется работать с растворителем для простоты и удобства протекания реакции. Растворитель также полезен для регулировки температуры реакции. В используемом растворителе триазин должен растворяться, остальные же компоненты реакции с растворителем взаимодействовать не должны, К такого рода инертным растворителям следует отнести ацетонитрил, этилацетат, тет рагидрофуран и т.п. Обнаружено, что температура реакции может колебаться в пределах 25110° С. Соотношение сложного эфира фосфор ной к.ислоты и триазина в целях достижения оптимальных результатов должно быть 3-:1 . Реакцию обычно ведут при атмосфер ном давлении. В случае последовательного получения вначале получают 0,0-диарил-N-фосфонометилглицинонитрил, Затем его смешивают с пространственно затрудненным фенйлазометином с последующим нагревог 1 в вакууме. Предполагается образование промежуточного азо-аддукта, после чего нагрев продолжают до прекращения выделения про странственно затрудненного анилина. Затем реакционную смесь обрабатывают выделяя желаемый метилен-бис-продукт Пространственно затрудненные фенилазометины, необходимые для осущес вления предлагаемого способа, имеют фенильное кольцо, содержащее замести тели в обоих орто-положениях. Эти за местители оба могут представлять собой низший алкил за исключением 2,6-ди-трет-бутила. Кроме того, в качестве заместителя в одном орто-поло жении можно использовать галоид или низший алкоксил, в то время как во втором орто-положении в качестве.заместителя остается низший алкил, ,Цру гие положения на кольце такхсе могут быть замещены, К пространственно затрудненным фенильным группам следует отнести, например, 2-метил-6-этил, 2,6-диэтил, 2-метил-6-трет-бутил, 2-хлор-б-трет-бутил, 2-бром-6-трет-бутил, 2-метокси-б-трет-бутил и т.п Вообще было обнаружено, что без пространственного затруднения азеометиновый реактив тримеризуется в гексагидротриазин. Глицинонитрильные ре-активы, получаемые предлагаемыми методами, зачастую содержат примеси, которые могут мешать получению желаемых метилен-бис-соединений, поэтому предпочтительным является вначале получить сильную кислотную соль глицинонитрила, осаждающуюся в целях быстрого выделения этих примесей. После этого соль нейтрализуют с получением желаемого глицинонитрильного реактива. Во время процесса нейтрализации следует быть осторожным во избежание гидролиза арильных сложнозфирных групп. Взаимодействие глицинонитрила с азометином начинается при комнатной температуре, что подтверждено ЯМР. Применять можно и температуры примерно до 125с-, но предпочтительнЕлм является температурный диапазон примерно 60-80 -С, В то время как реакция протекает хорошо при атмосферном давлении, пространственно затрудненный анилин, образующийся при этом, может начать взаимодействовать с желаемым продуктом, образуя нежелательный аддукт. Поэтому.рекомендуется этот пространственно затрудненный анилин удалять при его образовании, что лучше всего осуществлять с применением понИженного давления (при зтом анилин во время реакции перегоняется) , Молярное соотношение глицинонитрила и азометина предпочтительно около 2:1. Пример 1. Ацетонитрильный раствор (10 кш) ди-(3,4-диметилфенил) фосфита (8,7 г, 0,03 моль) добавляют в ацетонитрильный раствор (50 мл) 1,3,5-трицианометилгексагидро-1,3,5-триазина (2,04 г, 0,01 моль) с последующим нагревом смеси 90 ч при 55°С. Фильтрацией, твердого продукта и выпаркой растворителя получают масло цвета красного бургундского вина, содержащее согласно ЯМР желаемый продукт и аминаль этого продукта, Хроматографией масла (8,0 г) на силикагеле (450 г) с циклогексаном(этилацетатом в соотношении 50%/50%, фракции по 60 мл)получают О,О-ди (3 4-диметилфенил) -N-фосфонометилглицинонитрил (фракции 30-41) . Фракции 20-25 из колонны хроматографирования по выпарке растворителя дают 1,62 г масла с „22 1,5387. Кристаллизацией этого масла из тетрахлорметанизооктана получают белый твердый продукт, который определяют как Н,К-метилен-бис-{О, (3,-4-диметилфенил) -N-фосфонометилглицинонитрил, т.пл, 79-80°С, Пример 2. йцетонитрильньтй раствор (100 мл) ди-(м-толил)фосфита (10,7 г, 0,04 моль) и 1,3,5-трицианометилгексагидро-i,3,5-триазина(2,72г, 0,0133 моль) нагревают до 50°С в течение 3 дней. Раствор окрашивается в цвет красного вина, затем растворитель выпаривают, получая 12,4 г красного масла (92,4% после регенерации). Масло (9,0 г) хроматографируют на силикагеле, элюируя циклогексаном/этилацетатом в соотношении 60%/40%, получая фракции по 60 мл. Фракции 45-63 представляют собой чи тый Оf0-ди(м-толил)-N-фосфонометилглицинони4-рил. Фракции 28-40 из колонны выпаривают в вакууме, получая белый твердый продукт, т.пл, 113114°С, который определяют как N,Nметилен-бис-0,0-ди(м-толил)-N-фосфо нометилглицинонитрил, Найдено,: С 62,58; Н 5,72; N 8,23, Вычислено,%: С 62,50 Н 5,69; Ы 8,32. Пример 3, Ди(п-метилтиофенил)фосфит (30,4 г, 0,082 моль) и 1,3,, 5-трицианометилгексагидро-1,3,5 триазин (5,6 г, 0,) нагревают до в течение 1 ч.Полученн му темному красно-коричневому маслу дают охладиться до комнатной темпер туры и растворяют затем в тетрахлор тане (200 мл). Этот раствор добавля к силикагелю (30 г), перемешивают и фильтруют, затем снова добавляютк силикагелю (20 г) с перемешиванием и фильтрацией. Половину полученного раствора за счет адгезии сцепляют с силикагелем (12,5 г) и затем хроматографируют на силикагеле (450 г), элюируя циклогексаном/этилацетатом .в соотношении 60%/40% (фракции по 60 мл). ФраКции 28-39 соединяют, по лучая 1,2 г N,Ы-метилен бис- О,0-ди -(п-метилтиофенил)-Н фосфонометилглицинонитрила п 1,6151. П р. и м е р 4. Дифенилфосфит (234 г, 1,0 моль) добавляют в ацето нитрильный раствор (300 мл) 1,3,5-трицианометилгексагидро-1,3,5 триазина (63 г, 0,333 моль),.нагревая 3 ч при 75-82с. Раствор охлаждают и концентрируют в вакууме, получая черное масло, по составу глaвны 1 об разом глицинонитрил. Пробе этого масла (101 г) дают з счет адгезии пристать к растворенно му в хлороформе силикагелю с добавлением дополнительного количества с ликагеля и выпаркой растворителя, после чего этот продукт хроматографируют на силикагеле (1,1 кг), элюи руя хлороформом (фракции по 1 л). Фракции 13-14 соединяют, концентрируют и перекристаллизовывают из дихл9Рметанциклогексана сполучением 5i г О,0-дифeнил-N-фocфoнoмeтилглицинонитрила. Фракции 11-12 соединяют, концент рируют с получением масла, удаляя фильтрацией твердый продукт. Маточный раствор от фракций 11-12 хромато графируют на силикагеле (760 г), элю ируя циклогексаном/этилацетатом в соотношении 60%/40% (фракции по юо мл). Фракции 40-49 соединяют и перекристаллизовывают из холодного тетрахлорметана, получая Ы,Ы-ме1;иле -бис-(О,0-дифенил-Ы-фосфонометилглицинонитрил), т.пл. 98-99 С. Найдено,%: С 60-59; Н 4,79; N 8,97. Вычислено,%; С 60,39; Н 4,90; N 9,09. Пример 5. Смесь 0,0-дифенил-N-фосфонометилглицинонитрила(78,05 г, 0,258 моль) и 2,6-диэтилфенилазометина (21,06 г, 0,129 моль) помещают в перегонный аппарат ( с трубкой с шаровым расширением с каталитическим количеством (около 10 мг) метилата натрия. Смесь нагревают около 1 ч в вакууме при 65-75°С/0,02-0,07 мм рт.ст. Процесс перегонки 2,6-диэтиланилина начинается почти сразу и продолжается почти 1 ч. Вакуум сбрасывают, затем добавляют тетрахлорметан (500 мл) до кристаллизации масла. Горячий раствор фильтруют,- давая ему затем отгладиться до комнатной температуры. Тверда1й продукт собирают и промывают холодньм тетрахлорметаном, маточный раствор концентрируют, получая твердый продукт, который соединяют с прежним, получая общее количество 72,5 г. Продукт определяют как N,Nметилен-бис-(О,О-дифенил-М-фосфонометилглицинонитрйл), т. пл. 100 100,50с. Пример 6. Получают смесь 0,0-ди (п-метоксифенил)-N-фосфонометилглицинонитрила , (7,4 г, 0,02.моль) и 2,6 диэтилфенилазометина (1,63 г, 0,01 моль), затем протекает экзотермическая реакция. По истечении приблизительно получаса смесь помещают в выпарной аппарат с трубкой с шарообразным расширением, нагревая в вакууме около получаса при 6070с/0,1 км рт. ст. с перегонкой 2,6-диэтиланилина, Оставшийся продукт охлаждают, перемешивают и растворяют в горячем тетрахлорметане. Раствор фильтруют, после чего к полученному маслу добавляют эфир, затем дважды сливают. К маслу добавляют хлороформ, после чего концентрированием полу-, чают продукт, определяемый как N N-метилен-бис- 0,0-ди-(п-метоксифенил) -N-фосфонометилглицинонитрил в виде рыжевато-коричневых призм, т. пл. 90- 92°С. Найдено,%: С 57,06; Н 5,22; N 7,63, С 57,07; Н 20; Вычислено, %; N 7,61. Пример 7. Получают смесь О,0-ди-(4-хлор-З-метилфенил)-N-фосфонометилглицинонитрила (2,8 г, 0,007 моль) и 2,6 диэтилфенилазометина (0,57 г, 0,0035 моль), происходит слегка экзотермическая реакция. Смесь помещают в перегонный аппарат (с трубкой с шаровидным расширением) и нагревают при 75-80°С/0,1 мм рт.ст. около получаса; при этом перегоняется 2,б-дизтиланилин, Полученное мас лс охлаждают и кристаллизуют из тетраклорметана/метилциклогексана, получая белый твердый продукт. Его определяют как Ы,Ы-метилен-бис О,0-ди-(4-хлор-З-метилфенил)-N-фосфонометилглицинонитрил, т.пл. 89,5 90f5 C,
Найдено,%s С 51,77; Н 4,25; N 7,01.
Вычислено,: С 51,87; Н 4,23 N 6,91.
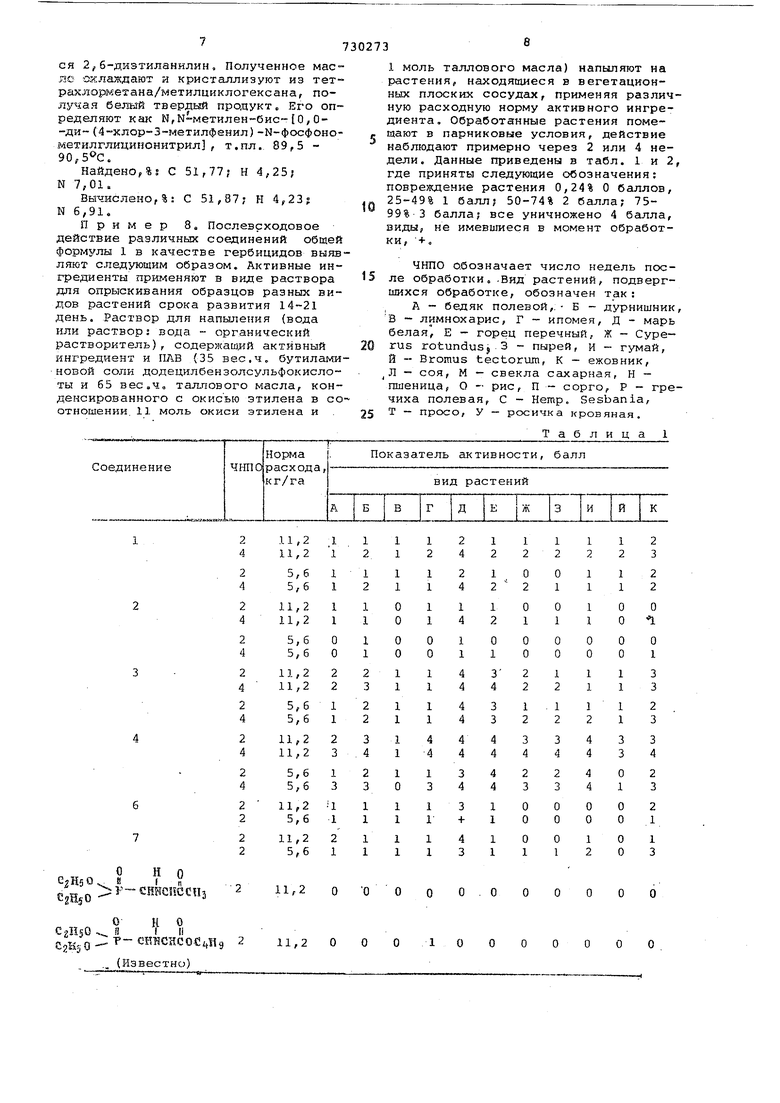
Пример 8. Послевсходовое действие различных соединений общей формулы 1 в качестве гербицидов выявляют следующим образом. Активные ингредиенты применяют в виде раствора для опрыскивания образцов разных видов растений срока развития 14-21 день. Раствор для напыления (вода или раствор; вода - органический растворитель), содержашяй активный ингредиент и ПАВ (35 вес,ч, бутиламиновой соли додецилбензолсульфокислоты и 65 вес.ч, таллового масла, конденсированного с окисью этилена в соотношении. 11 моль окиси этилена и
1 моль таллового масла) напыляют на растения, находящиеся в вегетационных плоских сосудах, применяя различную расходную норму активного ингредиента. Обработанные растения помещают в парниковые условия, действие наблюдают примерно через 2 или 4 недели. Данные приведены в табл. 1 и 2, где приняты следующие обозначения: повреждение растения 0,24% О баллов, 25-49% 1 балл; 50-74% 2 балла; 7599% 3 балла; все уничножено 4 балла, виды, не имевшиеся в момент обработки, + :
ЧНПО обозначает число недель после обработки. .Вид растений, подвергшихся обработке, обозначен так:
А - бедяк полевой,:- Б - дурнишник
В - лимнохарис, Г ипомея, д - марь белая, Е - горец перечный, Ж - Суреrus rotundusj 3 - пырей, и - гумай, И - Bromus tectorvun, к - ежовник,
Л - соя, М - свекла сахарная, Н - пшеница, О - рис, П - сорго, Р гречиха полевая, С - Hemp. Sesbania, Т - просо, У - рсх:ичка кровяная.
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения диариловых эфиров -фосфонометилглицинонитрила или их солей | 1978 |
|
SU704457A3 |
| Гербицидный состав | 1977 |
|
SU810066A3 |
| СТАБИЛИЗИРОВАННАЯ ПОЛИМЕРНАЯ КОМПОЗИЦИЯ, СТАБИЛИЗАТОР, ВХОДЯЩИЙ В ЕЕ СОСТАВ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2230758C2 |
| КОМПОЗИЦИЯ ДЛЯ ПОКРЫТИЯ | 1992 |
|
RU2107704C1 |
| ГИДРОКСИЗАМЕЩЕННЫЕ СТЕРИЧЕСКИ ЗАТРУДНЕННЫЕ N-АЛКОКСИАМИНЫ | 2000 |
|
RU2243216C2 |
| ГИДРОКСИФЕНИЛТРИАЗИНЫ, СОДЕРЖАЩИЕ АРОМАТИЧЕСКУЮ КАРБОЦИКЛИЧЕСКУЮ КОНДЕНСИРОВАННУЮ КОЛЬЦЕВУЮ СИСТЕМУ | 2006 |
|
RU2418791C2 |
| ЗАМЕШЕННЫЕ БЕНЗОТРИАЗОЛЫ И СТАБИЛИЗИРОВАННАЯ КОМПОЗИЦИЯ И ПОКРЫВНАЯ СИСТЕМА, ИХ СОДЕРЖАНИЯ | 1992 |
|
RU2126393C1 |
| ПРОИЗВОДНОЕ ПИПЕРИДИНА | 1992 |
|
RU2062777C1 |
| ЗАМЕЩЕННЫЕ БЕНЗОТРИАЗОЛЫ, СТАБИЛИЗИРОВАННЫЕ КОМПОЗИЦИИ И ПОКРЫВНАЯ СИСТЕМА | 1992 |
|
RU2127264C1 |
| N-МЕТИЛИРОВАННЫЙ БИС-4-ПИПЕРИДИЛФОСФИТ И СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ, СТОЙКОЙ К ОКИСЛИТЕЛЬНОМУ, ТЕРМИЧЕСКОМУ И СВЕТОВОМУ ВОЗДЕЙСТВИЮ | 1992 |
|
RU2086557C1 |

О
п
С2Н50 3
11,2
О Н о
CzKsO .8 li
р- СНБСНСОС ИЗ с 2% О
., (Известно)
О О
Гербицидный состав, содержащий действующее начало на основе произеодных фосфонометилглицина и добавки, выбранные из группы носитель, разбавитель и наполнитель, о т л и чающийс я тем, что, с целью усиления гербицидного действия, он содержит в качестве производного фосфонометилглицина соединение общей формулы
Таблица 2
где R - , фенил, замещенный однократно метилом, метокси, метилтио, или 3,4-диметилфенил, 4-хлор-3-метилфенил,
в количестве 5-95 вес.ч.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1980-04-25—Публикация
1977-11-18—Подача