37
с соответствующими фенолятами в среде диметплсульфоксида при 1ОО-11О С.
Эпоксиды формулы 1 (А и Б воюетеэпоксисиое кольцо) и гидрохлориды формуЛЬ г (А - хлор; Б - водород) получают эпоксидированием или гидррхлорированием соответствующего ненасыщенного соединения формулы I (А и Б вместе - углерод-углеродная связь).
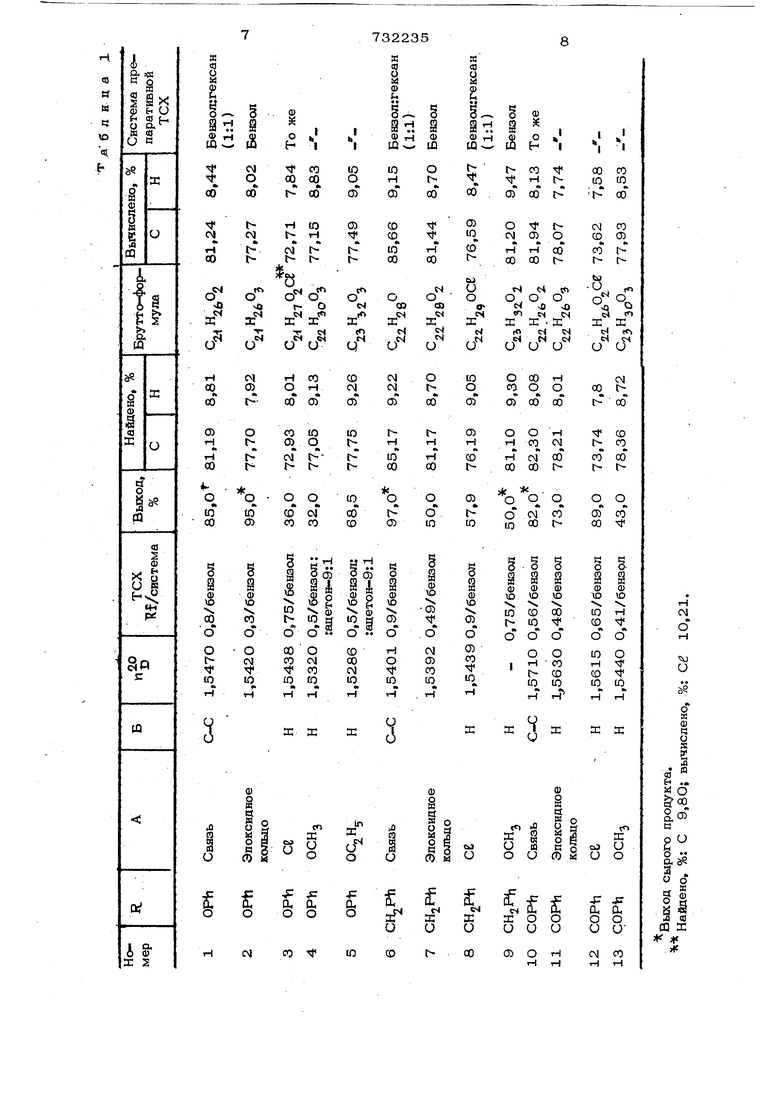
Показатели синтезированных соединений формулы I приведены в табл. 1,
Биологические испытания соединения формулы I и известного соединения 111 на комарахA&des показали.что наиболее активным является соединение формулы 1, (гда А - хлор, Б - водород, R ), пр1-1чем его активность выше активности эталона. Соединения формулы I (где А и Б вместе - эпоксидное кольцо, F - OCgHgj А - хлор, Б водброд, R - А - ОСНд, Б - водород,;
- . А - Б водород,. , R - А - , Б - водород, R CHoQHg) показали активность, равную активности эталонов. Остальные соединения не активны или мало активны.
П р и.м е р 1, К раствору 1,04 г (О,О26 моль) порошкообразного едкого натра в 9 мл диметилсульфоксида прибавляют 5,58 г (0,ОЗ моль) 4-оксидифени-. лового эфира, реакционную массу перемешивают в течение 1 ч при ЮСРС и при ливают 3,22 г (О,О2 моль) хлорида формулы Е (А и Б - вместе - углерод-уг леродная связь) при этой же температуре, перемешивают в течение 1,5 ч, охлаждают до комнатной температуры, реакционную массу разбавляют водой и экстрагируют эфиром. Эфирный раствор промывалот водой, 2 н, раствором едкого натра и сушат над хлористым кальцием. Эфир отгоняют, и получают 5,3 г (85%) соединения формулы Г (А и Б вместе - углерод-углеродаая связь, R - ), Аналитический образец получают препаративной тонкослойной хроматографией (ТСХ) на кремниевой кислоте,I
ИК-спектр, 1590, 15ОО, 1250, 1ОЗО,
Аналогично получают соединения формулы 1, где:
А и Б вместе - углерод-углеродная связь, Р - , из хлорида формулы If (А и Б вместе - углерод-углеродная связь) и ц бензилфенола, ИК-спектр, : 1590, 15ОО, 125О, 1ОЗО;
А и Б вместе - углерод-углеродная связь, R - , из хлорида форму-2235 4
лы 1 (А и Б вместе - углероо-углеродлая связь) и п- бензоилфепола,- ИК-спектр, смГ :166О, 1600, 1580, 1250, 103О;
А - OCh, Б - водороя, R - , 5 из хлорида формулы Ц (А ОСИ,, Б - водород) и 4-70КСИдифенилового эфира, ИКспектр, см : 283О, 1590, 1500, 1250, 103О.
А - , Б - водород, R ., 10 из хлорида формулы И (А - ОС2Нс, Б водород) и 4-оксидифенилового эфира, ИК спектр, 159О, 150О, 1250, 103О;
А - ОСИ, Б - водород, R - , 15 из хлорида формулы Ц (А - ССН, Б водород) и п-бензтфенола, ИК-спектр 2830, 1590, 1500, 1250, 1030;
А оснз, вадород. R - ,
из хлорида формулы Ц (А - ОСНд, Б - во20 дород) и п-бензоилфенола, ИК-спектр, см: 283О, 1590, 1660, 150О, 1250, ЮЗО. П р и м е р 2, Через раствор 0,5 г соединения формулы I (А и Б вместе - углерод-углеродная связь, R - ) в
10 мл абсолютного спирта при пропускают сухой- хлористый, водород до полного насьпцения. Затем добавляют пятикратный объем воды и экстрагируют эфиром, эфирный экстракт, промывают водой
30 и сушат над сульфатом магния. Эфир отгоняют и получают 0,5 г сьфого продукта формулы 1 (А ™ хлор, Б - водород, R ,ОС Н g-), Аналитический образец получают препаративной ТСХ на кремниевой кисло35 те, ИК-спектр, см: 1590, 1500, 1030, 1250.
Соешшения формулы 1 (А - хлор, Б водород, R - CU2C(li и А хлор, Б водород, R-COC Hg) получают аналогично
0 из соедш ений формулы 1 (А и Б вместе углерод-углеродная связь, R - и А и Б вместе - углерод-углерош-шя связь, R - COCgHc) соотве1х;тве1шо. Пример 3,К охлажденной до смеси 1 г (0,О055 моль) соединения формулы 1 (А и Б вместе - углерод-углеродная связь, R - .) в 72 мл ТГФ и 48 мл воды прибавляют порциями в течение 30 мин 1,08 г (0,ОО6 моль) N-бромсукцинимидаи перемешивают в течение 45 мин. Затем реакционную массу экстрагируют эфиром, эфирные экстракты промывают 1%-ным раствором соляной кислоты, водой и сушат над сульфатом нат рия. Растворитель отгоняют в вакууме при температуре не выше 30 С, Остаток (1,2 г) растворяют в 20 мл абсолю-гаого спирта и к раствору приливают при О С раствор этилата натрия, приготовленный из 0,15 г (0,0066 моль) натрия и 20 м абсолютного спирта. Смесь перемешивают 3 О мин при О С, затем спрфт отгоняют в вакууме, остаток разбавляют водой (15 мл) и экстрагируют эфиром. Эфирный экстракт промывают водой и сушат над сульфатом натрия. Эфир отгоняют, остаток (о, 7 г) вещества формулы 1 (Аи Б вместе - эпоксидное кольцо, R - очищают препаративный ТСХ на кремниевой кислоте. ИК-спектр, 1595, 1500, 1030, 1250. Соединения формулы 1 (А и Б вместе - эпоксидное кольцо, R - CH«C,Ht. и о D А И Б вместе - эпоксидное кольцо, R ) получают аналогично из соединений формулы 1 (А и Б вместе - углерод-углеродная связь, R - и А и Б вместе-углерос -углероднеш связь, Р - COCfHj) соответственно . Показатели синтезированных соединений формулы I представлены в табл. 1. Пример 4. При испытании на комарах Aedes личинки третьей стадии помещают в растворы различных концентраций (экспозиция - с момента обработки до окукливания). Вещества вводят в воду в 0,1 мл ацетона, для каждой концентрации используют не менее 10О личинок (по 25 в одной повторности). Эффект определяют по числу погибших насекомых, а концентрацию, при которой погибает 7 356 5О% личинок (СК-50) - по линиям регрессии на пробитлографической бумаге. Результаты испытаний приведены в табл. 2. Результаты биологических испытаний на личинках комаров c ecptpt-i показали, что наиболее активным является соецкнение формулы I (А - хлор, Б - водород, R - .) которое по активности превосходит эталоны. Соединения формулы 1 (А и Б вместе - эпоксидное кольцо, R - OCgHg, А - ОСН-З В - врдсрод, R - А - ОСуН, Б - водород, , А - ОСНэ, Б - водород, R - ) показали активность, равную актнвноста эталонов. Предлагаемые соединения могут найти применение в медицине и ветеринарии для борьбы с комарами - переносчиками опасных заболеваний человека и животных. Изучение соединений с ювенильной актавностью, влияющих на метаморфоз насекомых, является новым направлением в химии инсектицидов. Преиму1дество-1изобретешш заключается в возможности синтетического получения соединений с ювенильной актиы1остью, ингибирующйх развитие комаров. Применение соединений форму;лы 1 расширяет асс тиМент гормональных инсектицидов, которыо являются третьим поколением ядохими катов.
9
73223510
Таблица 2



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения дигалогенангидридов 1-бром-2-алкоксиэтенилфосфонистых кислот | 1983 |
|
SU1142479A1 |
| Способ получения -хлоркарбоновых кислот или их производных | 1976 |
|
SU646905A3 |
| Способ получения цис- и транс-изомеров замещенных дигалоидвинилциклопропанкарбоновых кислот или их эфиров | 1976 |
|
SU940644A3 |
| СПОСОБ ПОЛУЧЕНИЯ 3- | 1970 |
|
SU433677A3 |
| Способ полуяения бицикло/2,2,2/ октана | 1975 |
|
SU587856A3 |
| Способ получения производных 9-хлорпростана или их солей | 1980 |
|
SU1026652A3 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕРМОПЛАСТИЧНОГО МАТЕРИАЛА ДЛЯ ЗАПИСИ ИНФОРМАЦИИ | 1966 |
|
SU225015A1 |
| Способ получения -аминосульфенилированных производных 2,3-дигидро-2,2-диметил-7-бензофуранилметилкарбамата | 1974 |
|
SU652893A3 |
| Эфиры или амиды замещенной 3-метил-3-фенилпропен 2-овой кислоты как инсектициды с ювенильной активностью | 1975 |
|
SU681045A1 |

ЖлАЛо/Ч
.4
ЛлААо odgHs
10,083,2
ЛАДА
Не активно
Не ак-гавно
4,521,8
Не актийно
11
... .v732-2354,:: ,12
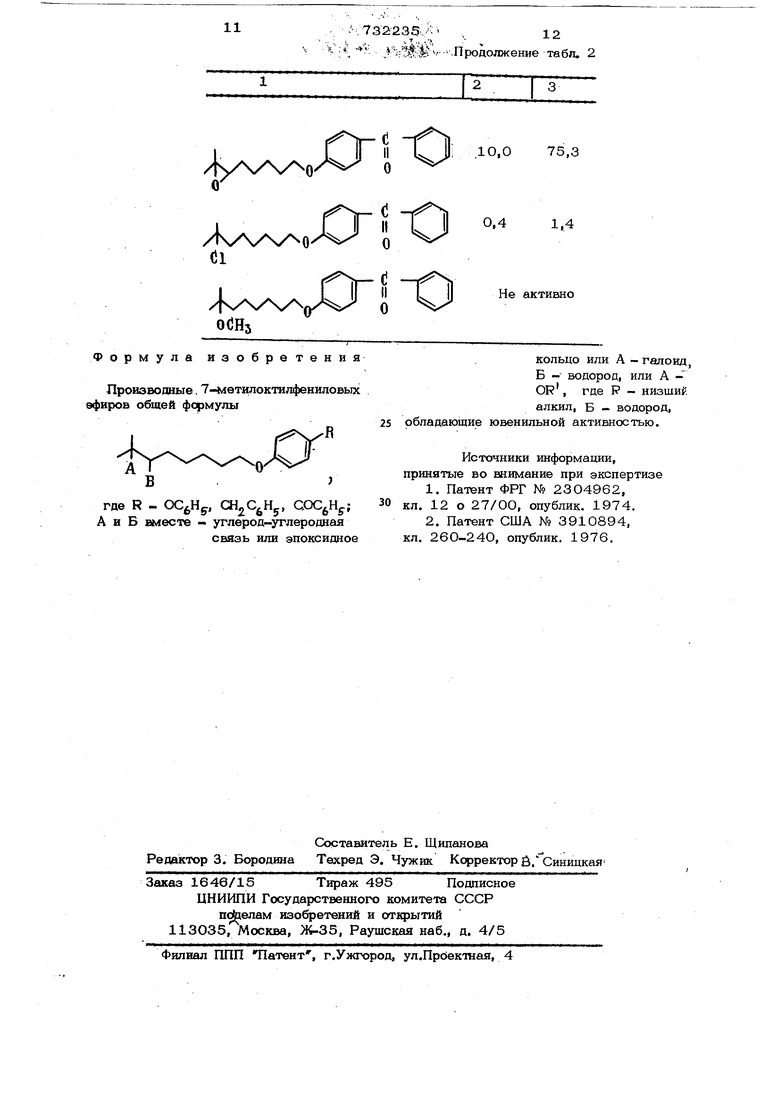
. - -.Продолжение та б л. 2
,10,075,3
1 0.41,4
Не активно
Формула изобретения
Производные, 7-метилоктилфениловьпс эфирен общей формулы
В
6
где R - , , А и Б вместе - углерод-углеродная
связь или эпоксидное
кольцо или А - галоид Б - водород, или А OR , где R - низшик алкил, Б - водород, обладающие ювеиильной активностью.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1980-05-05—Публикация
1977-08-30—Подача