(54) СПОСОБ ПОЛУЧЕНИЯ -АЦЕТИЛЕНОВЫХ СПИРТОВ:



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 3-пропенил-7- @ 2-(2-аминотиазолил-4)-2-гидроксииминоацетамидо @ -3-цефем-4-карбоновой кислоты или ее сложных эфиров в виде Z- или Е-изомеров или их смесей | 1986 |
|
SU1428204A3 |
| Способ получения 2,6-диэтинилпиперазинов | 1973 |
|
SU492518A1 |
| Способ получения -аминоенонов | 1977 |
|
SU730681A1 |
| Способ получения 3-тиовинилцефалоспоринов | 1981 |
|
SU1160936A3 |
| Способ получения производных 2-(тиенил-2)- или 2-(тиенил-3) этиламина | 1982 |
|
SU1148563A3 |
| Способ получения алкоксиизоксазолидинов | 1986 |
|
SU1384586A1 |
| Способ получения производных дигидропиридина (его варианты) | 1983 |
|
SU1258324A3 |
| Способ получения производных 2-(тиенил-2)- или 2-(тиенил-3) этиламина | 1982 |
|
SU1145930A3 |
| Способ получения производных 3-аминовинилцефалоспорина | 1980 |
|
SU1031409A3 |
| Способ получения диэфиров гидрохинона | 1981 |
|
SU1109048A3 |

1
Из обретение относится к способу получения р -ацетиленовых спиртов, которые находят применение в синтезе гормоноподобных веществ, используемых в фармацевтической промлшленности.
Известен способ получения р -ацетиленовых спиртов путем взаимодействия ацетиленидов лития или натрия с л -окисями при температуре (-50) (-40°С) в жидком аммиаке. Выход целевого продукта 5-45% tU.
Недостатком известного .способа является невысокий выход целевогр продукта, а также то обстоятельство, что он может быть использован тольR
R-C-CH-J-CHCR I он
где,есаи К(Нз,, то Н н-«JsH; , CeHj-,
п-(нз-(5е1ч , n- ji-CjH/i- , )
-((IH)2-C- , (з)2- ;сНг-СН2
«(
ко для ацетилена и простейших 4k -окисей, так как растворимость монозамещенных ацетиленидов лития вжидком аммиаке резко уменьшается при использовании вместо ацетилена и ниэ.комолекулярных 1-алкинов, 1-гептина, 1-октина, а также моноацетилёнов с ароматическими заместителями. Поэтому протекание процесса становится
10 гетерогенным, что и приводит к уменьшению выхода.
Цель изобретения - увеличение выхода и расширение ассортимента конечного продукта.15: Поставленная цель достигается способом получения -ацетиленовых спиртов общей форкулы
(1)
сн
WX
2 1
(in-i-dHj
-.V- . ri r: - jy :--fr l-.
,у..3745888,4
или если , то R j
если К Й8Н50-(И2 , , mo )2-(- ,
,(H5)2
««( ,V s/i
млм если , mo , /z-CHj-dgH , n-Cl-dg «4 j
П-(;НзО-(5бН4, Л-(«Н5)2Н -Й6Н4 , ((IHjlj- - (OH3)j(J-, есям B tieHg , R VH , mo , «-CjH
взаимодействием несимметричных Ы -ок .сей общей формулы- .
)(;. (0)
R оi
где R и R
имеют вышеприведенные знчения,
с соответствующим ацетиленидом лития в среде растворителя с посэтедуюьщм выделением целевого продукта, отличительная особенность которого состоит в том, что в качестве растворителя используют смесь гёксаметанол «еязол и процесс ведут при температуре 0-250С.
Выход целевого продукта 50-85% от .теории.-, .
В отличие от-известного способа рёёкцйя протекает в гомогенной среде S мягких уело&иях..--
Предлбженный способ отличается уШвёрсальностью и позволяет вводить в реакцию несимметричнозамещёнчые . .с -Окиси и алкины разнообразного строения, увеличить выход целевого продукта, а также, наряду с известными, получить и .новые соединения.
Изобретение-иллюстрируетсМйрЙйерами.
Пример . Получение 1,4-дифенил-З-бутин-1-ола.
Д 50 МП абсолютного бензола добавляют 1,4 г металлического лития, зарезанного в виде мелкой стружки. Систему продувают током сухого аргона. После этого в колбу доба вЛяют 70 МП гексаметапола. Через 5-10 мин перемешивания начинается растворение лития в гексаметаполе, сопровождающееся разогреванием реакционной
. -. ; - ; .;.--;--- - :---:-;:;
После полного растворения лития (2-4 ч), добавляют раствор 10,2 г фенилацетилейа в 20 мп бензола. Реакционную смесь перемешивают 5 ч при комнатной температуре, затем оставляют на ночь. Полученный раствор ацетиленида лития охлаждают льдом и к нему по каплям добавляют раствор 11,6 г окиси стирола в 10 мп абсолютного бензола. Реакционную смесь перемешивают 3 ч и оставляют .Йа следующий день реакционную смесь выливают на лед. Водный слой экстрагируют эфиром, эфирные
W(5H5)2
вытяжки и Основной органический слой прогнивают водой для удаления гекса- метапола и сушат безводным сульфатом магния. Эфир и бензол отгоняют из колбы с дефлегматором.
Остаток вносят в хроматографическую колонку. Параметры колонки:
0 100 см X 3 см, давление на входе 90 г/см, адсорбент - силикагелЬ с величиной зерна 40-100 мкм, злюент: диэтиловый Эфир-гексан с постепенно увеличивающимся содержанием эфира. После одной перекристаллизации из смеси пентан-эфир 20:1 получают 11,78 г (53% от теоретического) продукта, т. пл. 57,5°С.
СпеКтр ПМР, 10%-ный раствор в ССР спектрометр Varian, lOO МГц, сигнал, химический сдвиг (м.д.в шкале d) , количество протонов по интегральнрй кривой, константа спин-спинового йзаимодействия (в гц) ; (отнесение) : дублет 2,71, 2Н J 6,2 ( - СН,- ); синглет 2,87, 1Н (ОН), триплет 4,77, 1Н, J 6,2; (-(JH-) ; мупь-гиттет 7,2,(-)Н), (2-CgH). ПМР-спектр полностью соответствует предполагаемой структуре. ..
. Для доказательства химического окружения гидроксила снят ПМР-спектр в диметилсульфоксиде (ДМСО) 10%-ный раствор : квартет 4,80 1Н, J б гц (-in-); дублет, 5,56, IH, J б гц
5 (-ОН), (так какв ДМСО не снимается спин-спиновое взаимодействие через кислород, то наличие дубЛета свидетельствует О структуре вторичного спирта).Пример 2. Получение 2-метил-5-мётил-4-пентин-2-ола.
Синтез проводят в условиях, ансшогичных примеру 1, с тем же соотношением реагирующих веществ и растворителей, на iO,2 г фенилацетилена берут 7,2 г окиси изобутилена. Выход 10,6 г (60% от теории), т. пл. . ПМР-спектр, 10%-ный раствор в ССРд, 100 Мгц: синглет 1,28, 6Н, (-Cf ; синглет 2,34; 1Н, (-ОН); синглет
0 2,47, 2Н, (-СН-); мультиплет 7,2, 5Н, (-CgHj).
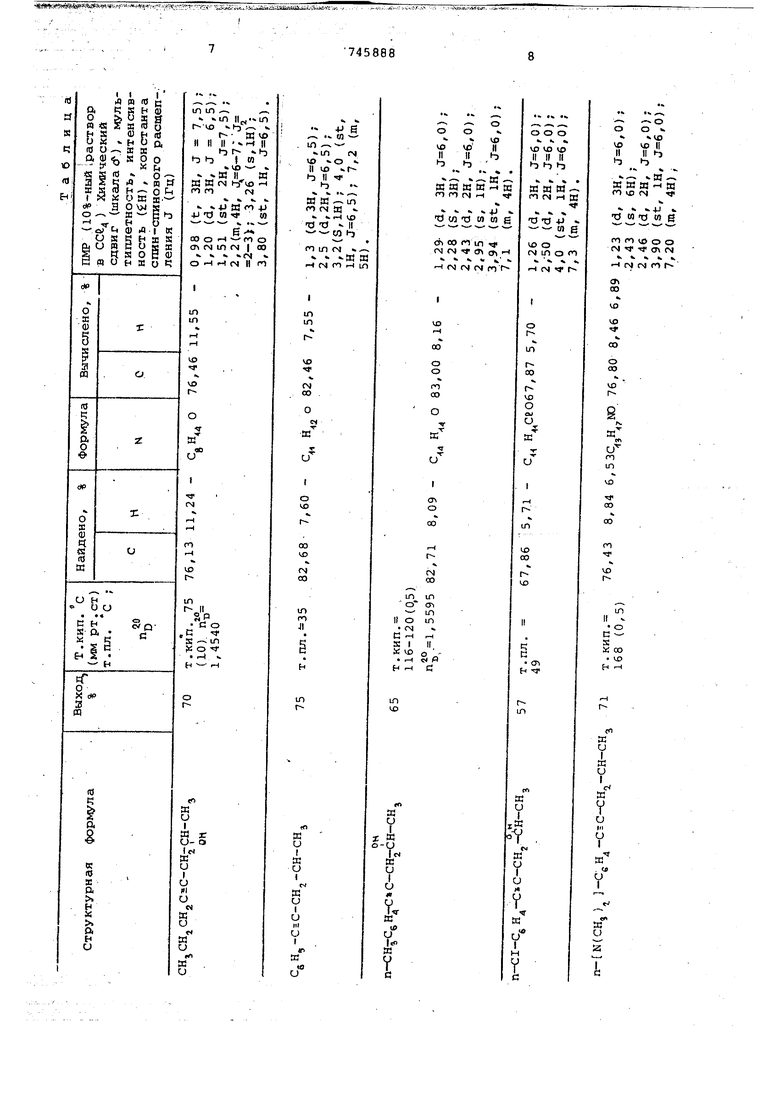
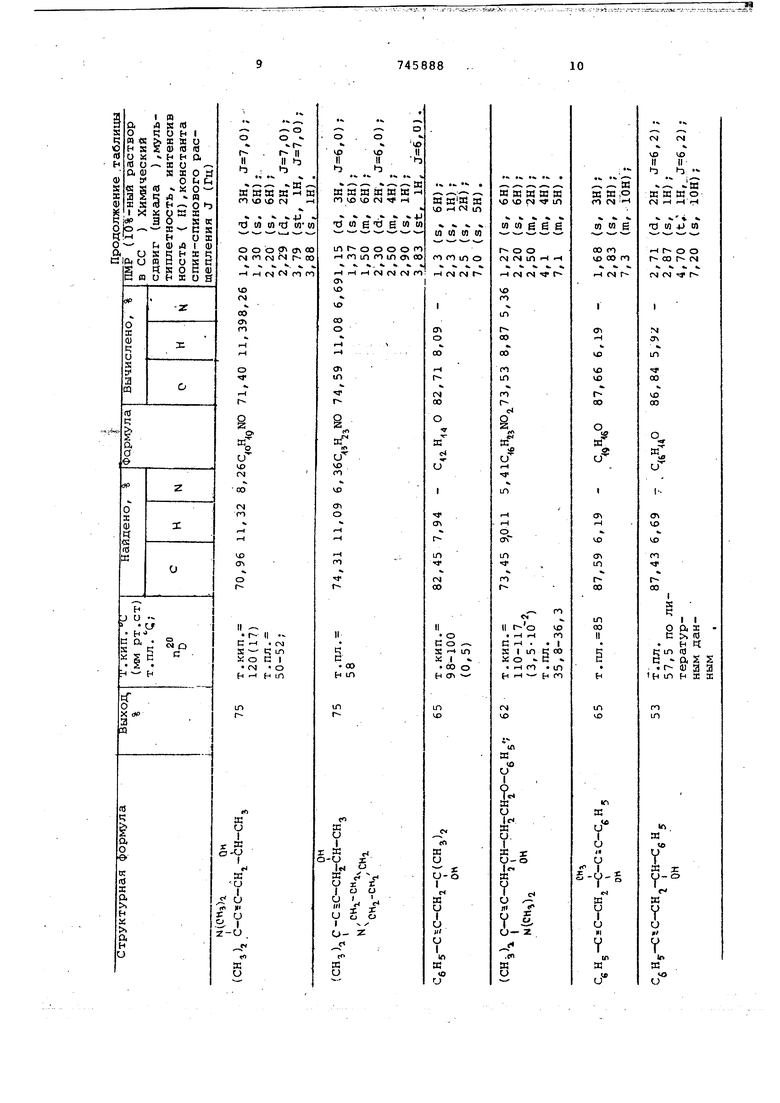
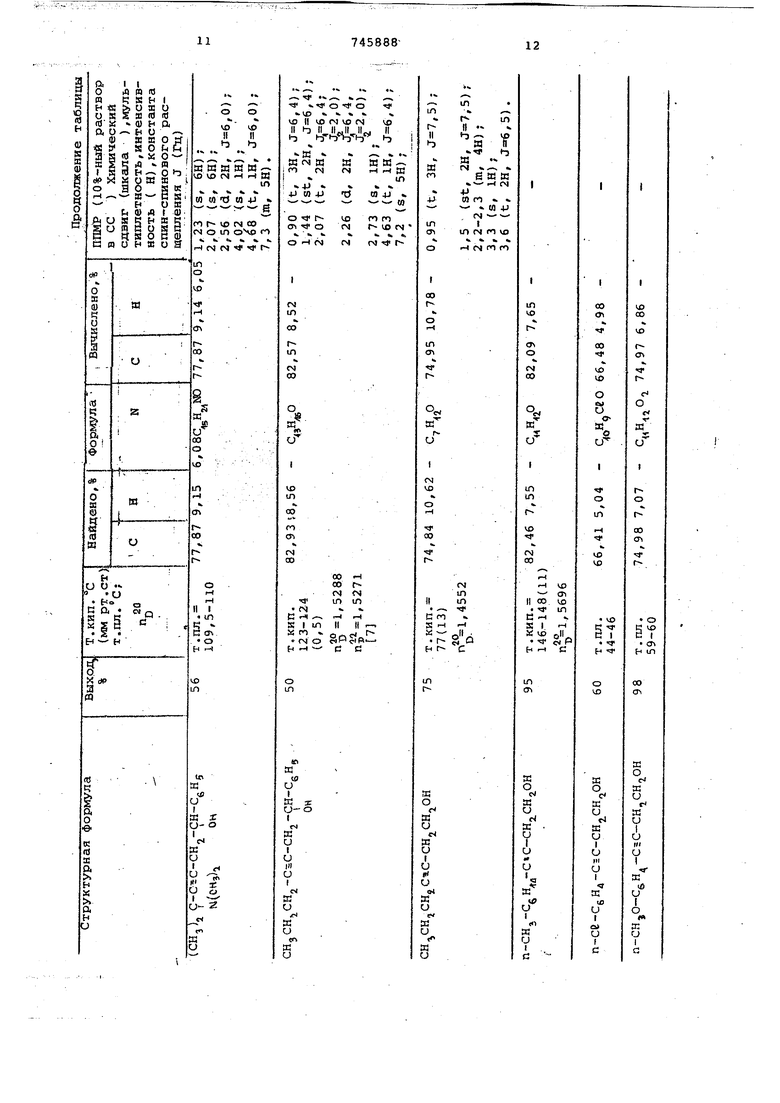
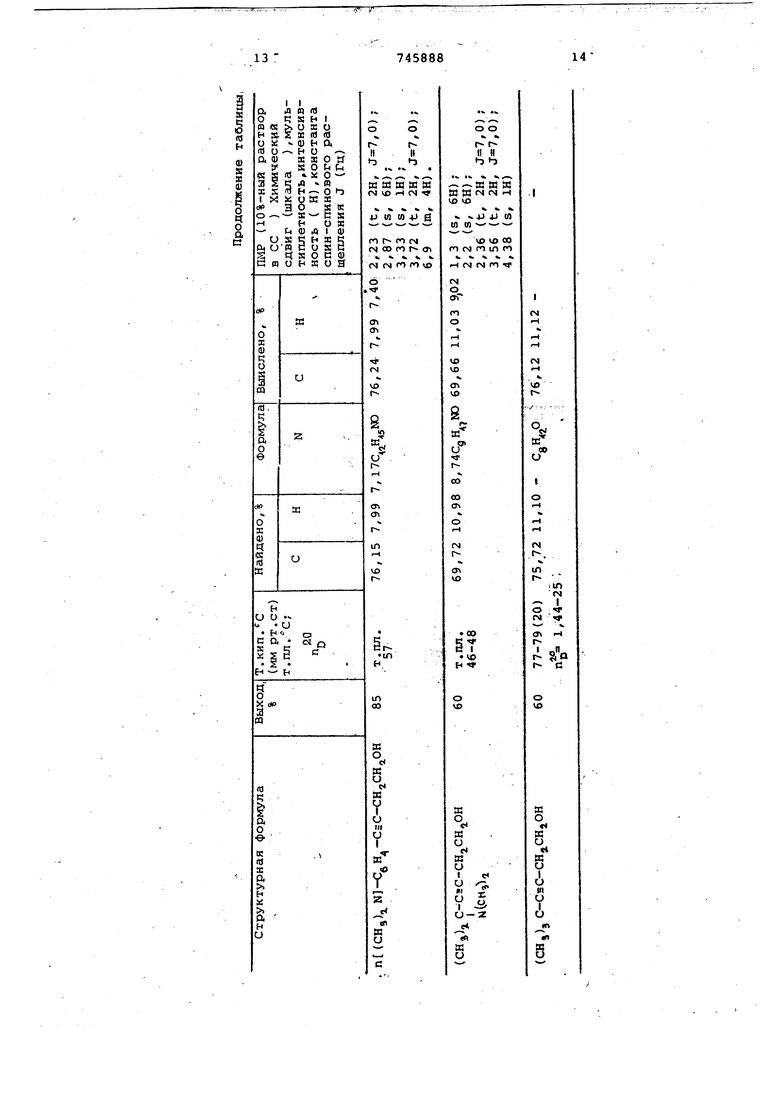
В 10%-ном растворе ДМСО гидроксильный протон не расщеплен, синглет 5 /б м.д. (шкапам), ПМР-спектр полностью соответствует предполагаемой структуре указанного выше соединения. Пример 3. Получение 1-фенокси-б-диметиламино-6-аметил-4-гептин-2-ола. I Синтез проводят в условиях, аналогичных примеру 1, с тем же соотношением реагирующих веществ и растворителей, на 16,7 г 3-диметиламино-З-метил-1-бутина берут 22,5 г фенилглицидилового эфира. Выделение целевого продукта аналогично примеру 1. Получают 16,2 г (62% от теори т. кип. ИО-111°С (3, рт.ст т. пл. . Вычислено для Hjj NO , % С 73,53 Н 8,87; N 5,36%. . Найдено, %: С 73,45 Н 9,11; N 5,41. ПМР-спектр, 10%-ныЙ раствор в ССе ; синглет 1,23, 6Н (-СНд), сйнглет 2,2, 6Н (N-CH,) , дублет 2,5, 2Н (-СН, -С5С) , ;Й 6,0 ГЦ, синглет 4.02,1Н (ОН-), квинтет 4,1 1Н (-СН-) J 6,0, дублет 4,2; 2Н, (-CH,); J 6,0 ГЦ, мультиплет 7.3,5Н (-CgH,). 10%-1-ный раствор в ДМСО: гидроксильный протон расщеплен в дублет 5,2 м.д. (шкала cf ). П№-спектр йолностью соответст- , вует предполагаемой структуре указанного выше соединения. Остальные соединения получают аналогично. В таблице приведен выход, физические константы, результаты элементного анализа и ПМР-характеристики полученных ацетиленовых спиртов. Приняты следующие сокращения ПМР мультиплетность Ъинглет - S, дублет - иг триплет - t, секстетSt, мультнплет - т. Константа спинспинового расщепления - J (Гц),
745888
Формула изобретения
Способ получения -ацетилено спиртов общей формулы
R.
(JH2-(J.CR
(Г) ОН
где, еЫи.Р «CH, , то CfeHj-, n-Ch,-CeH, ,, п(СНд), (CH,)-G- .
Н-(СНз)2
(СН.), -Сили если
I Лн
I .СЩ-ЙН
2v
СН, 1Г
Cftj-dHjR R CH4, ТО R-CfHg, или если R CgH5-0-CH, , то R(CH,)-C
I
CH CHjCH,,,-, или если , то
,H, п СН5-СвН4г п се-СвН4, n CHjO-CgH4, п(СНз) N -CgH4,
(CH,)j-C- , (CH)j-C- ,
м(,
или если , , то ,
взаимодействием несимметричных «А-окисей общей формулы
R,
1
и и 2 (П)
V ,|Х
где R и R имеют приведенные выше значения, с соответствующим ацетиленидом лития в среде растворителя, с последующим выделением целевого продукта, отличающийся тем, что, с целью увеличений выхода и расширения ассортимента конечного продукта, в качестве растворителя исползуют смесь гексаметапол - бензол и процесс ведут при температуре
Источники информации, принятые во внимание при экспертизе
1, Шостакйвский М.Ф, и др. ЖОХ, 35, 809, (1965) (прототип), ч
Авторы
Даты
1980-07-05—Публикация
1977-12-27—Подача