Непосредственное получение диаммоний фосфата в твердом виде наталкивается на большие трудности, так как соль эта отличается значительной растворимостью, в сравнении с мало растворимым моно- и особенно три-аммонийфосфатом, и может существовать при ограниченных условиях. Другое неудобство заключается в том, что при нагревании его растворов отщепляются значительные количества аммиака. Кроме того, при непосредственном получении этой соли она всегда бывает более или менее, смотря по условиям работы, загрязнена примесью моно- или три-аммонийфосфата. Поэтому для получения чистого диаммонийфосфата обыкновенно предпочитают переход через легко кристаллизующийся три-аммонийфосфат, который путем осторожного нагревания может быть без труда переведен в диаммониевую соль.
Изобретатели нашли, что аммонийфосфат, практически свободный от вышеуказанных примесей, может быть получен и прямым путем, если проводить нейтрализацию таким образом, чтобы на 1 молекулу фосфорной кислоты все время приходилось 1,5-2 молекулы аммиака. Целесообразнее всего исходить из насыщенного при обыкновенной температуре раствора чистого диаммонийфосфата. В этот раствор вливают сначала, при энергичном размешивании, столько, по возможности концентрированной, фосфорной кислоты, чтобы отношение молекулярных весов достигало 1:1,5. Затем вводят одновременно концентрированную фосфорную кислоту и газообразный аммиак, соблюдая отношение молекулярных весов 1:1,5, чтобы выдержать указанное отношение компонентов в растворе и не перейти на сторону более кислых растворов. Наконец, производят охлаждение до обыкновенной температуры, пропуская одновременно газообразный аммиак или вслед за этим, пока отношение молекулярных весов достигнет 1:2. При этом осаждается, в виде чистого диаммонийфосфата, почти вся взятая в работу фосфорная кислота.
Для установления необходимых для правильной работы границ молекулярных отношений можно воспользоваться методом титрования с подходящими индикаторами или электрическим методом.
Пример 1. В насыщенный на холоду раствор диаммонийфосфата, дающий нейтральную реакцию с крезоловой красной и содержащий в 1 куб. м воды около 630 кг фосфата, вливают сначала, 66%-ную фосфорную кислоту до тех пор, пока раствор не станет давать окраску от бромкрезолпурпура; для достижения этой окраски требуется обыкновенно на 1 куб. м раствора около 240 кг названной кислоты. Затем вводят одновременно газообразный аммиак и фосфорную кислоту в количествах, соответствующих отношению молекулярных весов 1,5:1. Правильное отношение количеств этих реагентов можно контролировать следующим способом: время от времени отбирают пробу, и, если необходимо, разбавив и охладив ее, испытывают на окраску бромкрезолпурпуром. Хотя самый раствор, вследствие значительной теплоты нейтрализации, и разогревается очень сильно, с испарением воды, введенной с фосфорной кислотой, но при этом не происходит потери аммиака. Чтобы избежать также испарения больших количеств воды, целесообразно поддерживать температуру не выше 80-90°. Прибавив на каждый куб. м основного раствора 150 кг аммиачного газа и еще 880 кг фосфорной кислоты или кратное этих количеств, производят постепенное охлаждение до обыкновенной температуры, а затем вводят вновь аммиачный газ до тех пор, пока раствор опять станет менять окраску с крезоловой красной для этого потребуется аммиачного газа 105 кг или кратное этому количество, в соответствии с примененным для реакции количеством фосфорной кислоты. При этом диамонийфосфат выпадает в количестве, приблизительно эквивалентном количеству израсходованной фосфорной кислоты; он свободен от моно- и три-аммонийфосфата, имеет форму крупных, легко отделяющихся друг от друга кристаллов и, после освобождения от воды и просушки, представляет собой готовый товар. Маточный раствор снова идет в работу, в качестве исходного материала.
Если для указанной работы применяется фосфорная кислота еще большей концентрации, то для достижения 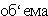 исходного раствора при нейтрализации его производят более значительное охлаждение или прибавляют аммиак частью в виде водного раствора. При пользовании разбавленной фосфорной кислотой избирают для реакции несколько более высокую температуру; можно также для усиления испарения воды устроить добавочную топку. Работа с разбавленным раствором в некоторых случаях предпочтительнее, чем применение более концентрированной фосфорной кислоты, поскольку она получается путем выпаривания, так как при выпаривании отчасти нейтрализованной жидкости не происходит значительного
исходного раствора при нейтрализации его производят более значительное охлаждение или прибавляют аммиак частью в виде водного раствора. При пользовании разбавленной фосфорной кислотой избирают для реакции несколько более высокую температуру; можно также для усиления испарения воды устроить добавочную топку. Работа с разбавленным раствором в некоторых случаях предпочтительнее, чем применение более концентрированной фосфорной кислоты, поскольку она получается путем выпаривания, так как при выпаривании отчасти нейтрализованной жидкости не происходит значительного 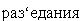 посуды; кроме того, одновременно могут быть выделены примеси и притом потери аммиака весьма незначительны, если выпаривание производится в вакууме. В частности, для испарения воды из растворов не очень слабых достаточно охлаждения в вакууме.
посуды; кроме того, одновременно могут быть выделены примеси и притом потери аммиака весьма незначительны, если выпаривание производится в вакууме. В частности, для испарения воды из растворов не очень слабых достаточно охлаждения в вакууме.
В настоящее время предложено для получения аммиака из аммиак-содержащих газов или паров, например газов коксовых печей, применять растворы фосфорной кислоты или моно-аммонийфосфата и т.п.; в этом случае выкристаллизовывается диаммонийфосфат, который может быть отделен от раствора. Из твердого же аммонийфосфата при нагревании выделяется свободный аммиак. Однако, без соблюдения особых условий, необходимых для существования диаммонийфосфата, продукт этот получается не в чистом виде, а в виде смеси колеблющегося состава, более или менее богатой аммиаком.
Между тем, ранее предложенный способ более прост и легче технически исполним; он дает из аммиака и технической фосфорной кислоты твердый диаммонийфосфат в легко рассыпающейся форме, достаточной чистоты, равномерного состава и притом выдерживающий все аналитические пробы.
При предлагаемом способе получается равномерный продукт, величину зерен которого можно удерживать в любых границах, при чем вода, введенная с фосфорной кислотой, легко может быть удалена выпариванием, без заметной потери аммиака, и, кроме того, может быть использована одновременно и большая часть теплоты, образующейся при этой реакции. Что касается вводимых с фосфорной кислотой посторонних примесей, как, например, железо или фосфат алюминия, то они могут быть легко удалены фильтрацией раствора перед насыщением его аммиаком.
Пример 2. В одну часть раствора диаммонийфосфата, содержащего сернокислый аммоний, т.-е. в маточный щелок, получаемый в конце работы, вливают 2-3 части разбавленной смеси аммиака с фосфорной кислотой; последнюю получают нейтрализацией аммиаком сырой фосфорной кислоты, добытой действием серной кислоты на сырой фосфат и содержащей 20% Н3РО4 и 2% H2SO4; при этом соблюдают отношение молекулярных весов 1:1,5. После нейтрализации кислоты аммиаком, должен быть отфильтрован выделившийся фосфорнокислый алюминий. Указанную смесь диаммонийфосфата с аммиаком и с фосфорной кислотой выпаривают до удельного веса, приблизительно 36° Бомэ, причем на практике не происходит потерь аммиака. Затем, при насыщении аммиаком до отношения молекулярных весов 1:2, охлаждают смесь до обыкновенной температуры и отфильтровывают от выделившейся соли, содержащей около 50-51% Р2О5 и 25,4% NH3, на ряду с некоторым количеством сернокислого аммония. Таким образом, получается вновь исходный щелок, который можно опять вводить в круг работы, так как он свободен от избытка сульфата.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПОЛУЧЕНИЕ ФОСФАТОВ АММОНИЯ | 2013 |
|
RU2632009C2 |
| СПОСОБ КОНТРОЛЯ ПРОИЗВОДСТВА РАСТВОРОВ МОНО- И ДИАММОНИЙФОСФАТОВ | 1991 |
|
RU2006460C1 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ВОДОРАСТВОРИМЫХ УДОБРЕНИЙ | 2003 |
|
RU2228322C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИЩЕВЫХ ФОСФАТОВ АММОНИЯ | 2008 |
|
RU2368567C1 |
| Способ получения жидких комплексных удобрений | 1991 |
|
SU1835399A1 |
| Способ получения удобрения из аммонийфосфатных маточных растворов | 1980 |
|
SU929612A1 |
| СПОСОБ ПОЛУЧЕНИЯ АММОНИЙГИДРООРТОФОСФАТА | 2005 |
|
RU2284292C1 |
| Способ получения кормового диаммонийфосфата | 1986 |
|
SU1433951A1 |
| Способ получения дикальцийфосфата | 1989 |
|
SU1685867A1 |
| Способ получения очищенного моноаммонийфосфата из упаренной экстракционной фосфорной кислоты | 2021 |
|
RU2759434C1 |
1. Способ непосредственного получения твердого диаммонийного фосфата, отличающийся тем, что в насыщенный на холоду раствор диаммонийного фосфата вводят фосфорную кислоту с аммиаком, поддерживая отношение их молекулярных весов между 1:1,5 и 1:2, удаляют выпариванием введенную с фосфорной кислотой воду при отношении молекулярных весов 1:1,5 и, наконец, вводя добавочное количество аммиака до повышения отношения молекулярных весов до 1:2, выделяют на холоду диаммонийный фосфат.
2. Видоизменение способа, описанного в п. 1, отличающееся тем, что маточный щелок, содержащий диаммонийный фосфат, размешивают в течение продолжительного времени с фосфорной кислотой и аммиаком, поддерживая при нагревании молекулярное отношение фосфорной кислоты и аммиака около 1:1,5, удаляют излишнюю воду выпариванием, выделяют часть щелока и охлаждают его с применением вакуума или без него, после чего нейтрализуют аммиаком до молекулярного отношения 1:2 в целях выделения диаммонийного фосфата и возвращения обратно в работу оставшегося маточного щелока.
Авторы
Даты
1929-01-31—Публикация
1926-08-30—Подача