Изобретение относится к способу получения новых производных бензодиазепинона, обладающих ценными фар макологическими свойствами. . Цель изобретения - получение новых, полезных соединений, расширяющих арсенал средств воздействия на живой организм, достигается путем синтеза последних, основанного на известной реакции аминирования галоидалкилов вторичными аминами l. Реакцию обычно осуществляют в индиф
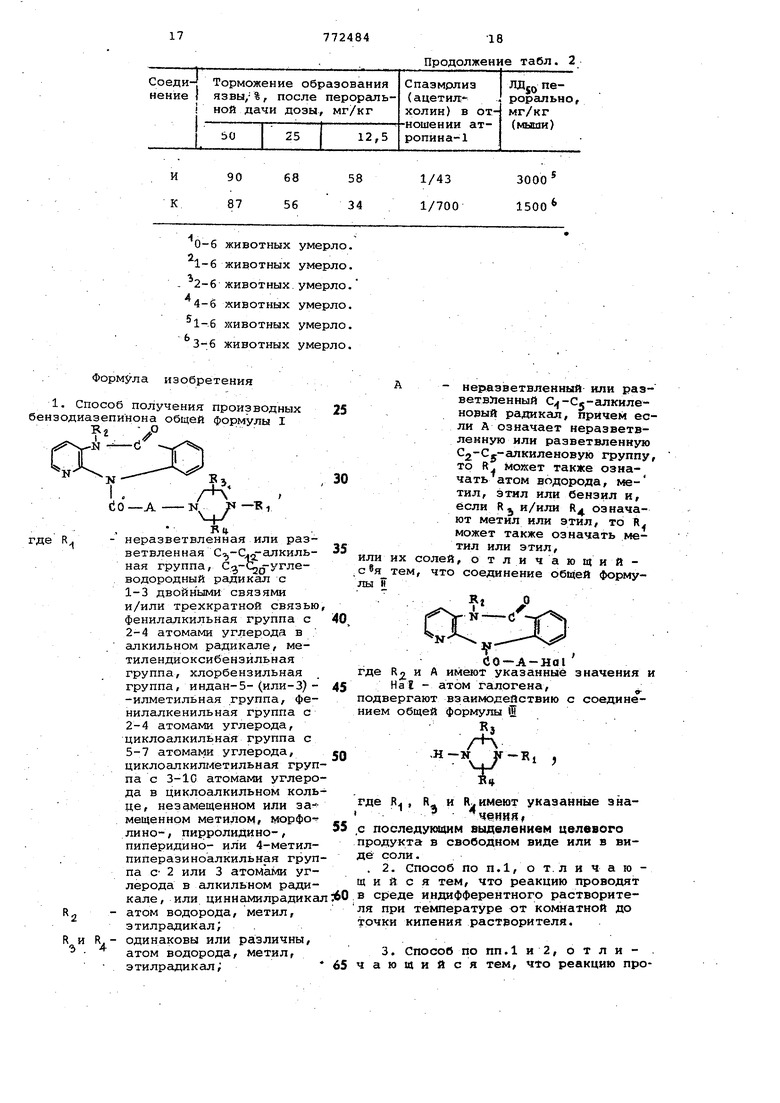
- неразветвленная или разгде R, ветвленная С,и-С 2-алкильная группа, Сэ,-02о-углево- 25 дородный радикал с 1-3 двойными связями и/или трехкратной связью, фенилалкильная группа с 2-4 атомами углерода в алкиль-30
ном радикале, метилендиоксибензильнаяс группа, хлорбензильная группа, индан-5- (или-3) -илметильная группа, фенилалке- нильная группа с 2-4 атомами углерода, циклоалкильная группа с 5-7 атомами ферентном растворителе (спирты, ди.оксан, толуол и другие) в присутст-. ВИИ связывающего галоидводород средства при температуре от комнатной до температуры кипения растворителя. В качестве связывающего галоидводород средства применяют избыток вторичного амина или карбонат или бикарбонат щелочного металла. Предлагается способ получения производных бензодиазепинона общей формулы I углерода, циклоалкилметильная группа с 3-10 ат мами углерода в циклоалкильном кольце,незамещен ном или замещенЕ1ом- метил морфолино-, пирролидинопиперидине- или 4-метилп перазиноалкильная группа с 2 или 3 атомами углеро в алкильном радикале, ил циннамилрадикал; Rj - атом водорода, метил, этилрадикал; RaH одинаковы или различны, атом водорода, метил, эт радикал; А - неразветвленный или разв вленный С.-Сд.-алкиленовы радикал, причем если А о начает неразветвленную ил разветвленную С2 С5--алки леновую группу, то Rj мо жет также означать атом водорода, метил, этил ил бензил и, ecли.R, и/или R означают метил или этил, то R. может также означать метил или этилрадикал, или их солей, заключающейся в том, что соединение общей формулы |Т с о-А-Hal где RgH А имеют указанные значения На - атом галогена, подвергают взаимодействию с соедине(Нием общей формулы Ш Кз ; где R , R,H R имеют указанные значения. Целевой продукт выделяют в свободном состоянии или в виде соли Реакцию предпочтительно проводят Б среде индифферентного растворител при температуре от комнатной до точ кипения растворителя. В качестве ра створителя пригодны спирты, такие как этанол, Н-пропанол, изопропанол кетоны, такие как ацетон, или простые Эфиры, такие как диоксан или тетрагидрофуран, ароматические углеводороды, такие как бензол или толуол. Целесообразно проводить реакцию в присутствии связывающего галоидводород агента, в качестве которого можно применять, например, карбонат или бикарбонат щелочного металла, третичный органический амин, такой как, например,триэталамин, пиридин или диметиланилин, или же избыток соединения формулы ШСоли получают взаимодействием соединения общей формулы I с неорганической или органической к с;лот )Г;, такрй как, например, солянач, Оромистоводородная, серная, фосфорная, винная, фумаровая, лимонная, малеиновая, янтарная или щавелевая. Пример 1. 5,11-Дигидро-11- 4-(2-метилаллил)-1-пиперазинил -ацетил -бН-пиридо 2,З-Ь 1,4 бензодиазепин-б-он. 8,62 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2,З-Ь 1,4 бензодиазепин-б-она, 3,5 г карбоната натрия и 4,6 г 1- (2-метилаллил)-пиперазина в 100 мл абсолютного этанола нагревают с обратным холодильником в течение 2 ч. Отсасывают в горячем состоянии, фильтрат упаривают примерно до 40 мл и охлаждают. Получаемые кристаллы перекристаллизовывают из этанола, добавляя активированный уголь; т.пл. 205-207 0; выход 75% от теоретического. Пример 2. Дигидрохлорид . 5,11-ДИГИДРО-11- I 4-(3-метил-бут-2-енил)-1-пиперазинил -ацетилJ-бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-она. 8,62 г 11-хлорацетил-5,11-дигидро-бТ-1-пиридо 2 , З-Ь 1, 4 бензодиазепин-б-она, 3,5 г карбоната натрия и 5,07 г 1-(З-метилбут-2-енил)-пиперазина (Н -СН2-СН С(СН,,)2 ) в 100 мл изопропанола нагревают с обратным холодильником в течение 2,5 ч. Отсасывают в горячем состоянии, фильтрат упаривают до, 40 мл и охлаждают. Получаемые кристаллы растворяют в 100 мл абсолютного этанола при нагревании и добавляют рассчитанное количёство концентрированной соляной кислоты. При охлаждении выкристаллизовывается Дигидрохлорид; т.пл. 208211°с; выход 70% от теоретического. Пример 3. 5,ll-Дигидpo-ll- 4- (2 , 2-диметилпропил) -1-пиперизинил -ацетил -бН-пиридо 2,,4 бензодиазепин-б-он. 7,15 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2 , 3-ь 1,4 бензодиазепин-б-она, 2,9 г карбоната калия и 4,5 г 1-(2,2-диметилпропил)-пиперазина в 100 мл абсолютного этанола нагревают с обратным холодильником в течение 5- ч. Отсасывают в горячем состоянии. Получаемые из фильтрата кристаллы перекристаллизовывают из изопропанола, применяя активированный уголь; т.пл. 232-234°с; выход 40% от теоретического. Пример 4. 11- (4-АЛЛИЛ-1-пиперазинил)-ацетил -5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-он. 8,62 г 11-хлорацетил-5,11-дигидро-6Н-пиридо 2, З-Ь 1, 4 бензодиазепин-б-она и 8,3 г 11-.аллилпиперазина в 100 мл этанола нагревают с обратным холодильником в течение 2 ч. Реакционную смесь упаривают, кристаллический остаток перекристаллизовывают из 30 мл изопропанола и затем из 94%-ного этанола, применяя активированный уголь; т.пл. 230-233°с; выход 47% от теоретического.
Пример 5. Дигидрохлорид-дигидрат 11- (н-бут-2-енил)-1-пиперазинил -ацетил}-5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин 6-она.
8,62 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2,,4 бензодиазепин-б-она и 8,7- г 1-(н-бут-2-енил)-пиперазина ( R - CHj СН СН-СН,,) в 100 мл диоксана нагревают с oepaTBhttхолодильником в течение 3 ч и затем в вакууме упаривают. Остаток очищают на колонне с силикагелем и маслянистое основание в горячем состоянии растворяют в 70 мл изопропанола. Подкисляют соляной кислотой, причем выкристаллизовывается дигидрохлорид. Перекристаллизовывают из 94%-ногр этанола. Получаемые кристаллы содержат 2 моля кристаллизационной воды и плавятся при 207-210°С. Выход 35% от теоретического.
Пример б. Дигидрохлорид 5, И-дигидро-И- (4-нерил-1-пиперазинил)-ацетил 3-бН-пиридо 2 , 3-Ь 1 / 4 бензодиазепин-б-она.
Получают из 5,8 г 11 хлорацетил-5,11-дигидро-бН-пиридо12,,41бензодиазепин-6-она, 2,4 г карбоната натрия и 5,3 г 1-нерилпиперазина в 100 мл абсолютного этанола по описанному в примере 1 методу. Получаемый сырой продукт очищают, на колонне с силикагелем и в абсолютном этаноле, концентрированной соляной кислотой переводят в дигидрохлорид. Перекристаллизовывают из абсолютного этанола; т.пл. 188-191с; выход 65% от теоретического.
Пример 7. 5,11-Дигидро-11- 4- (об-метилбензил) -1-пиперазинил -ацетил-б Н-пиридо 2 , З-Ь l, 4 бeнзoдиaзeпин-б-oн.
5,8 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-б-она, 3 -Jitn триэтиламина и 4,2 г 1- (oL-метилбензил)-пиперазина
/. ,
размешивают в 40 мл
диоксана при 80°С в течение 2 ч.Темный раствор упаривают в вакууме и остаток поглощают в хлороформе/воде и экстрагируют путем встряхивания. Органическую фазу очищают активным углем, сушат сульфатом натрия и упаривают в вакууме.. Остаток Перекристаллизовывают из смеси уксусного эфира и циклогексана; т.пл. 20420б с; выход 62. от теоретического. , П р и м е р 8. 5,11-Дигидро-11- 4-(2-морфолиноэтил)-1-пиперази-, нил -ацетил -бН-пиридо.2 З-Ь 1, 4 бензидказепип-6-он.
Получают из 8,62 i- i 1 хлороГ1,етил-5,11-дигидро-бН-пиридо 2,З-Ь 1,4 бензодиазепин-б-она, 3,5 г карбоната натрия и 6,1 г 1-(2-морфолиноэтил)-пиперазина в 100 мл абсолютного этанола по описанному в примере 1 способу; т.пл. 227-229С (из Н-пропанола); выход 63% от теоретического.
Пример 9. 11-Ц4-(1-Лдамантилметил )-1-пиперазинил}-ацетил -5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-б-он. , Получают из 4,4 г 11-хлорацетил-5 ,11-дигидро-бН-пиридо 2 , 3- Ь 1/4 бензодиазепин-б-она, 1,8 г карбоната натрия и 3,75 г 1-(l-aдaмaнтилмeтил)5 -пиперазина в 80 мл абсолютного этанола аналогично примеру 1.
Перекристаллизовывают из смеси Н-пропанола и диметилформамида/ т.пл. 284-287°С при разложении , выход 64% 0 от теоретического.
Пример 10. 5,11-Дигидро-11-5 4-(3,4-метилендиоксибензил)-1-пиперазинил -ацетил -бН-пиридо 2,3-Ь} 1,4 бензодиазепин-б-он.
5 8 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2 , 3-bJ l, 4 бензодиазепин-б-она и 14 г 1-(3,4-метилендиоксибензил ) -пиперазина в 400 мл абсолютного бензола нагревают с обратным
0 холодильником в течение 18 ч. Охлажденную реакционную смесь смешивают с этанолом, подщелачивают аммиаком и в вакууме упаривают. Остаток Перекристаллизовывают из водного изое пропанола и затем из изопропанола; т.пл. 192-193°с; выход 51% от теоретического.
Пример 11. Гидрохлорид 5 , И-дигидро-И- ( 2 , 4-диметил-1-пипе0 разинил)-ацетил -бН-пиридо 2,3-Ь 1,4 бензодиазепин-б-она.
8,6 г 11-хлорацетил-5,11-дигидро-бН-пиридо 2 ,З-Ь 1f 4 бензодиазепин-б-она, 3,1 г карбоната натрия и
5 4,5 г 1,3-диметилпиперазина в
100 мл абсолютного этанола нагревают с обратным холодильником в течение 3,5 ч. После отсасывания фильтрат упаривают досуха. Остаток очищают
на колонне с силикагелем. К получаемому основанию добавляют этанол и соляную кислоту. После перекристаллизации из этанола получают гидрохлорид с т.пл. 301-303°с; выход 20% от теоретического.
Пример 12. 5,11-Дигидро-5-метил-11- 4-(3,4-метилендиоксибензил )-1-пиперазинил -ацетйл -бН-пиридо 2,,4 бензодиазепин-б-он. Получают из 4,4 г 11-хлорацетил-5,11-дигидро-5-метил-6Н-пиридо 2 , 3- Ь 1, 4 бензодиазепин-б-она, 3,8- г карбоната натрия и 8 г 1- (3,4-метилендиокси)-бензил -пиперазина в 200 мл абсолютного этанола аналогично примеру 1/ т.пл. 200-202°С
(из этанола), выход 52% от теоретического .
Пример 13. 5,11-Дигидро-11- з-(4-пренил-1-пиперазинил)-пропионил 6Н-пиридо 2, 3- Ь 1, 4 бензодиазепин 6-он.
6,6 г 11(3-хлорпропионил)-5,11-дигидро-бН-пиридо (2 , 3-Ь 1/4 бензодиазепин-6-она, 2,56 г карбоната натрия и 4,0 г 1-пренилпиперазина в 90 мл абсолютного этанола нагревают с обратным холодильником в течение 2 ч. Отсасывают в горячем состоянии и фильтрат упаривают до 20 мл. Кристаллический осадок отсасывают и перекристаллизовывают из изопропанола, т.пл. 199-201°С, выход 62% от теоретического.
Пример 14. (4-Бензил-1-пиперазинил) -пропионил - 5 ,11-дигидро-бМ-пиридо 2 , 1, 4 бензодиазепиы-б-он.
8,0 г 11-{3-хлорпропионил)-5,11 Дигидро-бН-пиридо 2 , 3- b 1,4 бензодиазепкн-б-она и 30 мл 1-бензилпиперазина в 100 г-ш изопропанола нагревают с обратнЕлм холодильником в течение 1ч. В вакууме упаривают досуха, к остатку добавляют раствор едкого натраИ основание экстрагируют хлороформом. Хлороформ отгоняют и остаток перекристаллизовывают из ксилола, т.пл. 2О5-207°С; т.пл. дигидрохлорида 212-214 С° (метанол); выход 18% от теоретического.
П р к м ер 15. 5,11-Дигидро И- з- {1--пиг1еразинил)-пропионил -бН-пиридо 2,3-Ь 1,4 бензодиазепин б--он.
К кипящему раствору 8,6 г пиперазима в 50 NUI этанола, размешивая, по каплям любазляют теплый раствор 6,0 г 11-(3-хлорпропионил -5,11-дигидро-бН-пиридо 2 ,,4 бензодиазепки-б-она в 12 мл диметилацетамиГ.а и 40 лл этанола. Затем нагревают с обратк:-:м холодильником в течение 1- ч. 1-3 всдкууме упаривают досуха и остаток очищают на колонне с силикагелем. З.чоат упаривают досуха и остаток перекристаллизозывают из ацетоннтрила, т.пл. 280-282°С (разложение); выход 70% от теоретического.
Пример 16. 5,11-Дигидро-11 3 1- (2-фенилэтил)-1-пиперазинил --пГропконил -6Н-пиридо 2, З-Ь 1,4 бензодиазопин 6-он.
5,4 г 11-(3-хлорпропионил)-5-11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-б-она и 3,8 Г 1- (2-фенилэтил)-пиперазина размешивают в 25 мл диоксана з течение 2,5 ч при . Окрашенный в красный цвет раствор упаривают досуха, остаток растворяют в смеси хлороформа и раствора бикарбоната натрия и хлороформенную фазу упаривают в вакууме. Остаток два раза -перекристаллизовывают из Н-пропанола; т.пл. 192-194°с; выход 65% от теоретического.
Пример 17. 5,11-Дигидро-5-метил-11- 2-(4-метил-1-пиперазинил)-пропионил -6Н-пиридо 2, З-Ь 1, 4 бен5 зодиазепин-6-он.
9,5 г 5-метил-11-(2-хлорпропионил )-5,ll-дигидpo-6H-пиpидo 2 , З-Ь 1,4 бензодиазепин-6-она, 3,2 г карбоната натрия и 4 мл 1-меQ тилпиперазина в 120 мл этанола нагревают с обратным холодильником в течение 7 ч. Отсасывают в горячем состоянии, фильтрат концентрируют до; 50 мл и отделяют кристаллический осадок. Фильтрат упаривают досуха и ос таток перекристаллизовывают из изопропанола; т.пл. 206-208°С, выход 36% от теоретического.
П.ример 18. Дигидратфумарат 5,11-ДИГИДРО-11- 4-(4-метил-1-пипера0 зинил)-бутирил -6Н-пиридо 2 , З-Ь 1,4 бензодиазепин-6-она.
6 г 11-(4-хлорбутирил)-5,11-дигидрр-6Н-пиридо 2,З-Ь 1,4 бензодиазепин-б-он и- 6 г 1-метилпиперазина
5 в 200 мл абсолютного диоксана нагревают с обратным холодильником в течение 1 ч, отсасывают в горячем состоянии, фильтрат упаривают в вакууме досуха, остаток промывают водой и
0 очищают на колонне с силикагелем. Получаемое основание с рассчитанным количеством фумаровой кислоты кипятят в течение 3 ч в 60 мл этанола. После охлаждения выделяется дигидрогенфума, рат. Перекристаллизовывают из эта:нола; т.пл. 199-201с (при разложении); вйход 31% от теоретического.
Пример 19. 5,11-Дигидро-11- . (4-метил-1-пиперазинил)-валерил -бК-пиридо 2,,4 бензодиазепин0 -б-он.
5,0 г 11-(5-хлорвалерил)-5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-она, 1,6 г карбоната натрия и 3 мл 1-метилпиперазина в 100 мл
5 этанола нагревают с обратным холодильником в течение 20 ч. Отсасывают в горячем состоянии, фильтрат (Упаривают досуха и остаток очищают на колонне с силикагелем, т.пл. 1510 153°С (.после перекристаллизации из уксусного эфира); выход 37% от теоретического.
Указанную в примерах 5,6,11,15, 18,19 очистку сырого продукта на колонне с силикагелем проводят с при-. менением смеси хлороформа, метанола,циклогексана и концентрированного аммиака в соотношении 68:15:15:2 в качестве растворителя и элюента.. Аналогично примерам 1-19 получа0 IOT соединения, Приведенные в табл.1. Новые соединения: А 5,11-дигидро-11-J 4-(2-метилаллил)-1-пиперазинил -ацетилJ-6H-пиридо 2,З-Ь 1,41бензодиазепин5 -6-он; Б днгндрохлорид 5,11-дигидро-II- A-(3-метил-бут-2-енил)-1-пипе разинил -ацетил -6Н-пиридо 2 , , 6ензодиазепин-6-он; В 5,11-Дигидро-11-Ц4-{2,2-диметилпропил)-1-пиперазинил -ацетил -бН-пиридо 2 , 3- Ь fl, 4 бензодиазепин -6-он; Г 11-I 4-(1-адамантилметил)-пи пераэинил -ацетил}-5,11-дигидро-бН-пиридо 2,,4 бензодиазепин-б-он;Д 5,11-Дигидро-11-5 4-(3,4-мeтилeйдиoкcибeнзил)-l-пипepaзинил -ацетил -бН-пиридо 2,,4 бензодиазепин-б-он;Е гидрохлорид 5, И-дигидро-И- {2,4-диметил-1-пиперазинил) -ацетил -бП-пиридо 2,,4 бензодиазепин -б-он; Ж 5,11-дигидро-5-метил-11- 4-(З , 4-метилендиокси6ензил) -1-пиперазинил -ацетил -6Н-пиридо 2, З-Ь l ,4 бензодиазепин-6-он; 3 11- (4-оловоамил-1-пиперазинил)-ацетил -5,11-дигидро-бН-пиридо 2, 1,41бензодиазепин-б-он; И (4-бензил-1-пиперазинил)-пропионил -5,-11-дигидро-бН-пиридо 2,3-ь 1,4 бензодиазепин-б-он; К 5,11-дигидро-11-р- 4-(2-фeнилэтил)-l-пипepaзинил -пропионил -бН-пиридо 2,3-ьЗ TI,4 бензодиазепин-6-онбыли исследованы на действие,тормозящее образование язвы, вызванной стрессом у крыс, и спазмолитическое действие, в отношении атропина, принимая во внимание острую токсичность Испытание действия, тормозящего об разование язвы. Накормленных крыссамок с весом тела между 220 и 260 г сажают по одиночке в маленькие проволочные клетки и затем в вертикальном положении помещагот в водяную ванну, имеющую постоянную температуру , на 16 ч, таким обичазом, чтобы только голова и грудина находились на поверхности воды. Активные вещества перорально давали крысам за 5-10 мин до погружения в воду. Для каждой субстанции брали 5 животных. Контрольные животные одинаковым образом получали 1 мл 0,9%-ного физиологического раствора поваренной соли или 1 мл 1%-ного раствора тилозы. По истечении 18 ч крыс умертвили повышенной дозой хлорэтила, вынули желудок, вскрыли его вдоль большой кривизны и растягивали на пробковой пластине. Спазмолитическое действие определяли в пробирке на толстой кииже морской свинки. Для создания спастического состояния использовггли ацетилхолин, а для сравнения - атропинсульфат. Спастическое средство давали 1 мин до дачи спазмолитического средства, время воздействия спазмолитического средства составляло 1 мин. Можно было наблюдать и у крыс, что атропиноподобные побочные действия, например торможение секреции слюны, при даче веществ полностью отсутствуют или в значительной степени уменьшены. Острую токсичность определяли после пероральной дачи активных веществ на некормленных белых дышах весом тела 18-20 г. Время набл одения - 14 дней. На каждую дозу брали группу из б Гришей. Результаты опытов пркведень Б табл. 2. Спазмолитическое действие вешс-стБ А-К по сравнению с сульфатом атропина значительно-слабее, вместе с этим и слабее свойственные атропгтну побочные эффекты. Т а б л и ц а 1








| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ5,П-ДИГИДРО-6Н-ПИРИДО-[2,3-Ь]-[1,4]-БЕНЗО-ДИАЗЕПИН-6-ОНА | 1972 |
|
SU331554A1 |
| Способ получения производных бензо-диАзЕпиНОНА или иХ СОлЕй | 1978 |
|
SU797578A3 |
| Способ получения пиридобензодиазепинонов или их солей | 1977 |
|
SU786900A3 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2081870C1 |
| Способ получения гетероциклических соединений | 1975 |
|
SU673173A3 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СМЕСИ ИХ ИЗОМЕРОВ И ИХ СОЛИ | 1992 |
|
RU2017740C1 |
| Способ получения замещенных в 5-ом положении 5,10-дигидро-11 н-дибензо (в,е) (1,4)диазепин-11-онов | 1969 |
|
SU512704A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛЛИЛЛМИНОАЛКАНОИЛАМИДОВ | 1972 |
|
SU342350A1 |
| Способ получения пиридобензодиазепинонов или их солей | 1975 |
|
SU578878A3 |
| Способ получения производных тиенотриазолодиазепина или их солей | 1978 |
|
SU747429A4 |

Сн,
-сн,(iH
21
СН:.
-сн -сн,.,-сн,,
22
Мз
-СИ 23- Он- ciHj -tiHj
тического 8
(водный изопропанол)
44
Дигидрохлорид 239-241, разл. {абсолютный этанол)
53
Дигидрохлорид 240-242, разл. (этанол)
48
Дигидрохлоридгидрат 210-213 абсолютный этанол)
- dH. -(СНг
Продолх(ение табл. 1
Н 248-250 (этанол) 34
.i::T.2
-СН„-СН СН,
-СН
-СН
-ен2-Й (н;
-СН,
CHj
46 - dH-йн с1нг
-сн 47-(CHj),
-сн .(iH,
48 -(iHz-ciH ci
49- (СН2)-СН н,dHj
II-си
50
((;-(iHrdHi-CH.e-(iH3 2
( геранип СН,CHj
5 -CHr 5HriH HriHr- -« - :Kj -сн
/ цитронеллил
CJHjliHj
-(JHr M ri-CHr (
:йнг-с
52
сн„Hjri- c
d- d cJH-dH2
(sfiapHesufl i
CHj о dHj dHj - (ЙнЛгСн-{Снг)г-йн
-riHzH.d I -CH.
1 -1ч.. / H «-. ч
6
7 -Снг-с нг- Л -CK.- dHj-йнг-сн 58
-(ЙНг),
П 2Лцсзлжени .... 1 ...
-4-Т 5 Г
СН, Н Н 16Т-166 (ацёто- нитрил)
H H и 248-250 (Н-про- 61 панол)
Н И Н 135-140 гидро- 65 хлорид 250-252, разл. (дпметилфоргиамид)
НИИ 140-142 (уксусный 51 эфир/циклогексан)
ИНН Дигидррхлорид-гид- 62 рат 216-218 (абс. этанол )
И Н Н Дигидрохлорид 229- 58 233, разл.(абс. этанол)
ИНН Дигидрохлорид-гид- 40 рат 231-234, разл (метанол)
ИНН Дигидрохлорид 188- 71 190, разл. (абс. этанол)
Н Н Н Дигидрохлорид 200- 68 204, разл. (этанол)
СИ Н Н Дигидрохлорид. 208-,, 61 210 (изопропанол)
Н Дигидрохлорид 180, 75 разл. Хабс. этанол)
194-197 (уксусный 36 эфир)
238-240 (М-пропа 61
НОЛ )
Дигидрохлорид-гидрат 209-212 (этанол)47
Н Гидрохлорид 263- 68 264 (Н-пропанол1
Н 173-175 (Н-пропа- 67
сн. нол)
Н 210-212 (М-пропа- 64 нол)
Продолжение табл. 1
772484
17
6 животных умерло. .
6 ЖИВОТНЫХ умерло.
6 животных.умерло.
6 животных умерло. 6 животных умерло. 6 животных умерло.
18 Продолжение табл. 2
Формула изобретения
г
К. -BI
неразветвленная или разде R
35 ветвленная Сэ,-Сл алкильная группа, С -С о-углеводородный ращикал с 1-3 двойными связями и/или трехкратной связью,
40 фенилалкильная группа с 2-4 атомами углерода в алкильном радикале, метилендиоксибензйльнаягруппа, хлорбензильная . группа, индан-5- (или-3) 45-илметильная группа/ фенилалкенильная группа с 2-4 атомами углерода, циклоалкильная группа с 5-7 атомами углерода,
50 циклоапкилметилъная группа с 3-10 атомами углерода в циклоалкильном кольце, незамещенном или за- мещенном метилом, морфо
55 ЛИНО-, пирролидино-, пиперидино- или 4-метилпиперазиноалкильная группа С 2 или 3 атомами углерода в алкильном радикале, или циннамилрадикал:60 атом водорода, метил,
R, этилрадикал;
R и R.- одинаковы или различны, атом водорода, метил,
65 этилрадикал;
А - неразветвленный или разветвленный С -С -алкиленовый радикал, причем если А означает неразветвленную или разветвленную С2-Су-алкиленовую группу, то R может также означать атом водорода, метил, этил или бензил и, если RJ и/или R означают метил или этил, то R может также означать метил или этил,
их солей, отличающийтем, что соединение общей форму(JO-A-HOI где R и A имеют указанные значения и
Hal - атом галогена, подвергают взаимодействию с соединением общей формулы 11
RS
vn
J К
где R, R- и R имеют указанные эна - е последуюцим вьоделвнявм целевого продукта в свободном виде или в виде соли.
. 2. Способ по П.1, о т. л и ч а ю щ и и с я тем, что реакцию проводят в среде индифферентного растворителя при температуре от комнатной до точки кипения растворителя.
водят в присутствии связывающеговающего галоидводород агента испольг
.галоидводород агента ,зуют карбонат или бикарбонат щелоч4.Способ по.п.З, о т л и ч аю -кого металла или третичный органичесщ и и с я тем, что в качестъе связы-кий амин.
вающего галоидводород агента исполь-„Источники информации,
зуют избыток соединения формулы Iji.5 принятые во внимание при экспертизе

Авторы
Даты
1980-10-15—Публикация
1978-05-30—Подача