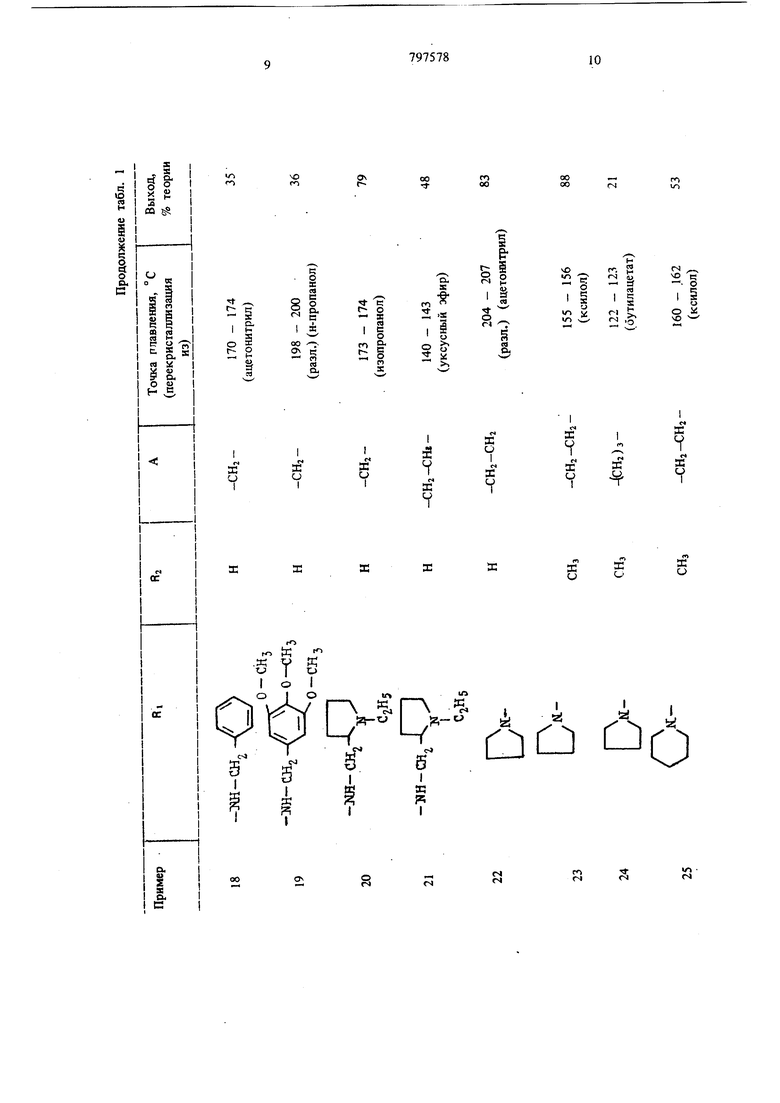
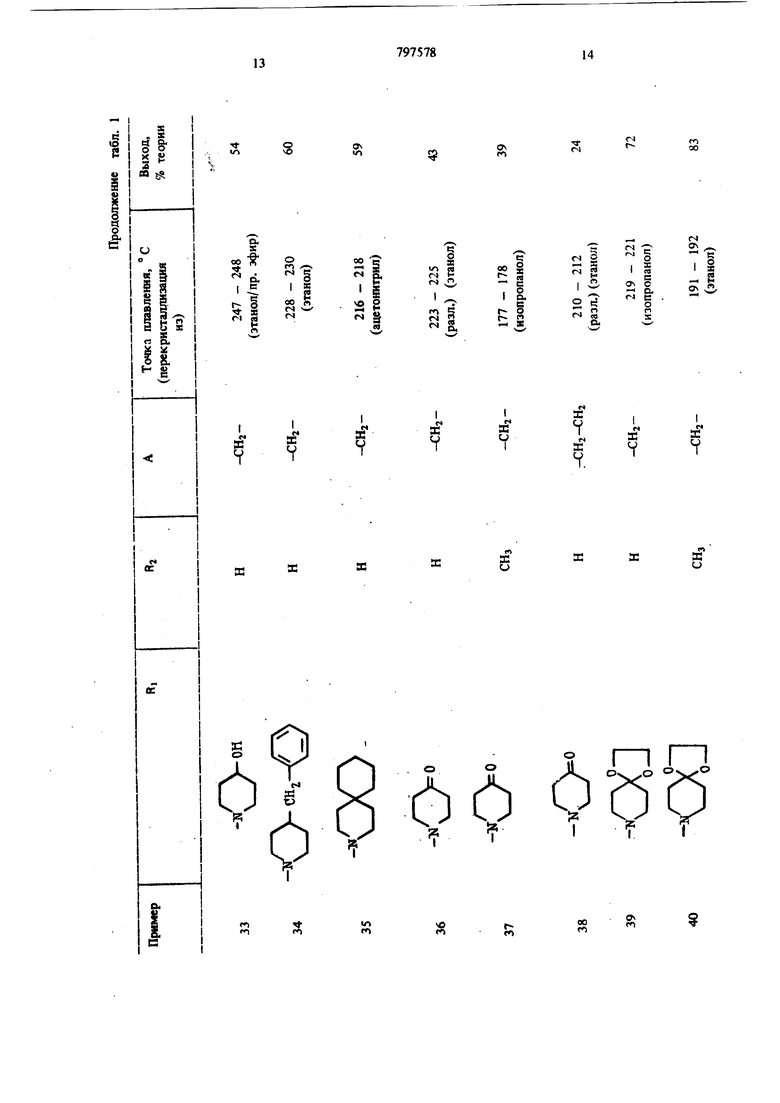
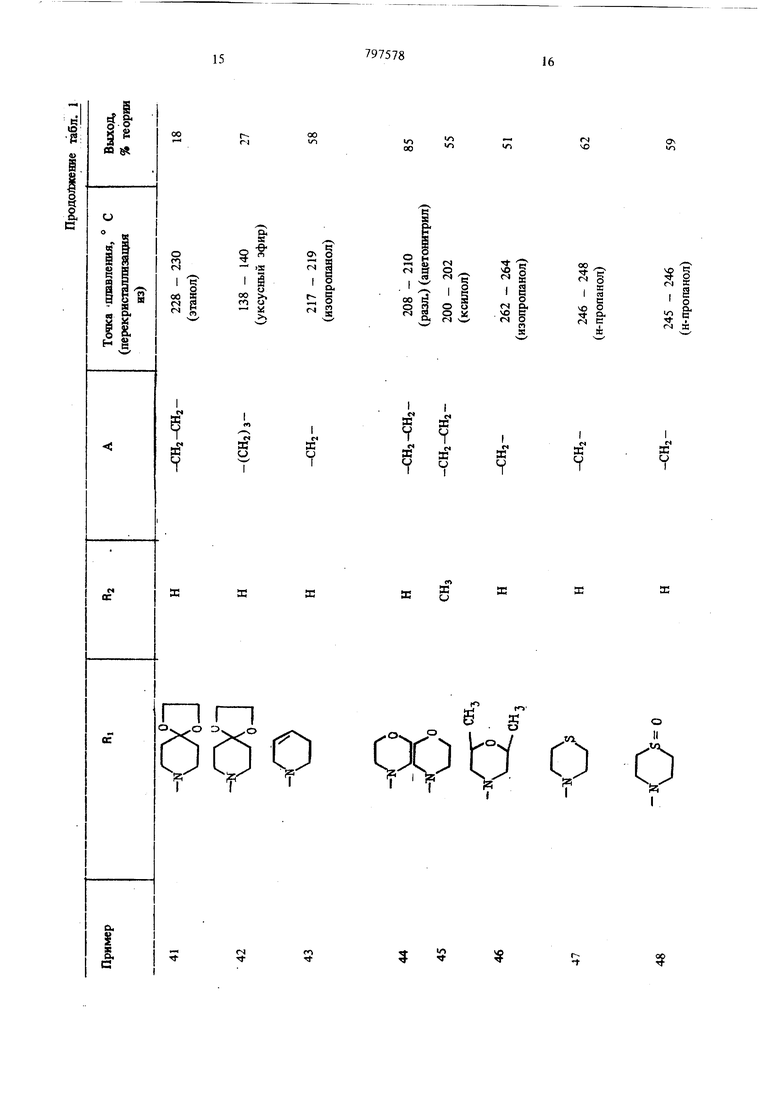
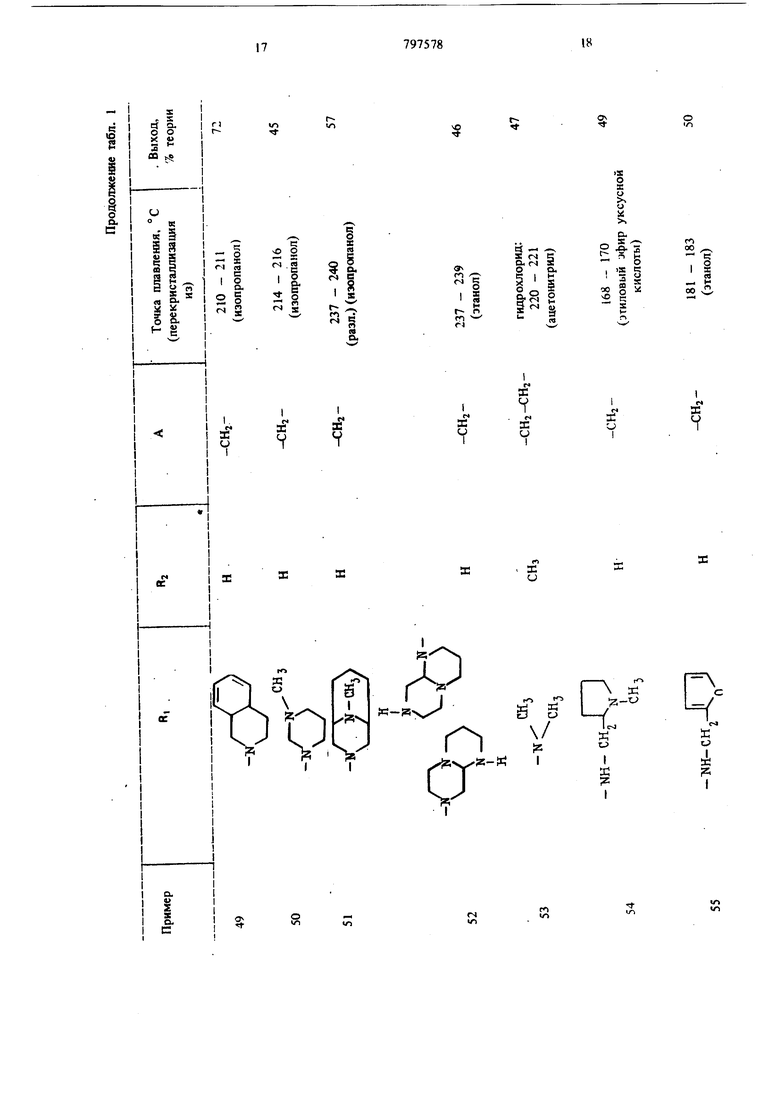
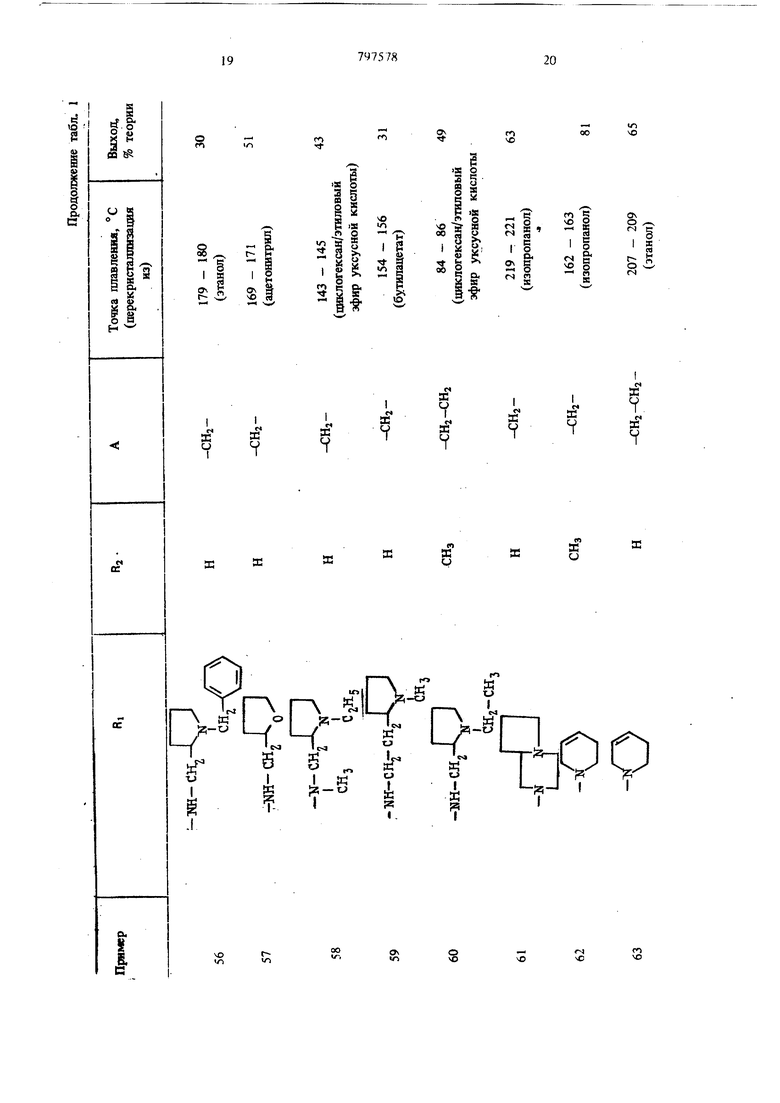
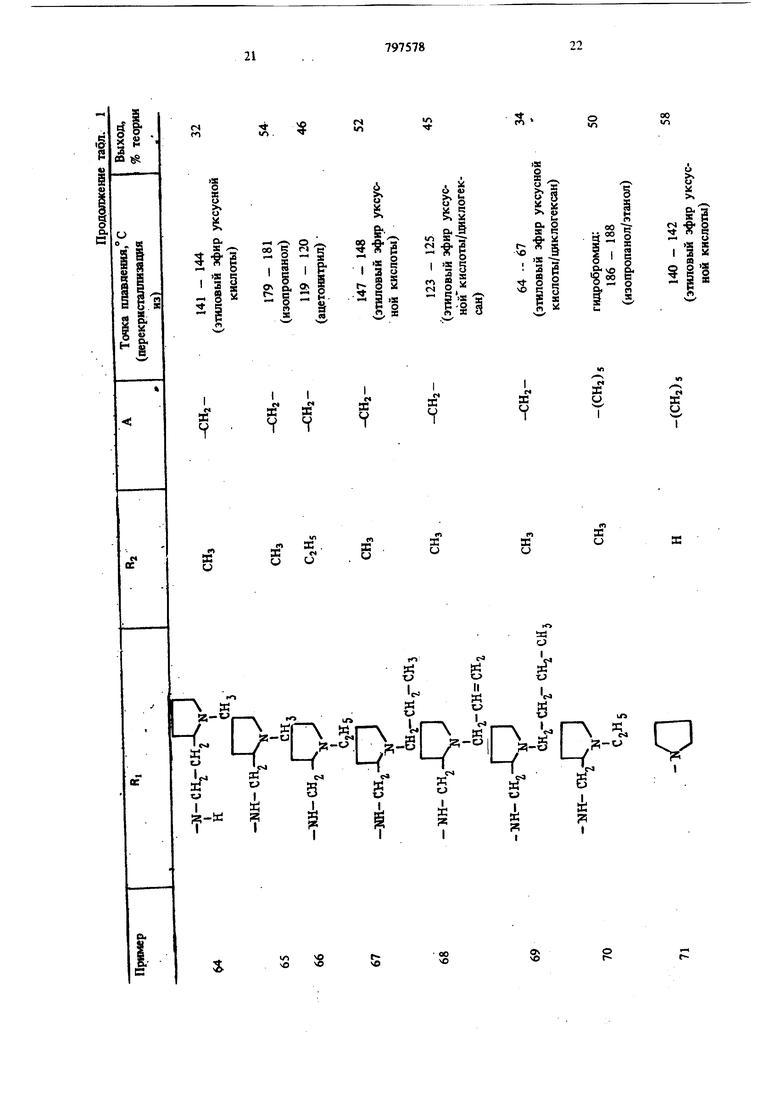
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ БЕНЗОДИАЗЕПИНОНА ИЛИ ИХ СОЛЕЙ этилом, или морфолиновую группу, если А означает неразветвленнуго алкиленовую группу с 2-5 атомами углерода, или их солей. Цель изобретения - получение новых полезных соединений, расширяющих арсенал средств воздействия на живой организм, Цель достигается путем синтеза последних, основанного на известной реакции аминировани галоидалкилов вторичными аминами. Реакцию обычно осуществляют в среде инер ного органического растворителя (спирты, эфи толуол и др.) при температуре . от комнатной до температуры кипения растворителя; желательно присутствие галогенводород связующего агента, в качестве которого используют или из быток вторичного амина, или карбонат или би карбонат щелочного металла 1. Производные бензодиазепинона обшей форм лы 1 получают взаимодействием соединения общей формулы П сс: в « CO-A-HQl где RI и А вышеуказанные значения, а На. означает атом галогена; с соединением общей формулы III RI - Н, где RI имеет вышеуказанные значения. Реакцию предпочтительно проводят в среде инертного растворителя при температуре от комнатной до точки кипения растворителя. В качестве растворителя пригодны спирты, так как зтанол, н-пропанол, изопропанол, кетоны, такие как ацетон, .или простые эфиры, такие как диоксан или тетрагидрофуран, ароматичес кие углеводороды, такие как бензол или толуол. Целесообразно проводить реакцию в при сутствии связующего галогенводород агента, в качестве которого можно применять избыто соединения формулы (ГП) или карбонат или бикарбонат щелочного металла, или третичный органический амин. Соединение общей формулы (Т) выделяют в свободном виде или в виде соли с неорганической или органической кислотой, такой как, например, соляная, бромистоводородная, серная, фосфорная, винная, лимонная, фумаровая, малеиновая, янтарная или щавелевая кислоты. Пример 1. 11- {(1-Этш1-2-пирролидинил) - метиламино ацетил -5,11- дигидро- 5-метил-6Н-пиридо 2,3-Ы 1,41бензодиазепин-6-он. 9,0 г 11-хлорацетил-5,11-дигидро-5-метил6Н-пиридо 2,3-Ы 1,41 -бензодиазепин-6-она. 3,5 г карбоната натрия и 4 г 1-этил-2-аминометил-пирролидина в 100 мл зтанола кипятят с обратным холодильником в течение 1,5 ч. Отсасывают в горячем состоянии, фильтрат упаривают досуха и остаток перекристаллизоБывают из ацетонитрила и затем из уксусного эфира. Точка плавления 169-171°С, выход 48% теории. Дигидрохлорид: т. lOi. 196-198° С (из этанола). Пример 2. 5,11-Дигидро-1и(4-метоксипиперидино) ацетил -бН-пиридо 2,3-Ь 1-4 бензоД1йазепин-6-он. 5,9 г 11-хлорацетил-5,11-дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазепин-6-она и 15 мл 4-метоксипиперидина в 200 мл бензола кипятят с обратным холодильником в течение 15 ч. Отсасывают в горячем состоянии, растворитель удаляют и остаток перекристаллизовывают из изопропанола. Точка плавления 219-220°С, выход 55% теории. Пример 3. 11-Дибензиламиноацетил-5,11-дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазеПИН-6-ОН. 6 г 11-хлорацетил-5,11-дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазепин-6-она, 4,2 г дибензиламина и 2,1 г тризтиламина в 100 мл абсолютнбго диоксана нагревают с обратным холодильником в течение 15 ч. После охлаждения отделяют получаемый гидрохлорид триэтиламина, фильтрат упаривают в вакууме досуха. Остаток два раза перекристаллизовывают из этанола. Точка плавления 187-189° С, выход 60% теории. Пример 4. 5,11-Дигидро-11- 3-(2-мегилпиперидино) пропионил -бН-пиридо 2,3-Ь 1,4 бензодиазепин 6-он. К 16 г 11-(3-хлорпропионш1)-5,11-дигидробН-пиридо 2,3-Ь 1,4 -бензодиазепин-6-она в 200 мл изопропанола добавляют 20 мл 2-метилпиперидина, кипятят с обратным холодильником раствор в течение 1 ч и в вакууме упаривают досуха. Остаток смешивают с водой, подщелачивают аммиаком и экстрагируют хлороформом путем встряхивания. Остаток хлороформенного экстракта очищают на колонне с силикагелем. Элюат упаривают в вакууме и остаток перекристаллизовывают из изопропанола. Точка плавления 197-199°С (при разложении), выход 65% теории. Пример 5. 11-(3-Бeнзилaминo)-пpoпиoнил -5,ll-дигидpo-6H-пиpидb 2,3-Ь 1,4 бензодиазепин-6-он. 6,0 г 11-(3-хлорпропионил)-5,11-дигидро-бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-она. 2,3 г карбоната натрия и 4,4 i беизиламина в 80 мл этанола нагревают с обратным холодиль ником р течение 4 ч. Отсасывают в горячем состоянии, отгоняют спирт и остаток очищают на колонне с силикагелем. Элюат упаривают и остаток дважды перекристаллизовывают из н-пропанола. Точка плавления 155-158°С, выход 41% тео рии. Пример 6. Гидрохлорид (дизтиламино)бутирил 1-5,11-дигидро-5-метил-6Н-пиридо(2,3-Ь 1,4 бензодиазепин-6-она. 4,3 г 11-(4-хлорбутирил)-5,11-дигидро-5-метил-бН-пиридо 2,3-Ь 1,41 бензодиазепин-6-она и 1,9 г диэтиламина в 70 мл диметилформамида оставляют стоять при комнатной температуре в течение трех недель. Затем упаривают в вакууме досуха и остаток перекристаллизовывают из изопропанола. Получают гид хлорид с точкой плавления 233-235°С. Выход 54% теории. Пример 7. 5,1 l-Дигидpo-ll-(4-пиppoлидинo-бyтиpил)-6H-пиpидo 2,3-Ь 1,4 бензодиазепин-6-он. 5,5 г 11-(4-хлорбутирил)-5,11-дигидро-6Н-пиридо 2,3-Ь 1,4 6ензо:шазепин-6-оиа, 1,4 г пирролидина и 2,Г г карбоната натрия в смеси 80 мл абсолютного этанола и 20 мл абсолютнего диоксана нагревают с обратным- холодиль НИКОМ в течение 10 ч. Отсасывают в горячем состоянии, фильтрат упаривают в вакууме досу ха и остаток очищают на колонне с силикаге лам. Элюат упаривают досуха и остаток перекристаллизовывают из ацетонитрила. Точка плавления 163-165°С, выход 55% теории. Пример 8. 11-(1-Этил-З-пиперидил) -аминоацетил -5,11-дигидро-6Н-пиридо 2,3-Ь) 11,4 бензодиазепин-6-он. 1,2 г 11-хлорацетил-5,11.дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазепина, 2,8 г карбоната натрия и 3,8 г 1-этил-З-аминопиперидина в 100 мл этанола нагревают с обратным холодил ником в течение 5 ч. Отсасывают в горячем состоянии, фильтрат упаривают досуха и остаток очищают на колонне с силикагелем. Элюат упаривают и остаток перекристаллизовывают из уксусного эфира. .. Точка плавления 147-148°С, выход 58% . теории. Пример 9. Дигидрохлорид 5,11-дигидро-11- t (гексагидро-4-метил- Ш-1,4-диазепин- 1-ил ацетил -бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-о 8,6 г 11-хлорааетил-5, 1-дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазепин-6-она, 3,5 г карбоната натрия и 4,5 г гексагидро-1-метил-1Н-1,4-диазепирш в 100 мл этанола кипятят с обратным холодильником в течение 2,5 ч. Отсасывают в горячем состоянии, отгоняют спирт и остаток растирают с лиоксаном. Получаемые кристаллы растворяют в этаноле и путем добавления концентрированной соляной кислоты переводят в Дигидрохлорид. После перекристаллизации из 94/с-ного этанола получают вышеуказанный дигидрохлорид с точкой плавления 241-243°С (.при разложении). Выход 47% теории. Пример 10. 5,11-Дигидро-1 l-(5-пиppoлидинo-вaлepил)-6H-пиpидo 2,3-Ь 1,4 бензодиазепин-6-он. 4,5 г 11-(5-хлорвалерил)-5,11-дигидро-6Н-пиридо 2,3-Ь 1,4 бензодиазепин-6-она и 10 мл пирролидина в .100 мл этанола кипятят с обратным холодильником в течение 12 ч. Спирт отгоняют, остаток растворяют- в смеси хлороформа с водой, органическую фазу упаривают досуха и остаток перекристаллизовывают из уксусного эфира. Точка плавления 156-157 С выход 45% теории. Пример 1L 11-{(1-Бензил-2-пирролидинил)метиламино ацетил -5,11-дигидро-5-метил-бН-пиридо 2,3-Ь 1,4 бензо;шазспин-6-он. 14,3 г П-хлорацетил-5,П-Дигидро-5-мегил-бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-она, 5,3 г карбоната натрия и 11,4 г 2-аминометилЬоензил-пирролидина в 300 мл абсолютного диоксана кипятят с обратным холодильником в течение 2 ч. Отсасывают в горячем состоянии, диоксан .отгоняют и остаток очищают на колонне с силикагелем. Элюат упаривают и остаток дважды перекристаллизовывают из этилового эфира уксусной кислоты. Точка плaвлe mя 123-124°С, выход 47% теории. Указанную в примерах 4, 5, 7, 8 и 11 очистку сырого продукта хроматографией на колонне с силикагелем проводят с применением смеси из хлороформа, метанола, циклогексана и концентрированного аммиака в соотнощении 68:15:15:2 в качестве растворителя и элюента. Аналогично примерам 2-11 получают соединения, приведенные в табл. 1.
(
ГЛ
o







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных бензодиазепинона или их солей | 1978 |
|
SU772484A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ5,П-ДИГИДРО-6Н-ПИРИДО-[2,3-Ь]-[1,4]-БЕНЗО-ДИАЗЕПИН-6-ОНА | 1972 |
|
SU331554A1 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СМЕСИ ИХ ИЗОМЕРОВ И ИХ СОЛИ | 1992 |
|
RU2017740C1 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1992 |
|
RU2081870C1 |
| Способ получения пиридобензодиазепинонов или их солей | 1975 |
|
SU578878A3 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛЛИЛЛМИНОАЛКАНОИЛАМИДОВ | 1972 |
|
SU342350A1 |
| Способ получения пиридобензодиазепинонов или их солей | 1977 |
|
SU786900A3 |
| Способ получения производных имидазо (1,5-а) /1,4/- диазепина или их солей | 1976 |
|
SU730308A3 |
| Способ получения пиридобензодиазепинонов или их солей | 1976 |
|
SU567407A3 |
| Способ получения соединенийиМидАзО (1,5-A)(1,4)диАзЕпиНАили иХ фАРМАцЕВТичЕСКи пРиМЕНи-МыХ СОлЕй | 1975 |
|
SU814278A3 |

a
fS
S &
m
&
7
(N
5 , K о S
I
о
I
a-o a
9 f и S
s ГЧ CT)
a
u
4
§5
a.
§ о о.
8
Л1 E;
- r о 01О
71
I S -e00 и Si
г 5s
I
a: u
Я
CJ
К (
QC
as о
к
f
u
|0 ,0гП
5 Sg s
in J«
W W
to
СЛCO
s
о
/
/
f
2; I
w «
СЧC4
О о
/
CN
ЧО
11
1Л
ЧО r
r
b
OQ Й
I о
я о
rf
8
r
(X
I &
(
§1 S
00 .
t S
О; c
Q.
n
CO
a
СЯ &
ж
и
I
m
c oo
ГЛ 1Л
CO
t S
SI
f- S
vO
cs
rs с
-
-. §
a.
- EJ Л
11
I I m
«I
о
Tj- V
- S
S- S
n
I i
В.
a
S 1
I
M
S
ж
ac
f
о
I
r
(S)
S f
Ж
I U
-
5
U
о
cc
ДййЛ
Ov
i §.
I e
n
Tt
СЧ
ГЛ r
N
ч
ft
S
f
в ё
O.
s
о
ГЛ fM
I ё
I с
oo
s
(S
f
n M
S (X
:
I
I
«
4
(E
ГЧ
гл oo
V
t
(N
OS
fN
r
I
I
ГЧ g
00
Ю «
OO
n
, Г4 t
- В
«-a
с N 1 л
.I
a
I
ON Г
о 5
2
.§
О n
r: n
ГЛ 5
ГЧ 2
я
5:;
CU
N §.
x
f
Y
f
(Ч
Y
«
s
g
u
66Ф59
S
;
r f
It
oo
00
Г-1ЛГ)
ffl
&
i
2о
О
csя
fS
s
i
I
Q.
§
00
-I
ou ts 4
2 g
Г42
4
Ё
f ё
я
B
U
я
r
и ОС I I I-I o.-.0 э .0 pop
(N t
9
Л
N
O
1Л
VD
IT)
H
т}(N Й I
VO
§
X
,
s
О
о
3
О о N О,
&
о е
S о i6
о.
N О
(S о
; i
п
Ч
1C
с
S
X U
f
as
g
i
rts. s CX6
(f
о |л
s
i
u X о V ч
Б. S .
ГЛ 00
1
S fN К & I
1 5
Isl
е I н
л м
« § 5
ss
чо 5
2 « S
S
m
п
X
CJ
X О
л к
Ч
tp
/
к и
5: tj
|Z
ri
I
I
К
i
I
о.
I
о /1
if
1Л «Л1
t
гл ш
in
Hf a° s
(S
« 5
§ 5
о a
Я s
n о
ff X
:$
S
ё u U
1
g. к
2 б
Й
5;
r- ч;
к
я f
з: и
я
iff
ЧО
00
r
ЧО
s
fN 5
B
tN
к .
f
я
ri
f
Kl
я
я u
u
-н
оо
V)
и
&
tt ,
II
и
1§§
§5
i
g Новые соединения: А - l 1- (1-этил-2- тирролицинил) метиламине ацетил} -5,11-дитидро-5-метил бН-пиридо 2,3-Ь 11,4 бснзодиазепин-6-он;Б - 5,11-дигидро-11-(-метоксйпиперидино) ацетил -бН-пиридо 12,3-Ы (1,4 бeнзoдиaзeпин6-oн;В - 5,1 Ьдигидро- - 3-(2-метилпипери-дино) пропионил)-6Н-пиридо (2,3-Ь 1,4 бензодиазепин-6-он;Г - 5,11-дигидро-11-(3-пиперидиног1ропиощ1л -бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-он; Д - 5,11-дигидро-11-(4-пирролидино-бутирил -бН-пиридо 2,3-Ь 1,4 бензодиазепин-6-он; исследованы на их тормозящее образование язвы, вызванной стрессом. Накормленные крысы-самки весом тела между 220 и 260 г сажают по одиночке в маленькие проволочные клетки и затем в вертикальном положении помещают в водяную ванну, имеющую постоянную температуру в 23°С на 16 ч таким образом, чтобы только толова и грудина находилась на поверхности воды. Активные вещества перорально дают крысам за 5-10 мин до погружения в воду. Для каждой субстанщ1и берут 5 животных. Контрольные животные одинаковым образом получают мл 0,9%-ного физиологического
при 1500 мг/кг из 4-х животных умерли 2.
при 1000 мг/кг из 5-ти животных умерли 2.
при 1000 мг/кг из 5-ти животных умерло 1.
при 2000 мг/кг из 5-ти животных умерли 3.
при 1500 мг/кг из 6-ти животных умерло 1,
Спазмолитическое действие веществ А-Д по сравнению с сульфатом атропина знаяительТаблиц
но слабее, наряду с этим слабее также свойственные атропину побочные зффекты. раствора поваренной соли или 1 мл 1%-ного раствора тилозы. По истечении 18 ч крысы умерщвлены повышенной дозой хлорэтила, вынимают желудок и вскрывают его вдоль большой кривизны и растягивают на пробковой пластине. Анализ проводят по известному способу Marazzi-Uberti und Turba и по описанному выше методу Takagi und Okabe, Спазмолитическое действие определяют в пробирке на толстой кишке морской свинки. Для создания спастического состояния используют ацетилхолин, а для сравнения - атропинсульфат. Спастическое средство дают 1 мин до дачи спазмолитического средства, время воздействия спазмолитического средства составляет 1 мин. Можно наблюдать и у крыс, что атропиноподобные побочные действия, как, например, торможение секреции слюны, при даче веществ А-Д полностью отсутствуют или в значительной степени уменьшены. Острую токсичность определяют после пероральной дачи активных веществ на некормленных белых мышей весом тела 18-20 г. Время наблюдения 14 дней. Результаты опытов сведены в табл. 2. 27 Формула изобретения 1. Способ пол чения производных бензодиа зепинона общей формулы 1 где А - неразветвленная или разветвленная алкиленовая группа с 1-5 атомами углерода; RI- свободная амино- трет.-бутиламино М-циклогексил-Ы-метиламино-, дибензиламино бензиламино-, триметоксибензиламино- 1-этил-2-пирролиданилметиламино-, 1-этил-З-пипери диниламино-, 9-метил-3,9-диазабицикло 3.3.1 нонан-З-нл-, 1, 2, 5, 6-тетрагидро-1-пиридил-, 4-бензилпиперидино-, 1, 2, 3, 6, 7, 8, 9, 9а- октагидро-4Н-пиразино (1,2-а) пиримидин-1 (или-8) ил-, 3- или 4-оксипиперидино- или метоксипиперидино-, I, 2, 3, 4-тетрагидро-2ИЗОХИНОЛИЛ-, 3-азаспиро (5,5)индекан-3-ил, 4-оксопиперидиногруппа или ее этиленкеталь гексагидро-3-метил- 1-пиримидинил-, тиоморфолинб-, 1-оксидо-тиоморфолино-, гексагидро-4-метил-1Н-1,4-диазепин- -ил-, 2, 6-диметилморфолинО| 1,4-диазабицикло 4.3.0)нона -4-ИЛ-, 1, 2, 5, 6-тетрагид)о-пирид- -ил-, (1-м тнп-пирролидин-2-ил)-этиламино-, (Ьметилпирролидин-2-ил)метиламино-, {1-н-пропилпирролидин-2-ил) метиламине-, (1-аллил-пирро лидин-2-ил)метиламино-, (1-н-бутнп-пирролидин-2-ил) метиламино-, (1 -бензил-пирролидин-2-ил)метиламино-, (фуран-2-нл)метиламин( (тетрагидроф)фан-2-ил) метиламине-, N-(1-зтил-пирролидин-2-ил)метил) -N-метил-метил амино-, (1-зтил-пирролидин-З-ил) метиламиношш (1-аллил-пирролидин-З-ил) -метиламиногруппа;R2- атом водорода, метил, ;зти.тфаяикал; причем RI может также означать диметиламиНО-, диэтиламиио-, дипропиламийо-, ди-изопропиламино-, ди-н-бутиламино-, ди-изобутиламино-, пирролидино-, пиперидиновую группу, пиперидиновую группу, замещенную метилом или этилом, или морфолиновую группу, если А означает неразветвленную или разветвленную алкиленовую группу с 2-5 атомами углерода, или их солей, отличающийся тем, что соединение оЪщеи формулы J i co-A-Nae где R и А имеют вышеуказанные значения, а Hat означает атом галогена; подвергают взаимодействию с соединением обшей формулы III RI - X, где RI имеет вышеуказанные значения; с последующим выделением целевого продукта в свободном виде или в виде соли. 2. Способ по п. 1,отличающийс я тем, что процесс проводят в среде инертного растворителя при температуре от комнатной до точки кипения растворителя. 3. Способ по ПП.1 и 2, о т л и ч а ю щ и и с я тем, что процесс проводят в присутствии связующего галогенводород агента. 4.Способ по пп. 1-3, отличающийс.я тем, что в качестве связующего галогенводород агента используют избыток соединения формулы III. 5.Способ по пп. 1-3, отличающий,с я тем, что в качестве связующего галогенводород агента используют карбонат или бикарбонат щелочного металла или третичный органический амин. Источники информации, принятые во внимание при экспертизе 1. Патент СССР N 567407, кл. С 07 D 243/38, 1974.
Авторы
Даты
1981-01-15—Публикация
1978-05-29—Подача