Предлагается новое соединение, а именно комплекс нового краун-эфира 3', 6'-диоксопиридазо-[1,2-a] -1,2-диаза-5,8,11- триоксациклотридекан-KCl (1) формулы • KCl где n 3,
• KCl где n 3,
проявляющий антимутагенную активность.
Это соединение может найти применение в различных областях народного хозяйства, в частности, при работе с различными химическими промышленными веществами, при использовании различных цитостатиков (в онкологии), химиотерапевтических и фармакологических средств, обладающих мутагенной активностью.
Предложенное соединение и его биологическая активность в литературе не описаны. В литературе описаны родственные соединения, антимутагенная активность которых не изучена. В качестве антимутагенов широко известны 2-меркаптоэтиламин (МЭА), диметилсульфоксид (ДМСО), L-цистеин и тиомочевина. Однако названные соединения сравнительно слабые протекторы, действие их не универсально и ограничено отдельными тест-объектами.
Целью изобретения является изыскание нового высокоактивного, слаботоксичного, устойчивого и удобного для применения антимутагена, а также расширение арсенала средств, воздействующих на живой организм. Указанные свойства определяются новой химической структурой нового соединения (1).
Комплекс краун-эфира синтезирован взаимодействием 3,6-диоксопиридазина с 3,6,9-триокса-1,11-дихлорундеканом в присутствии гидроокиси калия по следующей схеме:

 • KCl
• KCl
Индивидуальность полученного комплекса краун-эфира доказана ТСХ (Silufol UV-254, элюент пиридин-вода, 30:1, проявление ультрахемоскопом).
В ИК-спектре синтезированного соединения присутствуют полосы поглощения, характерные для карбонильной группы в области 1680 см-1 и простой эфирной группы в области 1150 см-1. Молекулярный вес определен масс-спектрометрическим методом.
П р и м е р. 3',6'-Диоксопиридазо-[1,2-a]-1,2-диаза-5,8,11-триоксациклотридекан·KCl (1).
Суспензию 11,3 г (0,1 моль) 3,6-диоксопиридазина в 100 мл этанола нагревают до кипения и прибавляют раствор 11,2 г (0,2 моль) гидроокиси калия в 100 мл 75%-ного этанола. Смесь кипятят в течение 1 ч и прибавляют по каплям 23,1 г (0,1 моль) 3,6,9-триокса-1,11-дихлорундекана. Кипячение продолжают 24 ч. Осадок отфильтровывают и отгоняют растворитель. Остаток растворяют в 50 мл воды и экстрагируют эфиром. Затем водный слой нейтрализуют соляной кислотой. Фильтруют от осадка, выпаривают досуха и прибавляют 50 мл абсолютного этанола. Выпавшие кристаллы фильтруют и сушат. Получают 4,5 г (26,1%) комплекса краун-эфира (1) с т.пл. 255-256оС.
Найдено, C 41,64; H 5,14; N 8,25.
C12H18N2O5 · KCl
Вычислено, C 41,80; H 5,26; N 8,12.
Изучена острая токсичность комплекса краун-эфира (1) и известных контрольных соединений. Результаты приведены в табл.1.
Как следует из табл.1, соединение I оказывает очень слабое токсическое действие (ЛД50 равно 3000 мг/кг веса животного).
Антимутагенное действие комплекса краун-эфира. Антимутагенное действие изучено на биохимических штаммах: Escherichia coli Р-678, ауксотрофный по треонину, лейцину и витамину В1, Actinomyces rimosus 222 (исходный штамм BS-21), ауксотрофный по лизину, и на индикаторных штаммах Salmonella typhimurium TA-1534, несущий мутацию типа сдвига рамки считывания генетического кода, генотип his D 3052, LPS+, Repair Δ uvr B; TA-1535, несущий мутацию типа замены основания в молекуле ДНК, генотип his G46, LPS-, rfa, Repair Δ uvr B и ТА-1950, несущий мутацию типа замены основания в молекуле ДНК, генотип his G46, LPS+, Repair Δ uvr B. Эти штаммы являются ауксотрофами по гистидину.
Антимутагенное действие исследуемого соединения изучали различными методами на вышеуказанных тест-объектах по разным направлениям.
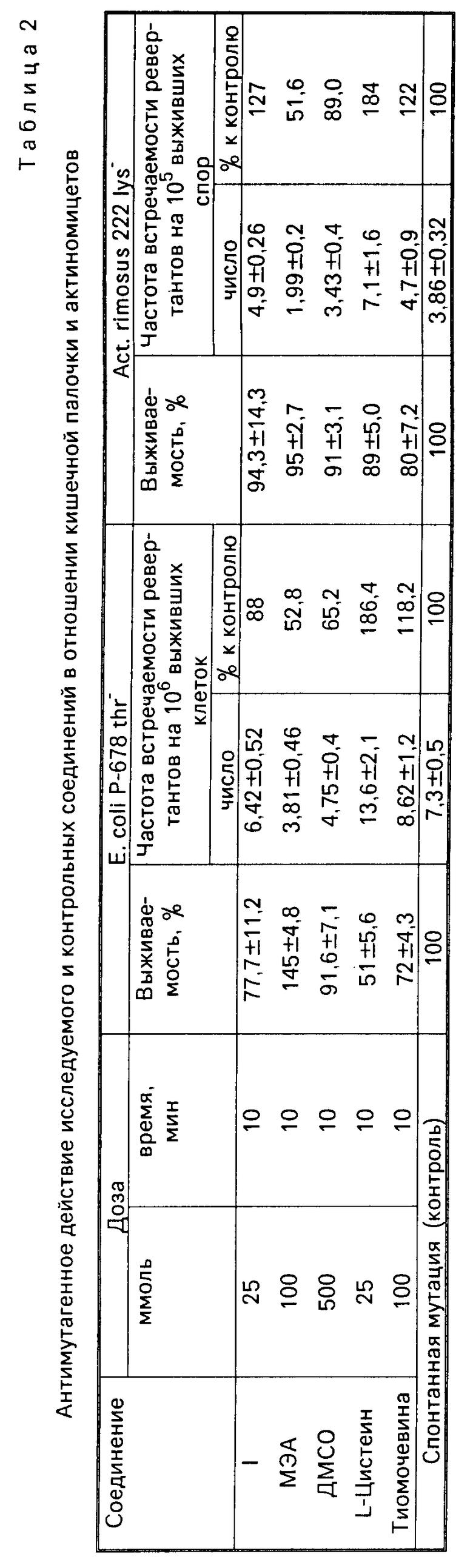
Результаты изучения антимутагенного действия исследуемого соединения и контрольных протекторов в отношении треонинового локуса кишечной палочки и лизинового локуса актиномицетов приведены в табл.2. Как видно из табл.2, соединение I, МЭА и ДМСО оказывают антимутагенное действие в отношении кишечной палочки, а последние и в отношении актиномицетов. Тиомочевина и L-цистеин не оказывают антимутагенного действия на эти тест-объекты.
В табл. 3 представлены результаты изучения антимутагенного действия соединения I и контрольных протекторов в отношении гистидинового локуса сальмонелл ТА-1534 с нормальным бактериальным липополисахаридом (LPS), служащим барьером проникновения веществ в клетки, и ТА-1535 с разрушенным LPS. На штамме ТА-1534 антимутагенное действие оказывает лишь соединение I и МЭА, остальные контрольные соединения не оказывают заметного действия. В отношении штамма ТА-1535 соединение I снижает число спонтанных мутаций на 32% и по активности превосходит контрольные.
Изучено влияние комплекса краун-эфира на мутации, индуцированные химическим мутагенезом (см. табл.4). Из данных табл.4 видно, что соединение I сильно снижает частоту встречаемости ревертантов, индуцируемых новым мутагеном N-(2-метил-4-изопропоксибензенсульфонил)-N'- бутилтиомочевиной (513076). Последний индуцирует мутации по треониновому локусу кишечной палочки в 3500 раз больше контроля. При совместном испытании вышеназванного мутагена с комплексом краун-эфира в 20 раз уменьшается число мутаций, индуцируемых мутагеном самостоятельно.
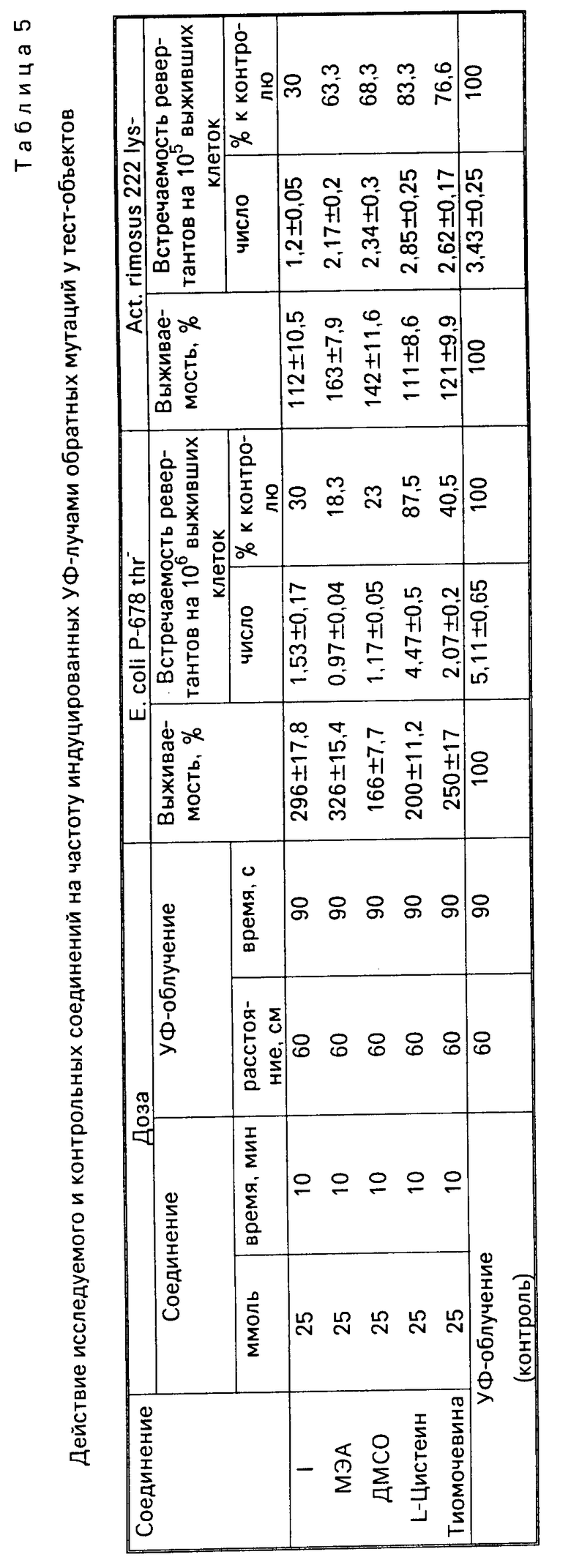
Результаты изучения антимутагенного действия соединения I и контрольных соединений в отношении кишечной палочки и актиномицетов, облученных УФ-лучами, приведены в табл.5. Из табл.5 видно, что соединение I оказывает сильное влияние на мутации, индуцированные УФ-лучами; снижает выход мутаций по обоим локусам тест-объектов в одинаковой степени на 70% по сравнению с контролем. По антимутагенному действию на актиномицетах соединение I превосходит контрольные препараты.
Соединение I, изученное методом учета мутагенеза в системе с метаболической активацией на штамме сальмонелл ТА-1950 с нормальной бактериальной липополисахаридной системой, затрудняющей проникновение веществ в клетку, в небольшом проценте случаев оказывает антимутагенное действие.
Таким образом, на различных тест-объектах выявлено антимутагенное действие у комплекса краун-эфира. Это соединение снижает выход спонтанной мутации у кишечной палочки на 12% у штаммов сальмонелл на 15 и 32% уменьшает число мутаций, индуцированных УФ-лучами, у кишечной палочки и актиномицетов на 70% Соединение I сильно влияет на мутации, индуцированные химическим мутагеном, снижает число ревертантов в 20 раз по сравнению с контролем. По антимутагенному действию и слабой токсичности соединение I по многим признакам превосходит известные протекторы, изученные в идентичных условиях.



Комплекс краун-эфира пиридазинового ряда с хлористым калием формулы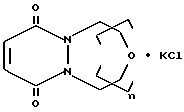
где n = 3,
проявляющий антимутагенную активность.
Комплекс краун-эфира пиридазинового ряда с хлористым калием формулы
где n = 3,
проявляющий антимутагенную активность.
| M | |||
| M | |||
| Htay, o | |||
| Mefh - Cohn | |||
| N = Birdgen Heterocyeli Part IV | |||
| Tetrahedron Zett, 1976, с.469 | |||
| Батикян Г | |||
| Г., Арутюнян Р | |||
| М | |||
| Некоторые аспекты применения протекторов при химическом мутагенезе у человека | |||
| Биологический ж | |||
| Армении, 28, N 1, 1975, с.3 | |||
| Симонян Н | |||
| В | |||
| и др | |||
| Влияние гаммафоса и цистеина на выживаемость бактерий | |||
| Биолог | |||
| ж | |||
| Армении, 27, N 2, 1974, с.91 | |||
| Бариляк И | |||
| Р | |||
| и др | |||
| Эффект протекторов при химическом мутагенезе | |||
| Цитология и генетика, 12, N 1, 1978, с.50. |
Авторы
Даты
1996-02-10—Публикация
1979-07-04—Подача