ящим способом получения соединений общей формулы 1 или их солей, кот рый заключается в том, что 2-аминотиаэол jo6meft формулы 11 N где R-j и А имеют указанные значени подвергают взаимодействию с произво ным щавелевой кислоты формулы III с-о-тг- , где R - алкил с 1-4 атомами углеро R .- алкоксигруппа с 1-4 атомами углерода или атом хлора с последующим, в случае необходимос ти, омылением получаемого сложного эфира, и выделяют целевой продукт в свободном виде или в виде соли. Исходное соединение общей формулы Г1 или его кислотно-аддитивную соль растворяют в инертном раствори теле или суспендируют и каплями добавляют к производному щавелевой ки лоты. В качестве растворителя, соот ветственно, суспендирующего средств применяют бензол, толуол, ксилол, спирт или тетрагидрофуран, которые инертны по отношению к реагирующим соединениям. Для связывания образую щейся кислоты добавляют органическо основание, например, пиридин или тр этиламин. Так как реакция сильно экзотермична, производное щавелевой кислоты добавляют медленно, в случа необходимости при озслаждении, реакция завершается за 30-180 мин. Так как почти все тиазоловые соединения трудно растворимы, рекомендуется до разделения реакционную смесь при перемешивании оставлять стоять, например, в течение ночи. Разделение осуществляют известным способом - путем выпаривания растворителя, экстракции остатка под ходящим растворителем или смесью растворителей, например, простым эфи ром, уксусным эфиром, хлороформом или гексаном, очистки экстракта, упаривания растворителя и перекриста лизации. В некоторых случаях очистку производят с помощью хроматографии на колонке. Если необходимо получить целевой продукт общей формулы 1, где R, атом водорода, то эфирную группу отщепляют о ылением. Это осуществляют путем гидролиза в присутствии катализатора - основного или кислого средства, например, сильного основания, такого как гидроокись натрия или.калия, или минеральной кислоты. такой как соляная, серная или фосфорная . Соединения общей формулы I, где R - атом водорода, в случае необходимости можно переводить в их соли . Для этой цели кислоту растворяют в воде или суспендируют и добавляют необходимое основание до получения значения рН-7. Получение производных тиазол-2-оксамовой кислоты иллюстрируют примеры . П р и м е р -1. Этиловый эфир-4-(2-метоксифенил)-тиазол-2-оксамовой кислоты. К суспензии из б г гидройодида 2-аминр-4-(2 -метоксифенил)-тиазола в пиридине прикапывают 2,9 г этилоксалилхлорида и смесь в течение ночи Перемешивают пРИ комнатной температуре. После упаривания реакционной смеси досуха, остаток обрабатывают раствором бикарбоната натрия и несколько раз экстрагируют этиловым эфиром. Объединенные экстракты промывают три раза водой и один раз насыщенным солевым раствором и затем сушат над MgSOi. После упаривания досуха и перекристаллизации из этанола получают указанное соединение с выходом 4,2 г (70%). Т.пл. 118-122°С. Используемый в качестве исходного продукта гидройодид 2-амино-4-(2 -метоксифенил}-тиазола получают следующим образом. 15 г о-метоксиацетофенона и 15,2 г Ьгиомочевины тщательно перемешивают в колбе из искусственной смолы. К этой смеси небольшими порциями добавляют 27,7 г йода. По окончании добавления реакционную смесь в течение ночи нагревают на масляной бане до 100°С. После охлаждения добавляют 50 мл метанола, затем от 400 до 500 мл воды, твердую массу измельчают в ступке, суспензию фильтруют, промывают водой, небольшим количеством этилового спирта и простым эфиром и затем высушивают . Получают 27,7 г (83%) указанного соединения, которое без дальнейшей очистки используют в качестве исходного продукта. Пример 2. Этиловый эфир 4-(2 ,5- диметоксифенил)-тиазол-2-оксамовой кислоты.К раствору 3 г 2-амино-4-(2, 5-диметоксифенил)-тиазола в сухом пиридине каплями добавляют 2 г хлорангидрида этилового эфира щавелевой кислоты в 35 мл сухого пиридина. По окончании добавления перемешивают в течение 2,5 ч и в течение этого времени наблюдают ход реакции с помощью тонкослойной хроматографии. По окончании реакции смесь выливают в ледяную воду, образовавшийся- осадок фильтруют, промыв.ают водой и выслушивают. После перекристаллизации из этанола
И н-гексана/хлороформа получают 2,Уг указанного соединения с т.пл 143144 С.
Пример 3. Этиловый эфир 4-(Гпиридил-(2 ) -тиаэол-2-оксамовой кислоты.
Раствор 1 г 2-амино-4-{пиридил-(2 )-тиазола в 25 мл диэтилоксалата в течение 20 ч нагревают до 125°С. Смесь охлаждают, осадок отфильтровывают и перекристаллизовывают из этанола и затем из гексана/хлороформа.
Выход 0,5 г (64%), т .пл. 141-144°С.
П р и м е р 4. Этиловый эфир 4-(2-метоксифенил)-тиазол-2-оксамовсй кислоты.
Суспензию 2 г этилового эфира 4- (2-метоксифенил )-тиазол-2-оксамовой кислоты в 30 мл 1 н гидроокиси натрия нагревают при интенсивном перемешивании до получения прозрачного раствора. Путем подкисления 2 н соляной кислотой получают осадок, который после охлаждения смеси и разбавления водой отфильтровывают. Остаток взмучивают два раза водой (100 мл), отфильтровывают и промывают этанолом. Кислоту очищают путем перекристашлизащии из диметилформамида/этанола. Выход 1 г (55%), т.ш.. 195-197°С.
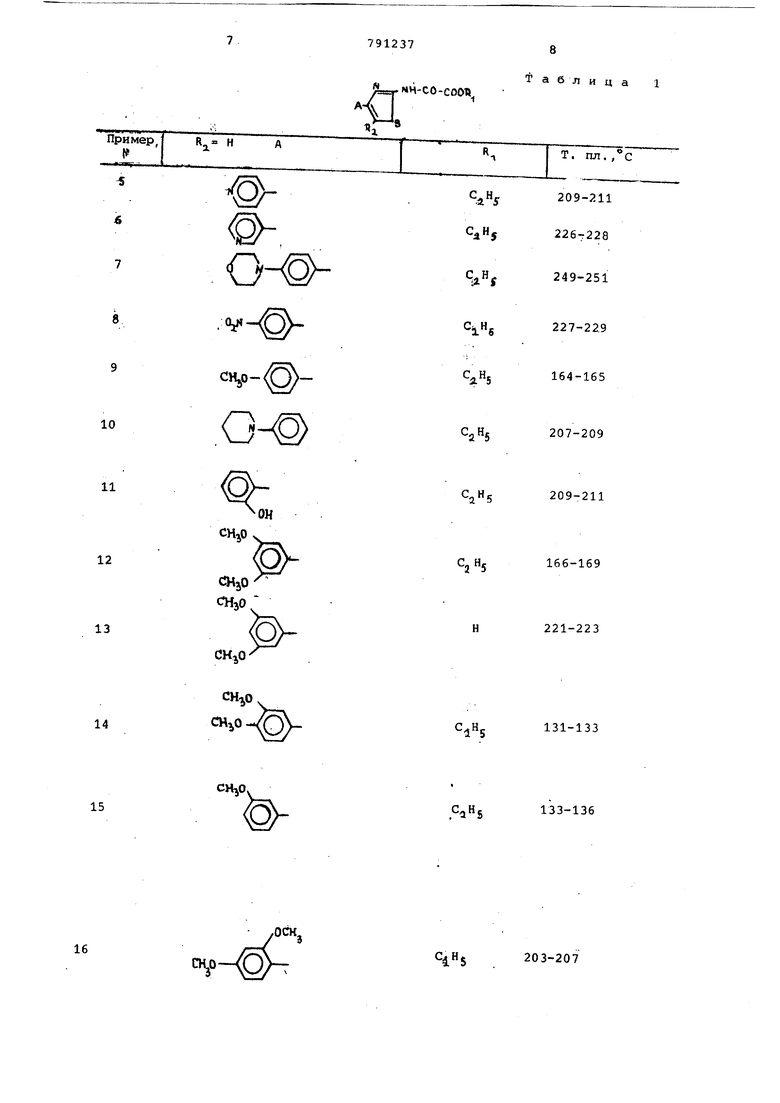
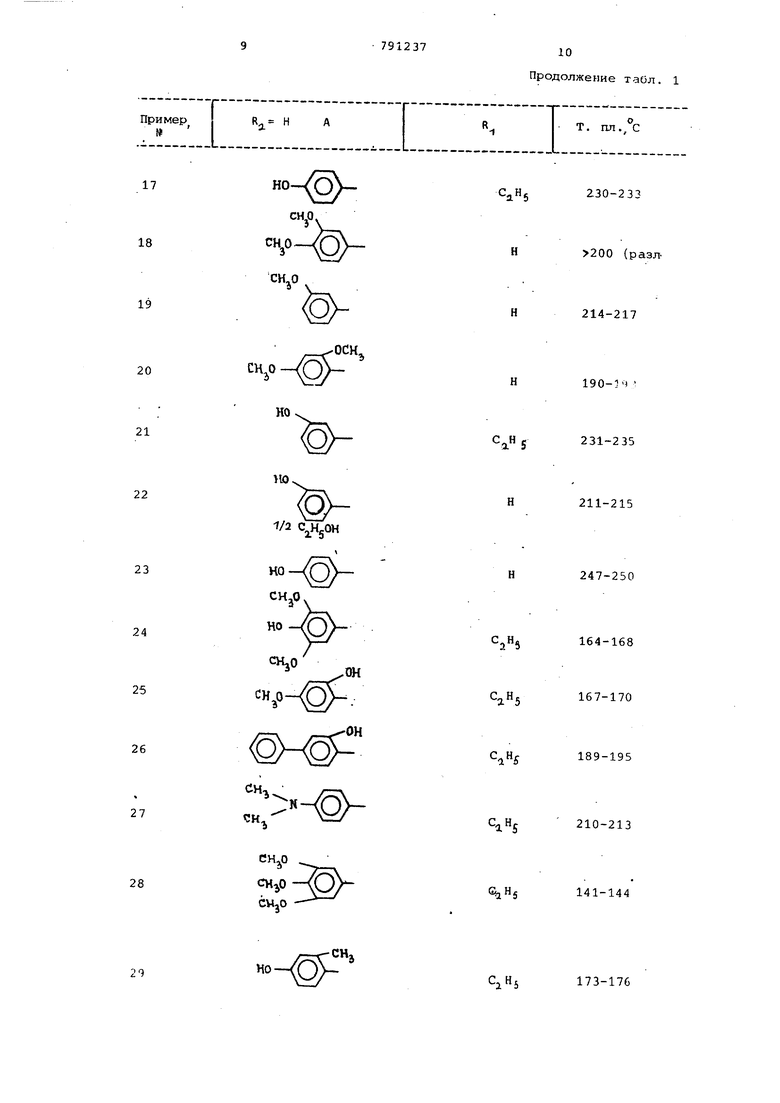
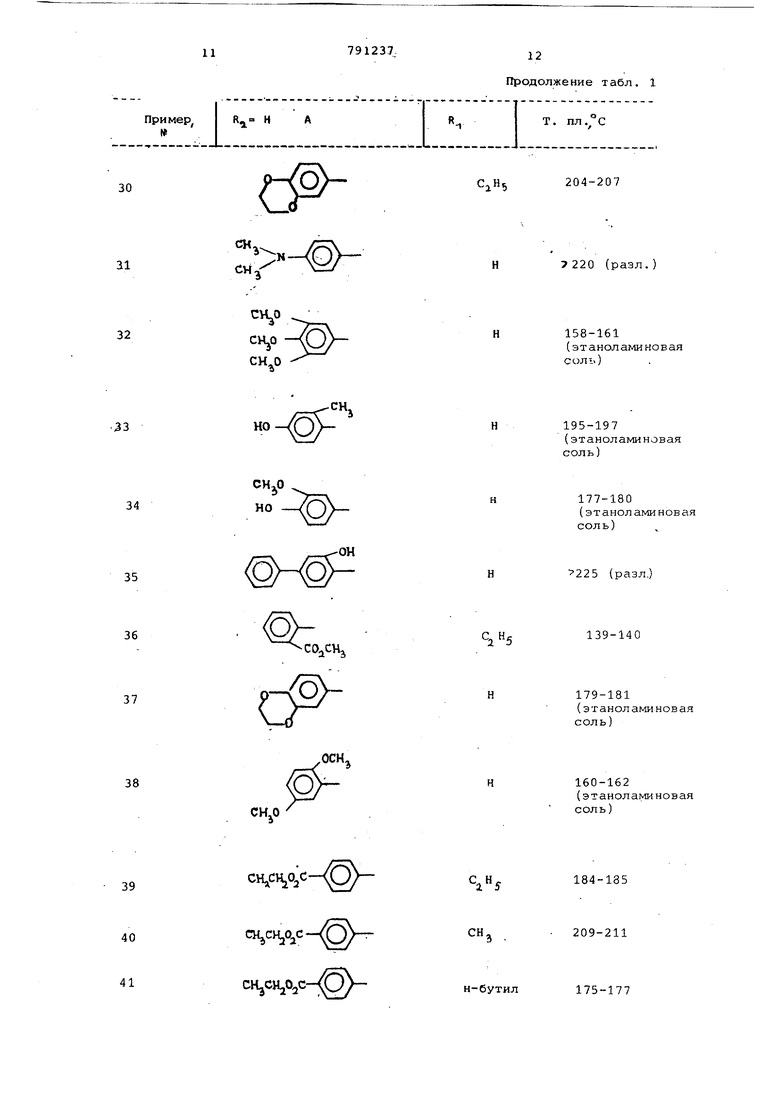
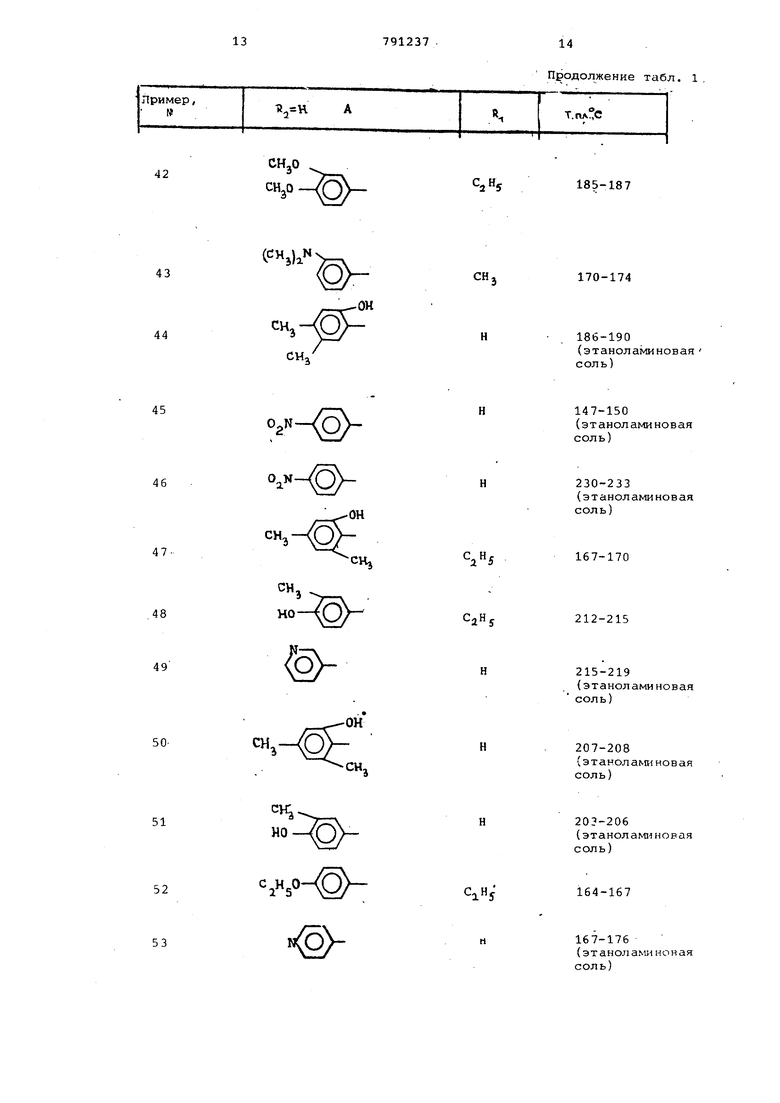
Аналогично получены соединения формулы I, предЬтавленные в табл.1.
Соединения формулы I или их соли обладают противоаллергическим действием. По отношению к извecтнo y противоаллергическому средству, такому, как 1,3-бис-(2-карбоксихромон-5-илокси)-2-оксипропан, имеют то преимущество, что они эффективны и при оральном введении. Кроме того, тормозящее действие в отношении аллергических реакций наступает при значительно меньшей дозировке и длится дольше.
Противоаллергическое действие определяли на крысах в так называемом ПКА-тесте (тест пассивной кожной анафилаксии). При этом кожу крысы сенсибилизируют посредством внутрикожного впрыскивания яично-альбуминовой антисыворотки различных разбавлений (неразбавленно и в разбавлении 1:3, Д:9, 1:27 и т.д.). На другой день животным вводят внутривенно яичный альбумин в синем растворе Эвенса
Путем измерения степени посинения определяли ПКА-титр. Подлежащие исследованию соединения в различных концентрациях внутривенно или перорально вводят вместе с синим раствором Эвен. са.Каждой крысе вводят 5 мг яичного альбумина,растворенного в 1 мл 0,25% красителя Эвенса в стерильном солевом растворе.
Через 25-30 мин после введения красителя и исследуемого вещества
животных умерщвляют и измеряют посинение внутренней поверхности кожи в мм . ПКА-титр является обратным по величине значением того раз:бавления сыворотки, при котором мож13 но определять посинение в диаметре, по меньшей мере в 5 мм. Сокра1цение ПКА-титра является мерой для торможения аллергических реакций, в данном случае против яичного альбумина.
20В табл. 2 показано оральное или
внутривенное антиаллергическое действие некоторых соединений формулы I или их солей.
Соединения формулы 1 и их соли
25 применяют при лечении аллергической астмы, сенной лихорадки, крапивницы, Ькземы, атопических дерматитов и других аллергических заболеваний.
30рЦля лечебных целей соединения формулы 1 могут.быть смешаны с обычными фармацевтическими наполнителями или носителями, желирующими, связывающими, смазывающими средствами, загусти35 телями или разбавителями, растворителями или средствами для достижения пролангированного действия, которые можно применять как энтерально, так и парентерально.
40
в качестве фармацевтических препаратов пригодны, например, таблетки, драже, пилюли, капсулы, растворы, суспензии, мази, порошки, настой45 ки, растворы для инъекции или аэрозоли, причем кроме соединений формулы 1 добавляют консервирующие или стбилизирующие средства, эмульгаторы, буферные вещества и т.д.
EfvФармацевтические препараты для парентерального применения и для ингаляции в общем составляют 5-50 мг на каждую дозу и при оральном введении 50-500 мг.
Таблица 1
JW«4-CO-COOV




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 4-оксо4н-пирано-(3,2-с) хинолин-2-карбоновых кислот или их солей | 1975 |
|
SU545262A3 |
| Способ получения производных аминопропанола или их солей, рацематов или оптически-активных антиподов | 1975 |
|
SU586835A3 |
| Способ получения производных хиназолона или их солей | 1977 |
|
SU733516A3 |
| Способ получения производных фенилпиперазина или их солей | 1977 |
|
SU664564A3 |
| АРИЛАЛКАНОИЛПИРИДАЗИНЫ | 1997 |
|
RU2201923C2 |
| НОВЫЕ СОЕДИНЕНИЯ 2-АРИЛТИАЗОЛА В КАЧЕСТВЕ АГОНИСТОВ PPAR α И PPAR γ | 2003 |
|
RU2296754C2 |
| Способ получения производных тризамещенных имидазолов или их солей | 1982 |
|
SU1205764A3 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА И ХИНАЗОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2130934C1 |
| Способ получения 2-карбокси-4оксо-4н,10н-/2/-бензопирано/4,3- / /1/-бензопиранов | 1973 |
|
SU482042A3 |
| 2,6-ЗАМЕЩЕННЫЕ-4-МОНОЗАМЕЩЕННЫЙ АМИНО-ПИРИМИДИНЫ КАК АНТАГОНИСТЫ РЕЦЕПТОРА ПРОСТАГЛАНДИНА D2 | 2005 |
|
RU2417990C2 |

15
оси.
16
CHjC
133-136
Ca«S
203-207
СдН
НО
эо -ЧО;
28
CHjO
Продолжение табл. 1
247-250
164-168
167-170
S«5
189-195
Cl
210-213
Ca«S
141-144
HS
Ho
C3,Hj173-176
Продолжение табл. 1
CHjO
42
%° -ЧОу
(
43
44
45
,47
Продолжение табл. 1
185-187
170-174
СН.
186-190
(этаноламиновая соль)
147-150
(этаноламиновая соль)
S«5
167-170
сн. 230-233 (этаноламиновая соль)
СН, НО
48
212-215
49
215-219
(этаноламиновая соль)
50207-208
(этаноламиновая соль)
%
51
™-чо:
203-206
(этаноламиновая соль)
52
164-167
СаНу
53
167-176
(этаноламяновая соль)
Продолжение табл. 1
54
220-223
Са.Н5
55
195-197
(этаноламиновая
соль)
56
197-199 (этаноламиновая
Соединение
4-фенил-5-метил-тиазол-2-оксамовая кислота, этаноламиновая соль
4- ( З-диметиламинофенил) -тиазол-2оксамовая кислота, этаноламиновая соль
4-(2 ,4 -диметоксифенил)-тиаэол-2-оксамовая кислота
4-(2 ,5 - диметоксифенил)-тиазол-2-оксамог. 1Я кислота, этаноламиновая соль
4-(2-метоксифенил)-тиазол-2-оксамо вая кислота
ЕД50.ЕД50,
мг/кг в.венномг/кг орально
2,04
1,6
Продсзлжение табл. 2
этиловый эфир 4-(пиридил-(А))-тиaэoл-2- оксамовой кислоты
метиловый эфир 4-( 3, 4-диметоксифенил)-тиазол-2-оксамовой кислоты
этиловый эфир 4-(4-этоксифенил)-тиазол-2-оксамовой кислоты
этиловый эфир 4-(3-мeтил-4fоксифенил)-тиазол-2-оксамовой кислоты
Формула изобретения
Способ получения производных тиазол-2-оксамовой кислоты общей формулы 120
SH-CO-COOR
тем, что, с целью получения новых соединений, расширяющих арсенал средств воздействия на живой организм, 2-силинотиазол общей формулы 11
NH.
и
а
25
Авторы
Даты
1980-12-23—Публикация
1979-06-20—Подача