(54) СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ АМИДОВ а-КЕТОКАРБОНОВЫХ КИСЛОТ
ольшом избыточном К11;1ич(.с1не. Например, на 1 моль ацилшанида применяют от 1 до 10 моей, предпочтителыю 1,1 1.5 моля кислоты.
В качестве кислоты предпочтительно применять серную кислоту, однако можно использо- 5 вать также и сульфокислты. например бензолсульфокислоту.
После гидролиза реак11ноиной смеси амидь кетокарбоновых кислот выделяют известными методами, например крис1аллиз; цией
дистилляцией.- .
Пример 1. В arfnapar, с(абженный мешалкой и защи1цен 1ый от влаги, помещают 131 г (1,0 моля) бензоилцианида, 148 г (2,0 моля) трет.бутанола и 50 мл метиленхло- рида и при перемешивании приблизительно при 5 С прибавляют по каплям 150 г (1,5 моля) концентрированной серной кислоты. По око1пании прикапыва1шя продолжают перемешивать реакционную смесь при комнатной 20 температуре в течение 1 ч, и затем всю смесь выливают в 400 г льда и xopoiuo перемешивают. Непосредственно после этого экстрагируют метиленхлоридом и раствор метиленхлорида испаряют. В результате получают 195 г N-трет.- 25 бутиламида фенилглиоксиловой кислоты, что соответствует выходу 95%, считая на использованный . Амид имеет температуру плавления 76-77° С.
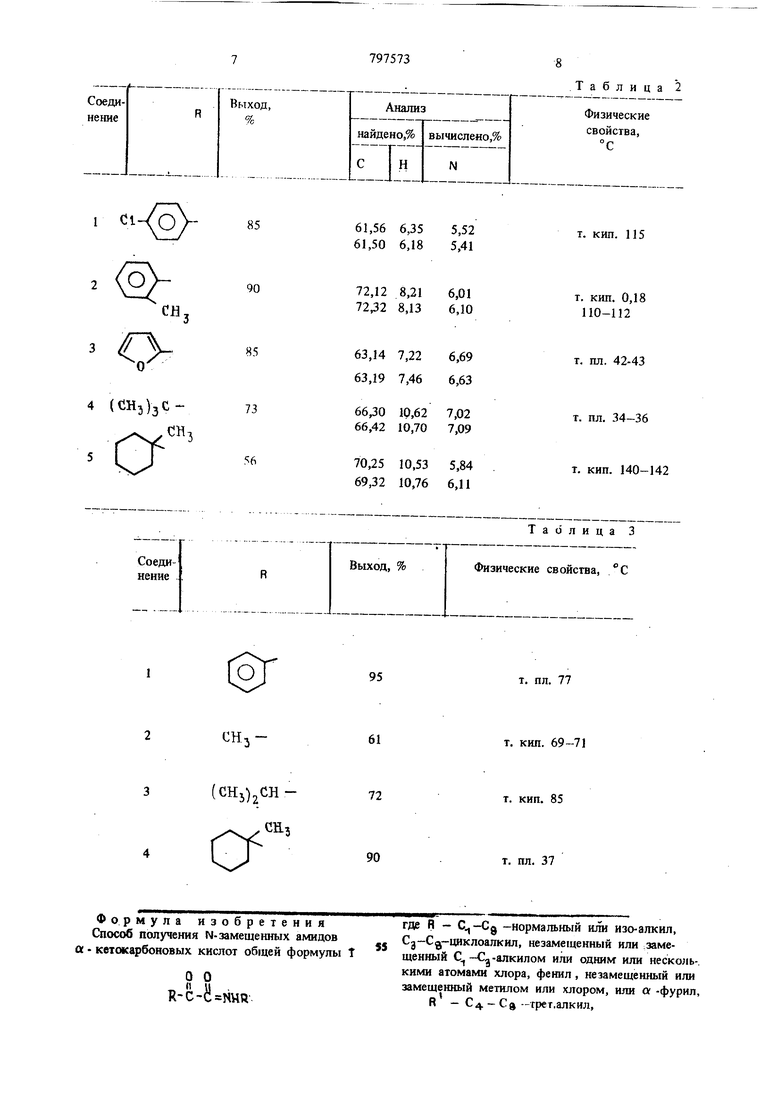
По способу, описанному в примере 1, полу- 30 чают следующие соединения РСОСОМНС(СНз)з (табл. 1), которые получаются либо в чистом виде, либо их очищают дистилляцией или перекристаллизацией.
Пример 2. Опыт проводят, как списано в примере 1, однако вместо трет.бутанола применяют 176 г (2,0 моля) трет.амилового спирта (2-метилбутанол-2).
Выделяют 210 г N-трет.-амиламида фенилглиоксиловой кислоты, что соответствует выходу 40 96%, статая на использованный цианид кислоты. Амид имеет температуру плавления 29-30 С.
Вычислено,%: С 71,2; Н 7,8; N ,
Найдено,%: С 71,06; Н 7,97; N .
По способу, описанному в примере 2, полу- j чают следующие соединения ЯСОСОМНС(СНз)2С2Н5 (табл. 2), которые очищают либо дистилляцией, либо перекристаллизацией.
Пример З.В аппарат, снабженный мешалкой и защищенный от влаги, помещают 50 111 г (1,0 моля) пивалоилдианида, 150 г (5 молей) концентрированной серной кислоты и 150 мл ледяной уксусной кислоты и при перемешива1ши при 0-5°С пропускают 112 г (2,0 моля) изобутилена в течение 1 ч. Непос- 55 редственно после этого нагревают реакционную смесь до комнатной температуры и продолжают перемешивать 4 ч. Затем смесь выливают в 500 г льда и после хорощего перемешивания
отсасывают выпавший амид. После высушивания в вакуумном сушильном шкафу выделяют 161 г чистого для анализа N-трет.бутиламида триметилпировиноградной кислоты, что соответствует выходу 87%, считая из использованной цианид кислоты. Амид плавится при 65°С. По способу, описанному в примере 3, получают следующие соединения РСОСОМНС(СНз)-з (табл. 3), которые либо выделяют в виде чистых продуктов, либо очищают дистилляцией.
Пример 4. Опыт проводят, как описано в примере 3, однако вместо введения изобутилена прикапывают 140 г (2,0 моля) 2-метилбутена-2. Выделяют 169 г М-трет.бутиламида триметилпировиноградной кислоты, что соответствует выходу 85%, считая на введенный цианид кислоты. Амид имеет температуру плавления 36° С.
Пример 5. Опыт проводят, как описано в примере 4, однако вместо пйвалоилцианида применяют 69 г (1,0 моля) ацетилцианида. После того, как реакционную смесь вливаю в лед, раствор экстрагируют эфиром, после чего эфир испаряют и остаток фракционируют.
Выделяют 88 г N-трет.амиламида пировиноградной кислоты, что соответствует выходу 56% считая на использованный планид кислоты. Амид имеет температуру кипеьшя 79° С при 14 мм рт. ст.
Вычислено,7о: С 60,7; Н 9,6; N 8,85.
Наидено,%;С 59,9; Н 9,92; N 8,38.
Пример 6. Опыт проводят, как описано в примере Э, однако вместо пропускания изобутилена прикапывают 224 г (2,0 моля) 2,4,4-триметилпентена-2 (Ь-диизобутилена). После того, как реакционную смесь выливают на лед, экстрагируют все метиленхлоридом и органическую фазу непосредственно после этого испаряют в ротационном испарителе при температуре бани 70°С, В результате получают 125 г масла, которое кристаллизуется в холодильнике. Это соответствует выходу 52%, считая на введенный цианид кислоты. N-Трет.-октиламид триметилпировиноградной кислоты имеет т. пл. 20-2 Г С.
Вычислено, С 69,66; Н 11,27; N 5,80,
Найдено,%: С 69,22; Н 11,42; N 5,78.
Строение подтверждено ПМР-спектром.
Пример 7. В защищенном от влаги аппарате смешивают 131 г (1,0 моля) бензоилцианида, )48 г (2,0 моля) трет.бутанола и 200 мл метилеихлорида и при - 20°С прибавляют по каплям 150 г (1,5 моля) концентрированной серп it кислоты. После окончания прикапывания перемешивают еще 1 ч при комнатной температуре и затем всю смесь выливают на 400 г ;гьда и перемешивают. Затем экстрагируют метиленхлоридом и раствор метилеихлорида упаривают. Получают 191 г N- трет.бутилаМИДа фенилглиоксиловой кислоты.
5. 79
что соответствует выходу 937f в пересчете на используемый Щ1а(ид кислоты.
П р 1 м е р 8. Опыт проводят как в примере 1, но вместо метилеихлорида используют 1,2-дихлорэтан. Серную кислоту прикапывают при 50°С.
Получают 180, 5 т амида, что соответствует выходу 88%,
Амиды а - кетокарбоновых кислот, которые могут быть получены по предлагаемому способу, являются новыми. Их можно применять в качестве промежуточных продуктов для синтеза гербицидов. Например, их можно перевести в 1,2,4-триазиноны путем взаимодействия, с тиокарбогидразидом в присутствии полярного растворителя (спирты, вода, диметилсульфоксид, диметилформамид и т. д) и в соответствующем случае в присутствии кислого катализатора (соляная кислота или серная кислота). Непосредственно после этого можно провести метилирование атома серы. Кроме того, эти соединения можно прямо применять в качестве фунгицидов.
Амиды а - кетокарбонов1 1х кислот могут быть переведены методом гидролиза в свободные а - кетокарбоновые кислоты, которые в свою очередь являются важными промежуточными продуктами в синтезе аминокислот.
Таблица 1
О
85
0
(СНэ)зС73
,сн.
а
56
Соединекие
7,22
6,69
т. пл. 42-43 7,46 6,63
7,02
т. пл. 34-36
7,09
5.84
т. кип. 140-142
6,11
Таолица 3
Физические свойства, С
Выход, %



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1,2,4-триазин-5-она | 1978 |
|
SU791236A3 |
| Способ получения -кетокарбоновой кислоты | 1977 |
|
SU793376A3 |
| Способ получения амидов -кето-КАРбОНОВыХ КиСлОТ | 1977 |
|
SU799651A3 |
| Способ получения 2-ацилокси-/4-аминобензил/-производных или их солей | 1980 |
|
SU884563A3 |
| Способ получения 2,2-диметокси-4,4-дифенил-5-замещенных-1,3,2-оксазафосфол-2-енов | 1980 |
|
SU888496A1 |
| Способ получения нитрилов кетокарбоновых кислот | 1977 |
|
SU745361A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1,2.4^ТРИАЗИН-5-ОНОВ | 1972 |
|
SU433681A3 |
| СПОСОБЫ И ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ ДЛЯ ПОЛУЧЕНИЯ МЕТИЛАМИДОВ α-МЕТОКСИИМИНОКАРБОНОВЫХ КИСЛОТ | 1995 |
|
RU2146247C1 |
| Способ получения пропан-1,2-диондиоксимов | 1977 |
|
SU671723A3 |
| Способ получения производных аминокислот или их физиологически совместимых солей | 1987 |
|
SU1836335A3 |

т. пл. 77
СНч(CHj),Формула изобретения Способ получения N-замещенных амидов а - кетокарбоновых кислот общей формулы Т () у R-C-C NHR
т. кип. 69-71
т. кип. 85
т. пл. 37 гдеН- -нормальный или изо-алкил, Cg-Cg-циклоалкил, незамещенный или замещенный С,-С -алкилом или одним или несколь-. кими атомами хлора, фенил, незамещенный или замещенный метилом или хлором, или о; -фурил, R - C -Cft-трет.алкил.
отличающийся тем, что ацилцианидгде R имеет вышеприведенные значения, или
общей формулы ГIсоответствующим алкеном в кислой среде при
R-CO-CNтемпературе от -20 до +50°С.
где R имеет вышеприведенные значения, обра-Источники информации,
батывают третичным спиртом общей фqp-j принятые во внимание при экспертизе
мулы . J.Ugi, U.Fetzer, Ber., 94, 1961. 1116
HO-R 21.
Авторы
Даты
1981-01-15—Публикация
1978-07-19—Подача