в которой одно из значений и R водород, другое - метокси, трифтор метил или фтор; одно из значений R и R - водород, другое - хлор, бром, фтор, трифторйетил или водород; одно из значений R° и R - водо род, другое - ,-алкокси, замещенный ..одним или более атомами фтора, заключающийся в том, что соед1гаение формулы где R имеет указанные значения, подвергают циклизации в присутствии дегидратирующего агента. Подходящими дегидратирующими реагентами являются фосфорная кислота муравьиная кислота, пентахлорид фосфора или пятиокись фосфора в. присутствии сильной кислоты и хлори ды алканойной и бензойной кислот и ангидриды кислот. Предпочтительными дегидратирующими реагентами яв ляются сильные кислоты, в частности метасульфоновая и концентрированная серная кислота, 1Шклизацию осуществляют при 2080С, предпочтительно при комнатной температуре. Обычно предпочтительно осуществлять реакцию без использования растворителя, хотя при желании могут быть применены растворители, включающие галогениро ванные бензолы и галогенированные алканы, включая хлорбензол, дихлорбензолы, хлороформ и хлористый мети лен. Все величины измеряются в метрической системе мер, а все температуры указаны в градусах Цельсия. Все пропорции и проценты указаны по весу. В нижеследующих примерах показан синтек типичных соединений, а нижеследующие примеры получения соответствут синтезу типичных исходных соединений. Во всех примерах соедин ния идентифицируются на основе анализа данных ядерного магнитного рез нанса, элементного микроанализа и в некоторых случаях на основе дан 34 ных анализа ИК-спектров и масс-спектроскопии. Получение 1. 1-(4-Пентафторэтоксибензоил)-4-(2,6-диметоксибензоил)-тиосемикарбазид. Порцию тиоцаната аммония весом 0,54 г добавляют в 10 мл тетрагидрофурана, смесь нагревают с обратным холодильником и добавляют к ней 1,5 г 2,6-диметоксибензоилхлорида, растворенного в 10 мл добавочного количества тетрагидрофурана. Сйесь перемешивают при температуре обратного холодильника в течение 20 мин, охлаждают до температуры окружающего воздуха, после чего прикапьшают 1,5 г 4-пентафторэтоксибензоилгидразина, растворенного в 20 мл тетрагидрофурана. Реакционную смесь перемещивают при температуре окружающего воздуха в течение 1,5 ч. Затем смесь высушивают путем исгшрения в вакууме и полученный остаток промывают диэтиловым эфиром. Затем эфир концентрируют под вакуумом и рекристаллизуют продукт, получая при этом 1,1 г указанного выше соединения, т. пл. 184-186°С. Пример 1. (4-пентафторэтоксифенил)-,3,4-тиадиазол-2-ил -2,6-диметоксибензамид. 1 г промежуточного соединения, полученного в ходе реакции получения препарата 1, медленно добавляют к 4 г метасульфокислоты, после чего смесь перемешивают при температуре окружающего воздуха в течение 4ч. Затем смесь медленно выливают на 100 г льда и тщательно перемешивают. После этого значение рН водной смеси доводят до 8,5 путем добавления концентрированного гидрата окиси аммония, а затем собирают твердое вещество путем фильтрации и рекристаллизовывают его из водного раствора этанола для того, чтобы получить 0,6 г неочищенного продукта. Очистку полученного вещества осуществляют, хроматографическими методами на силикАгеле с использованием растворителя, состоящего из 70% толуола и 30% этилацетата. После очистки выход продукта составил 200 мг вещества, т. пл. 227-229°С. Пример 2. (4-Трифторметоксифенил)-1,3,4-тиадиазол-2-илТ-2,6-диметоксйбензамид, т. пл. 2012030С.
Пример 3. N-C5-(6-MeTOKCK-2-бензо (в) фурил)-1,3,4-тиадиазол-2-илЗ-2,6-диметоксибензамид, т. пл. 215-2 7°С.
Пример 4. М-С5-(2-Инденил)-1,3,4-тиадиазол-2-ш1 -2,6-яиметоксибензамид, т. пл. 230-232с.
Примерз. (5-Метокси-2-бензо (в) фурил)-1,3,4-тиадиазол-2-ш1 -2,6-диметоксибеизамид, т, пл. 255-257с..
Пример 6. М 5-{5-Трифторметил-2-беизо (в) фурил)-1,3,4-гиадиазол- 2-ш 2,6-диметоксибеиз амид, т. пл. 242-245° С.
Пример 7. (б-Трифторметил-2-бензо (в) фурил)-,3,4-тиадиазол-2-ил}-2,6-диметоксибензамид, т. пл. 206-208 С.
Пример 8. ()TOp-2-беизо (в) фурил)-1,3,4-тиадазол-2-илJ-2,6-диметоксибензамид, т, пл. 244-245°С.
Формула изобретения
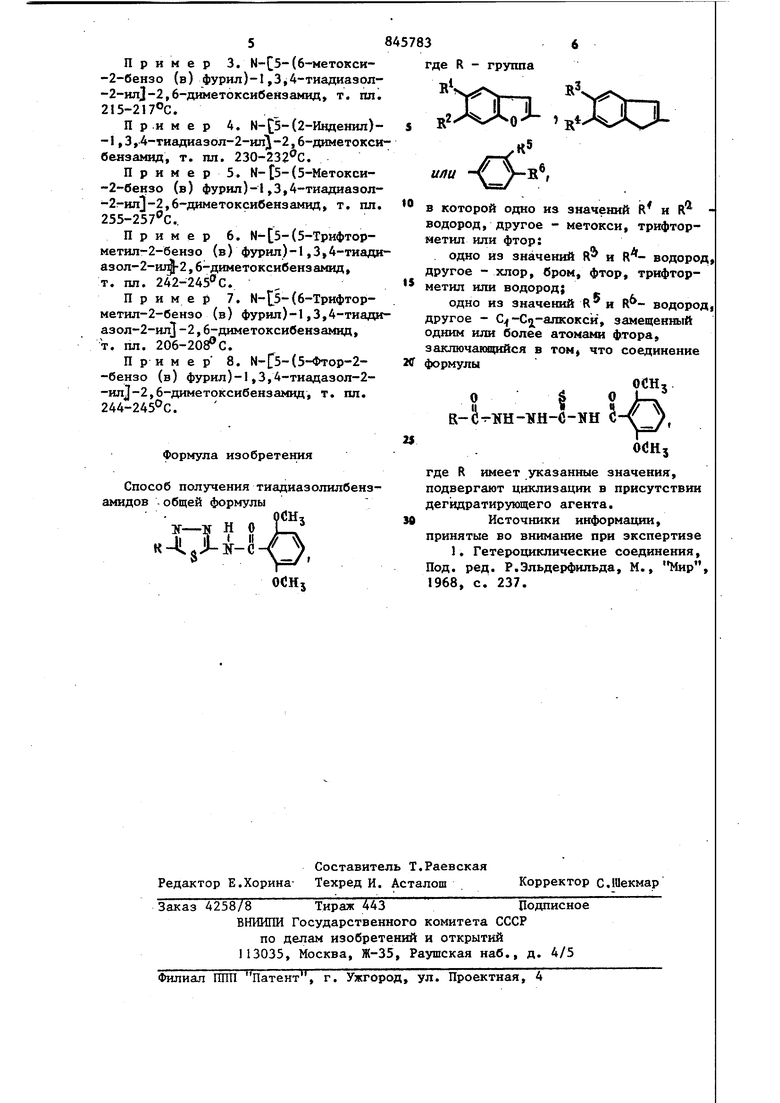
Способ получения тиадиазолилбензамидов общей формулы
« л
У--S н о
OCHi
где R - группа
в которой одно из значений R и R водород, другое - метокси, трифторметил или фтор:
одно из значений R и водород другое - хлор, бром, фтор, трифторметил или водород;
одно из значений R и водород другое - С -С5 -алкокси, замещенный одним иля более атомами фтора, заключающийся в том, что соединение
формулы
ОСИ
tО
о
UH-lfH-C-NH 5
8-SOtiHj
где R имеет указанные значения, подвергают циклизации в присутствии дегидратирующего агента. Источники информации,
принятые во внимание при экспертизе . Гетероциклические соединения, Под. ред. Р.Эльдерфильда, М., Мир, 1968, с. 237.



Авторы
Даты
1981-07-07—Публикация
1979-08-17—Подача