Изобретение относится к химии и технологии получения пурин- и пиримидин содержащих соединений, конкрет но к методам их анализа и препарати ного выделения. Известен способ хроматографическо го разделения смесей пурин- и пирим динсодержащих соединений в смеси растворителей третамиловый спирт, му равьиная кислота и вода I Недостаток этого способа - непол нота разделения пурин- и пиримидинсодержащих соединений в присутствии различных примесей. Известен также способ хроматографического разделения смеси пурини пиримидинсодержащих соединений в смеси растворителей н-бутанол, ацето ледяная уксусная кислота, 5% раствор с1ммиака, вода, взятых в соотношении 9П:2:2:4 2. Недостатком известного способа яв Яяетсй его невысокая эффективность в присутствии примесей органической и неорганической природы. Цель изобретения состоит в повышении эффективности разделения смеси. Указанная цель достигается f&Af что согласно способу хроматографического разделения смеси пурин- и пиримидинсодержащих доединений в растворителе, в качестве растворителя, используют 0,005-0,05 М раствор трилона Б или смесь, содержащую, об.%: 25%-ный водный раствор аммиака5-10 0,02-0,05 М раствор трилона Б15-30 Изопропиловый спирт До 100 или смесь, содержащую, об,%: 25%-ный водный раствор аммиака25-35 Ацетон10-25 0,02-0,05 М раствор трилона Б15-25 Изопропиловый спирт До 100 В качестве объектов исследования были взяты пуриновые и пиримидиновые основания, нуклеозиды, а также нуклеотилы: АТФ-аденозин-5-трифосфат АДФ-аденозин-5-дифосфат АМФ-аденозин-5-монофосфат УМФ-уридин-5-монофосфат УДФ-уридин-5-дифосфат. Пример На две пластинки с закрепленным слоем силикагеля Силуфол-254 наносят 2-3 капли нативного раствора АТФ. Помимо АТФ в нативном растворе содержатся в качестве балласта соли, пигменты, органичекие соединения. Элкирующую систему приготавливают следукхаим образом; берут 20% ацетона, 30%- 25%-ного водного раствора аммиака, 30% изопропилового спирта и 20% 0,05 М раствора трилона Б в воде, компоненты тщательно перемешивают взбалтыванием. Для сравнения готовят контрольную систему без трилона Б, заменяя трилон Б дистиллированной водой. Пластинки опускают в камеры, насыщенные парами эЛюат.а, Через 40 мин пластинки вынимают, подсушивают и проявляют в ультрафиолетовом свете.
При хроматографировании нативного раствора в контрольной системе получают отрицательные результаты все компоненты идут сплошной полосой.
В системе, содержащей трилон Б (динатриевую соль этилендиаминтетрауксусной кислоты), получают четкое деление на несколько .пятен. По положению свидетелей основные пятна идентифицированы как АТФ (Rf-0,35), АДФ(,46Ь A 4Ф{Rf 0,55) и аденин (.-0,73).
Пример2. На две пластинки с закрепленным слоем силикагеля - Силуфол-254 наносят 2-3 капл нативного раствора УМФ. Приготавливают следующую элюирующуго систему: ацетон 10%, 25%-ный водный раствор аммиака 34%, изопропиловый; спирт 36%, 0,02 М раствор трилона Б в воде 20%, компоненты тщательно перемешивают взбалтыванием. Для сравнения готовят контрольную систему без трилона Б, заменяя его дистиллированной водой. Хроматографирование осуществляют по примеру 1.
При хроматографировании нативног раствора в контрольнойсистеме деление компонентов смеси отсутствует. В системе, содержащей трилон Б, получают четкое делени на несколько пятен. По положению свидетелей основные пятна идентифицированлд как УМФ (Rf 0,45) к УДФ (,32).
Пример 3, На две полосы хроматографической бумаги наносят 3-5 пель нативного раствора АТФ, Элюиру тую систему готовят следующшу образом: берут 10% 25%-ного раствора аммиака, 70% изопропилового спирта и 20% 0,05 М раствора трилона Б в воде, тщательно перемешивают взбалтыванием. Контрольная система включает 10% 25%-ного раствора аммиака, 70% изопропилового . спирта и 20% води.
Разделение проводят методом нисходящей хроматографии. Время разделения 11-12 ч. После просушки хроматограммы проявляют в ультрафиолетовом свете.
При хроматографировании нативного раствора в контрольной системе получают отрицательные результаты.
В системе, содержащей трилон Б получают четкое деление на несколько пятен. По положению свидетелей основные пятна идентифицированы как соответствующие нуклеотиды (АТФ. АМФ
ЛПА 0 П П-7 D П 1П j; f 0,07, R 0,10, R 0,15, R. - 0, 57.
Пример4. На две полосы бумаги для хроматографии наносятся 3-5 капель гидролизата мицелия- инозина, Элюирующей системой является 0,01 М раствор трилона Б, Для контроля готовят систему согласно известному способу, включающую три компонента: 12 частей бутанола, 3 чати уксусной кислоты и 5 частей воды.
Разделение проводят методом нисходящей хроматографии. Время хроматогрфирования в контрольной системе составляет 16 ч, в растворе трилона Б 3 ч. (при равных расстояниях линии фронта от линии старта в обеих хроматограммах).
При хроматографировании нативного раствора в контрольной системе получают отрицательные рузультаты - все компоненты идут сплошной полосой, окрашенной в желтый цвет, обусловленный наличием пигмента.
В. растворе трилона Б получают четкое деление раствора гидролизата на 4 пятна, идентифицированные как аденин, гуанин, тимин и цитозин. СЭ5б. ,39, ,73, R 0,85,
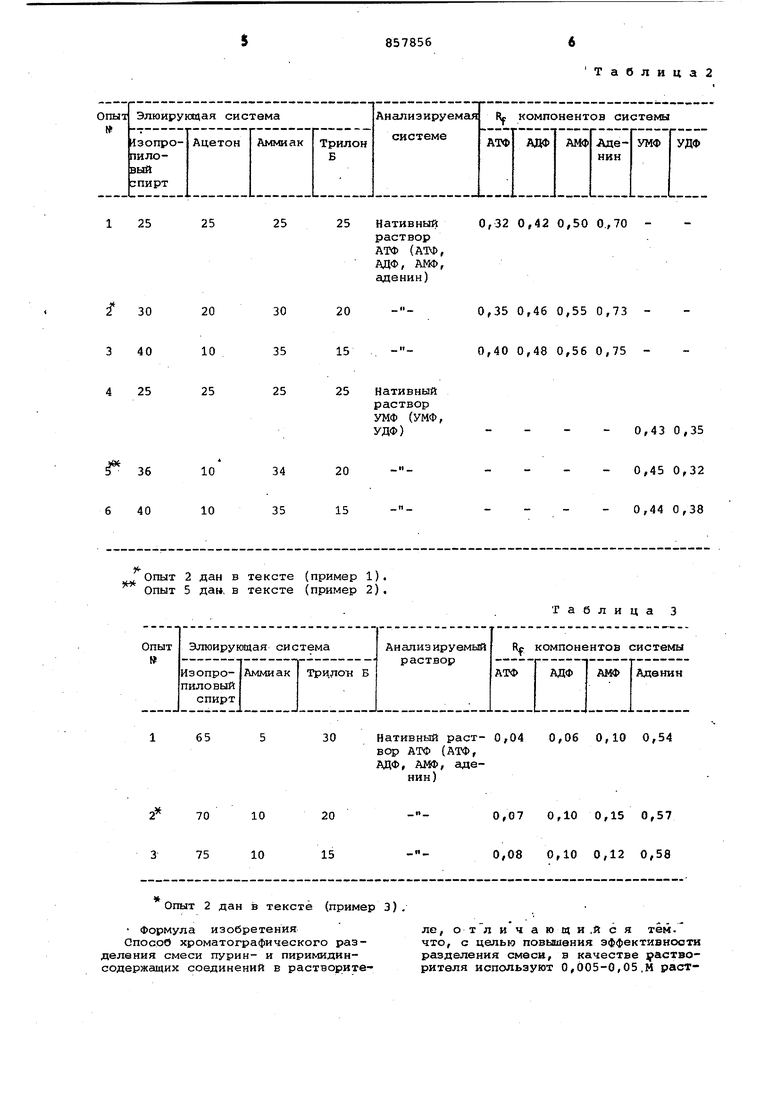
Варианты элюирующих систем и результаты хроматографического разделения приведены в табл. 1-3,
Таблица 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧИСТОТЫ АДЕНОЗИНА И ФОСФАДЕНА | 1998 |
|
RU2154825C2 |
| Способ определения кодеина в сложных лекарственных смесях | 1983 |
|
SU1133546A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОДЛИННОСТИ И ЧИСТОТЫ КСАНТИНОЛА НИКОТИНАТА | 2002 |
|
RU2226274C2 |
| Способ определения и обнаружения в моче антиретровирусных лекарственных средств в комбинированных сочетаниях | 2017 |
|
RU2655804C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЧИСТОТЫ ФТИВАЗИДА И МЕТАЗИДА | 2001 |
|
RU2225205C2 |
| Способ определения и обнаружения в моче фторсодержащих лекарственных средств в комбинированных сочетаниях | 2019 |
|
RU2710259C1 |
| Способ получения аденозин-5-монофосфата,меченного фосфором-32 | 1982 |
|
SU1127888A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОДЕИНА | 2013 |
|
RU2523408C1 |
| Способ определения в моче, слюне или плазме крови лекарственных веществ | 2023 |
|
RU2828792C1 |
| Способ определения производных 5-нитрофурана и полупродуктов их синтеза | 1990 |
|
SU1748057A1 |

опыт 2 дан в тексте (пример 4),
Опыт 2 дан в тексте (пример 1).
4k Опыт 5 дан, в тексте (пример 2),
30Нативный раст- 0,04
70 10
20
15
10
3 75
Опыт 2 дан в тексте (пример
Формула изобретения СпосоО хроматографического разделения смеси пурин- и пиримидинсодержащих соединений в растворитеТаблица2
Таблица 3
0,06 0,10 0,54
вор АТФ (АТФ, ДЦФ, АМ:, аденин)
0,07 0,10 0,15 0,57
0,08 0,10 0,12 0,58
ле, отл и ч ающи.й с я темчто, с целью повышения эффективности разделения смасн, в качестве ipacTBOрителя используют О,005-0,05,М раст7 857 вор трилона Б или смесь, содержащую об.%| 25%-ный водный раствор аммиака 5-10 0,02-0,05 М раствор трилона Б 15-30 Иэопропиловый спирт До 100 или смесь/ содержащую, об.%« 25%-ный водный раствор аммиака 25-35 8568 Ацетон 10-25 0,02-0,05М раствор грилона Б 15-25 Иэопропиловый спирт До 100 Источники информации . принятые во внимание при экспертизе 1 Хроматография в тонких слоях. Под ред. Э Штдль, М., Мир, 1965, с. 443. 2. Там же, с. 445 (прототип).
Авторы
Даты
1981-08-23—Публикация
1979-09-05—Подача