Предлагается новый способ получения кратно меченных биологически активных соединений. Меченный тритием аденозин находит широкое применение в экспериментах по биохимии и молекулярной биологии.
Известен способ получения (8-3Н) аденозина, по которому 16,5 мг (48 мкмоль) 8-бромаденозина, растворенного в 0,7 мл 1 н. КОН, подвергают взаимодействию с газообразным тритием в присутствии 20 мг катализатора (5% Pd/BaSO4), получая с выходом 40% (8-3Н)аденозин с удельной активностью 11,6 Ки/ммоль.
Известен также способ получения (8-3Н)аденозина путем обработки 8-бромаденозина в водно-спиртовой среде газообразным тритием в присутствии палладиевого катализатора (например, Pd/C) и щелочи. Целевой продукт выделяют известными приемами. Выход целевого продукта 50%, удельная активность 5-15 Ки/ммоль). По данному способу мольное отношение 8-бромаденозин: щелочь 1: 0,6 и на 1 мкмоль субстрата (8-бромаденозина) применяют 0,15 мг катализатора [2].
Недостатками известных способов являются небольшой выход и относительно невысокая удельная активность получаемого меченого аденозина, ограничивающая сферу его применения. Так для целого ряда экспериментов в области молекулярной биологии необходим меченный тритием аденозин с удельной активностью 40 Ки/ммоль. Максимальная теоретически возможная величина удельной активности (8-3Н)аденозина, получаемая известными способами и соответствующая введению одного атома трития, составляет 29 Ки/ммоль.
Целью изобретения является получение кратно меченного тритием соединения высокой удельной активности - более 40 Ки/ммоль.
Поставленная цель достигается новым способом получения нового (2,8-3Н2) аденозина. Способ получения (2,8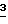 Н2) аденозина заключается в том, что 2-хлораденозин подвергают взаимодействию с газообразным тритием над катализатором 4-6% Pd/BaSO4 в присутствии щелочи при мольном соотношении 2-хлораденозин: щелочь 1:(3-3,5), используя на 1 мкмоль 2-хлораденозина (0,8-1,1) мг катализатора. При уменьшении количества щелочи или катализатора выход меченого аденозина уменьшается вследствие неполноты реакции. При увеличении количества катализатора возрастают потери меченого аденозина вследствие адсорбции на катализаторе. Увеличение количества щелочи в значительной степени затрудняет последующую очистку препарата от неорганических солей, что также приводит к потере меченого соединения. Уменьшение процентного содержания палладия, например, до 1-2% нецелесообразно, так как содержание палладия будет настолько мало, что катализатор может утерять каталитические свойства. Значительное же увеличение процентного содержания палладия, например до 10%, приведет к катализатору, по свойствам близкому к палладию без носителя, что в свою очередь может изменить механизм реакции каталитического дегалогенирования. Содержание палладия 4-6% является оптимальным для данного процесса.
Н2) аденозина заключается в том, что 2-хлораденозин подвергают взаимодействию с газообразным тритием над катализатором 4-6% Pd/BaSO4 в присутствии щелочи при мольном соотношении 2-хлораденозин: щелочь 1:(3-3,5), используя на 1 мкмоль 2-хлораденозина (0,8-1,1) мг катализатора. При уменьшении количества щелочи или катализатора выход меченого аденозина уменьшается вследствие неполноты реакции. При увеличении количества катализатора возрастают потери меченого аденозина вследствие адсорбции на катализаторе. Увеличение количества щелочи в значительной степени затрудняет последующую очистку препарата от неорганических солей, что также приводит к потере меченого соединения. Уменьшение процентного содержания палладия, например, до 1-2% нецелесообразно, так как содержание палладия будет настолько мало, что катализатор может утерять каталитические свойства. Значительное же увеличение процентного содержания палладия, например до 10%, приведет к катализатору, по свойствам близкому к палладию без носителя, что в свою очередь может изменить механизм реакции каталитического дегалогенирования. Содержание палладия 4-6% является оптимальным для данного процесса.
Получаемый по данному способу меченый аденозин содержит кратную тритиевую метку в положении 2 и 8 аденинового ядра, что доказывается величиной удельной активности, превышающей максимально теоретически возможную при введении одного атома трития, а также результатами кислотного гидролиза. Радиохроматографический анализ показал, что получаемая при гидролизе рибоза не содержит тритиевой метки, а удельная активность аденина, который содержит С-Н-связи только в положениях 2 и 8, равна удельной активности исходного аденозина.
П р и м е р 1. 12 мг (40 мкмоль) 2-хлораденозина растворяют в 1 мл 50% -ного (по объему этанола, добавляют 0,12 мл (120 мкмоль) 1н. NaOH, 36 мг 5% Pd/BaSO4 и раствор при постоянном перемешивании выдерживают в атмосфере газообразного трития (при атмосферном давлении). После прекращения поглощения трития (примерно через 3 ч) отделяют катализатор фильтрованием или центрифугированием, раствор нейтрализуют 1 н. HCl до рН 7,0-7,5, упаривают досуха в вакууме ротационного испарителя и для удаления лабильного трития трижды упаривают в вакууме ротационного испарителя, добавляя каждый раз по 10 мл 50% -ного этанола. Для удаления неорганических солей продукт подвергают гель-хроматографии на колонке с Сефадексом G-10 (13х650 мм). Фракцию, содержащую меченый аденозин и свободную от солей, разбавляют 50%-ным этиловым спиртом до радиоактивной концентрации 1-5 мКи/мл. Выход (2,8-3Н2)аденозина составляет 1340 мКи (460 ОЕ260, что соответствует 80%-ному выходу от взятого в реакцию 2-хлораденозина). Удельная активность 45 Ки/ммоль, радиохимическая чистота 99%).
Характеристики УФ-спектра поглощения (Н2О): λмакс = 260 нм; D250/D260 = 0,79; D280/D260 = 0,15.
П р и м е р 2. 12 мг (40 мкмоль) 2 -хлораденозина растворяют в 1 мл 50% -ного (по объему) этанола, добавляют 0,06 мл (60 мкмоль) 1 н. NaOH, 12 мг 5% Pd/BaSO4 и проводят реакцию дегалогенирования в течение 3 ч в условиях, аналогичных примеру 1.
Характеристика УФ-спектра поглощения (Н2О): λмакс = 264-265 нм; D250/D260 = 0,68; D280/D260 = 0,29, что соответствует УФ-спектру поглощения исходного 2-Cl-аденозина.
Основным преимуществом способа получения меченного тритием аденозина является существенное улучшение качества целевого продукта, выражающееся в повышении его удельной активности примерно в 3 раза, а также повышение выхода примерно в 2 раза по сравнению с (8-3Н)аденозином, имеющим метку только в 8 положении ядра.
СПОСОБ ПОЛУЧЕНИЯ (2,8-3H2) АДЕНОЗИНА, отличающийся тем, что 2-хлораденозин подвергают взаимодействию с газообразным тритием над катализатором 4 - 6% Pd/ BaSO4 в присутствии щелочи при мольном соотношении 2-хлораденозин : щелочь 1 : 3 - 3,5, используя на 1 мкмоль 2-хлораденозина 0,8 - 1,1 мг катализатора.
Авторы
Даты
1994-06-15—Публикация
1980-01-28—Подача