(54) СПОСОБ ПОЛУ-ЧЕНИЯ ДЕЗОКСИАНТРАЦЖЛРШОВ
1
Изобретение относится к способу получения новых производных антрациклина, обладающих противоопухолевой активностью.
Известен способ получения производных антрациклина путем синтеза последних,основанного на известной реакции каталитического гидрированиярЗЦель изобретения - получение новых соединений, расширяющих арсенал средств воздействия на живой организм.
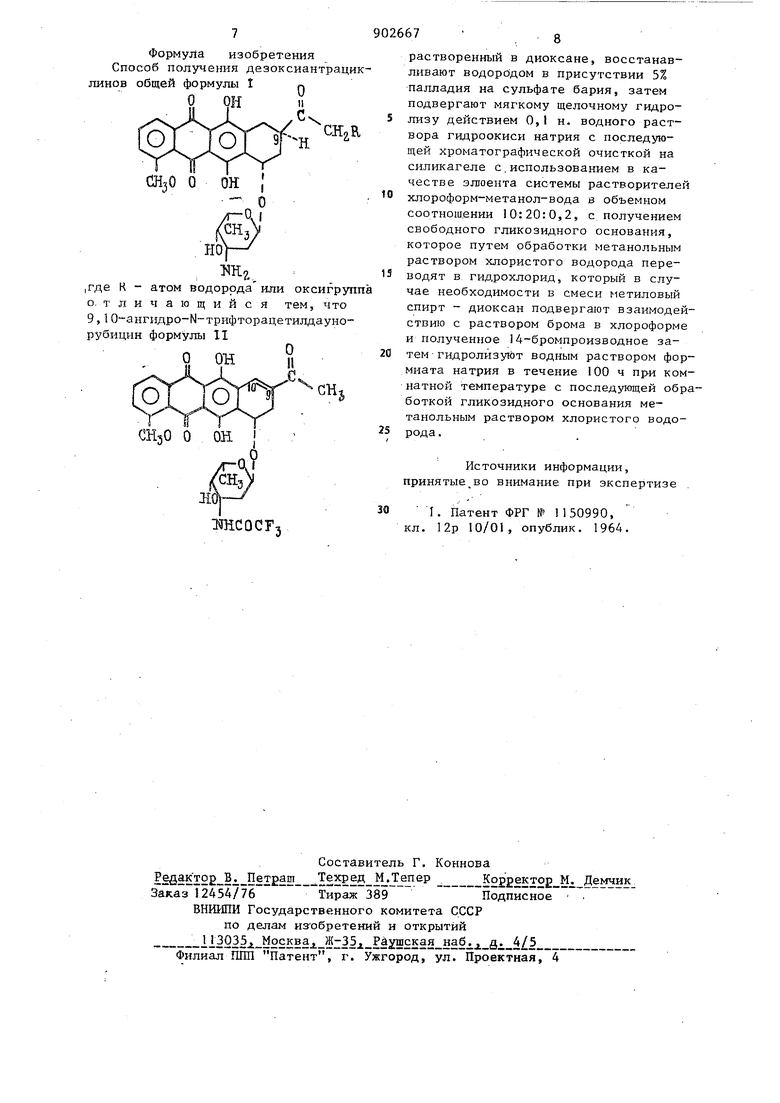
Поставленная цель достигается тем, что в способе получения дезоксиантраЦиклинов общей формулы
CH,.R , где R атом водорода или ок9, Ю-ангидро-М-трифтор- 25 сигруппа. ацетшщаунорубицин общей формулы1«HCOCF р,1створеннын в диоксане, носстаиавл вают водородом в присутствии 5% пал ладия на сульфате бария, затем подв r.uoT мягкому щелочному гидролизу ,.; -Гстинем Oji и. водного растворе гндрооккс.н натрия с послегдующей хро матографической очисткой на силикаг ле с использованием а качестве ЭЛБОента системы растворителей хлороформ-метаиол-вода в объемном соотно юеиия 10:20:0,2, с получением свободного гликозидного основания, которое обработкой метанольным раствором хлористого водорода переводят в гндрохлорид, которьш в случае необходимости в смеси метиловый спирт диоксан подвергают взаютодействию с раствором брома в хлороформе и полученное 14-бромпроизводное затем rs ponHs niOT водным раствором формиата натрия в течение 00 ч нри комнатной темнературе с последующей об работкой гликозидного основания метанольяьсм раствором хлористого во дорода. Целевой продукт выделяют из вестными приемами. Новые соединения формулы 1 облад ют противоопухолевой активностью и могут использоваться в качестве лечебных препаратов для лечения опухо лей у млекопитающих. Пример 1. 9-Дезоксидауноруб цин ( 1) KuVR 8А . 2,0 г 9,1О-ангущро-Н-трифторацет даунорубицин (II) растворяют в 50 мл диоксана и гидрируют при ком натной температуре под давлением в присутствии 4,0 г (5%) палладия на сульфате бария. За восстановлением сле41ят тонкослойной хроматогрз фией, осуществляемой на пластинках Кизельгель Мерк F2jj| с использованием системы растворителей хлороформ: ацетон в объёмном соотношении 4:, поскольку, чтобы избежать гидр генолиз гликозидной связи, гидриpOBaime должно ирерьгоаться при осхаточном содержании исходного маге риала около 20%. Сырой продукт, получаемый после фильтрования и выпаривания растворителя, растворяют в 30 мл ацетона и обрабатывают при О С 300 мл 0,1 н. водного раствора гидроокиси натрия. Затем рН раствора доводят до 8,3 и экстрагируют повторно хлороформом. Объединенные органические экстракты, высушенные над безводным сульфатом натрия, выпаривают досуха в вакууме и остаток очищают хроматографически на колонке с силикагелем, используя в качестве растворителя смесь хлороформ - метанол - вода в объемном соотнопении 10:20:0,2. Фракции, содержащие 9-дезоксидаунорубицин в виде свободного основания, объединяют и экстрагируют 0,1 н. соляной кислотой. Кислый водный красный раствор отделяют, регулир тат рИ до 8,3 с помощью 0,5 н, гидроокиси натрия и экстрагируют хлороформом вплоть до nojnioro перехода красного продукта в органическую фазу. Затем объедине1П1ые хлороформные экстракты, высущенные над безводнь М сульфатом натррш, упаривают под вакуумом до малого объема (20 мл) и подкисляют до рН 3,5 (красный конго) безводным хлористым водородом. Добавление избытка серного эфира позволяет получить 0,4 г хлор гидра та 9-дезокс1щаунорубиц1П1а с т.пл. 162 С (с разложением). Продукт подвергают очистке методом тонкослойной хроматографии на пластипках Кизельгель Мерк , используя в качестве элюир тощего растворителя смесь хлороформа, метилового спирта и воды в объемном соотношении 10:2:0,2; R| 0,25. Найдено, %: Н 5,64; С 58,60; N 2,48, С1 6,47; . Вычислено, %: Н 5,53; С 59,17; N 2,56; С1 6,47. П р и м е р 2, 9-дезоксидоксорубицин (i ) 85. 0,7 г гидрохлорида 9-дезоксидаунорубицина (|) растворяют в 40 мл смеси из безводного метанола и диоксана в объемном соотношении 1:3 и 0,7 мл этилортоформиата. К этому раствору прибавляют 2,8 мл раствора 1 ,.86 г брома в 20 мл хлороформа. После выдержки в течение 60 мин при комнатной температуре реакционную
.смесь выливают в 200 мл смеси диэтиЛОВО1-О эфира и петролейного эфира в объемном соотношении(2:I). Образовавшийся красный осадок после отфильтровыиания и промывания диэтиловым эфиром растворяют в смеси из 12 мл ацетона и 0,25 г водного раствора бромистого водорода. После выдержки в течение 12-15 ч при комнатной температуре смесь разбавляют и экстрагируют хлороформом. Водную фазу экстрагируют несколькими порциями н-бутанола и объединенные экстракты выпаривают в вакууме до небольшого объема для получе шя 14-бромгликозидш)го производного, которое после этого растворяют в 13,4 мл 0,25 н. водного раствора бромистого водорода и обрабатывают 1,0 формиата натрия в 10 мл воды.
Реакционную смесь выдерживают при комнатной температуре при перемешивании в течение 90-110 ч и после этого выпаривают досуха в вакууме
Полученный остаток, растворенный в 240 мл смеси из хлороформа и метанола в объемном соотношении 2:1, промывают двумя порциями 2,5%-ного водного раствора бикарбоната натрия и после этого повторно экстрагируют хлороформом.
I
Объединенные хлороформные экстракты сушат над безводным сульфатом натрия и выпаривают до небольшого объема в вакууме. Полученный красный раствор доводят до рН 3,5 при помощи безводного метанольного раствора хлористого водорода; после этого прибавляют избыток диэтилового эфира для осаждения 0,37 г 9-дезоксидоксорубицина в форме гидрохлор1ада (вы- ход 54%). Т.пл. составляет 170°С (с разложением). При тонкослойной
хроматографии на пластинках Мерк с системой растворителей хлороформметанол-вода в объемном соотношении 13:6:1 получают величину Rf 0,26.
Найдено, %: Н 5,17; С 57,57; С1 6,21
C HjoClNOio
Вычислено, %: Н 5,37; С 57,49; С1 6,29.
Биологическая активность.
Соединения, полученные предлагаемым способом, испытаны при содейст ВИИ Национального института здоровья г. Бефезда, штат Мериленд против яимфолейкоза Pigg в соответствии
с известной методикой, описанной в отчетах по хемотерапии рака.
Данные, приведенные в таблице, иллюстрируют противоопухолевую активность 9-дезоксидаунорубицина и 9-дезоксидоксорубицина в сравнении с даунорубицином и доксорубицином.
Соединения испытаны in vivo на CDF мьшах, зараженных опухолевыми клетками. На 5-й, 9-й и 13-й дни после трансплантации опухоли мышам введены интраперитониально инъекции (4-дневный перерывмежду каждой инъекцией) . Средняя продолжительность выживания в процентах от контрольных приведена в таблице. Формула изобр Способ получения дез линов общей формулы I /-0 I . PV НО)- атом водорода и чающийся 9,10 ангидро-М трифтора рубицин формулы II TOICOC растворенный в диоксане, восстанавливают водородом в присутствии 5% палладия на сульфате бария, затем подвергают мягкому щелочному гидролизу действием 0,1 н. водного раствора гидроокиси натрия с последующей xpo faтoгpaфичecкoй очисткой на силикагеле с.использованием в качестве элгаента системы растворителей хлороформ-метанол-вода в объемном соотношении 10:20:0,2, с получением свободного гликозидного основания, которое путем обработки метанольным раствором хлористого водорода переводят в, гидрохлорид, который в случае необходимости в смеси метиловый спирт - диоксан подвергают взаимодействию с раствором брома в хлороформе и полученное 14-бромпроизводное затем гидролйзуйт водным раствором формиата натрия в течение 100 ч при комнатной температуре с последующей обработкой гликозидного основания метанольным раствором хлористого водорода . Источники информации, принятые во внимание при экспертизе . I. Патент ФРГ № 1150990, кл, 12р 10/01, опублик. 1964.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гликозидов | 1979 |
|
SU963471A3 |
| Способ получения гликозида | 1987 |
|
SU1590045A3 |
| Способ получения 4-деокси-даунорубицина или 4-деокси-доксорубицина | 1981 |
|
SU1277902A3 |
| Способ получения антрациклин-глико-зидОВ | 1979 |
|
SU797583A3 |
| Способ получения гликозидов антрациклина | 1976 |
|
SU728719A3 |
| 8-ФТОРАНТРАЦИКЛИНГЛИКОЗИДЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ПРИСОЕДИНЕНИЯ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2095365C1 |
| Способ получения 4-деоксиадриамицин гидрохлорида | 1977 |
|
SU730310A3 |
| Способ получения гликозидов антрациклина | 1980 |
|
SU993822A3 |
| АНТРАЦИКЛИНОВЫЙ ГЛИКОЗИД И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 1990 |
|
RU2073681C1 |
| Способ получения хлоргидратов замещенных антрациклинов | 1979 |
|
SU867315A3 |


Авторы
Даты
1982-01-30—Публикация
1979-05-08—Подача