Изобретение относится к способу получения новых хлоргидратов замеще ных антрациклинов, обладающих ценны .ми противоопухолевыми свойствами. Известна реакция взаимодействия тетрациклиновых агликонов с произво ными даунозамина 1 . Цель изобретения - получение новых соединений, расширяющих арсенал срЬдств воздействия на живой организм. Поставленная цель достигается получением хлоргидратов замещенных антрациклинов общей формулы группа COCHj или СОСН/ ОН-, ОН; R - OCHjf R - Н, -группа COCHj или COCHijOHj или R -ОН; R - Н; R - OCHj,, аключающийся в том, что 9,10-ангидо- N -трифторацетилдауномицин фор О ОН NHtOCF, растворенный в метиловом спирте, сначала восстанавливают цианоборогидридом натрия в присутствии 0,1 н. водной соляной кислоты ири комнатной температуре до соответствующего 9, 10-ангидро-13-дигидро- N -трифторацетилдауномицина формулы ОН .СНОНСН,
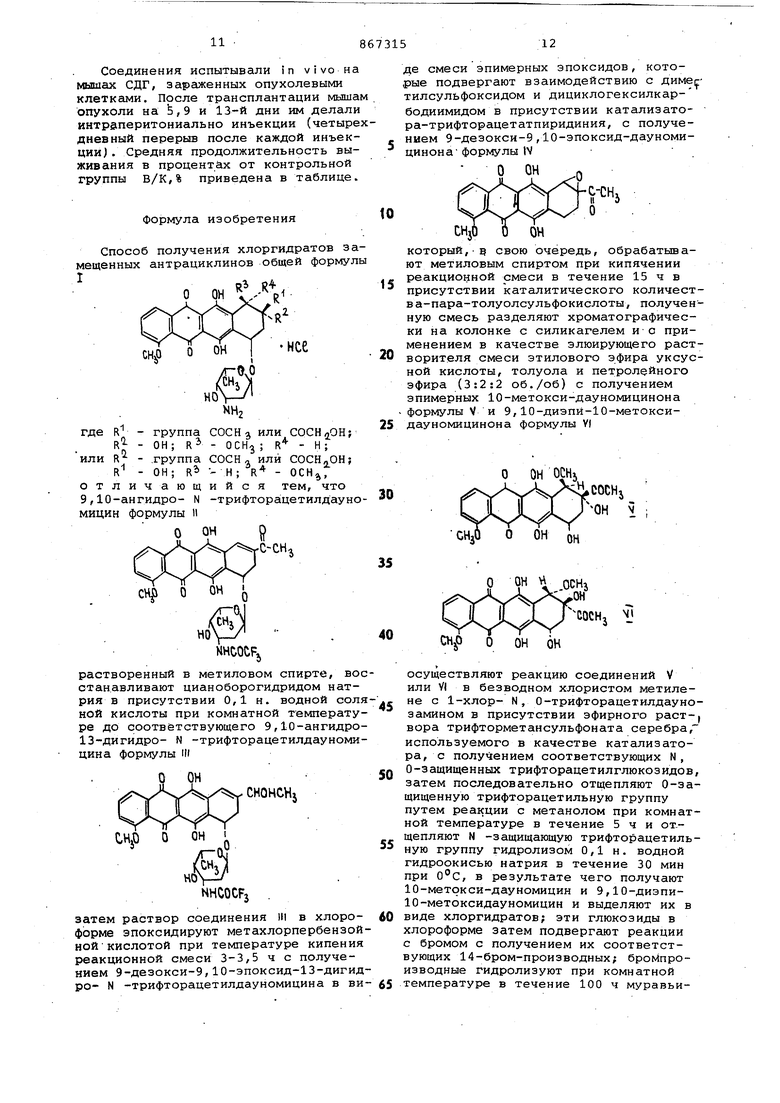
затем раствор соединения III в хлороформе эпоксидируют метахлорпербензойной кислотой, при температуре кипения реакционной смеси 3-3,5 ч с получением 9-дезокси-9,10-эпоксид-13-дигидро- N-трифторацетилдауномицина в виде смеси зпимерных эпоксидов, которые подвергают взаимодействию с диметилсульфоксидбм и дициклогексилкарбодиимидом, используя в качестве катализатора трифторацетат пиридиния, с получением 9-дезокси-9,10-эпоксиддауномицинона формулы
О
О ОН
который,в свою очередь, обрабатыва,ют метиловым спиртом при кипячении реакционной смеси в течение 15 ч в присутствии каталитического количества пара-толуолсульфокислоты, полученную сМесь разделяют хроматографическина колонке с силикагелем и с применением в качестве элюирующего растворителя смеси этилового эфира уксусной кислоты, толуола и петролейного эфира (3:2:2 об/об) с получением эпимерных 10-метокси-дауномицинЬна формулы V и 9,10-диэпи-10-метокси-дауномицинона формулы VI
О ОН
ОН
О ОН Н ,0(На - ОН
COCHj
Si
ОН он
осуществляют реакцию соединений Y или VI в безводном хлористом метилене с 1-хлор- N, 0-трифторацетилдаунозамином в присутствии эфирного раствора трифторметансульфоната серебра .используемого в качестве катализатора, о получением соответствующих N, О-защищенных трифторацетилглюкозидов, затем последовательно отщепляют 0-защищающую трифторадетильную rpyfiny путем реакции с метанолом при комнатной температуре в течение 5ч и отщепляют N-защищающую трифторацетильную группу гидролизом 0,1 н. водной гидроокисью натрия в течение 30 мин при 0°С, в результате чего получают 10-метоксидауномицин и 9, 10-диэпи-10-метоксидауномицин и выделяют их в виде хлоргидратов; эти глюкозиды в хлороформе затем подвергают реакции с бромом с получением их соответствующих 14-бром-производных бромпроизводные гидролизуют при комнатной температуре в течение 100ч муравьинокислым натрием с получением соответственно 10-метокси-адриамицина и 9,10-диэпи-10-метоксиадриамицина, которые выделяют в виде их хлоргидратов.
В качестве исходных реагентов для получения новых глюкозидов применяются антрациклиноны V и V/ , которые ранее были неизвестны. Их синтезируют из 9,10-ангидро- N - трифтораЦетил-даунорубицина формулы VII .
Чтобы осуществить эпоксидирование сопряженной двойной связи при С-9 и С-10 в соединении VII , сначала восстанавливают кетонную функциональную группу до соответствующего oL, ft ненасыщенного спирта. Восстановлением с использованием цианоборогидрида натрия в приемлемом смешивающимся с водой органичееком растворителе, таком как диоксан, или диметоксиэтан, в присутствии минеральной кислоты получают с количественным выходом соответствующее 13-дигидропроизводное формулы Viit . Это соединение затем подвергают реакции эпоксидирования, используя мета-хлорпербензойную кислоту в апротонном растворителе, таком как хлористый метилен,, хлороформ или ацетон.
Реакция эпоксиидирования протекает в диапазоне температур от 25 до , с образованием 9,10-эпоксид13-дигидро- N -трифторацетилдаунорубицина формулы Х в виде эпимерной смеси. Регенерацию кетонной функциональной группы с одновременным расщепленйем глюкозидной связи осуществляют окислением диметилсульфоксидом и дициклогексилкарбодиимидом,используя в качестве катализатора трифторацетат пиридиния. Выход реакции окисления определяется количеством катализатора: при отношении вещества к соли 1:1 с высоким .выходом получают соединение формулы х .
Последующее введение метоксильной группы, которое достигается раскры тием оксиранового кольца соединения X с помощью метилового спирта в присутствии каталитического количества пара-толуолсульфокислоты., позволяет получить смесь агликонов формул V и VI в отношении 7:2 (приблизительно). Эту смесь разделяют хроматографическ на силикагеле. Соединения V и VI различаются стереохимически при С-9 и С-10 центрах. Фактически, толь.ко соединение V дает 7,9-изопропилиденовое производное формулы )( путем обработки 2,2-диметоксипропаном, с гидроксильными группами при С-7 и С-9 в циположении.
Спектр ЯМР соединений .V и VI показал, что С-10 Н имеет эквагориальную ориентацию в соединении V и осевую ориентацию в соединении VI . Обработкой соединения VI 2,2-диметокси-пропаном получают 7-метокси-9,10-диэпи10-метоксидауномицинон формулы Х1 . Реакцию сочетания упомянутых агли конов формул V и VI с N, О-защищенны галоидированным сахаром формулы с целью образования глюкозидной связи осуществляют в приемлемом органическом растворителе, таком как хлорофор хлористый метилен, тетрагидрофуран, в присутствии соли серебра, являющей ся катализатором. Таким образом, полученный N.О-защищенный глюкозид сна чала обрабатывают метиловым спиртом для отщепления 0-защищающей тоифторацетильной группы у остатка сахара в результате чего получают N-защишен ные глюкоз иды VIV и XV . Эти продукты путем мягкой щелочной обработки прев ращают с количественным выходом в 10 метоксидаунорубицин и 9,10-диэпи-10метоксидаунорубицин(целевые продукты , где R СОСНз; R rt ° ОСНз: R Н; R ОН; R СОСНЗ; R Н;. R ОСНг,) . Другие два аналога доксорубицина получают из приведенных целевых прогдуктов через их 14-бромпроизводные. Новые соединения формулы I обладают противоопухолевой активностью и могу использоваться в качестве лечебных -препаратов для лечения опухолевых за болеваний у млекопитакиаих. Пример 1. 9,10 ангидро-.13дигидро-м-трифторацетилдаунорубицинформулы V11I . В 2000 мл метилового спирта растворяют 6,0 г (10 ммоль) 9ДО-ангидро- N -трифторацетил-даунорубицина формулы VU. PacTBOD подкисляют 50 мл 0,1 раствора соляной кислоты в воде и затем осуществляют реакцию с водным раствором NaCNBH (4,0 г в 200 м Н,О) . Реакционную смесь перемешиваю при комнатной температуре в течение 48 ч, поддерживая рн ниже 4 добавлением 0,1 н. водной соляной кислоты. После нейтрализации избытком твердого бикарбоната натрия раствор испаря ют досуха в вакууме, и остаток, раст воренный в хлороформе, промывают водой . Хлороформовый раствор сушат над безводным сульфатом натрия, и раство ритель окончательно удаляют в вакууме для получения сырого соединения Vlil. Чистый 9,10-ангидро-13-дигидроN-трифторацетил-даунорубицин получают путем хроматографической очистки на колонке с кремневой кислотой,, используя в качестве элюируюшего растворителя, систему хлороформ-ацетон (95:5 об/об). Продукт плавится при (с разложением). Максимумы поглощения в видимом спектре (СНСЦ) находятся при 520 и 556 мкм. Пример 2. Синтез 9-дезокси9,10-эпоксидо-13-дигидро- N -трифторацетилдаунорубицина формулы IX . К раствору 8 г (13,28 ммоль) 9,10ангидро-13-дигидро- N -трифторацетилдауномицина формулы V/C в 400 мл хлороформа добавляют 1,08 г (6 ммоль) мета-хлорналбензойной кислоты и реакционную смесь выдерживают при кипении в течение 3 ч. Первоначальный вишневый цвет раствора постепенно меняется на красный. Реакционную массу затем охлаждают и промывают водным насьиценным раствором NaHCOgi водой, и сушат над безводным сульфатом натрия. Растворитель вьшаривают досуха в вакууме. Остаток (2,0 г) с максимумом в спек;тре видимого света (CHClg) при 490, 504, 540 мкм (что согласуется с исчезновением двойной связи при С-9, С-10 соединения Vif ) представляет собой эпимерные эпоксиды и применяется в псследуклцих отгщиях без дополнительной очистки. Пример 3. 9-Дезокси-9,10эпоксид-дауномицинон формулы X . К перемешиваемому раствору 3,85 г (6 ммоль) 9-дезокси-9,10-зпоксид13-дигидро- N -трифторацетилдауномилина формулы IX в 100 мл безводного диметилсульфоксида в атмосфере азота последовательно добавляют 3,8 г (18 юль) дициклогексилкарбодиимида, 0,5 мл (6 мадоль) безводного пиридина и 0,23 мл (3 ммоль) трифторуксусной кислоты. Смесь перемешивают при комнатной температуре в течение 15 мин, затем разбавляют 500 мл хлорофорйа. Хлороформовый раствор тщателы. но промывают водой, сушат и выпаривают досуха. Остаток растворяют в этиловом эфире уксусной кислоты, отфильтровывают нерастворимую дициклогексилмочевину и фильтрованный раствор выпаривают досуха, получая соединение X с количественным выходом. ИК-спектр: 1720 см- 1580 и 1620 см хинон.. ЯМР-спектр (CDCU)cr : при 2,27 . (1, СНг-С 0) 4,10 (синглет, OGHj) и 4,81 Л1, Н-10). П р и ме.р 4. Синтез 10-метокси-дауноми.цинона формулы V и 9,10диэпи-10-метоксидауномицинона формулы VI . Раствор 4,3 г 9-дезокси-9,10-эпоксид-дауномицинона формулы X в 500 мл безводного метилового спирта нагревают при температуре кипения с обратным холодильником в течение 15 ч в присутствии каталитического количестг а пара-толуолсульфокислоты. Реакционную смесь затем охлаждают и выпаривают досуха. Остаток растворяют в 300 мл хлороформа, промывают водным . 5%-ным раствором бикарбоната натрия, водой, сушат над безводным сульфатом атрия и выпарив ают досуха. Сырой атериал представляет собой смесь соединений Y и V/ в отношении 7:2,при лизительно. Его подвергают хроматографическому. разделению иа колонке с кремневой кислотой, используя в к честве элюирующего вещества смесь этилацетата, толуола и петролейного эфира (3:2:2 об/об). Получают 1,5 г чистого соединени формулы V и 0,42 г чистого соединения, формулы У/ с 72%-ным выходом 10 метокси-дауномицинона формулы у . Т пл. 22оРс (с разложением). +206 (с 0,1, СНС1э). Масс-спектр: т/ё 428 (М), 396 (М-СНзОН), 353 (M-CHaOH-CHjCO)J ЯМР (CDCU) сЛ : 3,51 (синглет, C-lO-dCHj); 4,66 (дуплет, С-10 Н)j 5,31 (квадруплет, С-7Н), 13,6 и 14, (синглет, ОН фенола). 9,10-диэпи-10-метоксидауномицино формулы VI т.пл. 15бс (с разложени ем),. Масс-спектр: т/е 428 (М ). ЯМР-спектр (CDCl) : 3,64 (син глет, C-10-OCH,j)j 4,89 (синглет, С10Н), 5,12 (квадруплет, С-7Н), 13,8 и 14,21 (синглет, фенольный ОН). Пример 5. 7,9-Изопропилиден-10-метоксидауномицинон формулы XI . К раствору 0,1 г соединения VII в 10 мл безводного диоксана добавляют 5 мл 2,2-диметОксипропана и каталитическое количество пара-толуолсуль фокислоты. Реакционную смесь выдер. живают при 50°С в течение 48 ч, затем разбавляют 50 мл хлороформа и промывают водным насыщенным раствором бикарбоната натрия, водой и сушат над безводным сульфатом натрия. Получаемый выпариванием органическо го растворителя сырой остаток подве гают хроматографической о 1истке на колонке с кремневой кислотой, испол зуя в качестве элюирующего раствори теля смесь хлороформа и ацетона в отношении 95-5 об/об. Получают чи тый 7,9-изопропилиден-10-метокси-да номицинон формулы XI . Масс-спектр продукта: т/е 468 (М-) 410 (М-(СНз)о,СО) 378 (М-(СНа)2СО-СНо,ОН) . ЯМР-(СОС1з) СЛ : 1,2 и 2,47 (синглет, 2CHj)-, 5,47 (мультиплет, С-7Н Пример 6. 7-Метокси-9,10диэпи-10-метоксидауномицинон.формулы XII . Обработкой соединения VI 2,2-дим тoкdипpoпaнoм в соответствии.с мето дик (й. примера 5 получают 7-метоксй9,10-ДИЭПИ-10-метоксидауномицинон формулы XV . Масс-спектр: т/е 422 ()-i Пример 7. Синтез хлоргидрата 10-метоксидаунорубицина МАР87. К раствору 0,43 г (1 ммоль) 10метоКСидауномицинона формулы Y в 200 мл безводного хлористого метиле на добавляют 0,43 г (1,2 ммоль) 1хлор- N,0-трифт6рацетилдаунозамина. Затем при сильном перемешивании в течение Ю мин при комнатной температуре добавляют к раствору 0,32 г (1,2 ммоль) в 26 мл безводного серного эфира. Затем к реакционной смеси добавляют 0,2 мл (1,4 ммоль) безводного этилметилпиридина. Спустя 40 мин смесь обрабатывают насыщенным водньии раствором бикарбоната натрия и отделившуюся органическую фазу испаряют в вакууме. Остаток растворяют в 100 мл метанола и выдерживают при комнатной температуре в течение 5 ч. Остаток, который получают при удалении растворителя, прдвергают хроматографической очистке на колонке с кремневой кислотой, ис.пользуя смесь хлороформа и ацетона в отношении 4:1 об/об., в качестве элюирующего растворителя. Помимо непрореагировавшего соединения V получают 0,26 г чистого 10-метокси- N трифторацетилдаунорубицина формулы I. Т.пл. продукта 190°С (с разложением) . Осуществляют тонкослойную хроматографию на пластинке Кизельгель F (Мерк) с использованием системы растворителей хлороформ и ацетон .(4:1 об./об. R 0,3) ; ЯМР-спектр (СОС1з)сА : 1,30 (дуплет, СН 2,-CH)V 3,52 (синглет, С-10 ОСИ ); 5,30 (мультиплет, С - 7Н) и 5,53 (мультиплет, С-1 - HcixWH 7 Гц). 10-Метоксидаунорубицин (0,26 г) растворяют в 0,-1 н. водной гидроокиси натрия (50 мл) и после выдержки его при О С в течение 30 мин рН раствора регулируют до 8,6 и повторно экстрагируют раствор хлороформом. Объединенные экстракты, высушенные над безводным сульфатом натрия, концентрируют до малого объема и подкисляют до рН.4,5 0,1 н. метанольным хлористым водородом, в результате чего выделяют кристаллический -; тхлоргидрат Ю-метоксидаунорубицина. Т. пл. 159°С (с разложением). + 316 (с 0,05, СНзОН); тонкослойная хроматография на пластинке Кизельгель (Мерк) , используя в качестве растворителя систему из хлороформа, метилового спирта и воды (13:6:1 об./об). Rf 0,37. Пример 8. 9,10-диэпи-10метоксидаунорубицин MAR 96. Осуществляя реакцию сочетания между антрациклоном формулы V) и 1гхлорN,0-трифторацетилдаунозамином, как описано в примере 7v получают 9,10диэпи-10-метокси- N -трифторацетилдаунорубицин, из которого после щелочной обработки в мягких условиях 0,1 н. водной гидроокисью натрия в течение 30 мин при получают , 10-диэпи-10-метокси-даунорубицин в виде хлоргидрата. Продукт имеет т.
пл. 140С (с разложением) . + 252 (С 0,05, CHjOH).
Пример 9. Синтез 10-метокси-доксорубицина MAR 95.
Pac-FBOp 10-метоксидаунорубицина в смеси метилового спирта и диоксана обрабатывают бромом, в результате чего получают его 14-бромпроиз видное, последующей обработкой водным раствором муравьинокислого натрия при комнатной температуре в течение 100 ч получгиот 10-метокси-доксорубицин, выделяемый в виде хлоргидрата, Т. пл. (с разложением).
Осуществляют тонкослойную хроматографию на пластинке Кизельгель (мерк) HF254 используя в качестве
Противоопухолевая активность
10 (R)-метоксидоксорубицина и 9,10-диэпи 10-метокси-даунорубицина в сравнении с активностью даунорубицина и доксорубицйна ъ
растворякяцей системы смесь хлороформа, метилового спирта, воды и уксусной кислоты (8:2:0,6:1,4 об./об) Rf - 0,45.
. Пример 10. Синтез 9,10 диэпи-10-1«ютоксидоксорубицина.
Как и в примере 9, путем обработки 9,10-диэпи-10-метоксидаунорубицина бромом и затем муравьинокислым натрием получают 9,10-диэпй-10-метtqоксидрксорубицин формулы YI , который вьщеляют в видe хлоргидрата.
Приведенные в табл. данные иллюстрируют противоопухолевую активность новых антрациклиновых производных 1 & против лимфолейкоз а Р зев 10-(R)-метоксидаунорубицина,





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гликозидов антрациклина | 1980 |
|
SU993822A3 |
| АНТРАЦИКЛИНОВЫЙ ГЛИКОЗИД И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 1990 |
|
RU2073681C1 |
| 8-ФТОРАНТРАЦИКЛИНГЛИКОЗИДЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ ПРИСОЕДИНЕНИЯ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2095365C1 |
| Способ получения антрациклиновых гликозидов | 1986 |
|
SU1553015A3 |
| Способ получения рацемических аглюконов | 1983 |
|
SU1311616A3 |
| Способ получения 4-деокси-даунорубицина или 4-деокси-доксорубицина | 1981 |
|
SU1277902A3 |
| ПРОИЗВОДНЫЕ АНТРАЦИКЛИНОНА И ИХ ИСПОЛЬЗОВАНИЕ ПРИ АМИЛОИДОЗЕ | 1995 |
|
RU2167661C2 |
| 4-ЗАМЕЩЕННЫЕ АНТРАЦИКЛИНОНЫ И ГЛИКОЗИД АНТРАЦИКЛИНА | 1991 |
|
RU2024483C1 |
| Способ получения производных антрациклина | 1977 |
|
SU897111A3 |
| 6-N, 6-N-ДИБЕНЗОИЛ-9-(2,3-АНГИДРО- β -D-РИБОФУРАНОЗИЛ)АДЕНИН В КАЧЕСТВЕ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ В СИНТЕЗЕ ДИНАТРИЕВОЙ СОЛИ АДЕНИЛИЛ(2` - 5`)АДЕНИЛИЛ(2` - 5`)-9-(2,3-АНГИДРО- b - D -РИБОФУРАНОЗИЛ)АДЕНИНА | 1989 |
|
SU1626662A1 |

Даунорубицин
10- (R) -Метоксидаунорубицин
Доксррубицин
10- (R) -Метоксидоксорубицин
9,10-Дизпи-10-метоксидаунорУбицин
90 98
119
124 133
115 110
108 171 133 129 119
104 115 127 125 108
126 132 118 102
Соединения испытывали in vivo на мышах СДГ, зарс1женных опухолевыми клетками. После трансплантации мьошам опухоли на 5,9 и 13-й дни им делали интрэперитониально инъекции (четырехдневный перерыв после каждой инъекции). Средняя продолжительность выживания в процентах от контрольной группы В/К,% приведена в таблице.
Формула изобретения
Способ получения хлоргидратов замещенных антрациклинов общей формулы
он «VV
где R - группа СОСН j или СОСН,ОН; R - ОН; R - ОСНз : R - Н i
R;
R- - .группа СОСНо или СОСН.ОН;
или R
R - ОН; R - Н; R - ОСИ,,, отличающийся тем, что 9,10-ангидро- N -трифторацетилдауномицин формулы II
ОН9
гС-СН,
НО
NHtOtF
де смеси эпимерных эпоксидов, которые подвергают взаимодействию с диме||: тилсульфоксидом и дициклогексилкарбодиимидом в присутствии катализатора-трифторацетатпиридиния, с получением 9-дезокси-9,10-эпоксид-дауномицинона формулы IV
о он OCHj
о он н ,оснз
UH
COCHj I
о он он
1386731514
V.. нокислым натрием с получением соответ-Источники информации,
ственно 10-метокси-адриамицина и 9,10-принятые во внимание при экспертизе диэпи-10-метоксиадриамицина, которые 1. Патент СССР 583763,
выделяют в виде их хлоргидратов.кл. С 07 Н 15/24, опублик. 05.12.77.
Авторы
Даты
1981-09-23—Публикация
1979-05-08—Подача