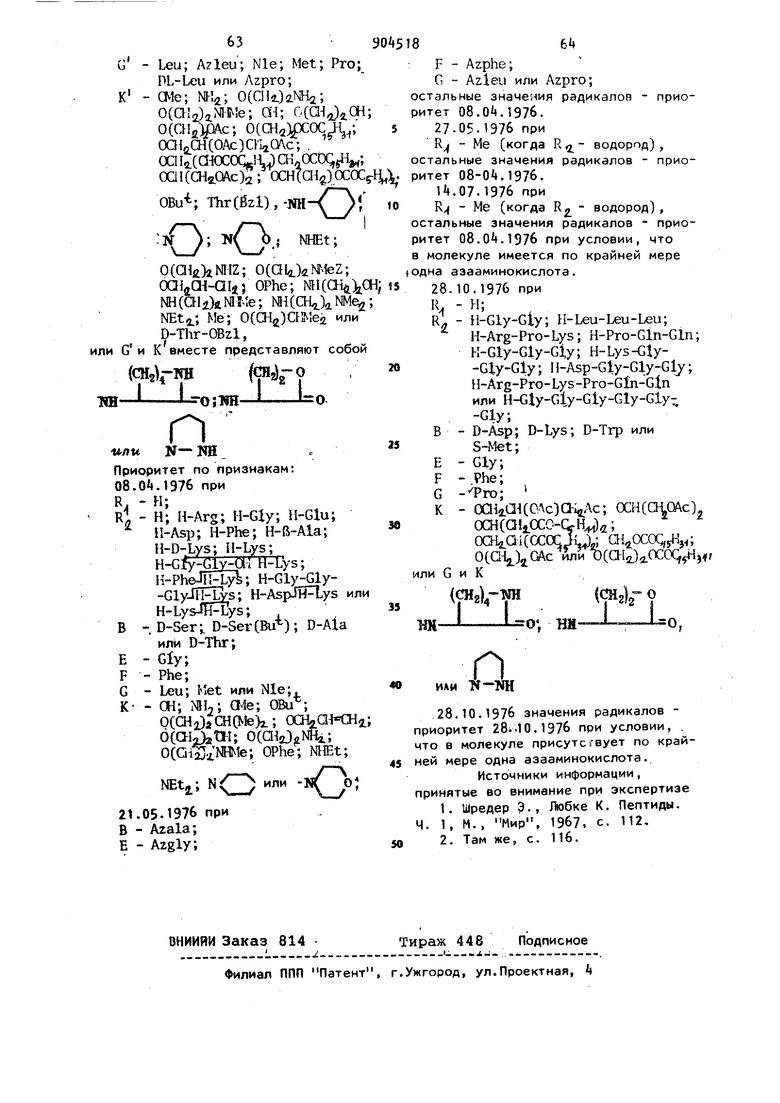
Ш У:3 i (OCaUL) CI I, OCOCJsHj,;
ooiCCHgaxc);; oaiiCHnOcoc -ii j,OBu Thr-Ш; О
NHEt;
OCQIJNHZ; OCCHjJaM.leZ; OCHiCH ak; OPh; ЫНСОу а ; NH(CH),iMfvie; ;v)H(CH2)2.fJMe2 5 Me; 0(CH2)2.
D-Thr-OH, . G и к вместе представляют собой
(9H2)(
ЭД,-|НW-0Q( ,
IL о; т или к-TIH jjj I
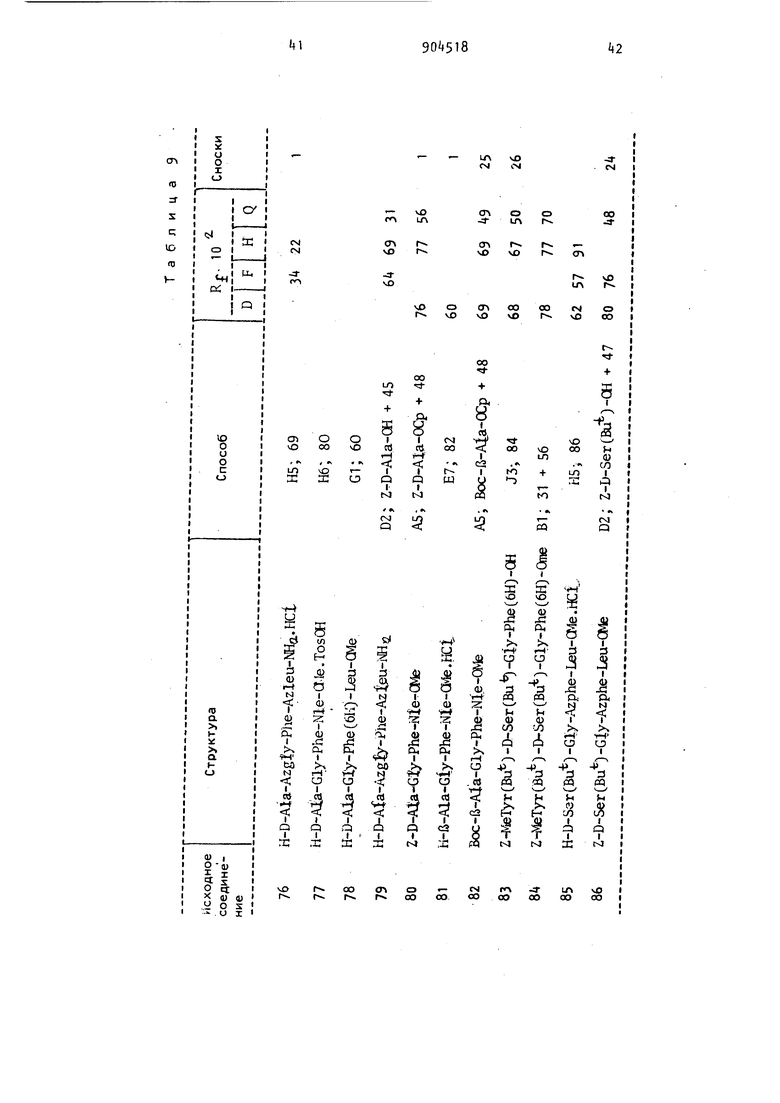
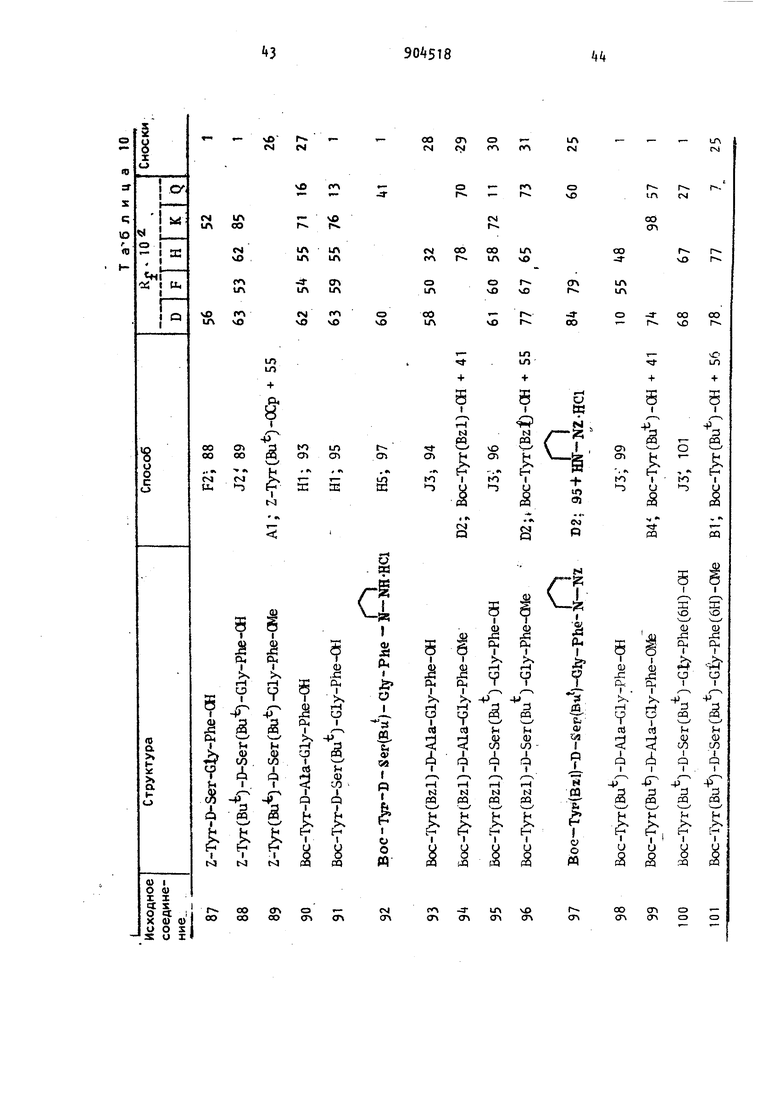
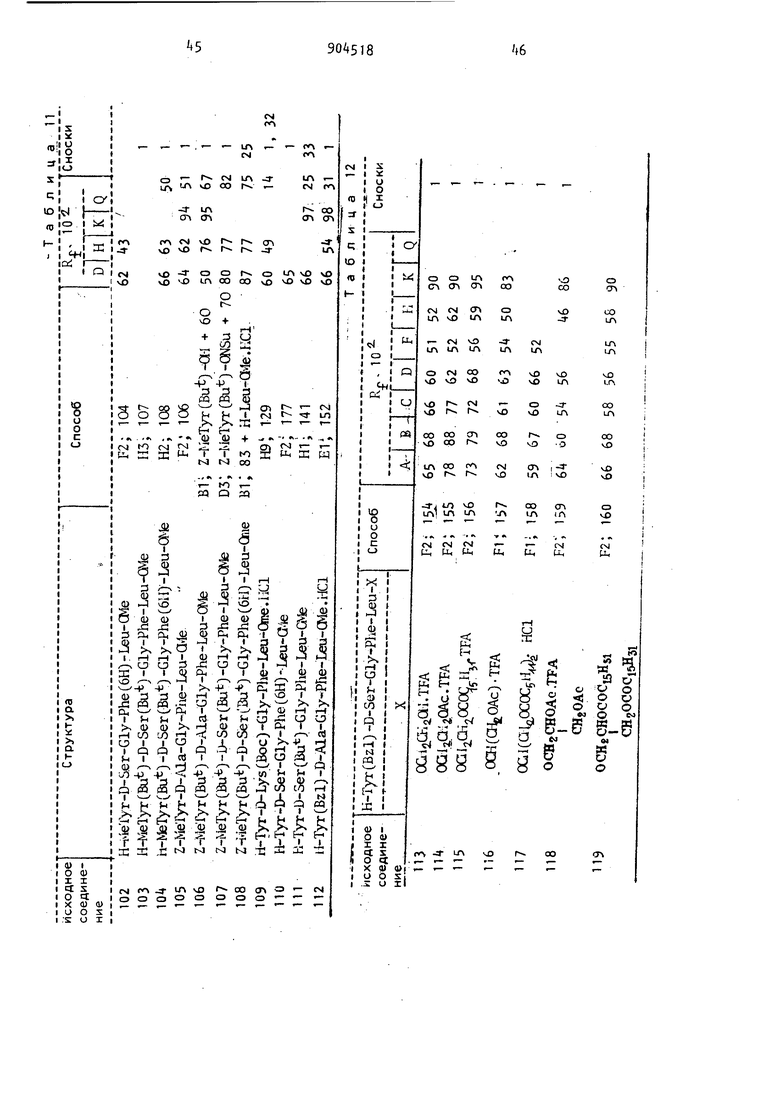
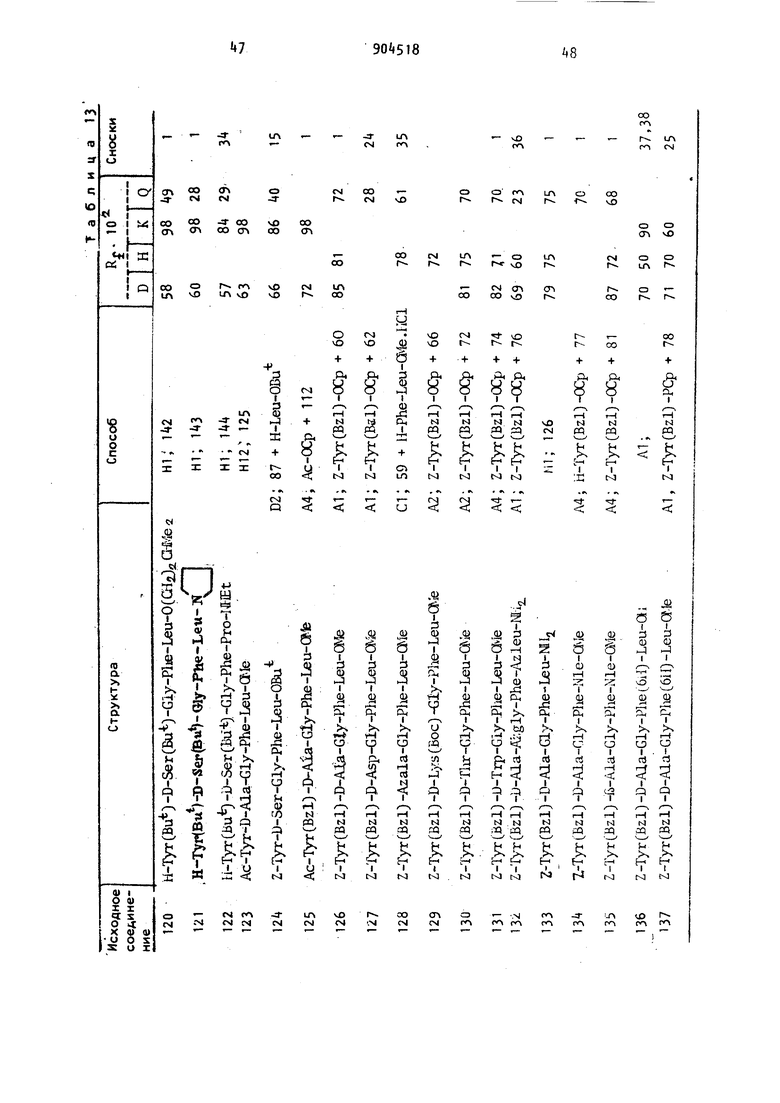
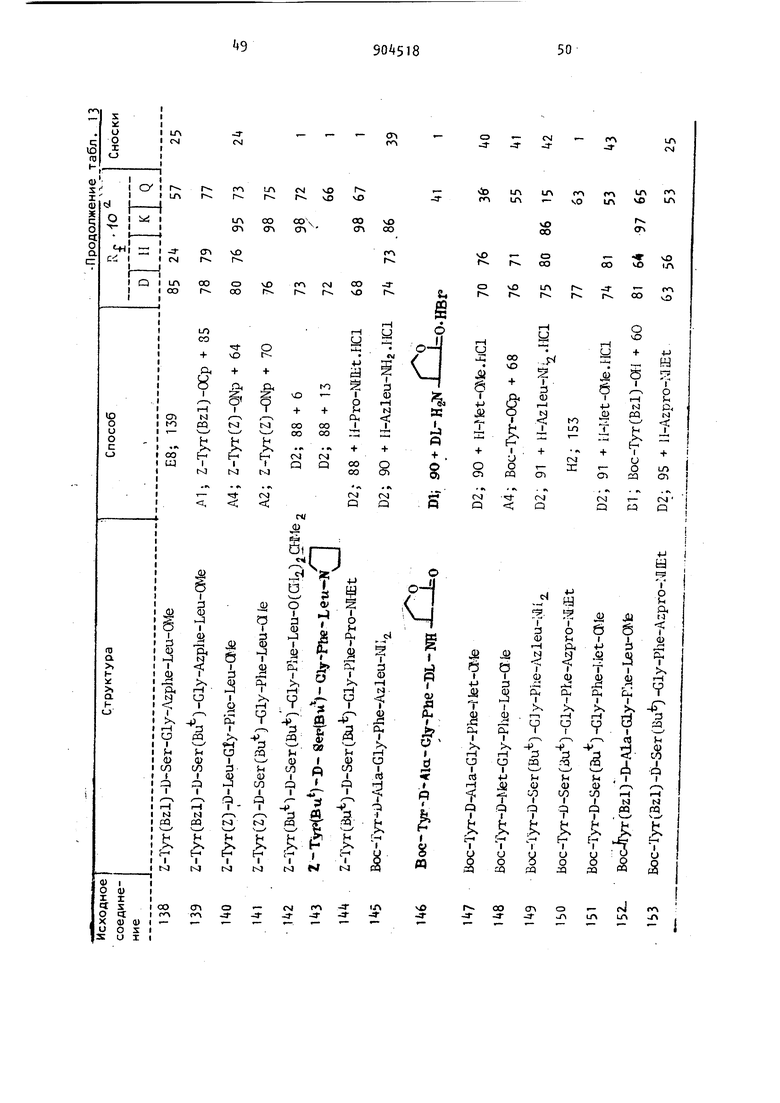
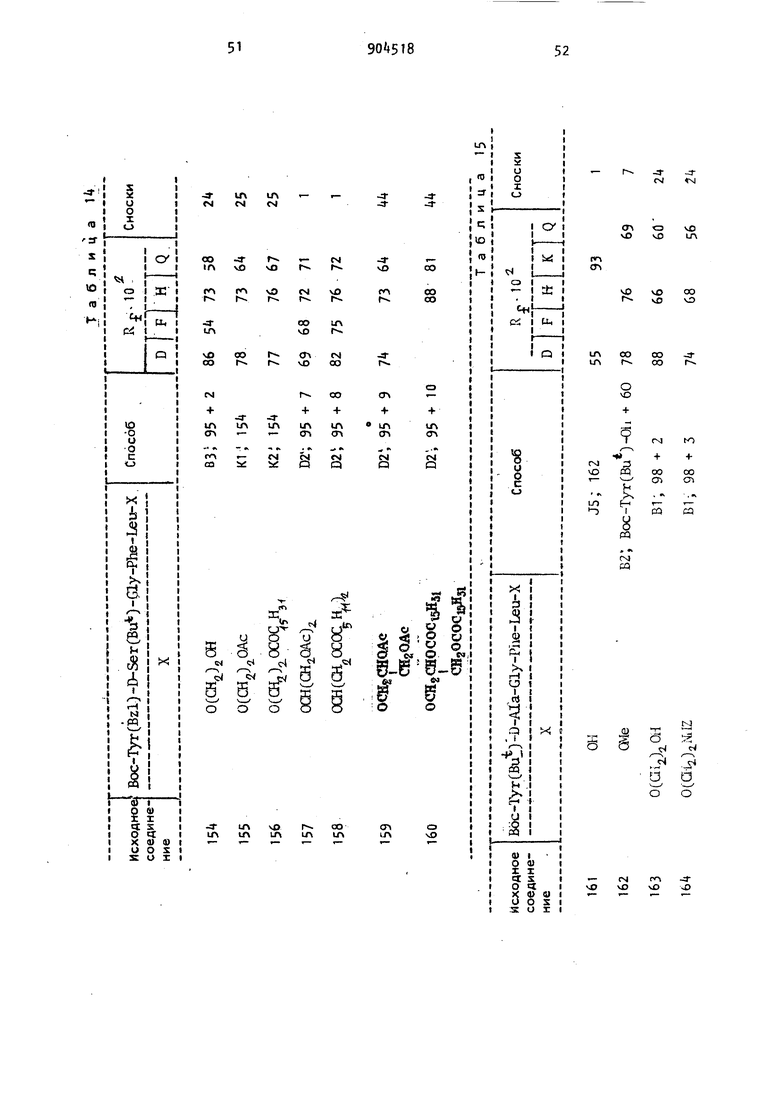
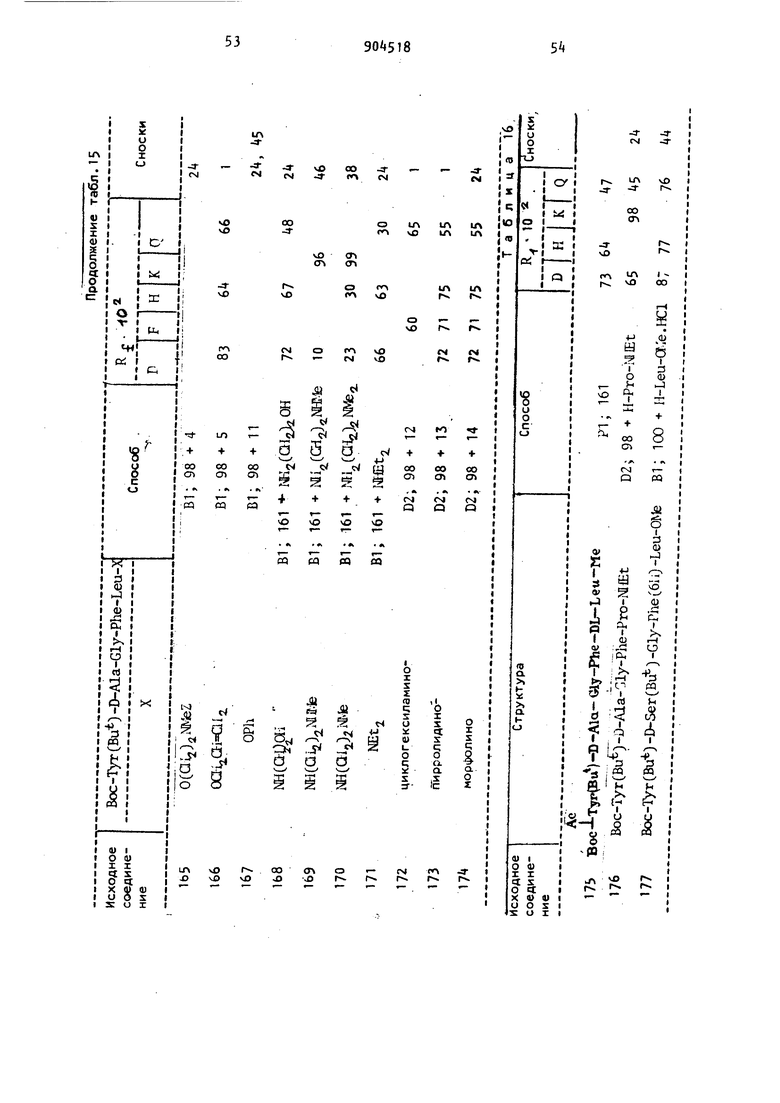
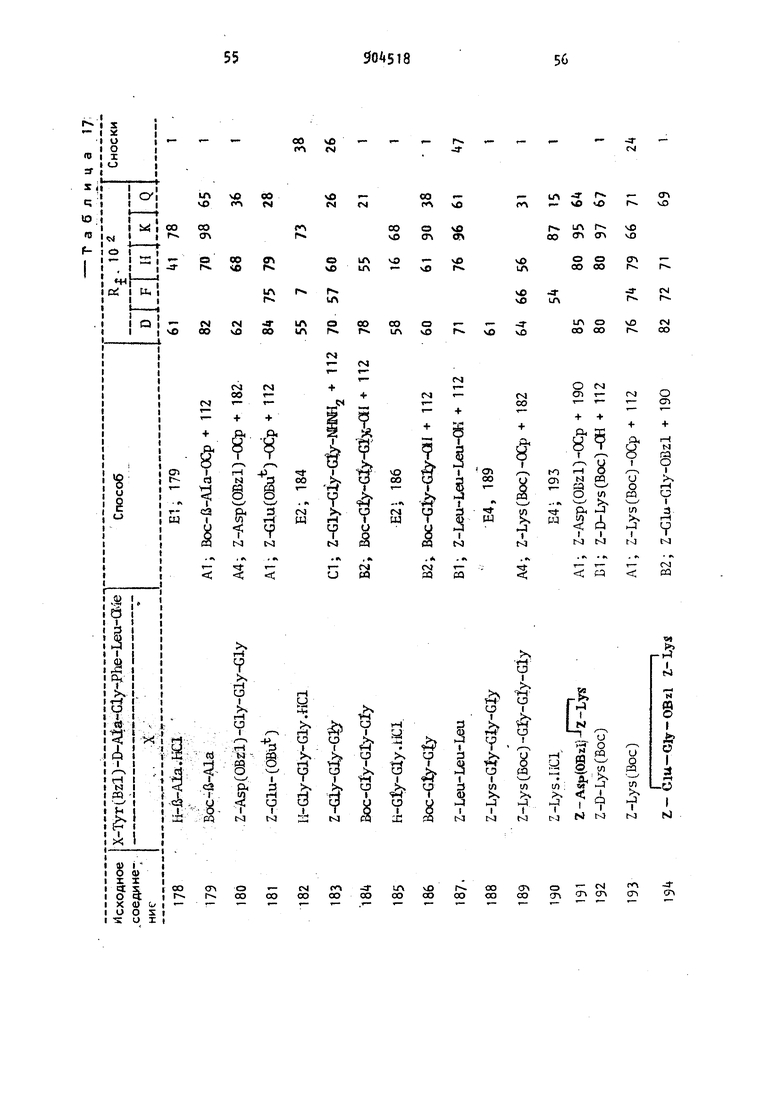
мнзаключающиеся в том, что отщепляют защитные группы в соединении формулы «i-T B-E-F-G-K НГ где R. - водород, метильный или ацеI тильный радикал; R -.водород; Z; Н-й-А1а; Z-Asp; Z-Lys; Z-LysfZ); Z-LysfBoc) H-r.ly-Glyj Z-Asp (OBzl) Z-Lys (Z)-Z-Lys; Z-ArgCZ/)-Pro-Lys{Z); Z-Gly-Gly-Gly; Z-Leu-Leu-Leu; Z-Glu-Gly-OBzl ZLys; Z-Pro-Gln-Gln; Z-Asp(OBzl)-Gly-Gly-Gly; Z-Lys-Gly-Gly-Gly или Z-Gly-Gly-GlyJl43 s; Z-Arg (Z), -Pro-Lys (Z) -Pro-Gln-Gln; Boc; H-Glu(OBu); Boc-Lys(Boc); H-D-Lys(Boc); H-Lys(Boc); Boc-Phe H-Lyi; Boc-Gly-Gly-Gly или Boc-Gly-Gly-Gly-Gly-Gly-Gly;Т - Тут; Tyr(Bzl); Tyr(Z) или Tyr(Bu); B - D-Ala; D-Asp; Azala; D-Leu; D-Ser; D-Thr; D-Trp; fb-Ala; D-Ser(Bu); D-Lys; - D-Lys(Boc) или P-Met; E - Gly или Azgly; F - Phe; Azphe или Phe(6lO ; G - Leu; Azleu; Me; Met; Pro; DL-Leu или Azpro; К - ate; NHi; 0(. 0(Gla)2NI№; Ш; 0(aii.)iai; 0(aia) Ora iOCOCJL,; ЛХИгШ(ОАс)О1гОАс;
Ю12 (Qtocoq j у .i oai(ai2. oai(a-ijOCOQ.fi,)
Thr(Bzl); ШН I
i MTR;
0(aii)eNHZ; 0(.teZ; OCI-IiOi Ciij.; OPhe; ХИ(ау.Ш; NHCCIia.)iMi.Ie; (aLWie,,; NEto.; №; 0(, или DjThr-OBzl, G и к вместе представляют собой
о XN
,-NH Получение исходных соединений осуществляют при использовании различных методов пептидной химии, например карбодиимидного или азидного метода получения смешанных ангидридов и т.п. . При этом получают исходные соединения, блокированные различными защитными группами. Например, для блокировки иминогруппы используют бензилоксикарбонил, трет, -бутоксикарбонил. Гидроксильную группу защищают бензилом или трет.-бутилом; карбоксильную группу защищают, получая эфирметиловый или этиловый спирт. Для снятия этих групп применяют известные методы. Так, бензил или бензилоксикарбонил удаляют гидрогенолизом; трет.-бутоксикарбонил или трет.-бутил - обработкой исходного соединения кислотой, например трифторуксусной, или хлористым водородом. Для удаления бензилоксикарбонила или трет.-бутоксикарбонила используют брбмистый водород в уксусной .кислоте. Метиловый или этиловый эфир расщепляют с помощью гидрогенолиза или щелочной обработкой исходного продукта. Восходящую тонкослойную хроматографию проводят на пластинах, покрытых силикагелем (Кизельгур G). Хроматографирование проводят в следующих системах растворителей: бутанол-1 - уксусная кислота - вода 4:1:5 об. ч. (RjA); бутанол-1 - уксусная кислота - вода - пиридин 15:3:12:10 об.ч. (); бутанол-2 (3 вес.%) - водный раствор аммиака 3:1 об.ч. (IvgC) ; ацетонитрил - вода 3:1 об.ч. (RjD); ацетон - хлороформ 1:1 об.ч. (R.fE); хлороформ - этанол 1:4 об.ч. (RrF); циклогексан - этил ацетат 1:1 об.ч. (RrG); циклогексан этилацетат - метанол 1:1:1 об.ч. (RjH); хлороформ - метанол - вода 11:8:2 об.ч. (); хлороформ - метанол 19:1 об.ч. (RrP) и хлороформ - метанол 9:1 об.ч. (RtQ). Некоторые из таких систем растворителей используют также для колоночной хроматографии на кремнеземе (рэство рители G, К, Q и Р). Во всех случая пластины оценивают в ультрафиолетов свете и обрабатывают флуоресцеином, нингидрином и реагентом - хлорйодис тым крахмалом. Если нет особых указаний, то показатель R г означает, что этими способами обнаруживают от дельное пятно. Гидролизаты кислого характера дл всех продуктов получают нагреванием пептида или блокированного пептида с 6 н.раствором соляной кислоты, соде0й а«цим 1 вес.об. фенола, в запаянной пробирке, из которой выкачен воздух, в течение 16 ч при ПО° Аминокислотный состав каждого гидролизата определен с помощью анализатора аминокислот Локарта. В каждом случае наблюдают соответствие с ожидаемым составом. Примеры 1-42. Блокированный полипептид подвергают восстановительному расщеплению. восстановительное расщепление осуществляют следуюи им образом. HI. Исходный материал в количест ве 1 ммоль растворяют в этаноле, содержащем до 25 воды, ив атмосфе ре азота добавляют 5 вес.1 катализа тора, содержащего 5 вес.% палладированного угля, и перемешивае мую реакционную смесь при 20-25С осторожно барботируют поток водорода. Для полного завершения реакции достаточно 5-6 ч. Водород заменяют азотом, и катализатор фильтруют через слой диатомовой земли. Продукт выделяют упариванием фильтрата в вакууме. Выход 90-95-. Н2. Осуществляют, как и в HI, но вместо водного этанола применяют .метанол. НЗ. Осуществляют, как и в HI , но применяют метанол в качестве реакционной среды. Н4. Осуществляют, как и в N1, но применяют водный этанол при добавлении 1 экв.ч. хлористого водорода. Н5. Осуществляют, как и в HI, но применяют водный метанол при добавлении 1 экв.ч. хлористого водорода. Нб.. Осуществляют, как и в HI, но применяют диметилформамид при добавлении 1 экв.ч. толуол-п-сульфокислоты. Н7. Осуществляют, как и в HI, но применяют метанол при добавлении 1 экв.ч. хлористого водорода. Н8. Осуществляют, как и в HI, но применяют в качестве реакционной среды смесь диметилформамида с бута нолом. Н9. Осуществляют, как и в HI, но применяют в качестве реакционной среды водную (90-95 об Л) уксусную кислоту. . ню. Осуществляют, как и в Н9, но добавляют 1-2 экв.ч. хлористого водорода. Н11. Осуществляют, как и в HI, но применяют в качестве реакционной среды водный диметилформамид Н12. Осуществляют, как и в HI, но применяют в качестве реакционной среды смесь водного этанола и хлороформа. Н13. Осуществляют, как и в HI, но применяют в качестве реакционной среды смесь метанола в диметилформамиде. Б результате получают полипептидные производные, приведенные в табл. 1. Примеры 43-б9- Блокированный полипептид подвергают расщеплению хлористым водородом по следующим методикам. 1. Исходное соединение растворяют в этигэцетате и добавляют раствор хлористого водорода в этилацетате в количестве, достаточном для получения 2-6 н.кислоты. Реакцию проводят при 20-25°С в течение 1-2 ч. Хлорги.чрат продукта осаждают и отфильтровывают. Выделение проводят упариванием в вакууме. Е2. Осуществляют, как и в Е1, но в качестве реакционной среды вместо этилацетата применяют метанол. ЕЗ. Осуществляют, как и в Е1, но рименяют хлористый водород в смеси етанола с этилацетатом. Е4. Осуществляют, как и в Е1, но рименяют уксусную кислоту для раст7эорения исходного материала с посл дующим добавлением хлористого водо рода в этилацетате. Е5. Осуществляют, как и в Е2, н в атмосфере азота в присутствии пр тивонагарного средства, например 2-меркаптоэтанола. Еб. Осуществляют, как и в Е1, н применяют диэтиловый эфир вместо этилацетата в качестве реакционной среды. А Е7- Осуществляют, как и в Е1 , н в качестве реакционной смеси вмест этилацетата применяют диоксан. Е8. Осуществляют, как и в Е1, н в качестве реакционной среды приме няют уксусную кислоту вместо этилацетата. Е9. Осуществляют, как и в Et, н в атмосфере азота в присутствии пр тивонагарного средства, например 2-меркаптоэтанола. ЕЮ. Блокированный материал пер мешивают с концентрированной солян кислотой (примерно 10 мл/г) при О в течение 10 мин. Избыток кислоты затем отгоняют в вакууме, по возмо ности при минимальной температуре, и полученный продукт сушат лиофили зацией. 8 результате получают полипепти ные производные, приведенные в табл. 2. Примечания (сноски) к табл. 2. 1.Соль НС1 2.Соль 2IIC1 3.Выделяют упариванием после фильтрования через диатомовую земл i. Выделяют осаждением 5.Осаждают добавлением эфира 6.Осаждают добавлением смеси метанола с эфиром 7.Кристаллизуют из смеси этилацетата с петролейным эфиром (т.кип. 60-80°С). 8.Получают в виде высушенного лиофильной сушкой порошка из воды или смеси воды с трет.-бутанолом. 9.См.сноску 8, в присутствии Н 10.Очищают хроматографией на кремнеземе с применением растворителя 0. 11.См.сноску 10, с применением растворителя К. 12. Очищают на Сефадексе G 15 в0,01 М растворе соляной кислоты 13- Очищают на Сефадексе G 25 в 5 об.% уксусной кислоты. 8 14.Т.пл. 202-205С 15.1 .пл. 16.Т.пл. 179-180С 17.Т.пл. 173-174 С 18.Т.пл. 142-Й)Ч 19.Т.пл. 118-120С 20.Т.пл. 138-1«0С 21.Т.пл. ni-lU C 22.Т.пл. 195-2004 (с разл.) 23.Т.пл. 120-122С 2k.. Т.пл. 174-17бС (с разл.) 25. Т.пл. 120-12tC Примеры 7088. Блокированный полипептид подвергают расщеплению с помощью трифторуксусной кислоты по следующим методикам. F1. Исходное соединение растворяют в трифторуксусной кислоте (10 мл/г) и проводят реакцию при 2025°С в течение 1-2 ч. Продукт выделяют в виде трифторацетата упариванием раствора в вакууме. Используя лиофильную сушку в присутствии нё большого избытка хлористого водорода , получают соответствующий хлоргидрат. F2. Осуществляют, как и в F1, но применяют родную (90 или 95 об.) трифторуксусную кислоту. РЗ Осуществляют, как и в F1, но применяют водную (90 или 95 об.) трифторуксусную кислоту в атмосфере азота в присутствии противонагарного средства, например 2-меркаптоэтанола, Примечания (сноски) к табл. 3 1.Соль НС1 2.Соль уксусной кислоты 3.Соль трифторуксусной кислоты (ТФК) i. Соль 2ТФК 5.Выделяют осаждением после фильтрования через диатомовую землю. 6.Осаждают добавлением петролейного эфира (т.кип. 60-80 С) 7.Выделяют в виде высушенного лиофильной сушкой порошка из воды или смеси воды с трет.-бутанолом. 8.См. сноску 7, в присутствии НС1. 9.Очищают на Сефадексе G 15 в 5 об. водной уксусной кислоты. 10.Т.пл. 150-155С 11.Т.пл. 166-1684 Пример 89. К 235 мг (330 мкмоль) раствора H-T T-D-Ser-Gly-Phe (6Н)-Ley-Qr.ie (исходное соединение 110) в метаноле (5 мл) добавляют 1 н.раствор гидроокиси натрия (1,0 мл,3 экв.ч.), смесь пере9
мешивают при температуре окружающей среды в течение 3 ч. Раствор упаривают в вакууме, разбавляют водой и подкисляют разбавленным раствором соляной кислоты. После осветления фильтрованием раствор подвергают лиофильной сушке, продукт растворяю в водном растворе уксусной кислоты и пропускают через колонку, заполненную Сафадексом G 15, элюат вновь лиофилизуют, получают H-Tyr-D-Ser-Giy-Phe(6Н)-Leu-ffl, R|C 0,38.
Пример 90. При обработке H-Me-D-Ser-Gly-Phe(6H)-Leu-One (.исходное соединение 102) в водном растворе гидроокисью натрия (2 экз.) с последующим проведением процесса по мьтодике примера 89 получают H-Me-D-Ser-Gly-Phe(6{|) -Leu-CH, R 0,«t.
Пример 91. 140мг (22 мкмоль) Ас-Туг-D-Ala-niy-Phe-Leu-0t:ie (исходное соединение 123) растворяют в 10 мл теплого диоксана и постепенно температуру раствора доводят до температуры окружающей среды, после чего добавляют 12 мл воды и 1 н.водный раствор гидроокис натрия (0,75 мл, 3,5 экв.ч.). Смесь интенсивно перемешивают при температуре окружающей среды в течение 2,5 ч, затем большую часть диоксана отгоняют в вакууме. Остаток подкисляют добавлением 1 н.раствора соляной кислоты. Полученную суспензию концентрируют в вакууме. К остатку добавляют водный аммиак вместе с водным 0,05 М- раствором ацетата аммония до получения прозрачного раствора. Изыбток аммиака упаривают и продукт чистят на колонке, заполненной Сефадексом G 25, в водном 0,05 М растворе ацетата аммония. Элюат лиофилизуют, получают Ac-Tyr-D-Ala-Gly-Phe-leu-CH, 0.56, 0,i(7. .
Способы, указываемые в таблицах значениями Н1-Н13 включительно, Е1-Е10 включительно и Fi-F3 включительно соответствуют значениям, приведенным, соответственно, в примерах 1-42, «3-69 и 70-88. Другие значения расшифровываются ниже.
Реакции активного сложного эфира
А1. Раствор подходящего аминосоединения (1 моль) и соответствующего активного сложного эфира (1,1 ммоль) в диметилформамиде ( ми1810
нимальный объем) выдерживают при 20-25 С до отсутствия положительной реакции с,нингидрином ч. Реакционную смесь концентрируют в вакууме и выделяют неочищенный продукт или осаждением его при добалении подходящего органического расворителя, или обработкой водой, или смесью воды и подходящего органического растворителя, например эфир При необходимости осуществляют дополнительную очистку.
А2. Осуществляют, как и в А1, за исключением того, что в качестве реакционной среды применяют этилацетат при С.
A3. Осуществляют, как и в А1, но при добавлении 1-оксибензотриазола (примерно 0,2 ммоль).
А4. Осуществ;ляют, как и в А1 , но реакционную смесь выдерживают
А5. Осуществляют, как и в А1, но при добавлении 1-оксибензотриазола (примерно 0,2 ммоль), и всю смесь выдерживают при °С.
Реакции смешанного ангидрида
81.Раствор подходящего кЗрбоксилсодержащего компонента (1 ммоль) в диметилформамиде (примерно 5 мл) охлаждают до температуры от -20 до и обрабатывают N-метилморфолином (1 ,05 ммоль), а затем изобутилхлороформиатом (1,05 ммоль). Смесь перемешивают при температуре от -20 до С в течение 5 мин, а затем добавляют раствор аминокомпонента
(1 ммоль) в диметилформамиде. При использовании соли аминокомпонента добавляют также N-метилморфолин (1 ммоль). Смесь перемешивают при 20-25°С до 2 ч завершения реакции, затем ее упаривают в вакууме. Остаток распределяют между разбавленным водным раствором лимонной кислоты и подходящим, не смешивающимся с водой органическим растворителем, обымно с этилацетатом.
Продукт переходит в органическую фазу, которую отделяют и промывают водным раствором лимонной кислоты и водным раствором бикарбоната натрия, сушат и упаривают в вакууме. Если не найден подходящий растворитель, то промывают сухое вещество, которое затем выделяют фильтрованием после окончательной промывки водой.
82.Осуществляют, как и в 81, но в качестве т-ретичного основания применяют триэтиламин. ВЗ. Осуществляют,как и в В1 , но применяют этилхлорформиат с образованием смешанного ангидрида. . Осуществляют, как и в 81 , но смешанный ангидрид получают с этилхлорформиатом и N-метилморфолином в тетрагидрофуране. 85. Осуществляют, как и в 81, но смешанный ангидрид получают с этилхлорформиатом и в качестве третичного основания применяют триэтиламин Реакция азида С1. Гидразид (1 ммоль) карбоксиль ного компонента растворяют в диметилформамиде (примерно 5 мл), охлаждают до и превращают а азид обработкой 6 М раствором хлористого водорода ( ммоль) в диоксане, а затем в трет.-бутилнитрите (1,2 ммоль). Исчезновение гидразида из раствора выявляют нанесением сме си на фильтровальную бумагу с после дующим добавлением смеси хлорного железа и феррицианида калия. Смесь перемешивают в течение 10 мин при и нейтрализуют добавлением эк вивалентного количества триэтиламина (т.е. ммоль) и необходимого aминoкoмnoнeнтa (1 ммоль), растворе ного в диметилформамиде (3 мл). При использовании соли анинокомпонента на этой стадии также добавляют требуемое количество триэтиламина (1 ммоль). Реакционную смесь затем перемешивают при О-А С в течение 18-24 ч. Осадок отфильтровывают, фильтрат упаривают в вакууме и оста ток, растворенный в растворителе, не смешивающемся с водой, промывают водной лимонной кислотой, водным раствором бикарбоната натрия и водой, продукт выделяют или упаривани раствора или фильтрованием, если выпадает осадок. Реакции N,N -дициклогексилкарбодиимидаД1 . Подходящий карбоксилсодержащий компонент (1 ммоль) растворяют в диметилформамиде (5 мл) и перемешивают при 4°С при добавлении N,N -дициклогексилкарбодиимида(1,1 ммоль) и необходимого амииокомпонента (1 ммоль). Смесь продолж ют перемешивать при С (или в некоторых случаях при 20-25 С) до отсутствия положительной реакции на нингидрин (до 18 ч). Если аминокомпонент берут в виде соли, то к реак 9 12 ционной массе добавляют в начале реакции триэтиламин (1 ммоль). Осаок отфильтровывают, продукт выделят упариванием фильтрата в вакууме, остаток растворяют в подходящем органическом растворителе, например в этилацетате, и промывают последовательно водным раствором лимонной кислоты, водным раствором бикарбоната натрия и водой, после чего высушенный экстракт упаривают или осаждают продукт добавлением подходящего осадителя, например петро|1ейного эфира (т.кип. 60-80 С). Д2. Осуществляют, как и в Д1, но при добавлении к реакционной смеси . 1-окси бензотриазола (2 ммоль). ДЗ. Подходящее карбоксилсодержащее соединение.(1 ммоль) растворяют в сухом тетрагидрофуране( 2 мл) и добавляют N-оксисукцинимид (1 ммоль) а затем раствор N|N-дициклогексилкарбодиимида (1 ммоль) в тетрагидрофуране (1 мл). Через IS мин добавляют аминокомпонент (1 ммоль) и смесь перемешивают при 20-25 С в течение ч, фильтруют, фильтрат упаривают в вакууме, продукт повторно растворяют в подходящем растворителе, например в этилацетате, и промывают раствор последовательно водным раствором лимонной кислоты, водным раствором бикарбоната натрия и водой, сушат и упаривают в вакууме. Реакция восстановления С1. Для получения производных гексагидрофенилаланина подходящее промежуточное соединение, содержащее фенилаланин (1 ммоль) растворяют в 80|-ном водном растворе уксусной кислоты, возможно содержащей некоторое количество хлористого водорода, добавляют катализатор Адамса из окиси платины (50-150 мг) и проводят восстановление пропусканием потока водорода через перемешиваемую смесь при 20-25С до завершения реакции. Катализатор отделяют фильтрованием раствора через слой диатомовой земли, фильтрат упаривают в вакууме. Гидролиз сложного эфира 1. Сложный эфир (1 ммоль) растворяют в водном ацетоне (1015 мл), содержащем гидроокись натрия (1,1-1,2 ммоль) и раствор перемешивают при 20-25 С До прекращения реакции, что подтверждают спустя 13 2-3 ч тонкослойной хроматографией. Смесь концентрируют в вакууие, остаточный водный раствор промывают этилацетатом. Смесь подкисляют доба лением лимонной кислоты и продукт либо экстрагируют подходящим раство рителем, например этилацетатом, либ выделяют упариванием, если это осуществимо. Экстракт промывают насыщенным ра солом, высушивают и упаривайт в вакууме, получают необходимое карбоксилсодержащее соединение. U2. Осуществляют, как и в Э1, но применяют смесь воды, метанола и ацетона. J3. Осуществляют, как и в Э1, но в качестве реакционной среды применяют водный метанол. 3, Гидролиз проводят с 1 экв.ч. гидроокиси натрия в.воде и продукт выделяют в виде его натриевой соли упариванием под вакуумом. 35- Осуществляют, как и и 31 , но в качестве реакционной среды применяют диоксан. Реакции ацилирования К1. К охлажденному льдом раствору соответствующего сложного моноэфира глицерина (1 ммоль) в хлороформе (1 мл), содержащем пиридин (3 ммоль) добавляют хлористый ацетил (3 ммоль) и смесь перемешивают при 20-25 С в течение 18 ч. Растворитель отгоняют в вакууме и остаток вновь растворяют в этилацетате, раствор промывают последовательно водой, насыщенным водным раствором бикарбоната натрия и водой. Высушенный экстракт упаривают в вакууме, остаток растирают с небольшим количеством метанола и фильтруют. Сложный моноэфир глицерина, необходимый для такого ацилирования, получают следующим образом. Сложный эфир, блокированный изопропилиденом (50 ммоль), в 2-метоксиэтаноле (300 мл) нагревают на паровой бане в течение 6 ч с борной кислотой (500 ммоль). Растворитель отгоняют в вакууме и остаток растворяют в этилацетате. После промывания водой раствор сушат и растворитель отгоняют в вакууме , получают сложный эфир в виде масла, которое подвергают дополнительной очистке хроматографией на колонке с применением кремнезема. К2. Осуществляют, как и в К1, но вместо хлористого ацетила применяют хлористый пальмитоил. КЗ. Блокированный бензилиденом сложный моноэфир глицерина (1 ммоль) и боную кислоту (k ммоль) в триметилборате (5 мл) нагревают на паровой бане в течение 20 мин. Триметилборат отгоняют, остаток нагревают допол ительно 20 мин на паровой бане. Полученный продукт снова растворяют в этилацетате (30 мл), промывают водой и извлекают в виде свободного моноэфира глицерина упариванием. Затем проводят ацилирование с помощью хлористого ацетила, как и в К1. К . Осуществляют, как и в К1 , но для окончательного ацилирования применяют хлористый гексаноил. Реакции этерификации L1 . Безводную блокированную аминокислоту (10 ммоль) растворяют в сухом пиридине (10 мл) при и добавляют бензолсульфохлорид ПО ммоль). Смесь перемешивают при О С в течение 15 мин,затем добавляют подходящий спиот (10 ммоль). Смесь перемешивают при ° С в течение 18ч, затем пиридин отгоняют в вакууме. Остаток растворяют в этилацетате п (150 мл) и раствор промывают последовательно водой, 1 н.раствором соляной кислоты, водой, 2 н.раствором бикарбоната натрия и водой. Сушат и отгоняют. Получают неочищенный продукт . L2. К перемешиваемому раствору соответствующим образом блокированной аминокислоты (5 ммоль) в пиридине (5 мл) при 0°С добавляют фенол (10 ммоль) и N, М-дициклогексилкарбодиимид (10 ммоль) и всю смесь перемешивают при 4 С в течение 18 ч. После фИJlЬTpoвaния смеси и упаривания пиридина в вакууме остаток растворяют в этилацетате (100 мл) и проывают последовательно водой, водным 2 н.раствором бикарбоната натрия водой. Экстракт сушат и упаривают, получают неочищенный сложный эфир. L3. Подходящим образом замещенную аминокислоту (10 ммоль) растворяют в ацетонитриле при и добавляют необходимое количество спирта (10 мл) вместе с пиридином (20 ммоль) и (N -дициклогексилкарбодиимидом 11 моль). Смесь перемешивают при °С в течение 18 ч, а затем фильтруют и растворитель отгоняют в вакууме Остаток обрабатывают этилацетатом и промывают последовательно водным раствором лимонной кислоты, водным раствором бикарбоната калия. Экстракт сушат, упаривают в вакууме , получают неочищенный сложный эфир. L. Осуществляют, как и в L3, но в качестве реакционной среды вместо ацетонитрила применяют ацетон Реакция с аммиаком Ml. Определенный сложный метиловый эфир пептида растворяют в минимальном количестве диметилформамида и приводят в контакт с избытком концентрированного раствора аммиака в этаноле в течение 3 Дн. при 20-25 С. Продукт выделяют осаждением водой Реакция с гидразином 1. Сложный метиловый эфир пептида (10 ммоль) растворяют в диметилформамиде (25 мл) и добавляют водный раствор гидрата гидразина (50 ммоль). Смесь перемешивают при 20-25 С в течение 18 ч, концентрируют в вакууме примерно до половины Вое 1 Тур(Ви) Rj D ОД, й М 0,Ь4 , р Р о Д , U а 0,47
Q1. к раствору соединения формулы Z-Tyr-(Bu)-aij выделенного из 55,2 г (ЮОммоль) его дициклогексиламиновой соли в сухом тетрагидрофуране (300 мл) добавляют 50 мл (800 ммоль) йодистого метила, 8,6 г гидри 1а натрия (300 ммоль) и смесь кипятят с обратным холодильником в течение 18 ч на бане при .
Избыток гидрида натрия разлагают добавлением этилацетата к охлажденной суспензии, а затем воды, получают почти прозрачный раствор, который концентрируют в вакууме.
Полученный водный раствор разбавляют водой (ISO мл) и промывают дважды. Доводят значение рН водного раствора до 3 добавлением лимонной кислоты и продукт экстрагируют этилацетатом (ijOO мл, 2Ч 200 мл). Экстракт промывают последовательно водой (ЮО мл), 10 вес.об.% водного раствора тиосульфата натрия (100 мл), а затем вновь водой до нейтральной
реакции промывных вод. Экстракт сушат над сульфатом магния, упаривают, получают масло, которое суспендируют в теплом петролейном эфире (200 мл, т.кип. 60-80С), затем растворяют в этилацетате, из охлажденного до С раствора выпадает в осадок продукт формулы Z-Me-(Bu)-(H, т.пл.
эб-ээ°с.
R1 к 5,33 г (17 ммоль) раствора соединения Phe-Azley-NHiHCl и 2, мл (17 ммоль) триэтиламина в 50 мл хлороформа добавляют 3,87 г (17 ммоль) раствора соединения формулы ZNHNH-CO-C1. Смесь выдерживают при температуре окружающей среды в течение 1б ч, а затем добавляют 400 мл этилацетата. Раствор промывают последовательно водой, 20 вес.об. водного раствора лимонной кислоты, высушивают над сульфатом натрия и упаривают в вакууме. Остаток чистят хроматографией на колонке с применением кремнезема, хлороформа, 2 об.% объема, и продукт осаждают добавлением воды. Другие реакции Р1. 729 г U ммоль) Boc-Tyr(Bu)-D-Ala-Gly-Phe-Leu-OI (исходное соединение 1б1), 0,55 мл (7 ммоль) чистого сухого пиридина и 0,3 мл (6,7 ммоль) свежеотогнанного уксусно го ангидрида перемешивают при 2022 С в течение 10 мин. Полученный раствор нагревают при ЭО-92С в течение 6 ч, затем охлаждают и обрабатывают водой (15 мл). Каменеподобное вещество отделяют, освобождают от верхнего слоя жидкости декантацией, промывают водой (5 15 мл) и растворяют в этилацетате (50 мл). Раствор промывают последовательно 10 вес.об.% водного раствора лимонной кислоты С f10 мл), водой (1 5 мл), 10 вес.об.% йодного раствора бикарбоната калия (3 л IDмл) и водой (3 10 мл), сушат (безводным сульфатом магния) и упаривают. Спектр ЯМР полученного твердого остатка (530 мг) показывает, что он представляет собой смесь L,D,L,L Ь,В,Ь,В-форм структурной формулы CHgCHHeg he-NH - СН - СОСН метанола в хлороформе и систем Р и Q в качестве элюентов. Получают соединение формулы Z-Azgly-Phe-Azley-Ш2, т.пл. 11б-120°С (с разл.). S1. 17i5 г (30 ммоль) раствора Z-Tyr(Bzl)-OCp и 4,38 г (30 ммоль) Boc-NffIeNHi в 50 мл диметилформамид выдерживают в течение 18 ч при температуре окружающей среды. После разбавления 500 мл этилацетата раст вор промывают последовательно водой 20 вес.об.% водного раствора лимонной кислоты и водой. Упаривание высушенного экстракта в вакууме приводит к получению твердого вещества которое обрабатывают непосредственно раствором хлористого водорода (100 ммоль) в этилацетате в течение 2 ч при температуре окружающей среды. Растворитель отгоняют в вакууме получают соединение формулы Г Z-T)T(Bzl)-NHNHMe, НС1, т.пл. 22322 С, RfD 0,82, R 0,6, 0,63 Э, г (20 ммоль) приведенного хлоргидрата растворяют в 200 мл хло роформа и добавляют 2,8 мл (20 ммол триэтиламина, а затем 2,8 мл (20 ммоль) метилового эфира изоцианатоуксусной кислоты. Смесь перемешивают в течение 18 ч при температу окружающей среды, растворитель упаривают в вакууме. Остаток растворяю в этилацетате, промывают последовательно водой, 20 вес.об. водного раствора лимонной кислоты, насыщенным раствором бикарбоната натрия и водой. Высушенный экстракт упаривают в вакууме, получают соединения формулы Z-Tyr(Bzl)-Azala-Gly-C fe, которое после перекристаллизации из смеси метанола с эфиром имеет т.пл. 107-108С. Примечания (сноски) к табл.. 1.Очищают осаждением 2.Т.пл. 160-161С (с разл.) 3.Перекристаллизовывают из петролейного эфира т.кип. 60-80 С) t. Перекристаллизовывают из смеси изопропанола с эфиром (т.пл.18Н83 5.Перекристаллизовызают из изопропанола (т.пл. ) 6.Колоночная хроматография на кремнеземе с применением хлороформа и 2 об. метанола в хлороформе 7.Колоночная хроматография на кремнеземе с применением хлороформа 8.Колоночная хроматография на кремнеземе с применением хлороформа и системы Р 9.Перекристаллизация из этилацетата (т.пл. 128-130с) 10.Колоночная хроматография на кремнеземе с применением 25 об. этилацетата в циклогексане 11.Колоночная хроматография на кремнеземе с применением системы G 12.Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80 0, т.пл. 9б-99С) 13- Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80С), т.пл. 202-2034) . Перекристаллизация из этилацетата (т.пл. 122-123°С) 15.Колоночная хроматография на кремнеземе с применением систем Р и Q 16.Перекристаллизация из этилацетата (т.пл. 177-17Э°С) 17- Г1ерекристаллизация из смеси этилацетата с петролейным эфиром (т.пл. 60-80°С), т.пл. 122-123С) 18.Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80С), т.пл. 108,5-110С) 19.Перекристаллизация и2 метанола (т.пл. 219-220С) 20.Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80°С), т.пл. 121-122°С) 21.Перекристаллизация из смеси толуола с бензолом 22.Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80°С), т.пл. ТЗЗ-ТЗЗ С) 23- Колоночная хроматография на кремнеземе с применением системы Р 2. Колоночная хроматография на кремнеземе с применением 3 об. метанола в хлороформе 25.Колоночная хроматография на кремнеземе с применением системы Q 26.Перекристаллизация из смеси этилацетата с петролейным эфиром (т. кип. 60-80°С), т.пл. 122-12 С 27- Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80С), т.пл. 115-118С 28. Перекристаллизация из водного метанола, т.пл. 1б2-1бЗ С 29- Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80°С), т.пл. 130-132 С 30.Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80 С), т.пл. 15б-157°С 31.Лиофильная сушка в присутстии НС1 32. Лиофильная сушка 33- Колоночная хроматография на кремнеземе с применением систем Р, Q и К З. Перекристаллизация из смеси этилацетата с циклогексаном, т.пл. 163-16 4 С 35. Перекристаллизация из смеси метанола с эфиром, т.пл. 130-131 С 36. Гидролиз сложного эфира в про цессе операции (исходное соединение 137)
Пример
Полипептид
-МеТут-D-Ala-Gly-Phe-Leu-Wfe ,
H-T)T-D-Ala-Azgly-Pl№-Azleu-h81j
Н-Туг-1)-А1а-С1у-Р1ю-Ьеи-0(СН2)М«2
ll-Tyr-D-Ma-Cly-Phe-Leu-OCD ЗгМГе
H-Tyr-D-Ala-ay-Phe-Leu- aiJ
H-Tyr-D-Ala-Gly-Pte-Nle-Ct.ie
il-Tyr-D-Ala-Gly-.4ie(6H)-Uu-aj
n-Tyr-D-Ala-Gly-Plie(6H)-Leu-(ie
I l-Ty r-i -Asp-Gly-Plie -Lcu-Onc II-Tyr-Azala-Cly-Plie-Leu-ate
U-Tyr-EKLeu-Gly-Plie-Leu-CMe
li-Tyr-D-Ser-Cly-Aziihe-Leu-afe
H-Tyr-U-Ser-Gly-Plje-Leu-0(CHj)aOH
H-Tyr-I}-Ser-Gly-Pl e-Leu-0(
H-iyr-I)-Ser-Gly-Pl -Leu-0(Q)
H- -Typ-D-Ser-Oly-Phe-Lett-OCHg
CHOAe (OAC
H-Tyr-D-Sep-Cl3f-l he-L«u-OCHj
CmWOCuHjl
H-Tyr-D-Ser-Gly-nie-Leu-OCHCaijQAc)
19 H-Tyr-D-Ser-Gly-Phe-Leu-OCHCayXXX jy
R .10
Ajsll I
5041 87 16
I
55 552060
65
69 77
6510
6130 83
6022
6148
5790
6652 , 85
6059 50 8ii 7
79 77 6653 86
67 50 6050 «б 95
71 65 67 50 87
(
68 62 59i9 i 89
5654 81
55 6в 9
67 73 73 СН«ОСОС|,Н}1
67 71 is 58 6d 44 9в
61 6 $4 S4 St )J 85 0 51820 37.Колоночная хроматография на кремнеземе с применением системы К 38.Перекристаллизация из смеси этилацетата с петролейным эфиром , (т.кип. 60-8ос) , т.пл. 172-17 С 39. Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80 С),т.пл. I O-lifl C 40. Колоночная хроматография на кремнеземе с применением смеси этилацетата с метанолом 1 . Перекристаллизация из смеси этилацетата с петролейным эфиром
21
(т.кип. бО-бО С) , т.пл. 1б2-1б5°С (с разл.)
42. Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. бО-ВО С), т.пл.
АЗ. Колоночная хроматография на кремнеземе с применением 1 об. метанола в хлороформе
4. Колоночная хроматография на кремнеземе с применением систем Q и К
. Т.пл. 121-122С
0i 5l822
+6. Перекристаллизация из этилацетата, т.пл. Л8-250С
7- Очистка на Сефадексе U1 20 в диметилформамиде
5 48. Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80 С), т.пл. 152-155 С
49. Перекристаллизация из смеси этилацетата с петролейным эфиром (т.кип. 60-80С), т.пл. 1б« -1б8С
50. Колоночная хроматография на кремнеземе с применением 5 об.% метанола в этилацетате
/т а б л и ц а )
















| название | год | авторы | номер документа |
|---|---|---|---|
| ПЕПТИД И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1994 |
|
RU2067000C1 |
| Способ получения пептидов | 1980 |
|
SU1316565A3 |
| ПРОИЗВОДНЫЕ БОРСОДЕРЖАЩИХ ПЕПТИДОВ | 1991 |
|
RU2017749C1 |
| Способ получения производных борсодержащих пептидов | 1988 |
|
SU1807988A3 |
| ПРОИЗВОДНЫЕ ПЕПТИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2087480C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИПСИХОТИЧЕСКОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2411248C2 |
| N1/N2-ЛАКТАМНЫЕ ИНГИБИТОРЫ АЦЕТИЛ-КоА-КАРБОКСИЛАЗ | 2011 |
|
RU2540337C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИПЕПТИДОВ | 1990 |
|
RU2037498C1 |
| Способ получения полипептидов или их солей | 1977 |
|
SU910116A3 |
| Способ получения пептидов | 1970 |
|
SU439967A1 |

105 Н7 1}2 К5 («7} Н9 1я,7 ИЗ 4J Н9 1)) Н9 I3& Н9 1J7 Н2 127Н2 128Н5 ЙО Н9 138 Н5 ПЗ НИ 1И Htl 115 H1I Ив НП 119 НП 114 Htl I. 117 Hit Соль ItCl очицапт хроматографией на креннеэеме с применением 25 о6.% смеси метанола и хлороформа и растворителя К Соль id осаждает добавлением смеси метанола с эфиром Соль с гнОАс получают в виде высушенного лиофильной сушкой порошка из воды или снеси воды с трет.-бутаиолон Соль с 2НОАс получают в виде высушенного лиофильной сушкой порошка или си воды с трет.-бутанолом в присутствии IIC1 Очищают хроматографией на кремнеземе с применением 25 об. смеси метанола и хлороформа, в присутствии растворителя К Соль с НО Ас Получают в виде высушенного лиофильной сушкой поролка из воды или смеси с трет.-бутанолом Выделяют упариванием после фильтрования через диатомовую землю -Получают в виде высушенного лиофильной сушкой порошка из воды или смеси воды с трет.-бутанолом; т.пл. Соль IIC1 выделяют упариванием после фильтрации через диатомовую земле Соль 1)С1 получают в виде высушенного лиО1 1Льной сушкой порошка из воды или смеси воды с трет.-бутанолом в присутствии id Соль IIC1 осаждают добавлением эфира; т.пл. Соль трифторуксусной кислоты (ТФК) осаждают добавлением смеси этилацетата с эфиром; т.пл. (разп.) . Соль ТФК выделяют упариванием пасле фильтрования через диатомовую земпю/ Соль ТФК выделяют упариванием после фильтрования через диатомовую землю, т.пл. (разл.) .Соль Т44( выделяют упариванием после фильтрования через диатомовую землю, т.пл. (разл.) Соль ТФК выделяют упариванием после фильтрования через диатомовую землю Соль ТФК выделяют упариванием после фильтрования через диатомовую землю т.пп. iJtu-He C Соль id получают в виде высушенного лиофильной сушкой порошка из воды или смебй вод;|| с трет.-бутанолом
Полипептид
Пример
i-Tyr-D-Ser-Gly-Plic-Leu-aSu
Н-Туг-О-ТЬг-ЙуЧЧю-Ьеи-ай
h-Tyr-D-Tip-GiyPl«-Leu-CKe il-Tyr-B-Ala-Gly-Piic-Nlc-aie
H-a-Ala-Tyr-U-Aia-Gly-Plic-Leu-aJe
-Asp-Tyr4)-Ala-Gly-P}ie-Lei -CMa
ll-Lys-NeTyr-D-SerGly-Wie-Uu-OMB
H-Lyi-Tjr-l)-AlQ-Cly-pJie--DL--NHJllss(
U-Lys(Boc)-Tyr-I)-Ala-Cly-Phc-leu-a.lc
li-Tyr-U-Ala-Cly-Pl e-Lcu-Thr-a
H-Gty-Gly-Tyr-D-Ala-Gly-ine-Leu-CMe 31 H-Aep H-Lyi-TyP-D-AlaJ2H-Ly8-H-Lye- r r-D-Alo- Cay-Phe-Leu-OMe
33li-Arg-Pro-Lys-TyT-D-Aia-Giy-Plie-Leu-Cr-te
З H-dy- y-Gly-TyT-D-Ala-Giy-Phe-Leu-ab
35H-Gly-Giy-Giy-Tyr-D-Ser-Gly-Pije{6H) -Leu-QJo
34li-Leu-Leu-Leu-Tyi:-D-Ala-Gly-Pl -Leu4 fe 37 38 39 i1
tit ll-Aig-IVo-Lys-Pro-Cln-Gln-Tyr-D-Ala-niy-MjC-Lou-CMe
R 1U
лЛЕЖИЕН
59
76
59
17 80 И
62
29 66
1,9
26 51 22
73 76 77 68 57 5520
5J
20
51 78 55 53
to liS
7 8 6 32
58
65 76 ko i9 2 13 88
40 69 32 6065
636030 Cty-Plie-; 11-С1и-0 у-ОЯ-Н-Ьу«-Туг-В-Д1а-О1у-рЬв-Ъ«м-СМе 36 60 27 H-Pro-Gin-Gili-Tyr-D-Ala-Gly-Plie-Leu-ateW H-Asp-Cily-Cly4Jly-:Tyr-D-Ala-Gly-Ph&-Leu«CHe ll-Ly5-ay4Uy-G|.y-Tyr-D-Ala-Gly-Wie-LeU-Cl.fe32 72 « H-Gly-Gly-ClyJH-LT«-TyP-D-Ala- Hy-Wie-Le i-OMe 28 66 25 42 Lew-OTfe iO 6« 19 3
25
смеси 6ОДЫ. с трет.-бутанопок а присутствии ЦС1
Соль UC1 выделяют упариванием после фильтрования чер«э диатоноеув землю
Выделяет упариванием после фильтрования через диатомовую землю
Соль IKJl очищают ма сефадексе С-15 в 5 об.% водной уксусной кислоты
Соль 1IC1 получают в виде высушенного лиофильной сушкой порошка из воды или смеси воды с трет.-бутанолом в присутствии IC1
Соль с 2ИС1 очищают хроматографией на кремнеземе с применением 25 обД снеси
метанола и хлороформа, с применением растворителя К
Выделяют упариванием после фильтровагин через диатомовую землю
Соль llCi очищают хроматографией на кремнеземе с применением 25 об.% смеси метанола и хлороформа
Соль ТФК (:а1деляют упариванием после фильтрования через диатомовую землю; т.пл.
Соль ilCl очищают хроматографией на кремнеземе с применением 23 об.Я оуеси метанола и хлороформа, с применением растворителя К НЮ Соль с 2(1С1 получают в виде высушенного или смеси воды с трет.-бутанолом 19 Н5 199 9, 183 Н9 203 Н9 187 НП 19 И9 217 Н9 180 Н9 188 -N9 195 Н9 198 Н9
26 Продотенмв т«вп. 1 Соль с УК.1 получают в виде высушенного лиофильной сушкой порошка из воды «ли смеси воды с трет -бутанолом Соль с ЗНОАс очищают хроматографией на кремнезене с применением 25 об.% смеем метанола и хлороформа, с применением растворителя К Соль 1С1 получают в виде высушенного лиофильной сушкой порошка из воды или смеси воды с трет.-бутанолом, е присутствии tlCi Соль с НОАс очицают на сефадексе G-25 в 5 об.% уксусной кислоты Соль НС1 очищают хроматографией на кремнеземе с применением 25 об.% смеси нетаиола-хлороформа и растворителя К Саль с 2ИС1 очищают на сефадексе G-25 в 5 об.% уксусной кислоты Соль с НОАс получает а виде высушенного яиофильной сушкой пороик на воды НИИ смеси воды с трет.-бутаноломj т.пл. 218-219 С Соль HQ очищают хроматографией на кремнеземе с применением 25 об. смеси нетдиола и хлороформа, с применением растворителя К Соль с очицают аналогично Сопь с 21IC1 очищают аналогично и получают в виде высуиенного лиофильной сумнйй пороика Очищает на сефад«ксе G-25 в 5 об. водной кислоты. Электрофорез при рН 6,5Перемепают на 0,78 по отношению к гистидину в качестве стандартной метки лиофильной сушкой порошка из воды
1/Ч D
CM- .a--LTl OO
a
r ГЛ UJЫ
vO
CM
-3VO
CM
oo
vO
о
r
CO
r
r-
UN
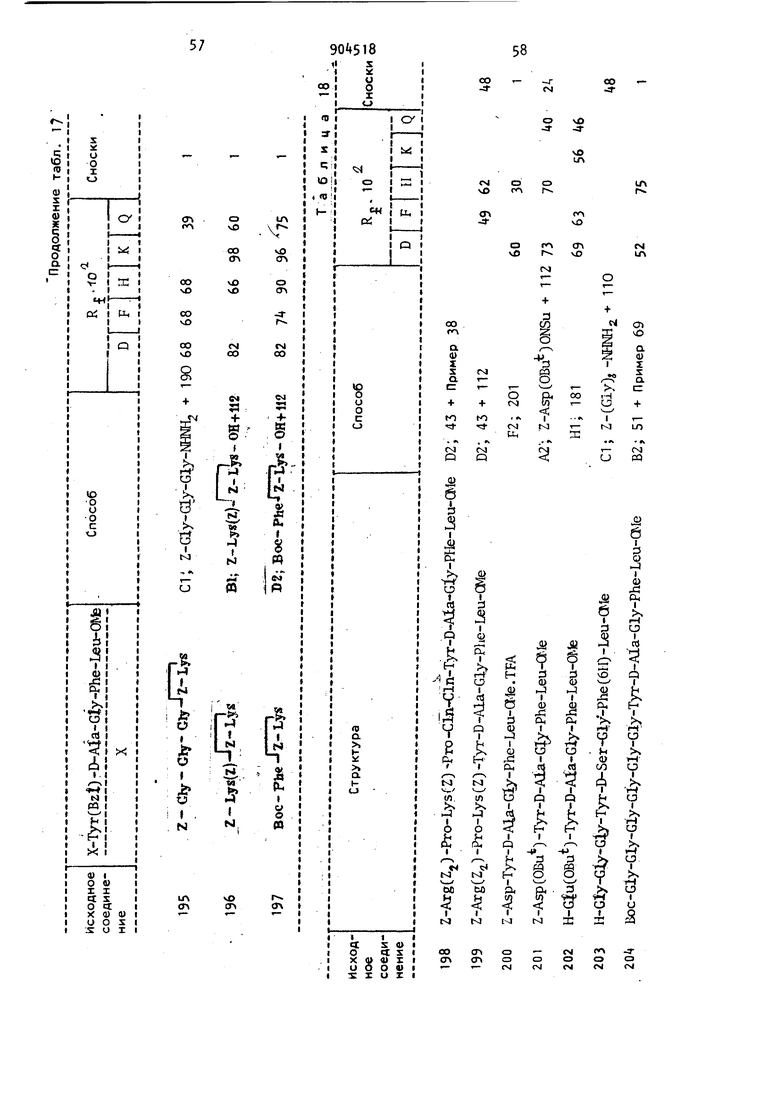
чО
OO
-a40
r
ir
f vO
oo
OO vO
d 9
OO
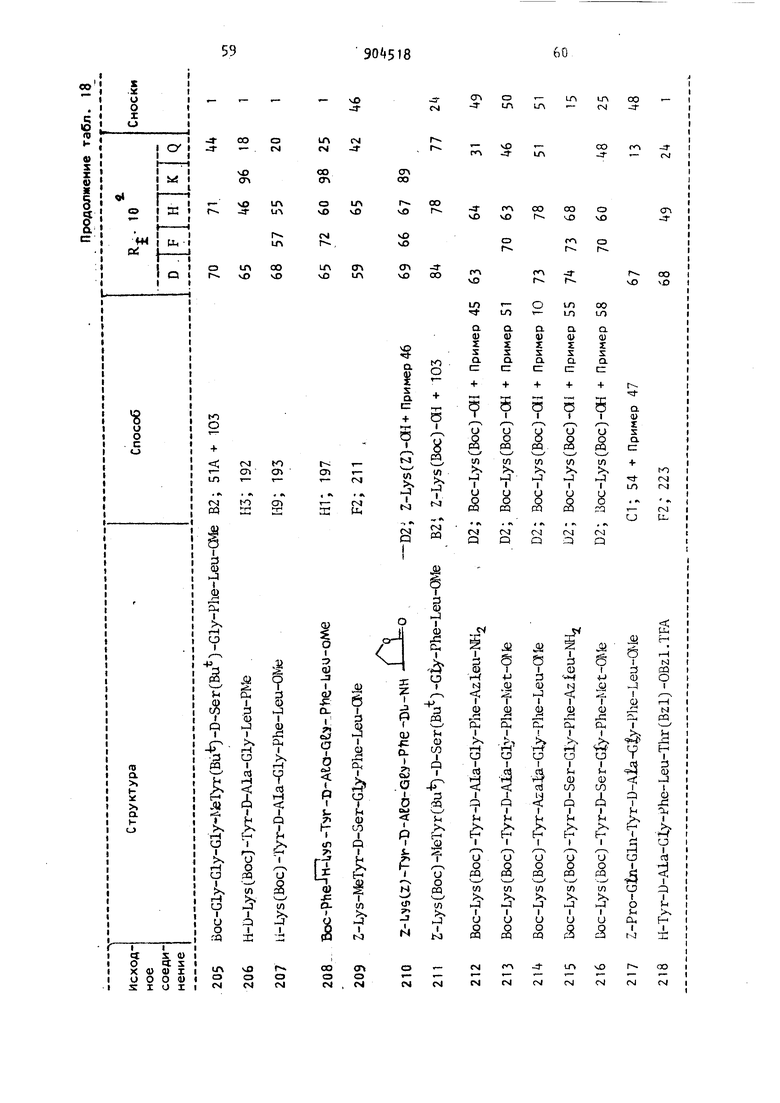
cr
СП
ГЛ
,- -Э-гОО
ОО
,- со
1Л со
СМ Ш
I- о
СП ОО
сг - о -а-тГ -асм
оо -а-а- г
ОО
г
ил ОО СО ОО
ОО
-т
0 -а-асм
О
1Г vC
см о
LA
л
-аО чО
vO vO
мэ
о
LA
LA
ОО
LA LA
Г LA
о
vO
чО
Г ч
О ОО
см г
чО
г
00
Ш LA
см 1Л
чО ч
с о
о
Г
ЗУ
0(ai2)CH .L1;
Boc-Leu-Ш + {-Ю(СН2)ОН
0(СН,)ЖгLi; Boc-Leu-Ш + HO(CH2),NHZ 73
0(C i meZLi; Boc-Leu-OH + ШССЬУй е
OCIijQI CHiLi;
Boc-Leu-ai + :i;3Qi2CH ai2
opiiLz;
Boc-Leu-CII + фенол Ql; Z-TyT(But)-a лH-Azphe-Lcu-OieiiCI El; Boc-AziAe-Le 3)НЧ 1лЧ:1л- С«ЬВос 3 2-С1п-С1пЧ1ВИ-Вс1С A4; Z-Gln-OCp 35Н-РЬв-А11еи- И2 36H-Phe-Nlc-OMB.Tosai 37Z-Phe-Nlc-CMe B5; Z-Hic-P NX 38Boc-Phe-Azlcu-: D2, Boc-Phe-ai 3SU-Pro-Lys(Z)-CMc.liCl 40Boc-Pro-Lys(2)-CHc B1; Boc-l rq-ai 41H-ibAla-Cly-rhc-Oie 2Z-t -Ala-Gly-Wie-a4e ЛЗ, Z-D-A a-OCp 43Z-Ajrg(Zi)-IYo-Lys(.Z)-ai w z-Ar6i:j)-i ro-Lys(Z)-a« АП :-An;{Zj)(Su 5H-Azgly-ilK-Azlcu-Nil.llCl 46Z-A2gly-Hie-A2lct Mi.|, Rl; Z-Azply-Cl 7h4;iy-Azi)lic-Leu-€He.llCl l eH4i}y-Phe-i4lc-Ofe.Tosai BS; Z-(Uy-ai + 36 fc9Z-Cly-Ilie-Mc-Ofc D2; Boc-Cly-ai 50Boc-Cly-AzpJie-Leu-afe 51Boc-Gly-Gly-Cly-ai 51AlX)c-Gl)-Gly-Gly-CKa B2; Boc-Cly-ni J SUBoc-Cly-Gly Cl)-CWe
38
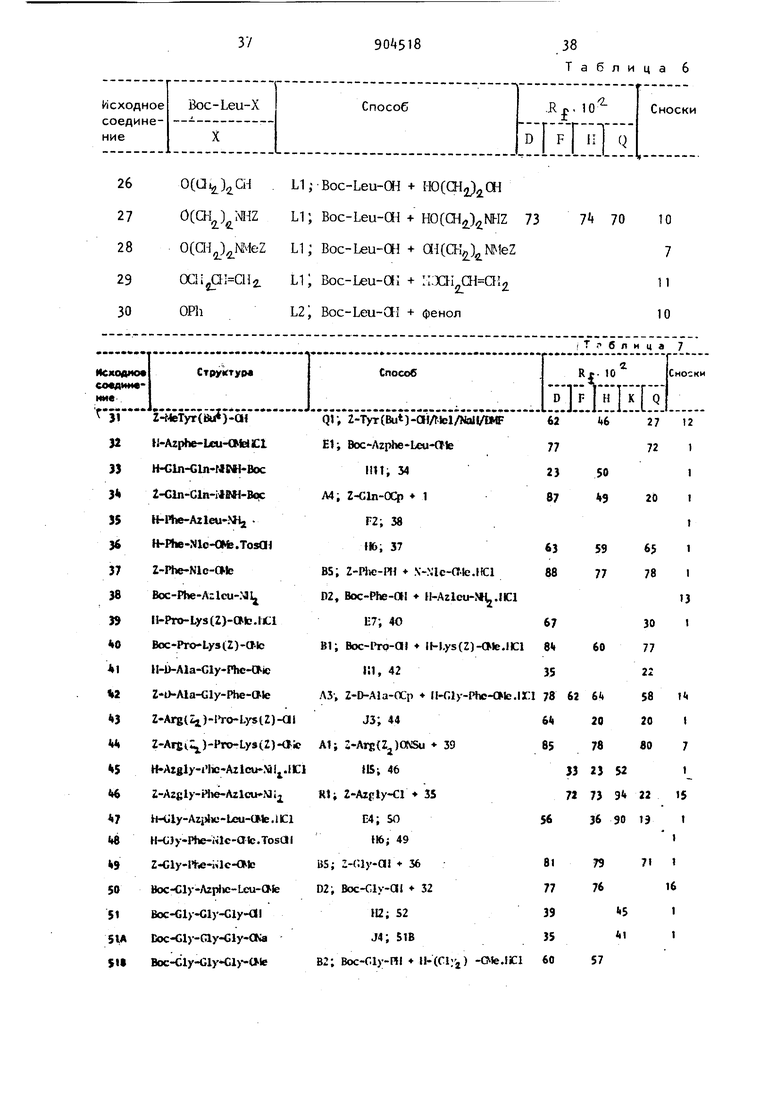
Таблица 6
7 70
10
11 10
блица 7 НИ; 34 E7; 40 1:1, 42 J3; 44 (IS; 46 D4; SO H6; 49 J4; 51B Atel/Nall/EMF -OMe 1 VIe-a-teJCl H-Azleu-Mi.llCl 6730 8 6077 ll-l.ys(Z)-CMe.JICl 3522 78 6264S8 II-{;iy-Phc-CWe.lX:i 642020 857880 39 332352 7273Э4 22 35 36 90 19 32 KCl-j) -Ofe.lJCl 60H-D-Aia.HCt 61Z-D-Afa A4; 62H-D-Asp 63Z-D-Asp(OBzt) A4-, 6 FT-D-IfiurTFA 65Boc-D-Leu B4; 66H-D-Lys(Boc) 67Z-D-Lys(Boc) B4-, 68H-D-Ivfet.HCl 69Boc-D-Ivfet A1, 70H-D-SerCBu) 71Z-D-SerCBu) B2, 72H-D-Thr 73Z-D-Tlir C1; 7 H-D-Trp.TFA A2} . 75Boc-D-Trp
Прооолжемие , 7
Таблица 8 H10; 6188 1 Z-D-A a-OCp + 5373 62 kB 1 H2; 67 1 Z-D-Asp(CBzt)-OGp+5322 F2, 651 Boc-D-Leu-Ш - 537& 79 7 15 H2- 671 Z-D-Lys(Boc:)-OH+5376 76 65 E5i 69 Boc-D-Met-OCp + 53 H3, 7161 57 88 46 1 Z-D-Ser(Bu)-ai-b5379 75 7 23 H2; 7358 36 71 20 1 Z-D-Thr-NHNH +5370 63 10 F3t 7561 55 27 1 Boc-D-Trp-OCp + 5379 70 9 60 2k
tCO -
-J-a S|
vO
о
-я-3О ГЛ
сэ
1Л
Г-v
r
n
ff
v
(TV
CM
r vO
1Л rg
oo о
- .CNJ
LT
vO
u-
OO vO
1Л vO
Ю O
Гч1
CTi
Ю
CTl
Й
cu
X
l-l
о
nj .H
7
a
tn
i
i
r о
tM
61 Формула изобретения Способ получения полипептидов формулы 1 ТтгВ-Б-F-G-R, где R, - атом водорода, метильный или ацетильный радикал, Rj - атом водорода, H-fJ-Ala; H-Asp; H-Lys-, H-lys(Boc); H-Gly-Gly; H-AspJlPtys, H-LysJTPLys, H-Arg-Pro-Lys; H-Gly-Gly-Gly; 11-Leu-Leu-Leu; H-Cru-Gly-ai H-Lys; H-Pro-Gln-Gln; li-Asp-Gly-Gly-Gly; H-Lys-Gly-Gly-Gly H-Gly-Gly-Gly-flbLys; II-Arg-Pro-Lys-Pro-Gln-Gln; Il-61u H-D-Lys; H-PheJlT-Sys или H-Gly-Gly-Gly-Gly-Gly-Gly; В - D-Ala; D-Asp; Azala; D-Leu; D-Ser; S-Thr; D-Trp; p-Ala; D-Ser(Bu); D-Lys или D-Met E - Gly или Azgly; F - Phe; Azphe или Phe(6H); G - Leu; Azleu; Nle; Met; Pro; DL-Leu или Azpro; К - ate; NHj; 0(CH.i)aNH2; oCaijliNIfffe; OH; 0(aij,)pH; OCCHiipAc; ОСау ОС-ОСД ; OCHtHrOAclGUQAcf oa{iCHCocoLi1f,)CH2oax:;. OCH(ai,3, Ю1(СНарСОС5Н„ Thr-OH; СП KI/ 0( 0( OCH-iai.CHi; OPh; NH(aic)aOH
904518
62
т 5 я и ц в 19 (Ш2) М1( Me; 0(a-I«l, П1;Чс; D-Tlir-Ш, и к вместе представляют собой гЬ-ж №1-0 f II ч I I , илиК- NH ичающийся тем, что отт защитные группы в соединении ы И NVf( / г Т-В -Е -F -G -К , / - водород, метильный или ацетильный радикал, - водород, Z; Н-й-А1а; Z-Asp; Z-Lys; Z-Lys(Z); Z-LysfBoc); H-Gly-Glyj Z-Asp(OBzl JZ4:ys; Z-Lys(Z)JZ(Lys); Z-ArgCZ }-Pro-Lys(Z); Z-Gly-Gly-Gly; Z-Lcu-Leu-Leu: Z-Glr-Gly-OBzl Z-Cys; Z-Pro-Gln-Gln; Z-Asp(OBzl}-Gly-Gly-Gly; Z-Lys-Glyj-Glv-Gly; Z-Gly-Gly-Gly-Tz s; Z-ArgCZ)-Pro-Lys(Z)-Pro-Gln-Gln; Doc; H-Glu((Bu); Boc-Lys(Boc); H-D-LysГВос); H-Lys(Вое); Boc-PheJH-Lys; Boc-Gly-Gly-Gly или Boc-GlyGly-Gly-Gly-Gly-Gly;- Тут; Tyr(Bzl), Tyr(Z) или TyrCBu);- D-Ala; D-Asp; Azala; D-Leu; D-Ser; .D-TIir; D-Trp; f -Ala; D-Ser(Bu-b); I;-Lys; D-Lys(Boc) или D-Met; - Giy или Azgly; - Phe; Azphe или Fhef6Il); Leu; Аг1еи; Nle; Met; Pro; PL-Leu или Azpro; К - СМе; 0(CHi)2.NH2; 0(.)aNIlMe; Ш; 0(CH2:ipAc; 0(CH2)jpCOCД ; OaioCH(OAc)CFiamc; . OCI liCQiOCOC iy CK. Oai(aVCAc)2; OCH(fflg)OCOC5-H. ри OBut;n,r№l)..w,-Q.,- „ О S 3. NHEt; Q(ai)zNHZ; ) OPhe; №1( is NHCaiiVNIl.Ie; NEti.; Me; 0(СНл)Ог1е2 или D-Thr-OBzl, или G и к вместе представляют собой («-о или N-jra Приоритет по признакам; 08.О. 1976 при R, - Н; Н; H-Arg; II-Gly; il-Glu; H-Asp; H-Phe; H-fi-Ala; H-D-Lys; il-Lys; H-Gjy-Gly-pl-I H-Lys; Н-РЬеЛМуЬ; H-Gly-Gly-Gly-fTFTys; H-AspJH ys или H-Ly&4MVs; -. D-Ser;. D-Ser(); D-Aia ИЛИ D-Thr; -Giy; -Phe; -Leu; Met или Nle;, -OH; NIIj; Ше; 0(СН2)аСН(Ме)г; OO QMHi; б( OCairOiNHi; 0(аЩШ1е; OPhe; NHEt; -Ot N 21.05И976 при В - Azala; E - Azgly; : ос ри 5 ос ос ри в од ил щ пр чт не пр Ч. 6 F - Azphe; G - Azieu или Azpro; альные значения радикалов - приоет 08,.1976. 27.05И976 при R - Me (когда R . - водород) , альные значения радикалов - приоет 08-04.1976. -- -ЗУбпри R, - Me (когда R2 - водород) , альные значения радикалов - приоет 08..1976 при условии, что олекуле имеется по крайней мере а азааминокислота. 28.10.1976 при - H-Gly-Gly; И-Leu-Leu-Leu; H-Arg-Pro-Lys; H-Pro-Gln-Gln; K-Gly-Gly-Giy; H-Lys4 ly-Gly-Gly; H-Asp-Giy-Gly-Gly; H-Arg-Pro-Lys-Pro-Glji-Gln или H-Gly-Gly-Gly-Gly-Gly-Gly;В - D-Lys; D-Trp или S-Met; E - Gly; F -.Phe; С - Pro К - оа4ш(слс)а-;4,с; (х:н(а10Ас) ocHcaiiOCO-qj-Hja; ош акосоеJu,; ,o()JGAc или (:)(CH)40ca: j f G и к (снг),-тга (CHzV , а 28.10.1976 значения радикалов оритет 28i.l0.1976 при условии, . в молекуле присутствует по краймере одна азааминокислота. Источники информации, нятые во внимание при экспертизе 1.Шредер Э., Лобке К. Пептиды. 1. М., Мир, 1967, с. 112, 2.Там же 5 с. 116.
Авторы
Даты
1982-02-07—Публикация
1977-04-08—Подача