Изобретение относится к усовершенствованному) способу получения сложных зфиров тиокарбаминовой кнслоты общей формулы
BI
г
I
где RI и RZ вместе с атомом азота представляют собой гексаметиленимин, или RI и Rj в отдельности представляют собой н-пропил, н-бутил, изобутил нли циклогексил;
R - этил, н-пропил, бензил или хлорбензил,
которые находят применение в различных областях и для различных целей, некоторые из них являются активными гербицидами, другие - эффективны в отношении подавления роста микроорганизмов, бактерий, а ряд из них - активные инсектициды.
Известен способ получения сложных эфирОв тиокарбаминовых кислот взаимодействием карбамоилхлорида с меркаптаном в присутствиикатализатора хлорида цинка 1.,
Однако при осуществлении данного способа необходимо использование раствЬрите:м, инертного по отношению к катализатору.
Известен также способ получения эфнров 5 тиокарбамииовых кислот, включающий получение натриевой соли меркаптана с последующим взаимодействием с карбамоилхлоридом в присутствии растворителя 2.
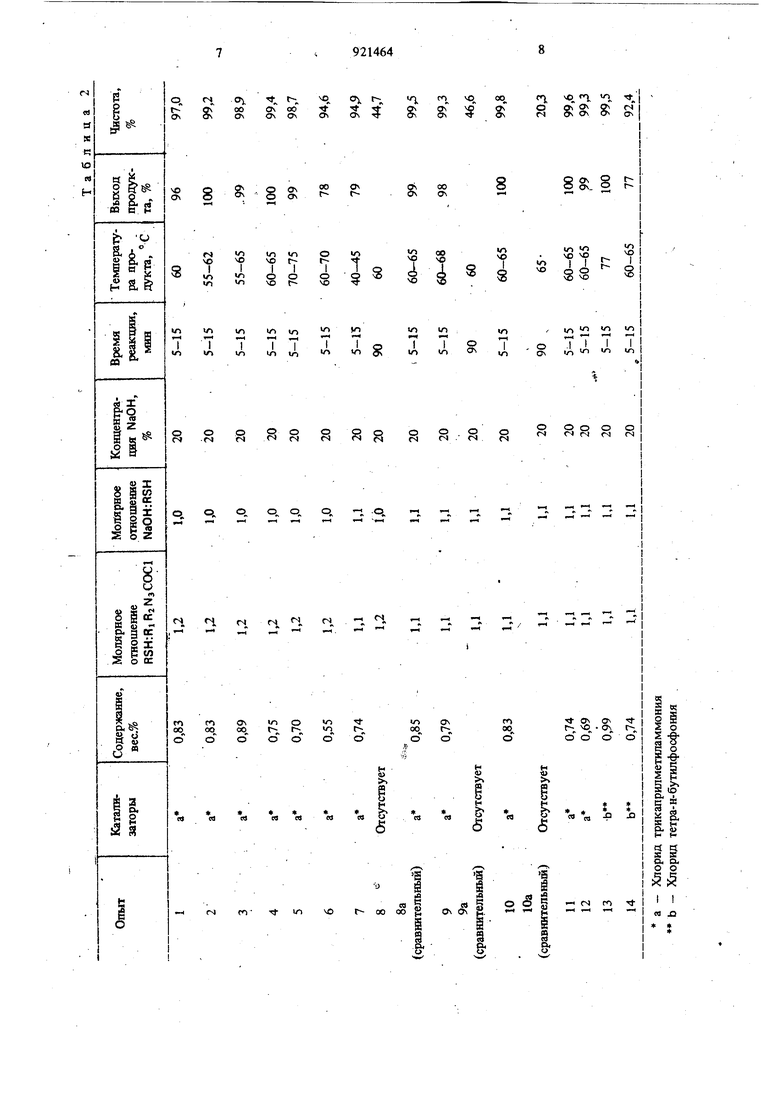
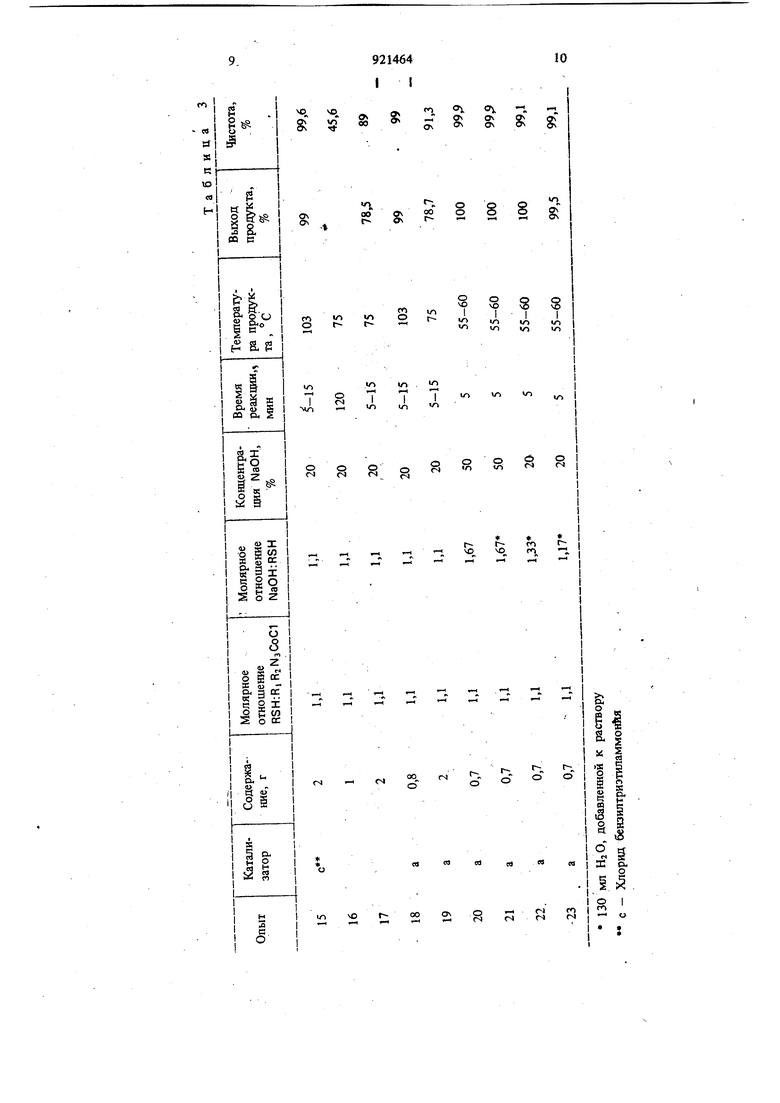
Однако использование натриевой соли мер10 каптана вызьтает дополнительные трудности, связанные с фильтрованием и транспортировкой твердого вещества. Применение растворителя ведет к снижению емкости реактора. Кроме того, проблемой может оказаться извлече15 ние растворителя, а выделяющийся во время получения натриевой соли водород осложняет применение этого процесса своей утилизацией. Известен также способ получения сложных зфиров тиокарбаминовых кислот с помощью 20 процесса, основанного на реагированин вторичного или первичного амина с карбонилсульфидом вприсутствии основного характера, которым может быть любой амин, включая третичный амин, с последующим реагированиел полупродукта с орга 1ическим сульфатом, например диалкилсульфатом или диаллилсульфатом 3. Однако этот процесс неприемлем из-за) потребности в специальном газотранспортном оборудовании, требуемом для добавления кар бонилсульфида. Кроме того, расходы на алкил сульфат оказьшаются невозместимыми, что ведет к росту издержек по процессу в целом. Наиболее близким к предлагаемому по технической сущности и достигаемому результ является способ по гчення сложных эфиров тиокарбаминовых кислот о&цей формулы Г путем взаимодействия карбамоилхлорида обще формулы-f RiР где RI и RZ имеют вышеуказанные значения, с меркаптаном общей формулы RSH1И где R имеет вышеуказанные значения, при температуре от 10 до 100 С в присутстви водного раствора, содержащего от 20 до 50 вес.% щелочи, с последуюиим разделением водной и органической фаз и выделением сложного эфира тиокарбаминсшой кислоты из органической фазы W., Недостатком этого способа является интен сивное перемешивание япя рбразсшаяия значительной площади пснзерхности раздела между двумя жижнми фазами, а также достаточно высокая чистота целевого продукт (показана в сравнительных примерах). Цель изобретения - повышение чистоты целевого продукта. Поставлениая цель достигается способом, получения сложных эфиров тиокарбаминовой кислоты общей формулы Т путем взаимодействия карбамоилхлорида оЪщей формулы Л С меркаптаном общей формулы Я/ при температуре от 10 до 100° С в присутствии водного раствора, содержащего от 20 до 50 вес.% щелочи, и катализатора - трикаприлметйламмония, хлорида тетра-н-бутилфосфония, хлорида бензилтриэтиламмония, используемого в количестве от 0,5 до 1 вес.%. П р и м е р . В 500-миллилитровый реактор, снабженный механической мешалкой, помещают водный раствор 20%-ного гидрата окиси натрия объемом i 10 мл. К указанному водному раствору добавляют 37 г (0,6 моль) этилмеркаптана, что составляет молекулярное соотношение между гидратом окиси натрия и этилмеркаптаном, равное 1,0. Затем к смеси добавляют 81 мл (0,5 моль) ди-н-пропилкарбамоилхлорида с растворенным в нем 0,8 г (0,83 вес.%) трикаприлметиламмонийхлорида, что даёт молярное соотнощеше этилмеркаптана к хлорангидриду карбаминовой кислоты равное 1,2. В процессе прибавления температура реакционной смеси и реактора поддерживается ниже . Р1гакционную.смесь переме- щнвают при этой температуре в течение 10 мин, прт этом образуется два слоя жидкости, которые разделяют и получают 88,2 г органического слоя (продукта), что соответствует выходу 96%. Органический слой нагревают до 50° С под вакуумом для удаления остаточной воды и меркаптана. Анализ методом газовой хроматографии подтверждает идентичность продукта и дает значение степени чистоты продукта, равное 97,0%. В эксперименте используют следующие катализаторы; хлорид трикаприлметиламмоний (а), хлорид тетра-н-бутилфосфоний (Ь) и хлорид бензилтриэтиламмоний (с). В табл. 1 приведены реагенты и продукты, в табл. 2 и 3 даны условия проведения реакции и результаты.
10
921464 I I Ц:9 Как видно КЗ табл. I и 3 особый интерес представляет сопоставление опытов 8 и 8а, 9 и 9а, а также 10 и 10а. Каждая пара демон стрирует изменение протекания реакции при наличии и при отсутствии фазо-переносного катализатора. Данные псжазывают значительны положительный эффект, достигаемый для каждого случая как в отношении времени реакции, так и в отношении чистоты продукта при использовании катализатора. Хотя сопьставпение опытов 16 и 9а не дае положительного зффекта от использования хлорида бензилт жзтиламмония по предс тавлен ным данньш, однако наблюдается рост скорос ти реакции, не показанный в таблице. Реакция р доходид до КОШ13, поскольку катализатор не растворим в карбак1оилхлориде. Окончание реакции достигается либо в случае, когда используется тот же катализатор, с карбамоилхлоридом, в котором ои растворим, либо в случае, когда используется другой катализатор который растворим в карбамоилхлориде, использованном в опыте 16. Положительный зффект и преимущества системы, таким образом, очевидаы для случаев, когде все компоненты растворимы. Фазопереиосной катализатор может действовать также как эмульгатор, облегчая тем самым перемешивание. Формула изобрете ни я Способ полз чения сложных эфиров тиокарбаминовой кислоты общей формулы I «,; f N-C-S-R . Ч где , и Rj вместе с атомом азота представляют собой гексаметиленимин, или RI и R в отдельности представляют собой н-пропил, н-бутил, изобутил или циклогексил; Я - этил, н-пропил, бензил или н-хлорбенпутем взаимодействия карбамоилхлорида общей формулы -с-се где RI и Яз имеют вцшеуказанные значения с меркаптаном общей формулы ifiT RSH. где Я имеет вышеуказанные значения, при температуре от 10 до 100° С в присутствии водного раствора, содержащего от 20 до 50 вес.% щелочи, с последующим разделением водной и органической фаз и вьщелением сложного эфира тиокарбаминовой кислоты из органической фазы, отличающийся тем, что, с целью повышения чистоты целевого продукта, взаимодействие осуществляют в присутствии катализатора - трикаприлметиламмояия, хлорида тетра-н-бутилфосфония, хлорида беизилтризтиламмония, причем катализатор используют в количестве от 0,5 до 1 вес.%. Источники информации, принятые во внимание при экспертизе 1.Патент США N 2983747, кл. 260-455, опублик. 1961. 2.Патент США № 2913327, кл. 71-100, опублик. 1961, 3.Патент США N« 3133947, кл. 260-455, опублик. 1964. 4.Патент США N 3836524, кл. 260-239, опублик. 1974 (прототип).

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения эфиров тиокарбоминовых кислот | 1974 |
|
SU685147A3 |
| АЛКИЛИРОВАНИЕ N'-ФЕНИЛ-N-АЛКИЛФЕНИЛЕНДИАМИНОВ В ИОННОЙ ЖИДКОСТИ | 2006 |
|
RU2422435C2 |
| АЛКИЛИРОВАНИЕ ПРОИЗВОДНОГО ДИФЕНИЛАМИНА В ИОННОЙ ЖИДКОСТИ | 2006 |
|
RU2418784C2 |
| АЛКИЛИРОВАНИЕ ПО КОЛЬЦУ АНИЛИНА С ИСПОЛЬЗОВАНИЕМ ИОННЫХ ЖИДКИХ КАТАЛИЗАТОРОВ | 2006 |
|
RU2427567C2 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОТЫ МОНТЕЛУКАСТ В ИОННОЙ ЖИДКОЙ СРЕДЕ | 2008 |
|
RU2436774C1 |
| Способ получения -бензиловыхэфиРОВ , -диАлКилТиОКАРбАМи-НОВОй КиСлОТы | 1977 |
|
SU803857A3 |
| СПОСОБЫ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АМИНОМЕТИЛПИРИДИНА И 2-ЦИАНОПИРИДИНА | 2001 |
|
RU2266900C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АРИЛ-1-ЦИАНОЦИКЛОБУТАНА | 1996 |
|
RU2179168C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИМЕТИЛ-2- ДИФТОРМЕТИЛ-4- (2-МЕТИЛПРОПИЛ)-6- ТРИФТОРМЕТИЛ-3,5- ПИРИДИНДИКАРБОТИОАТА | 1991 |
|
RU2014322C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИЗШИХ АЛКИЛМЕРКАПТАНОВ | 1993 |
|
RU2117942C1 |




Авторы
Даты
1982-04-15—Публикация
1977-09-02—Подача