Изобретение относится к новому K.riaccy химических веществ - крис1таллическим микропористым силикатам щелочных металлов с общей формулой Me p-nSiO - , где Me - литий, натрий, калий, рубидий, цезий,
п - М% 1-40, ш - И 1-20,
Me 2.0
обладающим молекулярно-ситовЫми свойствами, и споЬобу их получения.
Полученные кристаллические пористые силикаты щелочных металлов представляют собой микропористые кристаллические кремнеземистые сорбенты нового типа, по ряду свойств, в том числе молекулярно-ситовому действию, сходные с цеолитами. Они кислотоустойчивы, проявляют высокую адсорбционную способность уже после вакуумирования при , превосходя при этом по емкости известные высококремнеземистые цеолиты (морденит, клиноптилолит). Пористые силикаты могут быть использованы как адсорбенты в процессах очистки, осушки и разделения газов, паров и жидкостей при работе в агрессивных средах, в системах с лимитированными энергозатратами на. регенерацию, а также .как ионообменники.
Известно, что из системы - SiO при 50-90°С выделен кристаллический тетрасиЛикат натрия
5 BNa O-ISSiO.11Н2.О как самостоятельное химическое соединение с характерной рентгенограммой ij. Однако здесь не описаны свойства синтезированного силиката.
Известен синтез гидросиликата нат10рия с соотношением SiOj/Na2Р 9,4-13,1 кристаллизацией вязких силикатных растворов (15 вес.ч геля кремнезема, 3,6 вес.ч. NaOH, 30 вес.ч. вода, мольное отношение .), про15 осуществляется при в течение 3-4 недель .
Этот синтез воспроизведен с использованием вместо силикагеля. 30%-ного раствора коллоидного кремнезема и в
20 некоторых случаях силиката натрия, при соотношениях SiO2/Na2p в реакционных смесях 5-8 получен другой более тонкодисперсный кристаллический силикат натрия с соотношением
25 20. В работе приведены рентгенограммы синтезированных образцов и некоторые данные об их свойствах. Отмечено изменение структуры в процессе сушки на воздухе при 110 С,
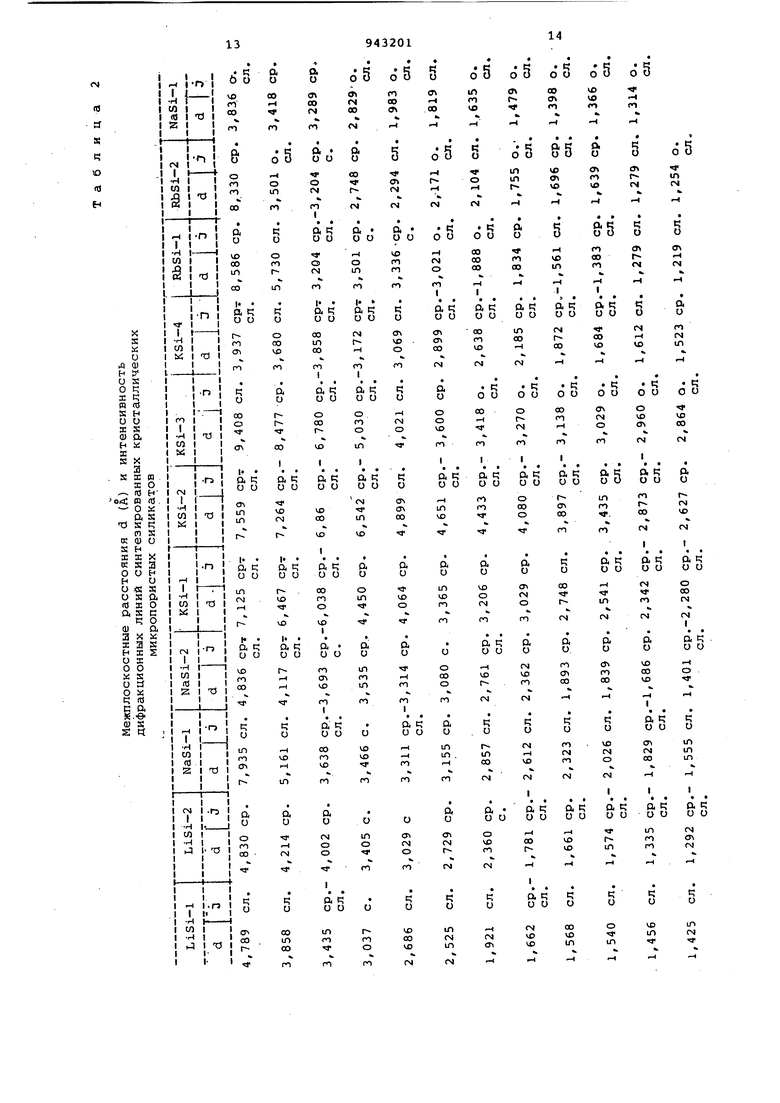
30 а. также при обработке кислотой (нейтрализация щелочи достигается при рН 4,5), размер и форма кристаллов сохраняются. Удельная поверхность образцов, определенная по адсорбции азота и метиленового голубого, приме но соответствует внешней поверхности пластинчатых агрегатов 25-30 м / Однако величины ионообменной емкости и хемособции бутокси-групп указывают на существование и доступность внутренних пор в кристаллах. При обмене Na nk ионы ацетилтриметиламмония от мечено некоторое увеличение межплоскостных расстояний - расширение межд слоями решетки. Последующим,ионным обменом получены К, Li, Ад, Со - фор мы полисиликатов. Известно, что прямым гидротермгшь ным синтезом кристаллы полисиликатов калия и лития получить не удалось 3 Известны кремнеземистые композиции, содержащие 10-30 вес.% окислов SiOo. и с соотношением от 4,2:1 до 6:1, которых 40-65 вес кремнезема находится в кристаллоидальной форме. Такие стабильные водонерастворимые кремнеземистые, композиции получают - смешением коллоидального аморфного кремнезема в виде порошка или кремнезоля с раствором силиката натрия и нагреванием смеси при 40-100С до образования прозрачного и устойчивого во времени раствора. Указанные композиции весьма устойчивы к гелеобразованию и осаждению, они используются как пленкообразователи и связки, обладающие высокой адгезионной способностью и устойчивые по отношению к воде C4J. Однако в известных работах не охарактеризованы сорбционные и молекулярно-ситовые свойства, не определены физико-химические условия: соотношение кймпонентов,температура, давление, время, необходимые для направленного синтеза кристаллов задан ного состава,, структуры и свойств; напротив, очевидна невоспроизводимость и противоречивость экспериментальных данных - в реакционных смесях одного и того же состава,по. разным источникам, образуются различ ные продукты. Кроме того, в качестве исходного сырья используют концентри рованный раствор коллоидного кремнезема, требующий специального сложного и дорогостоящего производства. Целью изобретения является синтез микропористых кристаллических силикатов щелочных металлов, обладающих молекулярно-ситовыми и другими полезными для практического применения- в сорбционной технике свойстваили а также создание простого, эффективного и регулируемого способа получения таких веществ .с заданным соста вом структурой и свойствами на основе доступного сырья. Синтез кристаллических пористых силикатов щелочных металлов с общей формулой Me O-nSiOiinHj O, где Me литий, натрий, калийJ рубидий, цезий, SiO - i-40 ш - fag-0 1-20, ггг-т; - 1 чи, m ... обладающих молекулярно-ситовыми свойствами, приведен впервые до сих пор такие пористые силикаты приведенной формулы, их свойства и способ получения в литературе не-.описаны. Новые порисзше кристаллические силикаты щелочных металлов могут быть получены только при соблюдении совокупности необхсэдимых условий, а именно: проведении реакции взаимодействия аморфного кремнезема с водными растворами щелочей при определенных соотношениях компонетов, моль: Me,O:SiO ; 1: (0,1-32, 0) : (2-95) в низкотемпературных (Т 90-200С) гидротермальных условиях и течение 0,5-30 сут с последующей отмывкой от избытка до рН 7-8,5 и сушкой при комнатной температуре. С целью ускорения процесса взаимрцействие ведут в присутствии затравок изоструктурных с синтезируемыми кристаллическими силикатами. Указанные соотношения подобраны экспериментально, исходя из найденных полей кристаллизации в изученных тройных системах. Температура меньше нецелесообразна в связи с увеличением времени синтеза, при образуются плотные кристаллические модификации кремнезема. В качестве источника кремнезема используют аморфную кремневую кислоту, силикагель, аэросил, белую сажу. Для ускорения процесса синтеза целевых продуктов с высоким выходом (60-90 г на 100 г исходного кремнезема) и фазовой частотой в реакционные смесивводят в качестве затравки (1-1Овес.% кристаллы, однотипные с образуклцимися в данной реакционной смеси (соответствующие силикаты, полученные без использования затравки, кристаллы кварца, кристобалита, тридимита) ., Процесс синтеза осуществляют в запаянных стеклянных ампулах из термостойкого и устойчивого к действию щелочей стекла или в автоклавах из нержавеющей стали стандартной конструкции, футерованных тефлоном. В качестве нагревательных приборов используют термостаты или обычные печи и сушильные шкафы с автоматическими регуляторами температуры. Полученные продукты отмывают от избыточной щелочности дистиллированной водой (рН промывных вод 7,08,5; сушку осуществляют при комнатной температуре 20-30С) . При ,0 наблюдается переход к кристалличес,ким поликремниевым кислотам. Для характеристики и описания по лученных кристаллических nopHclbix силикатов проведен химический, рент генофазовый и термографический аналиЗ, получены электронные микрофотографии, сняты ИК-спектры, определена плотность (по и СбНб), уде ная поверхность (по аргону), проведены адсорбционные измерения. Данные об оптимальных условиях получения и химическом соотаве, а также некоторые характеристики сили катов приведены в табл.1,; Пример 1. В тефлоновой ампуле емкостью 50 мл готовят водный раствор гидроокиси натрия (3,22 г NaOH, 31,8 г ) , затем к раствору при интенсивном перемешивании добавляют 15 г кремневой кислоты (ра мер частиц 0,25-0,5 мм). Объем реак ционной смеси 40 мл, соотношение компонентов, моль: .810,2 :1120 1:6,2:44,6. Ампулу помещают в автоклав. Кристаллизация продолжается 12 ч при 175С. Промывку кристаллов осуществляют дистиллированной водой до рН 8,0 сушку - при 20с. Выход кристаллов полисиликата натрия первого структурного типа (NaSi-1) - 12 г, что составляет 60% от теоретического. Химический состав, моль: Najp 13,1 SiO,,4 .Н,О. Пример 2. В стеклянной ампуле емкостью 50 мл готовят водный раствор гидроокиси натрия (6,46 г NaOH, 23,54 г ) . Затем в ампулу с щелочным раствором при интенсивнем перемешивании добавляют 20 г сидикагеля (в пересчете на сухой кремнезем). Размер частиц SiO 0,25-0,5 мм. Объем реакционной смес 30 мл, соотношение компонентов, моль: N8,2 0:SiO :H O 1:4,14:17,25. Ампулу помещают в автоклав. Кристаллизация продолжается 72 ч при 125С. Осадок промывают дистиллированно водой до рН 7,5 сушат при 25°С. Вы ход кристаллов полисиликата натрия второго структурного типа (NaSi-2) 12,5 г, что составляет 43% от теор тического. Химический состав, моль . 7,9 310-2:9,0 . Примерз. В тефлоновой ампу ле емкостью 50 мл готовят водный раствор гидроокиси натрия (6,46 г NaOH 23,54 г ) . Затем в ампулу щелочным раствором при интенсивном п ремешивании добавляют 20 г кремнев кислоты.Размер частиц 0,25-0,5 мм. Объем реакционной смеси 30мл, соотн шение компонентов, моль: Na2p:SiO 1:4,14:17,25. Ампулу помещаю в автоклав. Кристаллизация продолж ется 16 сут при 90°С. Осадок промывают дистиллированной водой до рН 8,0, сушка при . Выход кристаллов полисиликата натрия второго структурного типа (NaSi-2) 13 г, что составляет 45% от теоретического. Химический состав, моль: ,0 SiOjlO, . Пример4. В стеклянном реакторе емкостью 1000 мл готовят водный раствор гидроокиси натрия (125 г NaOH, 471 г HyjO) , Аморфную кремневую кислоту (400 г SiOj, размер частиц 0,25-0,5 мм) тщательно смешивают с 50 г полисиликата натрия второго структурного типа (размер частиц 2-6 мк), затем при интенсивном перемешивании порошкообразную массу вводят в раствор щелочи. Объем реакционной смеси 600 мл, соотношение компонентов, моль: Na OrSiO tH O 1:4,14:17,25, затравка 5 вес.% по- . лисиликата натрия второго структурного типа (NaSi-2). Кристаллизация продолжается 144 ч при 90°С, .Промывку кристаллов осуществляют дистиллированной водой до рН 8,0, сушку-при . Выход кристаллов полисиликата натрия второго структурного типа 336 г, что составляет 59 % от теоретического. Химический состав, моль: -9,5 SiO,,2 . Пример 5. В тефлоновой гилпуле емкостью 50 мл готовят водный раствор гидроокиси натрия (6,46 г NaOH, 23,54 г ) ; Затем в ампулу вводят порошкообразную смесь, состоящую из аморфной кремневой кислоты (20 г, размер частиц 0,25-0,5 мм) и полисиликата натрия второго структурного типа NaSi-2 (2,5 г размер частиц 2-6 мк). Реакционную смесь тщательно перемешивают. Объем реакционной смеси 22 мл соотношение компонентов, моль: SiOg rH O1:4,14:17,25. Ампулу помещают в автоклав . Кристаллизация продолжается 24 ч при . Промывка кристаллов осуществляется дистиллированной водой до рН 8,0, сушка - при , Выход кристаллов полисиликата натрия второго структурного типа (NaSi-2) - 16,5 г, что составляет 58% от теоретического. Химический состав, моль: Na2p8,9 SiOa.-10,0 . Пример 6. В тефлоновой ампуле емкостью 100 мл готовят водный раствор гидроокиси лития (11 г LiOH, 74 г ) . Аморфную кремневую кислоту (15 г) при интенсивном перемешивании добавляют к раствору щелочи. Объем реакционной смеси 80 мл, соотношение компонентов, моль: SiO 1:1,5:27,0. Кр сталлизация продолжается при 90 С 25 сут. . Промывку образцов осуществляют дистиллированной водой до рН 8,2, сушку - при на воздухе. Выход кристаллов силиката лития первого структурного типа (LiSi-1) - 12 г что составляет 67 % от теоретическо го. Химический состав, Monb, 3, SiOj. 2,0 . . , Прим ер 7 В тефлоновой ампу емкостью 200 мл готовят водный раст вор гидроокиси калия (12 г КОН, 88 мл ), затем к раствору при ин тенсивном перемешивании добавляют 100 гкремневой кислоты (размер час тиц 0,25-.0, 5 мм) . Объем реакционной смеси 140. мл, соотношение компоненто моль: KiO:SiO2;:SiO l:7,9:73,5. Тефлоновую ампулу помещают в автоклав и выдерживают в термостате 1 сут, при . Промывают кристаллы дистиллированной водой до рН 8,0 и. затем суша на воздухе при 28с. Выход кристалл полисиликата калия третьего структу ного типа (KSi-3) - 96 г, что составляет 83 % от теоретического. Химический состав, моль: К-О 29,73102 viO,5 . П р и м е р 8. В тефлоновой ампу ле емкостью 50 мл готовят водный ра вор гидроокиси рубидия (1,37 г RbOH 16,13 г. ), затем к раствору при непрерывном перемешивании добавляют 7,5 г кремневой кислоты. Объем реак ционной смеси 20 мл, соотнбшение компонентов, моль: Rb,j O:SiO2 :H,0 1:18,70:135,09, Тё лоновую ампулу помещают в автоклав. Длительность кристаллизации при 200 С 72 ч. Промывку кристаллов осуществляют дистиллированной .водой до рН 8,0, сушка на воздухе при . Выход кристаллов полисиликата рубидия пер вого структурного типа (RbSi-1) 8 г, что составляет 8.3 % от теорети ческого. Химический состав, моль: . 31,20SiO2- 12,ОН2.О. Пример9. В тефлоновой ампу ле емкостью 50 мл готовят водный раствор смеси гидроокисей NaOH и CsOH (0,58 г NaOH, 2, CsOH, 12,24 г Н), затем к раствору при непрерывном перемешив.ании добавляют 10 г аэросила ( MVi). бВъем реакционной смеси 25 мл, соотношение компонентов, моль: :SiOi-.,5:0,5:5,75:24,2. Тефлоновую ампулу помещают в автоклав и выдерживают при 25 сут. Промывку кристаллов осуществляют дистиллированной водой до рН 8,2,сушку - на воздухе при комнатн ой температуре. Выход кристаллов смешанного Na, Cs - полисиликата первого структурного типа (Na Cs Si-1) - 11 г, что составляет 75 % от теоретического. Химический состав, моль: 0,42 0,58Cs40-12,30S10.i8,70H При мер 10. В тефлоновой ампуле емкостью 50 мл готовят водный раствор смеси гидроокисей LiOH, . NaOH и iCOH (1,29 г LiOH, 2,15 г NaOH, 3,01 и КОН, 23,55 г ), затем к раствору при непрерывном перемешивании добавляют 20 г кремневой кислоты (размер частиц 0,25-0,5 мм). Объем реакционной смеси,40 мл, соотношение компонентов, моль: ..SiOyjiK O 1:1:1:12,7:52,1. Тефлоновую ампулу помещают в автоклав и выдерживают в термостате при 150С 3 сут. Промывку кристаллов осуществляют дистиллированной водой до рН 8,5, сушку - на воздухе -при . Выход кристаллов смешанного LiNaK - полиси.ликата (LiNaKSi-1) - 15 г, что составляет 53. % от теоретического. Химический состав, моль: 0,32 ,,,74LiO.. 6,2lH,f. Синтезированные ПО предлагаемому способу кристаллические силикаты и полисиликаты щелочных металлов представляют собой меловидные тонкодисперсные порсянки, нерастворимые в воде, спиртах, бензоле, ацетоне и других органических раствори-, телях, они могут храниться в течение длительного времени на воздухе при комнатной температуре без изменения свойств. Всего получено 16 индивидуальных соединений, относящихся к классу силикатов, различного состава, в том числе: силикаты лития (2 структурных типа), полисиликаты натрия (2 структурных типа) /- полисиликаты калия (4 структурных типа) полисиликаты рубидия (2 структурных типа) и смешанные LiNa-, LiK-, NaK-, NaCs-, LiNaK-полисиликаты. В табл.2 приведены данные .рентгенограммы полученных кристаллических силикатов щелочных металлов. Поскольку рентгеногралв«1ы образцов LiNaSi-1, NaKSi-1 Hr.LiNaKSi-l аналогичны рентгенограмме образца NaSi-1, рентгенограмма образца LiNaSi-2 аналогична NaSi-2, а LiKSi-1 - KSi-3, поэтому рентгенограм1иы образцов LiNaSi-1, NaKSi-1/LiNaKSi-1 LiNaSi-2, LiKSi-1 не приведены с целью уменьшения объема таблицы. ИК-спектры в области валентных и деформационных колебаний связей Si-0 также подтверждают структурную индивидуальность полученных силикатов. Размер частиц полученных. кристаллических силикатов от 0,1 до 10 мк (преимущественно 16 мк); наиболее типичная форма частиц: узловатые округ.пые агрегаты с хорошо развитой чешуйчатой поверхностью (NaSi-1, LiNaSi-1, NaKSi-1, NaCsSi-1), тонкие прймоугольные
пластинки (NaSi-2, LiNaKSi-1, LiNaSi-2), глобулы (LiSi-1), брусковидные и игольчатые кристаллы (LiSi-2), округлые и частично ограненные агрегаты (KSi-1), вытянутые овальные частицы (KSi-2). Форма частиц остальных силикатов менее определенная.
Плотность кристаллических силикатов и полисиликатов (1,702,80 г/см) зависит от структуры, содержания воды и типа катионов (см. табл.1). При определении плотности в качестве пикнометрической жидкости используется бензол .
Величины удельной поверхности бол шинства образцов, определенные кроматографическим способом по тепловой десорбции аргона (азота), составляют 5-25 и соответствуют, в основном, внешней поверхности кристаллов.
Катионы щелочных металлов, входящие в состав синтезированных веществ могут быть замещены на катионы други металлов при обработке растворами соответствующих солей, что открывает возможности для модифицирования свойств предлагаемых соединений.
Кристаллы силикатов и полисиликатов не разрушаются при обработке 0,1-1,0 н. растворами минеральных кислот (неб , HNO}, H,) , в результате полного удаления катионов щелочных металлов образуются кристаллические поликремневые кислоты, обладающие своеобразной структурой,адсоционными и ионообменными свойствами.
При взаимодействии кристаллически поликремневых кислот с растворами соответствующих щелочей в результате ионообменного поглощения катионов практически полностью восстанавливаются состав, структура и свойства исходных кристаллических силикатов и полисиликатов (необратимый переход и поликремневым кислотам наблюдается только в случае силикатов лития).
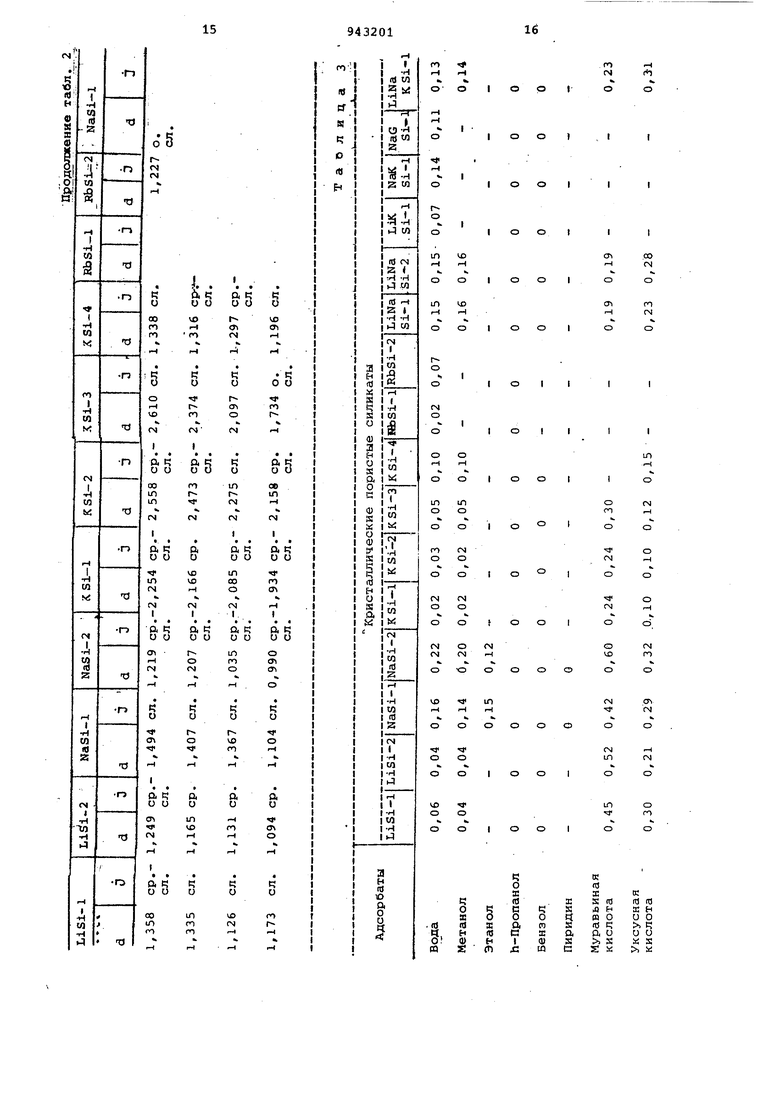
В табл.3 приведены результаты адсорбции различных веществ на кристаллических микропористых силикатах щелочных металлов (1ддс 20С; для паров ,3; для газов мм рт.ст.).
Синтезированные кристаллические силикаты щелочных металлов являются микропористыми адсорбентами. Их адсорбционные свойства и молекулярноситовое действие (см.табл.3) определяются рамером пор (4А) и средством к небольщим полярным молекулам (воДа, метанол, аммиак и др.). Кристаллические силикаты не сорбируют спирты, начиная с пропанола, бензол ,пиридин,ди- и триэтиламин;значительная часть их пор не доступна также небольшим, но относительно инертHfciM молекулам и СО, которые как и аргон (азот) адсорбируются в основном на внешней поверхности кристаллов. Полярные молекулы , NHj, NOxj, HCt заполняют внутрикристаллическое пространство силикатов уже при низких давлениях. Для полисиликатов натрия более всего и для некоторых других в меньшеймере характерна лабильность остова, сорбция сопровождается изменением hapaметров пористой и кристаллической структуры. Силикаты гшсорбируют значительные количества органических кислот (муравьиной, уксусной, пропионовой), причем не претерпевают разршения при многоцикловой работе.
В целом, по адсорбционной способности кристаллические силикаты щелочных металлов сходны с цеолитами типа А, но выгодно отличаются повышенной кислотоустойчивостью. В то же время кристаллические силикаты существенно превосходят кисдотоустойчивые высококремнеземистые цеолиты (морденит, клиноптилолит) по адсорбционной емкости. Кроме того, кристаллические пористые силикаты щелочных металлов по сравнению с цеолитами обладают способностью проявлять высокую адсорбционную способность уже после вакуумирования при комнатной температуре (см. табл.3).Отличительным свойством некоторых силикатов является изменение параметров пористой и кристаллической структуры в процессе адсорбции молекул с большим средством к поверхности, что характерно для глинистых слоистых минералов (монтмориллонита, вермикулита) с расширяющейся решеткой .
Высокая адсорбционная способность и избирательность, кислотоустойчивость и возможность низкотемпературной регенерации кристаллических пористых силикатов щелочных металлов обуславливают возможность их использования в качестве адсорбентов в процессах очистки, осушки и разделения газов паров и жидкостей, для работы в агрессивных средах, в адсорбционных системах защиты окружающей среды от загрязнений, а также в системах с лимитированными энергозатрата на регенерацию. Кристаллические мик;пористые силикаты щелочных металлов могут быть использованы также как ионообменники и носители катализаторов, способность к химическому модифицированию и кислотоустойчивос открывают возможность создания на их основе новых пористых кристаллических материалов с практически полезными свойствами. Кроме того, кристаллические пористые силикаты щелочных металлов представляют научный интерес как объекты исследбваняя в области физической химии KpeMHesef ма/ силикатов цеолитов,мийералообраэовёния (в частности, квар1 Жообразования), изучения структуда, хи мической природы поверхности дисперс ных твердых.тел и механизма сорбционных процессов.
Таблица Исходя из подобия физико-химических условий и аналогии систем, в Которых кристаллизуются цеолиты и силикаты, учитывая сходство их адсорбционных и молекулярно-ситовых свойств, предлагаемь1е кристаллические пористые силикаты щелочных металлов, обладакхцие молекулярно-ситовыми свойствами, названы сиолитами (Si - кремний, О - кислород, литое - камень).







| название | год | авторы | номер документа |
|---|---|---|---|
| Моющее средство для стирки | 1984 |
|
SU1225851A1 |
| Способ получения концентрированногоКРЕМНЕзОля | 1979 |
|
SU833496A1 |
| Способ получения силиката,обладающего кристаллической пористой цеолитной структурой | 1981 |
|
SU1092141A1 |
| Способ получения цеолита типа фожазит | 1980 |
|
SU975573A1 |
| Способ получения кристаллического цеолита | 1969 |
|
SU298160A1 |
| Способ получения сверхвысококремнеземного алкиламмониевого цеолита | 1982 |
|
SU1060568A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦЕОЛИТА ТИПА ПРИРОДНОГОФОЖАЗИТА | 1967 |
|
SU201337A1 |
| СПОСОБ ИЗОЛЯЦИИ ВОДОПРОНИЦАЕМОГО ПЛАСТА | 2004 |
|
RU2271444C1 |
| Способ получения эрионита | 1979 |
|
SU833499A1 |
| Способ получения фосфорсодержащего цеолита типа фожазита | 1983 |
|
SU1130527A1 |

2-15 I,ijO-2-45S10. 50-9 5%0 15-50 I.ijO-2-35Si( 50-95Hj 2-5 Na O-10-60Si02-40-95H,0 5-12 NSjO-2-45810 : 30-8ОН О 17-22Kj O-25-458102- 40-65Hj,O 12-77K.O-20-50Si02- 40-70H,,O 2-12 KjO.2-60SiO2 40-95HjO 7-30 KjO- 2-40SiQ -40-95HjO 5-25 . 2-60SiO.- 40-95HjO 25-30 Rhj O-2-403102 - 40-95Н 0,5-0,3 NaiO-0,3-9, 30-40SiQ 50-65H O l,6LJ.,4Na. 30SiO,- 65Н. 3, 2L1.0 -6 , 4OSiO, 5OH,O 1,2-2,4Ll20 -3,8-7, 6IL 030-408102. -50-65H,tP 2-4Na O- 3-6K -30-40SiO,.5(Ь65Н2.0 0,8-1,,7-3, 4Naj.O-30-40SiOa-50-65HiO-2,5-5, 1,9020 Ll,j, 0-2-4SlOa. 1,5-2H,50 2,0015 Lij O-1-2810 J.-0, 5-2Hj O 2.0310 Na O-10-2 0810 3,-10-2 OH.0 1,705 Na O-e-lOSiOj,- 10-20HjO 2,798 K,jO-12-158i0.j,- 3-4HjO 2,608 K,j,0-20,4SiOjL 7, 2,058 . 29-37810. 3-16H2.O 2,2060 6-8Si02.-4-4,5H.O 2,1525 Hb,j,0-20-558iOi-6-15Hj O 2,6012 3-4SiOt- 1-1, 0,l-0,7Na,0- 0,3-0,9CSj;02.0410-15 -12-20SiO,8-13Ii O 2.0517 0,3LljO-0,,6SiOj- 6, 4Н,0 1,857 0, 5LiiO 0, 5Na jO 4 , ,8Н. 2,039 0,5Li2.0.0,5K 0-14-16S10,j; ,7-8,6Hj,0 2,0110 0,7-0, 8Na,O -0, 2-0, .l4-188iOi. 9-10H40 2,01-10-20 0,1-0,,3-0,9Na20.7-208iOa.-5-lOKiO. 0,1-2,09 -0,4Ka.O
а s R o
(Q EH Формула изобретения 1.Кристаллические- микропористые силикаты щелочных металлов с овщей формулой MejOj nSiOeinH O, где Me Li, Na, К, Rb/,Cs, n - SlOj/M f 1-40, M - 2 « 1-20, обладающие . молекулярно-ситовьши свойствами, в качестве сорбентов. 2.Способ получения кристалличес ких MHKponoi HCTHx силикатов щелочных металлов по п.1, о т л и чаю щ и и с я тем, что аМорфный кремне эем Jпoдвeprгd6т взаимодействию с вод ным pacTBbpoM щелочи при соотношении компонентов,. моль:Ме2О:°810 sHjP 1 г(0,1-32,0)S(2т95), температуре 90-200 0 в течение 0,5-30 сут с по1следующей отмывкЬй ot избытка щелочи до рН 7-8,5 и сушкой при комнатной темНератУре 3, Способ по п.2, о т л и ч а ющ и и с и ,тём, что, с целью ускореиия процесса, взаимодействие ведут в присутствии затравок изоструктурных с синтезируемыми .кристаллическимй силикатами. Источники информации, принятые во Внимание при экспертизе 1.Baker C.L., Jue S.H., WieEs Т.Н. S.Aroer Chem Soc.i 72,5369, 1950. 2.L.Me.Cut6och, S.Amer. Chem. Soc. 74,10, 2453, 1952. . .3. Her RiK., S.Cot€oid Seience. 19, 648, 1964. 4. Патент США 3492137, кл. 106-74, 1970.
Авторы
Даты
1982-07-15—Публикация
1979-09-27—Подача