Изобретение относится к способам получения о-металлилоксифенола, кото рый находит применение в синтезе используемого в качестве инсектицида метилкарбамата 2,3-дигидро-2,2-диметил-7-бензофуранила. Известен способ получения о-метал лилоксифенола, заключающийся во взаи модействии пирокатехина с металлилхлоридом в амидном растворителе (диметилформамид, диметилацетамид, диме тилсульфоксид) при 100-120°С в прису ствии основного агента - окиси,или гидроокиси щелочноземельного металла 13. Недостатком данного способа является ограниченность его осуществлени в промышленном масштабе, поскольку он предусматривает сугубо конкретные растворители, которые или токсичны или дорогостоящи, или взрывоопасны (диметилсульфоксид) в присутствии металлилхлорида. Наиболее близким к предлагаемому является способ получения о-металлил оксифенола, ;заключающийся во взаимодействии пирокатехина с металлилхлоридом при перемешивании и темпера туре 70-75С в двухфазной системе: вода - бензол в присутствии едкого натра . Недостаток известного способа состоит в том, что имеет место протекание побочной реакции - алкилирование цикла, а также образование диэфиров, что снижает выход целевого продукта и приводит к смеси трудно разделяемых продуктов. Цель изобретения - повышение избирательности процесса. Поставленная цель достигается тем, что о-металлилоксифенол формулы -ОСНг-С а1г / получают путем взаимодействия при. перемешивании пирокатехина с металлилхлоридом в двухфазной системе: вода не смешивающийся с водой органический растворительJ выбранный из группы: низшие алифатические насыщенные монокетоны, низшие алифатические насыщенные мононитрилы, галоидуглеводороды, насыщенные алифатические углеводороды, насыщенные одноатомные алифатические спирты, насьпценные простые эфиры г1лифатического или аромати ческого ряда, в присутствии основног агента и катализатора производного четвертичного аммония общей формулы где R - алкил , оксиэтил; Rii - алкил оксиэтил; RgH R . имеют одинаковые или разли ные значения и каждый пред ставляет алкил галоген, кроме иода, радикалы S04 , S04H ; п - целое число, равное валент ности X, при температуре 70-130 С. Отличительной особенностью предл гаемого способа является использова Iние в качестве не смешивающегося с водой органического растворителя, вы ранного из группы: низшие алифатичеркие ненасыщенные монокетоны,низшие алифатические насыщенные мононитрилы, галоидуглеводороды, насыщенные алифатические Сд углеводороды, насыщенные одноатомные алифатические спирты, насыщеные простые эфнры алифатического или ар матического ряда, проведение процес са в присутствии катализатора - прои водного четвертичного аммония общей формулы R, - - Кг-V э где R - сшкил , оксиэтил; RQ - алкил CiJ-C, ОКСИЭТИЛ} RJ и имеют одинаковые или различ ные значения и каждый представляет собой алкил С 2 С, X .- галоген, кроме иода, радикалы SQ , 564 Н ; п - целое число, равное валентности X, при температуре 70-130 С. Предпочтительно процесс вести, и пользуя 0,6-2 моль металлилхлорида и 0,5-1,4 моль основного агента на 1 моль пирокатехина и 0,01-1 моль к тализатора на 1 моль основного аген та, в качестве которого используют едкий натр или карбонат натрия. Согласно предлагаемому способу процесс можно вести в металлилхлори де , тогда последний выполняет и рол растворителя. В качестве вспомогательного инер ного растворителя лучше использоват анизол. В реакционной среде соотношение между водой и органическими растворителями может изменяться в широких пределах. Однако наилучшие результаты получают при использовании реакционной среды, содержащей 1-4 об.ч, органического растворителя на 1 ч. воды. В реакционную среду основной агент , может быть добавлен за один прием в начале реакции, или его добавляют постепенно в течение всего процесса, что позволяет лучше контролировать протекание реакции, продолжительность которой составляет 2-6 ч. В качестве катализатора - производных четвертичного основания могут быть использованы наряду с индивидуальными соединениями, также и смесь метилтриалкиламмонййхлоридов, в которых алкил содержит 8-10 атомов углерода (А/дожен 464) или смесь хлоридов диоксиэтилдиалкиламмония, в которой алкил содержит 16-18 атомов углерода (Кемюлькат К012). Предложенный способ позволяет избирательно получить моноэфир,сводя к минимуму образование диэфиров и продуктов алкилирования бензольного кольца пирокатехина. Молярное отношение моноэфир / диэфир составляет 16:103, степень превращения пирокатехина - 43-89%, выход целе,вого продукта на превращенный пирокатехин - 66-82%, на исходный 33-56%. Пример 1,Используемый аппарат содержит трехгорлую колбу на 250 мл, снабженную вертикальным холодильником, перемешивателем, термометром, подводом и выводом аргона. После продувки аппарата аргоном в него загружают 12,1 г пирокатехина ( моль), 70 мл анизола, 13,5 г металлилхлорида (0,15 моль),5,68 г бисульфата тетрабутиламмония (0,016 моль), 0,7 г окиси натрия (0,017 моль). Смесь нагревают до 100°С при перемешивании в атмосфере аргона.Затем в течение 2 ч добавляют 4 г окиси натрия в растворе 20 мл воды. По. окончании вливания трубку, по которой поступает названный раствор,промывают 5 мл дистиллированной воды. Смесь выдерживают еще 2 ч при кипячении, после чего перемешивают и охлаждают до температуры окружающей среды. Паровую фазу хроматографируют и определяют, что в органической фазе содержится 3,7 г непревращенного металлилхлорида. К жидкой реакционной смеси прибавляют 70 мл дистиллированной воды и получают два слоя.Водную фазу пятикратно экстрагируют 60 мл этилацетата. Органические фазы объединяют . Путем хроматографии водной фазы определяют наличие 2,0 г непревращенного пирокатехина и 0,70 г о-диметиллилоксибензола. .Путем жидкостной хроматографии находят, что в органической фазе содержится 12,3 го-ме- .таллилоксифенола 0,075 моль),1,2 г п-металлилпирокатехина, 0,13 г о-металлилпи1эокатехина.
На основании этих данных конверсия пирокатехина составляет 84%.
Выход по отношению к превращенному пирокатехину, %: о-металлилоксифенол 82J о-диметаллилоксибензол 3,6- п-металлилпирокатехин 3 о-металлилпирокатехин 0,8. Молярное отношение моноэфир/диэфир равно 22, выход моноэфира по отношению к исходному пирокатехину составляет 69%.
Пример 2.В описанный аппарат загружают 35 мл анизола, 8,25 г пирокатехина (0,075 моль), 10 г металлилхлорида (0,11 моль),2,85 г трибутилэтиламмонийхлорида (0,011 моль).
Смесь нагревают до при перемешивании в атмосфере аргона. Затем в течение 2 ч 25 мин вводят раствор едкого натра, содержащего 2 г NaOH (0,95 моль) в 5,5 мл дистиллированной воды. По окончании введения этого расвора смесь выдерживают при указанных условиях в течение 1 ч 15 мин. По истечении этого времени водная фаза имеет нейтральную реакцию. Прекращают перемешивание и нагревание и оставляю смесь остыбать в атмосфере аргона.Выпавший в осадок хлорид натрия отфильтровывают и трехкратно промывают 15 мл анизола. Фильтраты объединяют и декан тируют. К водной фазе прибавляют
115 мл дистиллированной воды и отфильтрованный хлорид натрия. В этом растворе определяют 0,048 йон-г С1 и |1,8 Ю- ион-г (C2.H5)(C4H9bN В органической фазе, которая составляет 83 мл, определяют 0,010 ион-г tfe и 0,010 ион-г () (С4Н9)з .
Содержащийся в органической фазе хлорид трибутилметиламмония может быть удален промывкой водой. Для этого берут 10 МП органической фазы, которую промлвают один раз в таком же объеме дистиллированной воды.После декантирования определяют в органической фазе, г: о-металлилоксифенол 6,8; о-диметаллилоксибензол 0,052 о-металлилпирокатехин 0,16; п-металлилоксипирокатехин l,07f пирокатехин 2,43} 0,34-10 ион-г СЕ
В водной фазе определяют 0,11 г пирокатехина и 0,88-Ю ион-г 0,11
В результате превращение пирокатехина составляет 69%. Выход по отношению к превращенному пирокатехину,%: о-металлилоксифенол 77; о-диметаллилоксибензол 0,4 о-металлилпирокатехин 2, т.е. мольное отношение моноэф,ир/диэфир равно 192. Выход моноэфира по отношению к исходному пирокатехину составляет 53%.
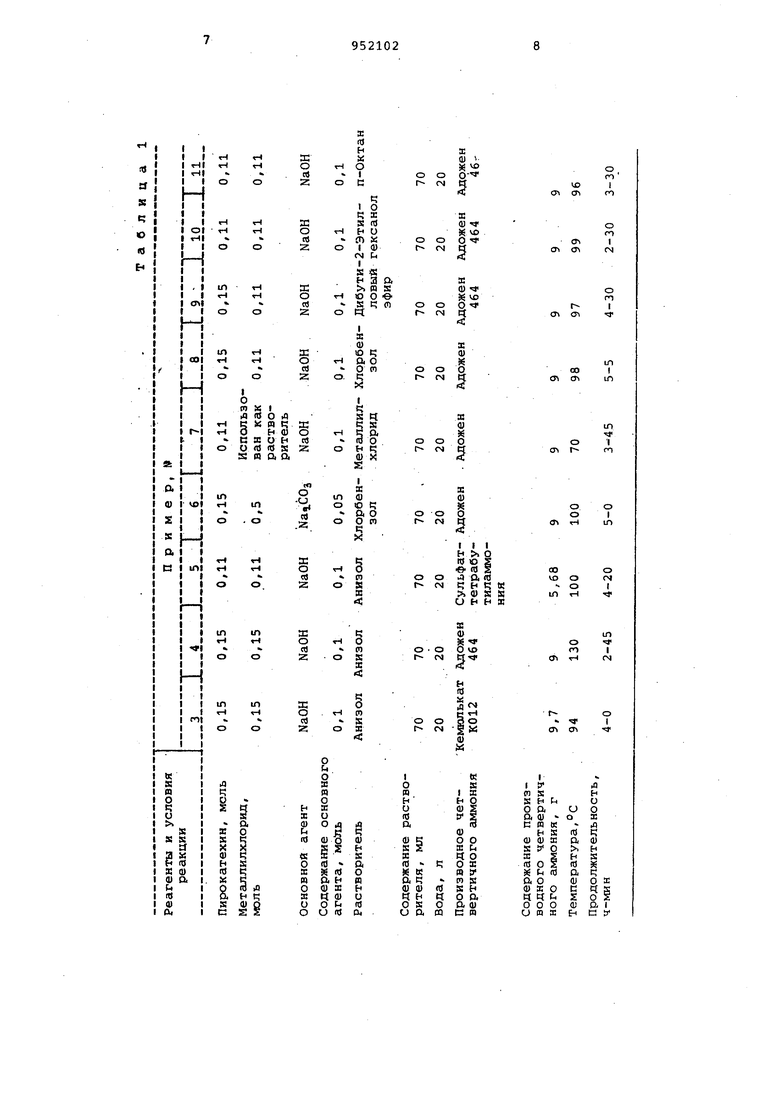
Примеры 3-16 . Эти примеры осуществляют аналогично примеру 1. Однако в примере 4 реакцию ведут в автоклаве под давлением. Условия процессов и полученные результаты приIведены в табл. 1, 2 и 3.
952102
10
Таблица 2


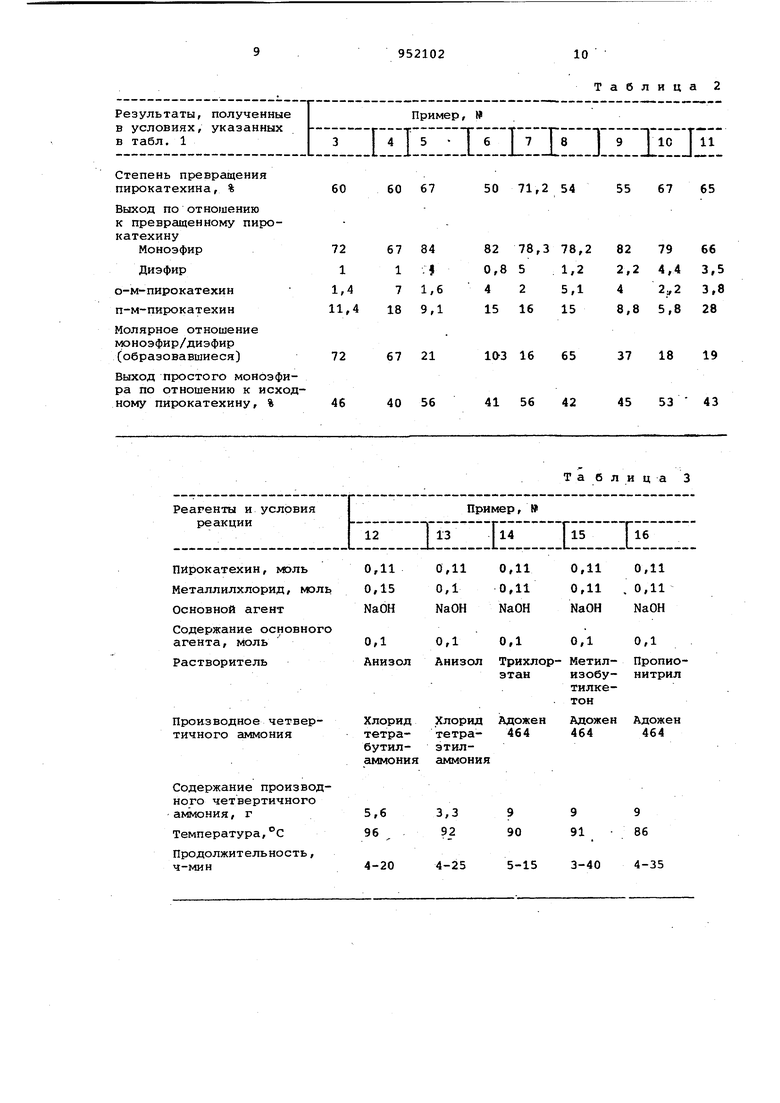


Продолжительность, ч-мин
4-25
5-15
3-40
4-35
20
Результаты,полученные в условиях, указанных в табл. 3
Степень превращения пирокатехина, %
Выход по отношению к превращенному пирокатехину, %
Простой моноэфир
Диэфир
ВЫХОД простого моноэфира по отношению к исходному пирокатехину, % Формула изобретения Способ получения о-металлилоксифенола формулы ОН СК, V-OCH -CeQli t. взаимодействием пирокатехина с металлилхлоридом пои пеоемешивании в двухфазной системе: вода - не смешивающийся с водой органический растворитель в присутствии основного агента при нагревании, отличаю щийся тем, что, с целью повышения избирательности процесса, в качестве не смешивающегося с водой растворителя используют низшие алифа гические насыщенные монокетоны, низшие алифатические насыщеннее моно нитрилы, галоидуглеводородц, насыщен ные алифатические углеводороды насыщенные одноатомные алифатические
Таблица 4
Пример,
.
89,6 43 7370
65 77 7780
21 1 910
58,2 33 5656 спирты, насыщеные. простые эфиры алифатического или ароматического ряда, п процесс ведут в присутствии катализатора-производного четвертичного аммония общей формулы г- К, где R - алкил Сх,-С4, оксиэтил; RI - алкил С, оксизтил; RзИ R4 имеют одинаковые или различ-, ные зна;чения и каждый представляет алкил X - галоген, кроме иода, радикалып - целое число, равное валентности X, при температуре 7о-1за с. Источники информации, принятые во внимание при экспертизе 1. Патент США 3927118, кл. 260-613, опублик. 1975 (прототип)
Авторы
Даты
1982-08-15—Публикация
1979-06-25—Подача