(54) СПОСОБ ПОЛУЧЕНИЯ ВЫСШИХ. ПЕРВИЧНЫХ
Изобретение относится к способу получения.высцшх первичных алкилмеркаптанов с 8-18 атомами углерода, : которые находят применение в качестве регуляторов молекулярного веса в производстве полимеров, в производстве пестицидов, флотоагентов и поверхностно-активных веществ.
Известен способ получения высших первичных алкилмеркаптанов, например, взаимодействием соответствующих алкилгалогенидов с гидросульфидом натрия водном диметилформамиде при нагревании. Выход целевого продукта 90-97% 1.
Недостатком способа является не- пользование диметилформамида, гидролизующегося в условиях синтеза и плохо регенерирующегося из водных растворов.
Известен способ получения высших первичных алкилмеркаптанов взаимодействием раствора соответствующих алкилгалогенидов в н-бутаноле в присутствии с кристаллическим гидро- . сульфидом натрия с перемешиванием при 70-110°С и насыщении реакционной смеси сероводородом, при содержании воды в реакционной смеси 2,02 моль и выше в расчете на моль гидросульфида натрия с последующим добавлеАЛКИЛМЕРКАПТАНОВ
.нием воды, отделением органической фазы и отгонкой из нее бутанола и целевого продукта с выходом 8088% ,11родолжительность процесса 8 ч Г2,
к недостаткам данного способа относится образование до 13% побочно образующихся сульфидов и длительность процесса, невысокая производи10тельность процесса.
Наиболее близким к предлагаемому является способ получения высших первичных алкилмеркаптанов с 8-18 атомами углерода заключающийся во взаимодействии алкилхлорида с насы15щенным сероводородом водным раствором гидросульфида натрия, из которого предварительно отгоняют воду в виде азеотропной смеси с н-бутано лом до остаточного содержания воды
20 1-2 моль на моль гидросульфида натрия,при 70-110с, атмосферном давлении и молярном соотношении алкйлхлорид: н-бутанол: гидросульфид натрия, равном 1:3;1,1:1,3, и переме25шивании в течение 4-5 ч с последующей обработкой реакционной смеси водным слоем из азеотропной смеси для растворения неорганических солей. Водную фазу, полученную после
30 .отделения органической фазы от про-.
дуктов синтеза, обрабатывают минеральной кислотой с одновременной отгонкой сероводорода и водно-бутанольной смеси и рециркуляцией последних в процесс }ia стадии насьш1ения и обработки реакционной смеси водой соответственно. Максимальный ВЕЛХОД целевого продукта 94%, конверсия хлоралкана до 98,9% 3. .
К недостаткам данного способа относятся неполная конверсия и выход целевого продукта, необходимость . ограничения содержания воды в реакционной смеси для обеспечения приемЬемой глубины конверсии алкилхлорида и скилсения продолжительности синтеза, наличие твердого осадка гидросульфида натрия в исходной реакционной смеси и образование твердого осадка хлористого натрия и не вступившего в реакцию гидросульфида натрия в продуктах реакции, увеличение цикла работ за счет времени,необходш- ого для отгонки водного азеотропа, необходимость дозирования воды для растворения солей в продуктах синтеза - что все в целом снижает эффективность процесса.
Целью изобретения является повышение эффективности процесса.
Поставленная цель достигается тем, что получение высших первичных алкилмерка-птанов с 8-18 атомами угЛерода заключается во взаимодействии алкилхлоридов с водным раствором гидросульфида натрия в среде н-бутанола при насыщении реакционной смеси сероводородом в замкнутой системе, при 110-130°С, при молярном соотношении алкилхлорид: н -бутанол, равном 1:8-12,,с последующим отделением органической фазы, отгонкой бутанола и выделением целевого продукта.
Выход 97,2-98,9%, конверсия хлоралканов 99,3-100%.
Гидросульфид натрия применяют в виде 22-27% водного раствора. J Указанная -цель достигается только при одновременном повышении температуры, давления и увеличении соотношения бутанол-хлоралкан. Изменение одного или двух из этих трех параметров относительно условий, приведенных в прототипе, не дает положительного эффекта.
С повышением давления В системе изменяются все основные закономерности процесса, вследствие повышения растворимости сероводорода в реакционной смеси и повышения растворимости гидросульфида натрия в органической фазе. В случае синтеза 1-додекантиола 100%-ная конверсия хлор.додекана достигается при 110-115°С при молярном отношении бутанол: хлордодекан, равном 10:1, и давлении, создающемся при нагревании
. реакционной смеси, насыщенной сероводородом при комнатной температуре (4,0 ати при 110°С, 4,5 ати при 115°СК При этом выход 1-додекантиола достигает 98-99%. Протекание реакции мало зависит от интенсивности перемешивания. Продолжительность реакции снижается до 2-3 ч, а при 130°С до 1,0-1,5 ч.
В указанных условиях может быть 0 использован прог1ышленный водный раствор гидросульфида натрия без предварительной отгонки воды, т.е. исключается необходимость в дозировании твердого кристаллогидрата 5 гидросульфида натрия или необходимость в азеотропной осушке реакционной смеси.
Применение водного раствора гидросульфида натрия концентрации не более 23% при молярном отношении реагентов RCB: бутанол 1:1,4:10 позволяет получать продукты реакции, не содержащие твердого осадка NaCe и не вступившего в реакцию NaSH. Опытным путем найдена максимально допустимая Jкoнцeнтpaцйя солей в нижнем водно-солевом слое . продуктов реакции 28% (для молярного отношения NaC -:Na5 l:04j. Учитывая поступление воды в реакционную 0 смесь с возвратным бутанолом, промышленный гидросульфид натрия, который производится: с концентрацией NaSH 22-27%, может применяться без предварительного разбавления. Из 5 цикла работы реактора исключаются две операции: дозирование воды или нижнего слоя гетероазеотропаи операция перемешивания для обеспечения растворения осадка солей. 0 Отсутствие твердых осадков в исходной реакционной смеси и в продуктах реакции позволяет оформить реакционный узел по непрерывному способу .
с Продукты реакции разделяют на два слоя: на органический и водносолевой. Причем оба слоя неОкрашены, граница раздела четкая, вспенивание по границе раздела фаз полностью отсутствует Последнее объясняется 50 подавлением побочных процессов за счет повышения растворимости сероводорода в реакционной смеси.
Из органического слоя в условиях вакуумной ректификации отгоняют бу55 танол и используют его повторно. Из остатка прямой перегонкой выделяют 1-додекантиол.
Гарантированное достижение полной конверсии хлоралкана позволяет отка0 эаться от технологически сложной системы .регенерации не вступившего в реакцию хлордодекана.
При отсутствии рецикла хлордодекана, связанного с длительным нагре 5 ванием 1-додекантиола, и при ограничении температуры нагрева 1-додекантиола при его выделении (не выие ) чистота получаемого 1-додекан тиола зависит только от наличия примесей в исходном.хлордодекане. Обычная примесь в хлордодекане и, следовательно, в 1-додекантиоле - 1-додеканол. Основная масса сероводорода, требуемого для насыщения реакционной смеси в разработанном процессе, находится в замкнутом цикле. Сероводород, необходимый для превращения примеси сульфида натрия в гидросульфид натрия и для восполнения потерь при рециркуляции сероводорода, получают обработкой соляной кис лотой водно-солевого слоя, содержащего .непрореагировавший гидросульфид натрия. Одновременно с отпаркой сероводорода из водно-солевого слоя в котором содержится до 1% бутэнола происходит отгонка .водно-бутанольно смеси и возврат ее в процесс, что обеспечивает полную регенерацию бутанола. Проводят лабораторныйсинтез 1-д декантиола в оптимальных условиях, позволяющих достигать максимальный выход целевого продукта, а также балансовый состав двухслойной систе Мы.продуктов реакции, В условиях синтеза 1-додекантиола могут быть синтезированы с высоким выходом и практически 100%-ной конверсией алкантиолы, содержащие 8-18 атомов углерода в углеводородной цепи, Пример, В ампулу из нержавеющей стали объемом 510 мл с рубашкой для термостатированного обогрева, термопарой и манометром помещают 67,262 г предварительно на сыщенного сероводородом водного раствора гидросульфида натрия, содержаще170 23,34% NaSH (15,699 г; 0,28 г-моль NaSH, Сюда же добавляю 40,956 г 10,2 г-моль) 100%-ного 1хлордодекана и 148,424 г (2,0Ог-мол н-бутанола, содержащего 0,12% воды. Молярное отношение хлордодекан; NaSH: бутанол равно 1,0:1,4:10, Реакционную смесь насыщают газообразным сероводородом, ампулу гермети-. зируют, устанавливают на встряхиваю щую машину, обеспечивающую 150 качаний в .минуту с амплитудой 35 мм, включают перемешивание и в течение .10 мин нагревают до , перемеши вание продолжают в течение 3 часов,, в результате нагревания реакционной смеси давление в ампуле поднимается до 4,5 ати, По окончании реакции ампулу быст ро охлаждают до комнатной температуры. Продукты реакции переносят в делительную воронку и разделяют на два слоя: органическийи водно-солевой. Оба слоя анализируют на содержание Хг-хлордодекана, 1-додекантиола, NaCt и NaSH потенциометрическими методами. Содержание воды в органическом слое и бутанола в водно-солевом слое определяют хроматографическим методом в соответствующих дистиллатах разгонок. Содержание дидодецилсульфида определяют по результатам анализа меркаптанной и сульфидной серы в кубовых продуктах после рек-Гификации органического слоя. Ампулу промывают 25 мл воды, промывание воды анализируют на содержание NaCE и NaSH, Полученные значения, 0,126 и 0,014 г, соответственно относят К водно-солевому слою. Состав отдельных слоев приведен в таблице. Содержание сероводорода, приведенное таблице, рассчитано по значениям его растворимости в воде, бутаноле и 1-додекантиоле при комнатной температуре. Целевой 1-додекантиол концентрации 99,7% выделяют ректификацией органического слоя. Выход 1-додекантиола 98,9%, конверсия 1-хлордодекана 100%,. Пример 2. В условиях примера 1 при 130°t: и продолжительности реакции 1,5 ч из 1-хлордодекана получен 1-додекантиол с выходом 97,2%, Конверсия 1-хлордодекана 100%, Пример 3, В условиях примера 1 из 1-хлороктана получают 1-октантиолс ,выходом 99,1%, Конверсия 1-хлороктана 100%, Выделенный ректификацией продукт имеет чистоту 99,8% (хроматографически;, содержание меркаптанной серы 21,88%, hi 1,4538, молекулярную массу 145,9 Чкриоскопически в бензоле, Пример 4, в условиях примера 1 при и продолжительности реакции 4 часа из 1-хлороктадекана получают 1-октадекантиол с выходом 97,6%, Конверсия 1-хлс1роктадекана 99,3%, Продукт после у даления растворителя содержал 10,97% меркаптанной серы расчетная чистота продукта 98,0%J, 1,4637, молекулярную массу 284,2 (криоскопически в бензоле/. Пример 5, В условиях примера 1 из смеси первичных хлоралканов с 10-14 атомами углерода в алкйльных радикалах, содержащей 16,82% связанного хлора, 2,6% высших алкаНОЛОВ со средней молекулярной массой 204,2, получают смесь соответствующих первичных алкантиолов со средним содержанием меркаптанной серы 15,14% молекулярной массой 200,9, Выход тиолов, рассчитанный по содержанию органического хлора в исходных хлоралканах и содержанию меркаптанной серы в продуктах реакции, - 97.7%. Конверсия хлоралканов 99,7.
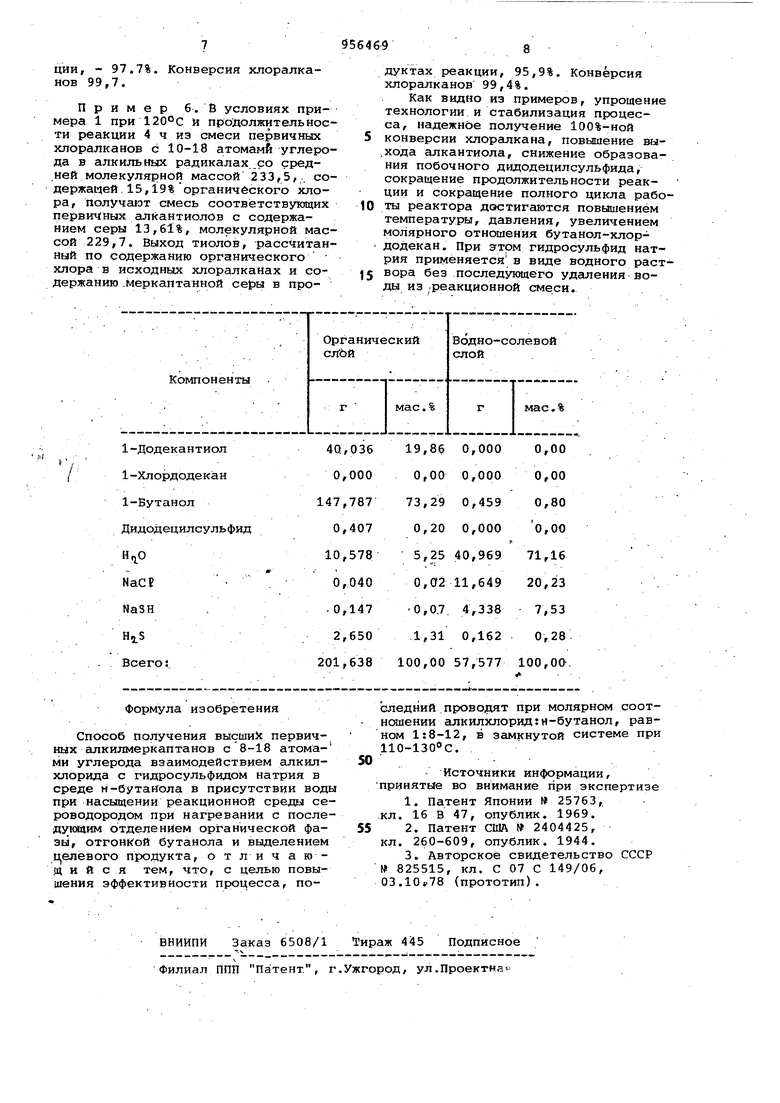
Пример б. В условиях примера 1 при 120°С и продолжительности реакции 4 ч из смеси первичных хлоралканов с 10-18 атомами углерода в алкильных радикалах со срюдней молекулярной массой 233/5,. содержащей 15,19%органического хлора, получают смесь соответствующих первичных алКантиолОв с содержанием серы 13,61%, молекулярной массой 229,7. Выход тиолов, рассчитанный по содержанию органического хлора в исходных хлоралканах и содержанию .меркаптанной серы в продуктах реакции, 95,9%. Конверсия хлоралканов 99,4%.
Как видно из примеров, упрощение технологии и стабилизация процесса, надежное получение 100%-ной конверсии хлоралкана, повышение вы.хода алкантиола, снижение образования побочного дидодецилсульфида, сокращение продолжительности реакции и сокращение полного цикла работы реактора достигаются повышением температуры, давления, увеличением молярного отношения бутанол-хлордодекан. При зтрм гидросульфид натрия применяется в виде водного раствора без последующего удгшения воды из .реакционной смеси.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения алкилмеркаптанов | 1974 |
|
SU537998A1 |
| Способ получения алкилмеркаптанов | 2023 |
|
RU2817954C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОХЛОРАЛКАНОВ | 1992 |
|
RU2009117C1 |
| СПОСОБ ОДНОВРЕМЕННОГО ПОЛУЧЕНИЯ ХЛОРОФОРМА И ТРЕТИЧНЫХ ХЛОРАЛКАНОВ | 2006 |
|
RU2322433C1 |
| СПОСОБ ПОЛУЧЕНИЯ МЕТАНСУЛЬФОКИСЛОТЫ | 2016 |
|
RU2648245C2 |
| Способ конверсии угля, торфа или древесины в газообразные углеводороды или летучие дистилляты, или их смеси | 1981 |
|
SU1642955A3 |
| Способ получения высших третичных алкилмеркаптанов | 1974 |
|
SU518489A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛМЕРКАПТАНОВ В МНОГОЗОННОМ РЕАКТОРЕ С НЕПОДВИЖНЫМ СЛОЕМ | 2007 |
|
RU2443686C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛМЕРКАПТАНОВ | 2015 |
|
RU2712218C2 |
| СПОСОБ ПОЛУЧЕНИЯ 5-АЦИЛ-ПЕРГИДРО-1,3,5-ДИТИАЗИНОВ | 2005 |
|
RU2291150C1 |


Авторы
Даты
1982-09-07—Публикация
1981-03-06—Подача