(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ КОМПОНЕНТОВ НИФУЛИНА



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения производных фенотиазина | 1977 |
|
SU726471A1 |
| Способ определения гетероциклических азотсодержащих оснований | 1983 |
|
SU1122947A1 |
| Способ определения фурацилина | 1983 |
|
SU1109609A1 |
| Способ количественного определения 4,6-динитроортокрезола и 2-ацетамино- 5- нитротиазола | 1985 |
|
SU1293588A1 |
| Способ определения аминотиазолов | 1982 |
|
SU1051411A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ПРОИЗВОДНЫХ АЛКИЛАРИЛСУЛЬФОНОВ | 2022 |
|
RU2800907C1 |
| Способ количественного определения лекарственных средств | 2023 |
|
RU2832907C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦИКДОМЕТИАЗИДА | 1994 |
|
RU2090866C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ГИДАНТОИНА, 1-АМИНОГИДАНТОИНА, ФУРАДОНИНА, ФУРАГИНА | 1991 |
|
RU2009483C1 |
| Способ количественного определения кватерона | 1988 |
|
SU1550385A1 |


Изобретение относится к аналитической химии, в частности к способам определения компонентов нифулина, и может быть использовано в химико-фармацевтической промышленности для контроля качества нифулина - препарата, применяемого в ветеринарии как лечебно-профилактическое средство.
Известен способ количественного определения активных компонентов нифулина (нитазола, фуразолидона, хлортетрациклина индивидуального или из биоветина) каждого в отдельности, а именно: нитазол, фуразолидон и хлортётракциклин определяют спектрофотометрически, выделяя только один из них в анализируемой пробе, путем обработки пробы растворителем, снятия электронных спектров и расчета количества компонента. Фуразолидон или биоветин (смесь хлортетрациклина, его кальциевой соли и инертных наполнителей) анализируют, кроме того, фотометрически путем растворения -анализируемой пробы в органическом или неорганическом растворителе, измерения оптической плотности каждого полученного раствора и расчета количества компонента при помощи калибровочного графика 1.
Недостатком известных способов являются поочередный анализ каждого компонента из-за невозможности избирательного определения нитазола, фуразолидона, хлортетрациклина индивидуального или из биоветина в препарате нифулин за счет близкого расположения полос поглощения каждого компонента на спектрах, кроме того,
10 один из компонентов - кальциевая соль хлортетрациклина в биоветине не растворима в органических растворителях, а другие не растворимы в воде, т. е. невозможно подобрать общий растворитель и получить однородный раствор, следовательно один из компонентов или его часть остаются вне сферы определения, что. снижает точность определения компонентов нифулина (ошибка ± 20-50%).
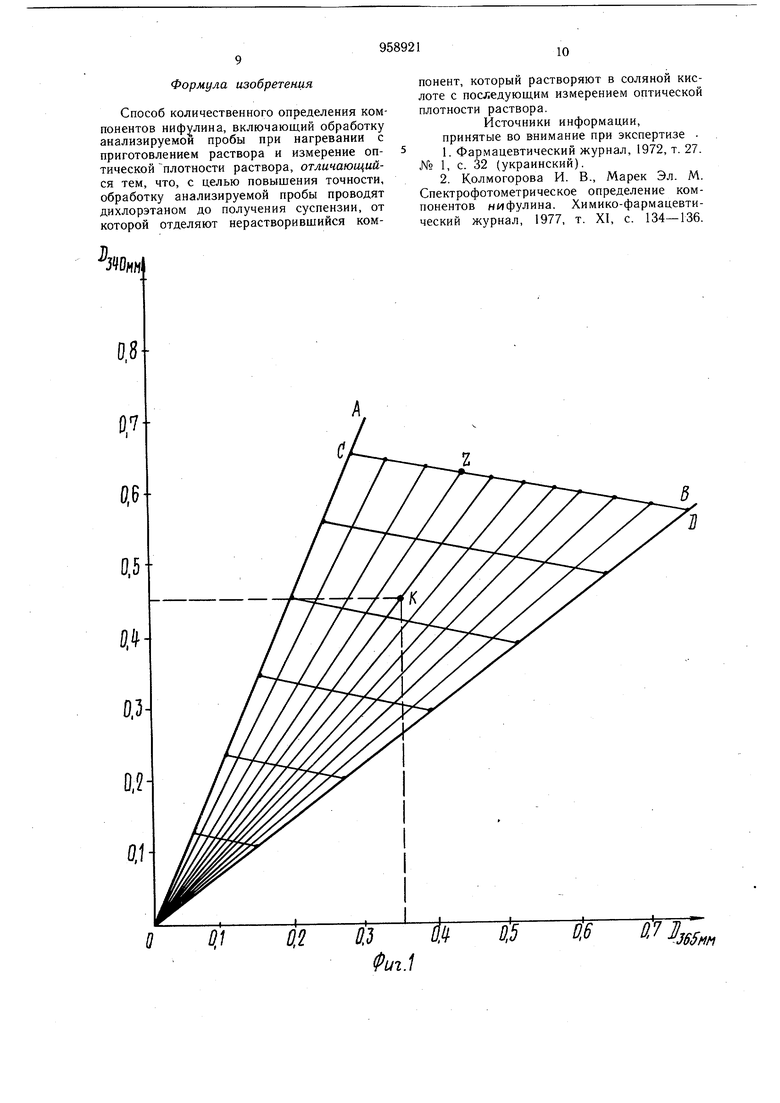
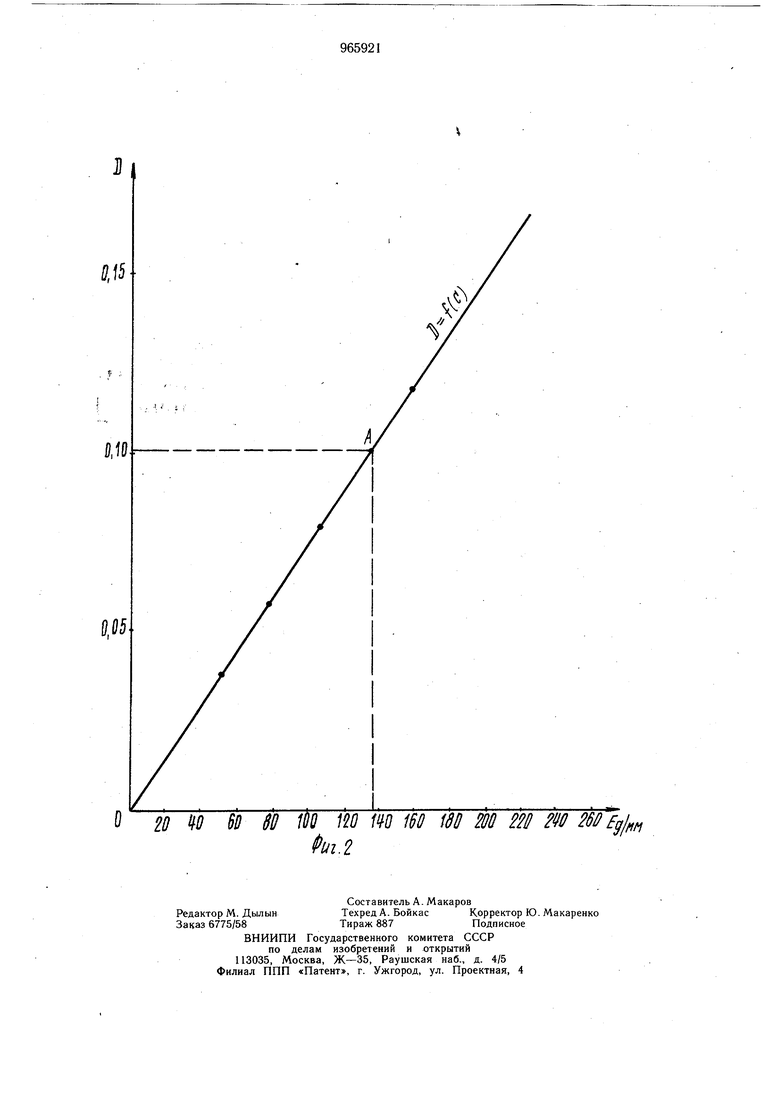
Наиболее близким к изобретению являет20 ся способ количественного определения компонентов нифулина (нитазола, фуразолидона и хлортетрациклина индивидуального), включающий обработку анализируемой пробы (точная навеска 0,025 г) при нагреваНИИ (80-85°С), измерение оптической плотности раствора D (при длинах волн Х 345, 357, 370, 384 им) и расчет количества компонентов, причем обработку анализируемой пробы проводят этанолом с получением раствора всех компонентов, а расчет количества каждого компонента осуществляют с использованием номограммы для трехкомпонентной системы (номограмму строят предварительно на основе экспериментальной обработки ряда стандартных растворов каждого компонента и расчета величин Д D Dj45 -DSTO и Д D Dj5 ледующим нахождением по номограмме точки, соответствующей составу пробы 2. Известный способ количественного определения компонентов нифулина является несоверщенным, так как он не применим для анализа нифулина, содержащего в качестве одного из компонентов широко используемый в промышленности биоветин - полупродукт производства хлортетрациклина (смесь хлортетрациклина, его кальциевой соли и инертных наполнителей) ввиду того, что составляющая биоветина - кальциевая соль хлортетрациклина не растворима в этаноле, поэтому количество хлортетрациклина, связанное в кальциевой соли, не поддается определению и, следовательно, точность определения. всех компонентов по номограмме не достаточна (ошибка ± 50%). Целью изобретения является повышение точности определения каждого компонента, Поставленная цель достигается тем, что согласно способу количественного определения компонентов нифулина, включающему обработку анализируемой пробы при нагревании с приготовлением раствора и измерение оптической плотности раствора, обработку анализируемой пробы проводят дихлорэтаном до получения суспензии, от которой отделяют нерастворивщийся компонент, который растворяют в соляной кислоте с последующим измерением оптической плотности раствора. На фиг. 1 дана номограмма для двухкомпонентной системы; на фиг. 2 - калибровочный график. Пример. Количественное определение компонентов нифулина многократно проводят в лабораторных условиях. Для этого методом средней пробы берут навески нифулина по + 0,0471 -0,0491 г содержащие: I анализируемая проба - нитазол, фуразолидон, хлортетрациклин индивидуальный;И анализируемая проба - нитазол, фуразолидон, биоветин. Затем анализируемые пробы переносят в мерные колбы емкостью 25 мл и обрабатывают дихлорэтаном при нагревании на кипящей водяной бане в течение 3-5 мин с получением суспензий (содержащих растворенные в дихлорэтане нитазол и фуразолидон и нерастворивщийся компонент - хлортетрациклин индивидуальный или биоветин), которые охлаждают и их объем доводят до метки.дихлорэтаном. После этого от суспензий фильтрованием отделяют нерастворивщийся компонент - хлортетрациклин индивидуальный или биоветин, который остается на фильтре. По 0,5 мл фильтрата (раствора нитазола и фуразолидона в дихлорэтане) из каждой колбы помещают в другие мерные колбы емкостью 25 мл и разбавляют до метки дихлорэтаном. Затем на фотоколориметре ФЭК-55М измеряют оптическую плотность этих растворов при длинах волн Л 365 и 340 нм.. Для расчета количества компонентов (нитазола и фуразолидона) используют предварительно построенную номограмму для двухкопмонентной системы (фиг.-1), для чего готовят растворы нитазола (I раствор) и фуразолидона (II раствор), в дихлорэтане по 25 мл с концентрацией 0,4 г/л. Из I раствора путём разбавления дихлорэтаном получают ряд растворов с концентрацией 1,0 X 10,0X10 г/л. Затем на фотоколориметре ФЭК-55М измеряют оптическую плотность (D) этих растворов при длинах волн Л 365 и 340 нм. По полученным данным строят ось ОА (фиг. I). . Аналогично с помощью ряда растворов, полученных путем разбавления дихлорэтаном из II раствора, строят ось ОВ. Точки на осях ОА и ОВ, соответствующие равным концентрациям компонентов (нитазола и фуразолидона), соединяют прямыми линиями. Одну из этих линий (например CD) разбивают на десять равных частей и через эти точки из начала координат (О) проводят лучи, соответствующие смесям с равными относительными концентрациями. Например, 0,340; 03,40 0-438. На пересечении прямых 0355 и Dj,лежит точка К. Через эту точку проводят линию параллельно CD. На ее пересечении с осью ОА или ОВ получается суммарная концентрация компонентов (нитазола и фуразолидона). Через точки К и О проводят прямую до пересечения с CD, с которой считывают соотнощение компонентов (нитазола и фуразолидона). Расчет количества нитазола и фуразолидона осуществляется по формуле V - iSxJ 0,5x-g где X - содержащие нитазола или фуразолидона, %; 25 - объем раствора анализируемой пробы, мл; С - содержание нитазола или фуразолидона в фотометриуемом растворе, г, найденное по номограмме;0,5 объем аликвоты, мл; § навеска нифулина, г. Оставшийся на фильтре нерастворившийся компонент (хлортетрациклин или биоветин) растворяют в 1 мл 2 н, раствора соляной кислоты. Полученный раствор переносят в мерную колбу емкостью 25 мл , и его объем доводят до метки дистиллированной водой. После этого по 1 мл приготовленного раствора помешают в две мерные колбы емкостью 50 мл, причем в одну из них (опытную) добавляют 5 мл 2 н. раствора соляной кислоты, а в другую (контрольную)- 5 мл дистиллированной воды. Колбы нагревают .на кипяшей водяной бане 5 мин и затем быстро охлаждают. В контрольную колбу добавляют 5 мл 2 н. раствора соляной кислоты и содержимое в обеих колбах, разбавляют дистиллированной водой до метки. Затем на фотоколориметре ФЭК-55М при длине волны Л 268 нм измеряется оптическая плотность раствора из опытной колбы, причем в качестве стандарта используют раствор из контрольной колбы. Для расчета количества хлортетрациклина индивидуального или из биоветина используется предварительно построенный калибровочный график (фиг. 2), для чего берут навеску кристаллического хлортетерациклина гидрохлорида и растворяют в 0,01 н. раствора соляной кислоты с таким расчетом, чтобы прлучился раствор с содержанием хлортетрациклина I мг/мл. Из этого раствора путем разбавления дистиллированной водой готовят .серию стандартных растворов, содержащих 25, 50, 75, 100 и 200 Ед/мл хлортетрациклина. Затем в две мерные колбы емкостью 50 мл вносят по 1 мл одного из стандартных растворов, причем в одну (опытную) добавляют 5 мл 2 н. раствора соляной кислоты, а в другую (контрольную) - 5 мл дистиллированной воды. Обе колбы в течение 5 мин нагревают на кипящей водяной бане, а затем быстро охлаждают до комнатной температуры. После охлаждения в контрольную колбу добавляют 5 мл 2 н. раствора соляной кислоты и объемы растворов в обеих колбах (опытной и контрольнй) добаводят до метки дистиллированной водой. Содержимое колб перемешивают и измеряют оптическую плотность раствора из опытной колбы при длине волны Л 268 нм, причем в качестве стандарта используется контрольная проба. Аналогично обрабатываются остальные растворы из серии первоначально приготовленных стандартных растворов. По экспериментально полученным данным строят график зависимости оптической плотности раствора (D) от концентрации хлортетрациклина в растворе (C);D f(C), представляюший собой прямую проходяшую через начало координат (фиг. 2). Для определения концентрации хлортетрациклина в исследуемом растворе после измерения его оптической плотности, это значение откладывают на оси ординат Д калибровочного графика; проводят прямую линию параллельно оси абсцисс до пересечения с прямой D ПС). На пересечении этих линий получают точку А, из которой .опускают перпендикуляр на ось абсцисс и на этой оси находят значение соответствующее концентрации хлортетрациклина в растворе. Расчет количества хлортетрациклина индивидуального или из биоветина осуществляют по следующей формуле Y -содержание хлортетрациклина, Ед/мг; -содержание хлортетрациклина в фотометрируемом растворе, Ед/мл, найденное по калибровочному графику; -объем раствора анализируе.мой пробы, мл; -навеска нифулина, мг. Одновременно проводят количественное определение компонентов нифулина (нитазола, фуразолидона, хлортетрациклина или из биоветина) известным способом. Результаты определения приведены в таблице. Как видно из таблицы, точность определения каждого компонента: нифулина предлагаемым способом в сравнении с известным значительно повышается: если по известному способу ошибка определения (относительное отклонение) может достигать 73,60%, то по предлагаемому способу она не превышает ± 0,20- 2,40%. Использование предлагаемого способа количественного определения компонентов нифулина (нитазола, фуразолидона, хлортетрациклина индивидуального или из биоветина) в сравнении с известным способом обеспечивает возможность определения компонентов нифулина в случае применения в качестве одного из них как хлортетрациклина, так и биоветина, причем точность определения каждого компонента повышается в среднем в 50 раз. Экономический эффект от использования предлагаемого способа количественного определения компонентов нифулина составляет 80960 р/год за счет высвобождения 2,75 т одного из компонентов нифулина - индивидуального хлортетрациклина при его замене на биоветин.
Формула изобретения
Способ количественного определения компонентов , включающий обработку анализируемой пробы при нагревании с приготовлением раствора и измерение оптической плотности раствора, отличающийся тем, что, с целью повышения точности, обработку анализируемой пробы проводят дихлорэтаном до получения суспензии, от которой отделяют нерастворившийся компонент, который растворяют в соляной кислоте с последующим измерением оптической плотности раствора.
Источники информации, принятые во внимание при экспертизе .

Авторы
Даты
1982-09-15—Публикация
1980-07-28—Подача