Изобретение относится к химической технологии, в частности к способу уничтожения водных отходов, содержащих неорганические азиды, которые образуются при производстве азидосоединений, применяющихся в качестве промышленных полуфабрикатов в органической химии, при производстве фармацевтических препаратов и .взрывчатых веществ.
Известен способ разложения азида щелочного металла путем окисления нитритом в присутствии сильных кис- , лот. При этом в реальных условиях чаще всего эту реакцию проводят, сливая избыток серной или азотной кислоты в нейтральный раствор азида натрия, содержащий избыток нитрита . натрия l.
Недостатки этого способа заключаются в следующем: опасность процесса в связи с возможностью появления в газовой фазе азотистоводородной кислоты,которая обладает большой чувствительностью к механическим воздействиям (по своей природе это инициирующее взрывчатое вещество), в ходе реакции вьщеляется закись азота, которая является токсичным веществом f процесс гзложен технологически и имеет сложное аппаратурное ,оформление.. .
Наиболее близким к предлагаемому с по технической сущности и достигаемому результату является способ разложения азида, согласно которому азид обрабатывают персульфатом кальция и процесс ведут в нейтральной «л или кислой, среде при 45-50С Г2.
Однако по известному способу реакция не проходит.до конца (т.е. не . происходит полное разложение азида) при очень малых концентрациях реагирующих компонентов при низких температурах, при которых распад протекает с очень малой скоростью. Проведение реакции в нейтральной или кислой среде может привести к образованию азотистоводородно кислоты, что
20 нежелательно в связи с большой возможностью ее взрыва, а следовательно, опасностью проведения процесса.
Целью изобретения является ускорение и безопасность ведения процес25са.
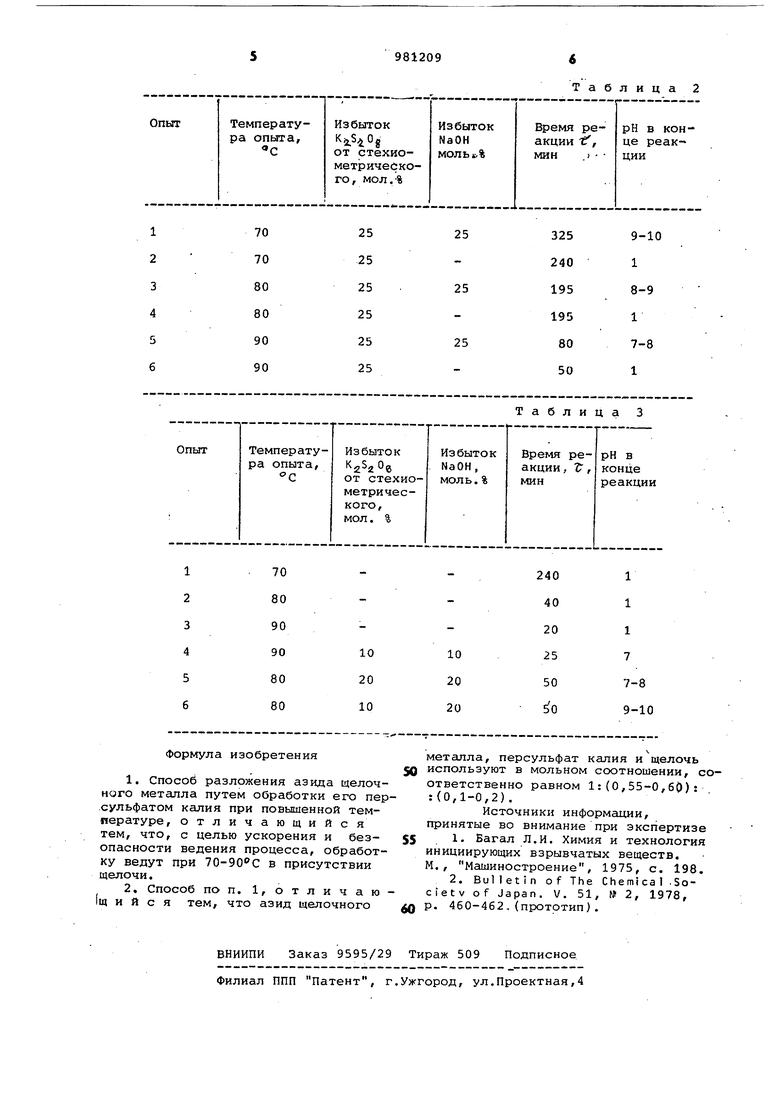
Поставленная цель достигается тем, что согласно способу разложения азида щелочного металла, обработку ведут персульфатом калия при 7030 присутствии щелочи. Азия щелочного металла, персульф калия к щелочь истполь-эуют в мЬлЬнбм соотнсииении, соответственно равном l (0,55-0,60) : (0,1-0,2). Ведение процесса в слабощелочных растворах исключает возможность выделения аэотистоводородной кислоты. При проведении процесса исключается также образование газообразных токсичных продуктов. Основными продуктами реакции являются газообразный азот и небольшие количества кисло рода. Выбор температуры проведения процесса обусловлен следующим: при температуре ниже распад азида протекает очень медленно (более 6 ч а при температуре выше 90°с образуй щиеся газообразные продукты реакции приводят к резкому вспениванию реакционной массы и возможности ее выброса из аппарата. Введение 20% избытка персульфата калия (от стехиометрического необходимо для полного завершения процесса окисления. Введение щелочи осуществляют для нейтрализации серной кислоты, получающейся при побочной .реакции взаимодействия персульфата калия с водой .Кроме того, при окислении отработан ных водных растворов ( после получения органических азидов, соДерзКатих в своем составе хлористый натрий возможно взаимодействие хлористого натрия с персульфатом калия с образованием свободного хлора, который в присутствии едкого натра связывается до хлорида или хлората натрия. Пример, В реактор загружают 500 мл 1,5%-ного водного раствора азида натрия, содержащего 12% хлористого натрия (7,5 г 60 г NaCI), засыпают 18,7 г персульфата калия и добавляют 1,1 г едкого натра. Нагревают смесь до При этом происходит выделение газообразных продуктов. Время реакции 28 мин, рН раствора после окончания процесса 7-8, Отсутствие азид-иона подтверждено качественной реакцией с FeCIj . Основные данные последующих экспериментов, выполненных аналогично примеру, представлены в табл. 1. Данные, полученные при проведении процесса с использованием раствора, содержащего 1,5% 15% NaNO, , представлены в табл. 2. Данные, полученные при проведении npoixecca с использованием раствора, содержащего 0,5-1,5% NaN без примеси других солей, приведены в табл. 3. Использование предлагаемого технического решения в сравнении с известными способами разложения неорганических азидов обеспечивает более полное и безопасное разложение ((уничтожение; отходов неорганических азидов. Во всех опытах не обнаружено следов азотистоводородной кислоты и других вредных выбросов. Осуществление предложенного способа в условиях пилотной установки показывает его высокую эффективность, надежность, безопасность и простоту. Таблица

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАЗОЛА И ЕГО СОЛЕЙ | 1997 |
|
RU2143427C1 |
| СПОСОБ ОБЕЗВРЕЖИВАНИЯ ЖИДКИХ ОТХОДОВ ПРОЦЕССА ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ АЗИДОВ, СОДЕРЖАЩИХ АЗИДЫ ЩЕЛОЧНЫХ МЕТАЛЛОВ | 2014 |
|
RU2598434C2 |
| СПОСОБ УТИЛИЗАЦИИ ЖИДКИХ ОТХОДОВ, СОДЕРЖАЩИХ АЗОТИСТОВОДОРОДНУЮ КИСЛОТУ | 1996 |
|
RU2123211C1 |
| Способ получения 3,4-бензокумарина | 1974 |
|
SU487069A1 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕТРАЗОЛА | 1988 |
|
RU2033993C1 |
| ГИДРАЗИННЫЙ СПОСОБ ПОЛУЧЕНИЯ АЗИДОВ ЩЕЛОЧНЫХ И ЩЕЛОЧНОЗЕМЕЛЬНЫХ МЕТАЛЛОВ | 2009 |
|
RU2472700C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,6-ФТАЛИЛФЕНОТИАЗИН-S, S-ДИОКСИДА | 2005 |
|
RU2276145C1 |
| СПОСОБ ПОЛУЧЕНИЯ БРОМБУТИЛКАУЧУКА | 2000 |
|
RU2177956C1 |
| Способ получения производных диазепина | 1974 |
|
SU497776A3 |
| Способ получения 5-меркапто-1,2,3-триазолов | 1979 |
|
SU961559A3 |

10 10 20 10 10 20 10 20
70 70 70 80 80 80 90 90
1
олее 300
10 20 300
6-7 280
7-8
40
10 20 10
55
6-7
50
7-8
60
3-4 20
35
7
Таблица 2
Таблица 3
Авторы
Даты
1982-12-15—Публикация
1980-10-20—Подача