( 5) СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ НИТРОТРИПТАМИНОВ ИЛИ ИХ ГИДРОХЛОРИДОВ
1 .
Изобретение относится к новому способу получения новых замещенных триптаминов, которые могут найти применение как потенциальные био (Логически активные вещества.
Известны различные замещенные триптаминов, например 5-нитротриптамин, который является аналогом новых замещенных.
Получение 5-нитротриптамина ведут диазотированием А-нитроанилина с последующей обработкой этиловым эфиром о(--ацетил-}г-фталимцдовалериановой кислоты при рН 5 и 3-5°С. Далее полученный продукт циклизуется в среде полифосфорной кислоты при 70120°С и затем омыляется едким натром в водноспиртовой среде, охлажда- ется и подкисляется соляной кислотой. Полученную кислоту в присутствие 10% ее медной соли кипятят в диметилформамиде. После выливания на лед и дефталилирования под действием гидразингидрата в метанольном
растворе при кипячении юлучают целевой продукт формулы;
Cri2 NH2
Однако выход целевого продукта не превышает 33 а жесткие условия циклизации (70-120°С и полифосфорная кислота) и разрушение продукта при декарбоксилировании и омылении сложно-эфирной группы, приводящее к разрушению фталимидного цикла, в значительной мере осложняют проведение процесса.
Цель изобретения - получение новых замещенных нитротриптаминов новым -способом, обеспечивающим более простые условия.
Поставленная цель достигается новым способом получения новых за:t
1Л
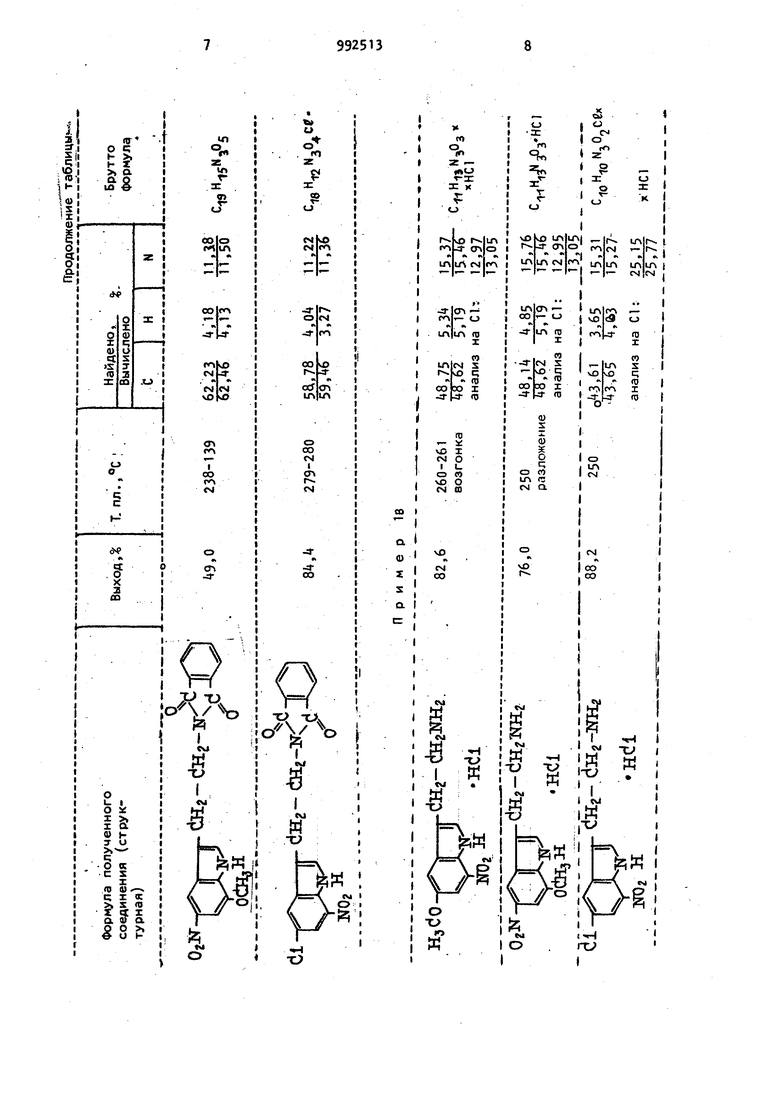
1 ) 9 б. В кипящий раствор 38,2 г сул фосалициловой кислоты в 382 мл укс ной кислоты вносят при размешивани порциями за мин 38,2 г (0,1 моль) 2-метокси-5-нитрофенилгидраэона J-фталимидомасляного аль дегида, смесь кипятят 10 мин и затем оставляют при 15-20°С на 12 ч. Выпавший осадок отфильтровывают промывают уксусной кислотой и водой Получают 26,9 г -нитро-7-меток си-М-фталилтриптамина в виде желто вато-зеленоватых кристаллов. Из ма точника после упаривания выделяют еще г продукта. Общий выход со тавляет 29,9 г (82%). т.пл. 237239 0. Найдено, %: С 62,16, Н ,06j N 11,32 Вычислено, %: С 62,, Н |.,13; N 11,50. Аналогично получают другие соот ветствующие замещенные N-фталиптрип тамины, физико-химические константы которых представлены в таблице. в. Суспензию 6 г (0,01б5 моль) -нитро-у-метокси-М-фталилтриптамина и 2,68 г (0,0535 моль) гидразингидрата в 200 мл абсолютного спирта кипятят с обратным холодильником при пё(эемешиваний 2 ч, отгоняют спирт, добавляют 3 г соды и 0 мл воды, нагревают 1ч при 70-80°С, от гоняют в вакууме 20 мл воды, охлаждают до , осадок отфильтровывают и промывают (3 раза по 10 мл ледяной водой и высушивают. Получают 3,8 г -нитро-7-метокситриптамина в виде желтых кристаллов с т.пл. 17 -17бс. Этот продукт, растворенный в уксусной кислоте, превращают в гидрохлорид обработкой спиртовым растеором хлористого водорода до рН U. Далее реакционную смесь охлаждают до 10-12°С и через 2 ч оСадок отфил тровывают , промывают уксусной кисло той и высушивают едким кали. Получают 3.72 г (83) гидрохлори ла +-нитро-7-метокситриптамина в виде светло-серых кристаллов с т.разл. 250°С. Найдено, %: С ,39; Н 5,03; N 15.36; С1 12,91 Вычислено, °4: С t«8,62; Н 5,19; N 15Л6; С1 13,05 10 В аналогичных условиях получают ругие замещённые триптамина, физикохимические константы которых приведены в таблиц П р и м е р 2. 0,382 г (0,1ммоль) 2-метокси-5-и Трофенилгидразона fталимидомасляного альдегида, 0,038 г (0, ммоль) сульфосалициловой кислоты-(80%-ной) и 3 мл (3,15 г, I 52 ммоль)уксусной кислоты кипятят 30 мин и далее обрабатывают, как . показано в примере 16, с получением 0,09 г (25,3) -нитро-7-метокси-Н-фталилтриптамина. Если кипячение ведут 2 ч, то получают 0,28 г (78j6%) целевого продукта с т.пл. 237-239 С.. П р и м е р 3. 0,38 г (0,1 ммоль) . 2-метокси-5-нитрофенилгидразона тфталимидомасляного альдегида, 3,8 г .(1,2 ммоль) сульфосалицйловой кислоты и 30 мл (31,5 г, 525 ммоль) уксусной кислоты кипятят 30 мин. затем упаривают в вакууме до небольшого объема (5 мл), разбавляют водой (10 мл), осадок отфильтровывают, промывают водой до нейтральной реакции и получают 0,286 г (80,4) +-нитро-7-метокси-И-фталилтриптамина с т.пл. 237-239 С. Пример (сравнительный). 0,38 г (0,1 ммоль) 2-метокси-5-нитрофенилгидразона у-Фталймидомасляного альдегида и 3 мл уксусной кислоты кипятят 2 ч,после чего разбавляют водой, экстрагируют хлороформом и выделяют исходный продукт, не содержащий даже следов (по ТСХ) 4-нитро-7-метокси-М-фталитриптамина. П р и м е р 5 (сравнительный). Аналогично примеру k ведут процесс с использованием 0,382 г (1, ммоль) сульфосалициловой кислоты в k мл спирта, после кипячении разбавляют аодой (20 мл),выделившийся осадок промывают водой и спиртом до нейтральной реакции, высушивают. Получают 0,3б5 г исходного 2-метокси-5-нитрофенилгидрезона -фталимидомасляного альдегида, не содержащего по данным TGX следов циклизованного продукта. Таким образом, только определенное соотношение сульфосалициловой и уксусной кислот по отношению к исходному гидразону обеспечивает его циклизацию. 1 Формула изобретения. Способ получения замещенных трип таминов общей формулы I тэ (iHeCiHzNHi где R - водород, нитрогруппа водород, хлор, нитро- или метоксигруппа; R - нитро- или метоксигруппа, или их гидрохлоридов, отлича ющийся тем, что соответствующий нитрофенилгидразин подвергают взаимодействию с альдегидом или аце талем общей формулы Q Мй1г)5-А, Г 3 где А - группа формулы или - CiH(iH3)2 в присутствии минеральной кислоты в среде низшего спирта при кипении реакционной смеси с последующей циклизацией полученного гидразона а присутствии смеси сульфосалициловой и уксусной кислот, взятых в мольном соотношении, равном (0,1i2-14,2): .(52-525): 1 , при кипячении с дальнейшей обработкой полученного замещенного нитро-М-фталитриптамина гидра-., зингидратом в среде низшего спирта - при кипячении и выделением целевого продукта в виде основания или превращением его в соответствующий гидрохлорид.



| название | год | авторы | номер документа |
|---|---|---|---|
| Гидрохлориды 8-замещенных 2,3,3 @ ,4,5,6-гексагидро-1Н-пиразино-/3,2,1- @ ,к/-карбазолов, обладающие психотропным действием | 1981 |
|
SU1694582A1 |
| Способ получения этилового эфира @ -ацетиламино- @ -карбэтокси- @ -(5-бензилокси-3-индолил) пропионовой кислоты | 1980 |
|
SU1018939A1 |
| СПОСОБ ПОЛУЧЕНИЯ СЕРОТОНИНА И ЕГО ФАРМАКОЛОГИЧЕСКИХ СОЛЕЙ | 2002 |
|
RU2227140C1 |
| Способ получения производных алкилмелатонинов | 1988 |
|
SU1553011A3 |
| СПОСОБ ПОЛУЧЕНИЯ 1- И 1,1-ДИЗАМЕЩЕННЫХ-4-ФЕНИЛ-2,3,4,9-ТЕТРАГИДРО-1H-БЕТТА-КАРБОЛИНОВ | 2004 |
|
RU2332418C2 |
| Способ получения 9-замещенных 2,3-дигидроимидазо [1,2-а] бензимидазола или их солей | 1981 |
|
SU952848A1 |
| ТРИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И ПРОИЗВОДНЫЕ ТЕТРАГИДРОХИНОЛИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2023712C1 |
| Способ получения 9-замещенных 2,3-дигидроимидазо /1,2-а/ бензимидазола или их солей | 1981 |
|
SU952847A1 |
| ПРОИЗВОДНОЕ 3-ОКСАДИАЗОЛИЛ-5,6,7,8-ТЕТРАГИДРО-1,6-НАФТИРИДИНА И ПРОИЗВОДНОЕ 5,6,7,8-ТЕТРАГИДРО-1,6-НАФТИРИДИНА | 1993 |
|
RU2107686C1 |
| 4-ГЕТЕРОЦИКЛИЛ-ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ХИНАЗОЛИНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1995 |
|
RU2137762C1 |


Авторы
Даты
1983-01-30—Публикация
1980-12-18—Подача