Изобретение касается новых биологически активных соединений, а именно гидрохлоридов 8-замещенных 2,3,За,4,5,6-гексагидро-1 Н-пиразино-( 3,2,1-),к)-карбазолов общей формулы
Ближайшим структурным аналогом указанных соединений является гидрохлорид 2,3,За,4,5,6-гексагидро-8-метил-1 Н-пирази - но-(3,2,1,1)-карбазола формулы
О О 4 СЛ 00 ГО






| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИДЕПРЕССИВНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ПАРЕНТЕРАЛЬНОГО ПРИМЕНЕНИЯ НА ОСНОВЕ СУЛЬФОНАТНЫХ СОЛЕЙ ПИРЛИНДОЛА | 2004 |
|
RU2281085C2 |
| ЗАМЕЩЕННЫЕ ИНДОЛЫ, ПРОТИВОВИРУСНЫЙ АКТИВНЫЙ КОМПОНЕНТ, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2010 |
|
RU2436786C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПИРАЗИДОЛА | 2006 |
|
RU2334983C2 |
| Способ получения производных пенициллина или их фармацевтически приемлемых солей (его варианты) | 1979 |
|
SU1151212A3 |
| СПОСОБ ПОЛУЧЕНИЯ ИМИДАЗОЛИЛЬНЫХ СОЕДИНЕНИЙ | 2003 |
|
RU2314296C2 |
| СРЕДСТВО, СНИЖАЮЩЕЕ ВЛЕЧЕНИЕ К АЛКОГОЛЮ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБЫ ЕЕ ПОЛУЧЕНИЯ, ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ | 2008 |
|
RU2401831C2 |
| Способ получения (1,2)-анеллированных 1,4-бензодиазепинов или их оптических изомеров или кислотно-аддитивных солей | 1982 |
|
SU1331431A3 |
| БЕНЗИМИДАЗОЛЬНОЕ СОЕДИНЕНИЕ И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2008 |
|
RU2451017C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭНАНТИОМЕРНО ЧИСТЫХ СОЕДИНЕНИЙ ИМИДАЗОЛИЛА, ЭНАНТИОМЕРНО ЧИСТАЯ КИСЛАЯ АДДИТИВНАЯ СОЛЬ ИМИДАЗОЛИЛА И D- ИЛИ L-ПИРОГЛУТАМИНОВОЙ КИСЛОТЫ, МОНОГИДРАТ ГИДРОХЛОРИДА ЭНАНТИОМЕРНО ЧИСТЫХ СОЕДИНЕНИЙ ИМИДАЗОЛИЛА | 1996 |
|
RU2162085C2 |
| АННЕЛИРОВАННЫЕ КАРБАМОИЛАЗАГЕТЕРОЦИКЛЫ, ФОКУСИРОВАННАЯ БИБЛИОТЕКА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ПОЛУЧЕНИЯ | 2005 |
|
RU2281947C1 |
Изобретение касается замещенных гетероциклических соединений, в частности гидрохлоридов 8-замещенных изопропи- лом или трет-бутилом, или адамантилом, или изобутоксилом или циклогексилом 2,3,За,4,5,6-гексагидро-1 Н-пиперазино 
НС1 (Г),
NHгде R - изопропил, трет-бутил, адамантил, изобутоксил, циклогексил.
ГА)
-N k NH-HCl
Это соединение в медицинской практике известно под названием пиразидол
Известно также использование в медицинской практике в качестве психотропного препарата имипрамина.
Пиразидол - антидепрессант с новым спектром психофармакологической активности. Выраженное тимоаналептическое действие препарата сочетается с особым регулирующим влиянием на центральную нервную систему, выражающимся в активирующем действии у больных с апатическими, энергическими депрессиями и с 5дативном эффекте у больных с ажитиро- в энным состоянием. К достоинствам препарата относятся малая токсичность и хорошая переносимость. Он не вызывает существенных побочных явлений, не обладает холинолитической активностью, что позволяет применять препарат у больных с сопутствующими заболеваниями, при кото- Дых противопоказано применение антихо- линергических препаратов (амитриптилина, имипрамина и др).
Малая токсичность и хорошая перено- фмость пиразидола дает возможность применять его у больных с сопутствующими Соматическими заболеваниями.
В редких случаях поя применении пира- Зидола отмечаются головные боли и некоторые другие побочные эффекты.
При применении имипрамина отмечаются еще более значительные побочные эффекты: нарушения сердечной проводимости, задержка мочеиспускания, запоры, нарушения аккомодации.
Целью изобретения является расширение арсенала потенциальных психотропных средств, обладающих более высокой психотропной активностью и меньшей токсич- . ностью, в том числе меньшим числом Побочных эффектов.
Поставленная цель достигается указан- ными гидрохлоридами 8-замещенных 2,3,За,4,5,6-гексагидро-1Н-пиразино-{3,2,1 ,к)-карбазоло8 общей формулы (I), содержащими в 8-м положении различные заместители.
Способ получения данных соединений основаны на известных реакциях: циклизации гидразонов по Фишеру, алкилировании производного 3,4-дигидрокарбазол-1(2Н)- она дибутиловым ацеталем бромуксусного альдегида и последующей циклизации образующегося соответствующего 6,9-заме- щенного 3,4-дигидрокарбазол-1(2Н)-она и его восстановления.
П р и м е р 1. Получение 2,3,3а,4,5,6-гек- сагидро-8-изопропил-1Н-пиразино-(3,2,1-|, 1фкарбазола гидрохлорида.
А. Получение исходного соединения - моно-4-изопропилфенилгидразона циклогексан-1,2-диона.
К смеси 68,6 г (0,4 моль) гидрохлор1лда
4-изопропилзнилина, 240 мл воды прибавляют последовательно 50 мл (0,5 моль) концентрированной соляной кислоты при перемешивании и прикапывают при 0-5°С раствор азотистокислого натрия из 28,8 г
(0,42 моль) нитрита натрия и 70 мл воды. Смесь выдерживают при этой температуре 20 мин и добавляют 36 г уксуснокислого натрия до рН 5-6, затем прибавляют 120 мл водного раствора натриевого производного
cr-формилциклогексанона (получен из 599 мл (57 г, 0,58 моль) циклогексанона, 49,3 мл (45,3 г, 0,61 моль) этилформиата и 88 мл 29,2%-ного метанольного раствора метила- та натрия). Реакционную массу перемешивают при 0-5°С в течение 1 ч. Осадок отфильтровывают, промывают водой, метанолом.
Получают 53,5 г (55 %) моно-4-изопро- пилфеиилгидразона циклогексан-1,2-диона
в виде кристаллического вещества желтого цвета, растворимого в ДМФА, в низших спиртах, т.пл. 126-127°С (из метанола), устойчив при хранении в защищенном от света месте.
Найдено, %: С 73,84; Н 8.18; N 11,24.
C15H20N20
Вычислено. %: С 73,73; Н 8.25; N 11,46.
ИК-спектр в вазелиновом масле: veo1660, VNH 3245 смн,
в условиях, аналогичных примеру 1А, получают моно-4-трет-бутилфенилгидра- зонциклогексан-1,2-диона (Пб), моно-4-ада- мантилфенилгидразонциклогексан-1,2-диона (Пв), моно-4-изобутоксифенилгидразон- циклогексан-1,2-диона (Пг).
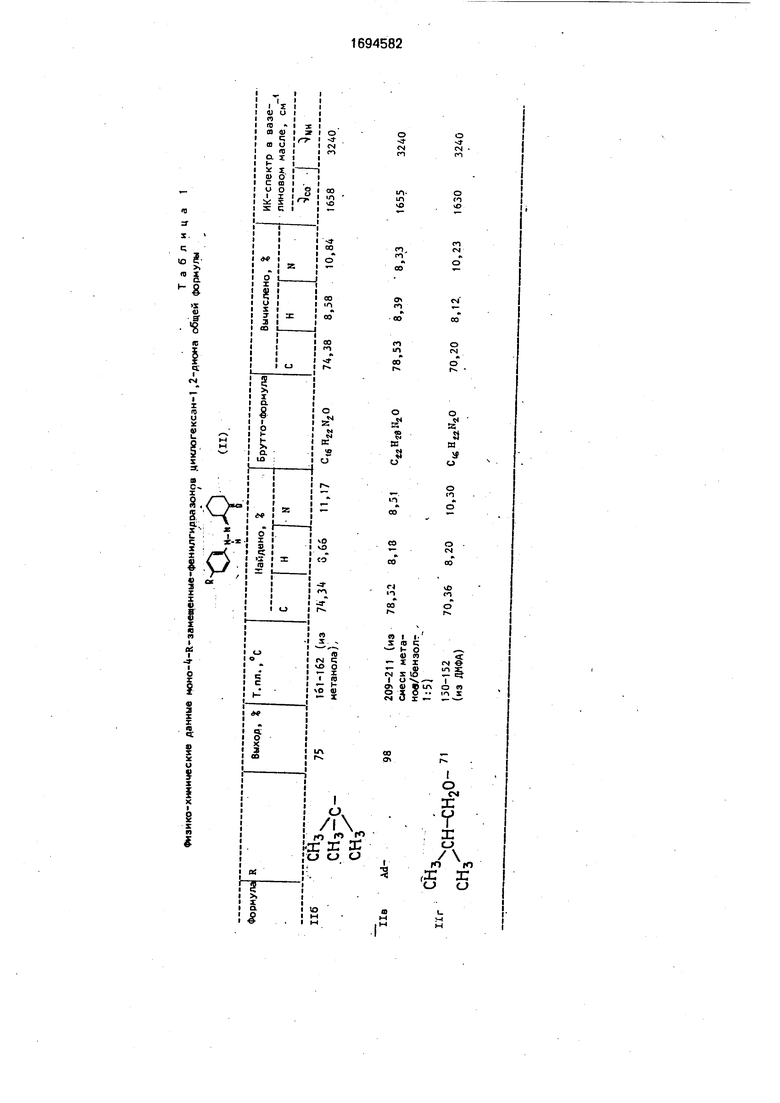
Физико-химические характеристики соединений приведены в табл. 1.
Б. Получение промежуточного соединения 6-изопропил-3,4-дигидрокарбазол- 1(2Н}-она.
Смесь 19 г (0,078 моль) Па, 34 мл 85
%-ной муравьиной кислоты, 9,4 мл ДМФА
кипятят 2 ч, после охлаждения выпавший
осадок отфильтровывают, промывают водои.
Получают 15,3 г (90,7 %) 6-изопропил- 3,4-дигидрокарбазол-1(2Н)-она, который после перекристаллизации из метанола представляет собой кристаллическое веще- ство белого цвета, растворимое в ДМФА, спиртах устойчивое при хранении, т.пл. 159-161°С.
Найдено, %: С 79,08; Н 7.55; N 6,21.
Ci5H17NO
Вычислено, %: С 79,26; Н 7,53; N 6,16.
ИК-спектр в вазелиновом масле: Vco 1635, VNH 3230 .
В условиях, аналогичных примеру 1Б, получают следующие соединения общей формулы (III):
6-трет-бутил-3,4-дигидрокарбазол-1(2 Н)-он, кристаллическое вещество белого цвета с желтоватым оттенком, растворимое в спиртах, устойчивое при хранении;
6-изобутокси-3,4-дигидрокарбазол-1 (2Н)-он, кристаллическое вещество бежевого цвета, труднорастворимое в спиртах, рас- творимое в ДМФА, устойчивое при хранении;
6-адамантил-3,4-дигидрокарбазол-1(2 Н)-он получают из смеси 46 г (0,137 моль) моно-4-адамантилфенилгидразонциклогек- сан-1,2-диона, 510 мл муравьиной кислоты, 1000 мл ледяной уксусной кислоты при кипячении в течение 2 ч, далее процесс проводят в условиях, аналогичных примеру 1 Б.
Это соединение после перекристаллизации из смеси метанол:бензол 1:5 представляет собой кристаллическое вещество белого цвета, растворимое в бензоле, толуоле.
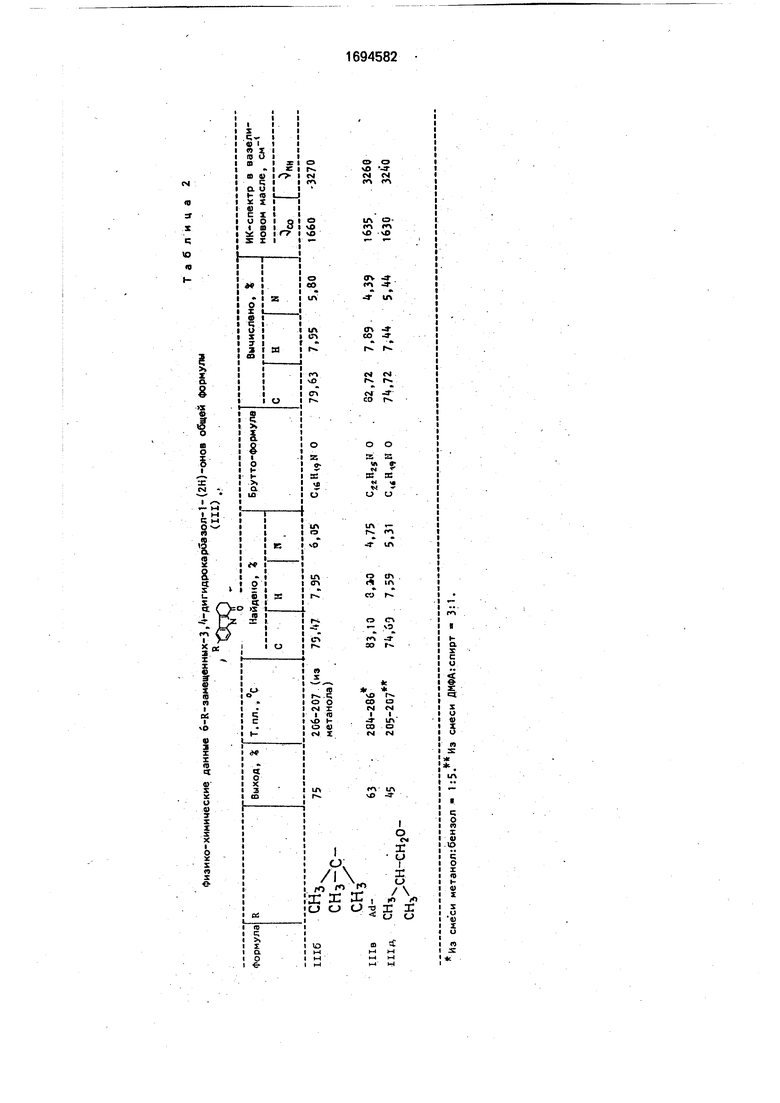
Физико-химические характеристики соединений приведены в табл. 2.
В. Получение 5,6-дигидро-8-изопропил- 4Н-пиразино-(3,2,1-.|,к)-карбазола.
Смесь 113,5 г(0,5 моль)6-трет-бутил-3,4- дигидрокарбазол-1(2Н)-онэ, 300мл ДМФА и 115 мл 25,8%-ного (0,55 моль) раствора ме- тияата натрия в метиловом спирте перемешивают 15 мин,, метанол отгоняют в вакууме. К остатку прикапывают 139 г (0,55 моль) дибутилового ацеталя бромуксусного альдегида, добавляют 150 мл ДМФА. Смесь кипятят при перемешивании 1 ч, охлаждают до -70°С, добавляют 200 мл воды и 200 мл бензола, перемешивают М0 мин, и переносят раствор в делительную воронку, куда предварительно заливают 1 л воды. Водный слой экстрагируют бензолом (3x100 мл). Бензольные экстракты объединяют и упаривают в вакууме. К остатку добавляют 550 мл уксусной кислоты и 340 г уксуснокислого аммония, кипятят 2 ч, охлаждают, добавляют 1 л воды и 200 мл четыреххлористого углерода и перемешивают. Отделяют органический слой, водный слой экстрагируют дополнительно (4x100 мл) четыреххлори- стым углеродом, объединенный экстракт че- тыреххлористого углерода сушат и упаривают в вакууме досуха, остаток растворяют в 3QO мл сухого эфира и добавляют эфирный раствор хлористого водорода. Осадок отфильтровывают, сушат, растворяют при кипячении в воде, добавляют активированный уголь, фильтруют, К охлажденному фильтрату прибавляют 25%-ный водный раствор аммиака до рН 9-10, экстрагируют 5 бензолом, бензол упаривают в вакуума.
Получают 85,6 г (68,6 %) продукта в виде кристаллического вещества желтого цвета, растворимого в органических растворителях, устойчивого при хранении в защищен- 0 ном от света месте.
Найдено, %: С 81,50; Н 7,25; N 11,25.
C17H1BN2
Вычислено, %: С 81,56; Н 7,25; N 11.19. УФ-спектр (в спирте) 5 Амаксчм1(1де) :264(4,72).
В условиях, аналогичных примеру 1В, получают нижеследующие соединения:
5,6-дигидро-8-трет-бутил «4Н-пиразяно- (3,2,1-,к)-карбазол - кристаллическое веще- 0 ство желтого цвета, растворимое в органических растворителях, неустойчивое на свету;
5,6-дигидро-8-адамантил-4Н-пиразино -(3,2,1-.|,к)-карбазол - кристаллическое ве- 5 щество желтого цвета, растворимое в спирте, неустойчивое на свету;
5,6-дигидро-8-изобутокси-4Н-пиразино- -(3,2,1-j,k)-Kap6a3Ofl - кристаллическое вещество желтого цвета, растворимое в орга- 0 нических растворителях, неустойчивое на свету.
Физико-химические характеристики этих соединений приведены в табл. 3.
Г, Получение целевого продукта - 5 2,3,За,4,5,6-гексагидро-8-изопропил-1 Н-пи - разино-(3,2,1-,1)-карбазола гидрохлорида.
Смесь 59,9 г (0,24 моль) 5,6-дигидро-8- изопропил-4Н-пиразино-(3,2,1-,к)-карбазо-. ла, 40 г скелетного никелевого катализато- 0 ра, 250 мл метанола гидрируют при 70 атм и . По окончании реакции катализатор отфильтровывают, промывают метгно- лом. Фильтрат упаривают в вакууме. Остаток - масло растворяют в 200 мл эфира 5 и добавляют эфирный раствор хлористого водорода. Осадок отфильтровывают, кипятят с хлороформом в течение 10 мин, отфильтровывают.
0 Получают 56 г (80 %) 2,3,3а,4,5,6-гекса- гидро-8-изопропил-1Н-пиразимо-(3,2,Н,к) - -карбазола гидрохлорида в виде белого кри - сталлического вещества с зеленоватым оттенком, т.пл. 246-248°С (разлож.) (из
5 65%-ного водного ацетона), труднорастворимое в воде.
Найдено, %: С 70,33: Н 7,97, CI 12,02; N 9,50.
C17H23CIN2
Вычислено, %: С 70,20; Н 7,97; CI 12,19; 9,63.
УФ-спектр. АмаксНМ (Ige) :230(4,52), , 75(3,95).
П р и м е р 2. Получение целевого про- 5 укта 2,3,3а,4,5,6-гексагидро-8-трет-бутил- Н-пиразино-(3,2.1-.|,к)-карбазола идрохлорида (16).
Смесь 22 г (0,083 моль) V6, 30 г пасты келетного никелевого катализатора, 250 мл 10 пирта гидрируют при 60-70 атм и 70-75°С. о окончании реакции катализатор отфильровывают, промывают спиртом, раствориель упаривают в вакууме.
Получают 18,3 г 2,3,3а,4,5,6-гексагидро- 15 8-трет-бутил-1Н-пиразино-{3,2,1,-,|)-карбазола в виде основания, которое обрабатывают эфирным раствором хлористого водорода. Осадок отфильтровывают, промывают ацетоном и хлороформом.20
Получают 15,8 г (63,3%) 16 в виде кристаллического вещества с желтоватым оттенком, труднорастворимого в воде и органических растворителях.
В условиях, аналогичных примеру 1Г, 25 получают 2,3,За,4,5,6-гексагидро-8-изобу- токси-1Н-пиразино-(3.,2,1-,к)-карбазола гидрохлорида (г) в виде кристаллического вещества белого с сероватым оттенком, труднорастворимого в воде и органических 30 растворителях.
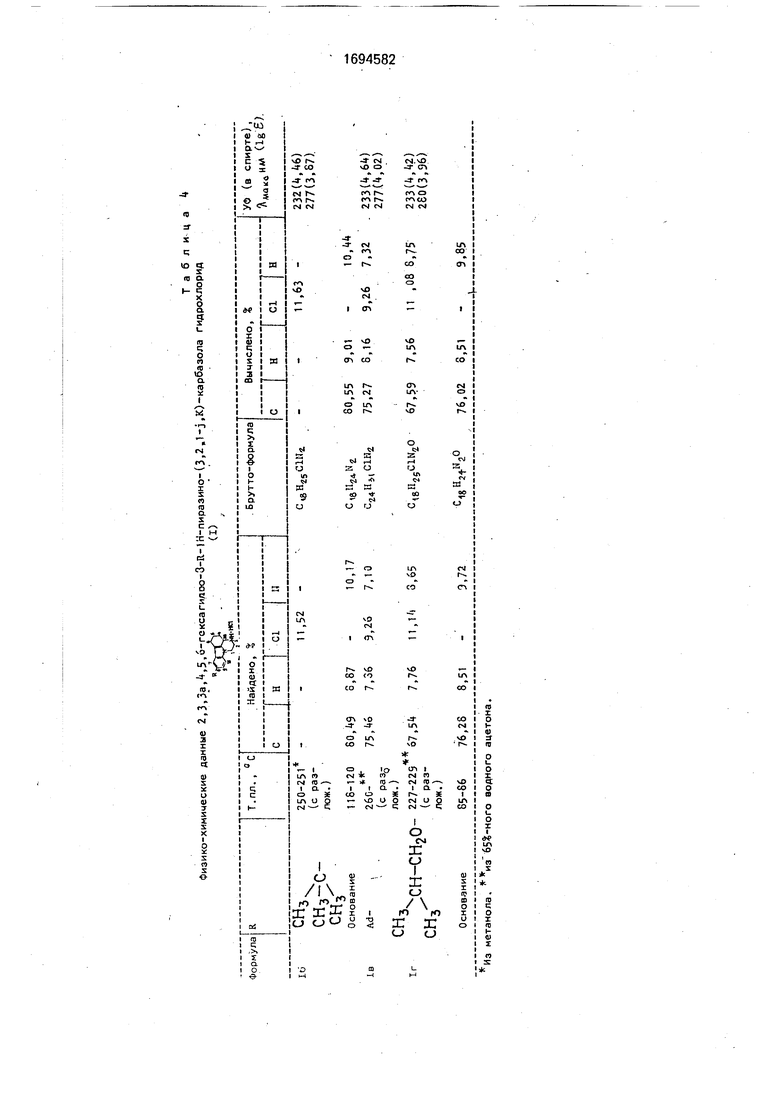
Физико-химические характеристики соединений 16, в, г приведены в табл. 4.
П р и м е р 3. Получение целевого продукта 2,3,За,4,5,6-гексагидро-8-адамантил- 35 1Н-пиразино-(3,2,1 -,к)-карба зола гидрохлорида (I в).
Смесь 35 г (0,10 моль) VB, 40 г пасты скелетного никелевого катализатора, 200 мл n-бутилового спирта, 400 мл этилового спир- 40 та гидрируют при 60-70 атм и 80-90°С. По окончании реакции катализатор отфильтровывают, смесь растворителей упаривают в вакууме. Остаток растворяют в 400 мл бензол - ацетоновой смеси (1:1) при кипячении, 45 обрабатывают эфирным раствором хлористого водорода, осадок отфильтровывают.
Получают 17 г (73,6%) IB в виде кристаллического вещества кремового цвета, практически нерастворимого в воде, 50 растворимого в метаноле.
П р и м е р 4. Получение 2,3,3а,4,5,6-гек- сагидро-8-циклогексил-1Н-пиразино-(3,2,1 :,к)-карбазола гидрохлорида (I).
А. Получение исходного соединения - 55 моно-п-циклогексилфенилгидразона цикло- гексан-1,2-диона (II).
К смеси 21,2 (0,1 моль) гидрохлорида п-циклогексиланилина, 18 мл концентрированной соляной кислоты и 61 мл воды прикапывают постепенно при перемешивании и температуре 0- 5 °С раствор азотистокис- лого натрия (из 8,3 г (0,106 моль) азотисто- кислого натрия и 22 мл воды). Смесь выдерживают при этой температуре и перемешивании в течение 20 мин, затем добавляют 13 г уксуснокислого натрия до рН 5,0-6,0. К реакционной массе приливают водный раствор натриевого производного о-формилциклогексанона в 125 мл воды (получен из 28,2 г(0,287 моль) циклогексано- на, 22,6 г (0,306 моль) этилового эфира муравьиной кислоты и 50,5 г (0,286 моль) 30,5%-ного метанольного раствора метила- та натрия). Реакционную смесь перемешивают при 0- 5 °С в течение 1 ч. Осадок отфильтровывают, промывают водой, метанолом. Получают 24.1 г (94%) II в виде кристаллического вещества желтого цвета, растворимого в различной степени в органических растворителях, неустойчивого при хранении на свету.
После перекристаллизации из диметил- формамида получают 15,1 г (53%) II, т.пл. 156-157°С.
Найдено, %: С 76,02; Н 8,36; N 9,95.
Cl8H24№O
Вычислено, %: С 76,01; Н 8,50; N 9,85.
ИК-спектр (в вазелиновом масле), см 1: v со 1655 VNH 3225.
Б. Получение 6-циклогексил-3,4-дигид- рокарбазол-1(2Н)-она (III).
Смесь 45,9 г (0,162 моль) II. 123 мл 85%- ной муравьиной кислоты и 12 мл диметил- формамида кипятят 2 ч. Смесь охлаждают, осадок отфильтровывают, промывают водой до нейтральной реакции, затем метанолом.
Получают 38,5 г(89%) III в виде кристаллического вещества белого цвета с кремовым оттенком, растворимого в спиртах или в смесях спиртов с органическими растворителями, например диметилформамидом, устойчивого при хранении. Т.пл. 220-222°С.
Найдено, %: С 80,69; Н 7,86; N 5,16.
CieH2iNO
Вычислено, %: С 80,86; Н 7,92; N 5,24.
ИК-спектр (в вазелиновом масле), см : v со 1630 VNH 3240.
УФ-спектр (спирт), А макс (Ige) нм: .240(4,25); 315(4,42).
В. Получение 5,6-дигидро-8-циклогек- сил-4Н-пиразино-(3,2,1-,к)-карбазола(/).
Смесь 45,7 г (0,17 моль) III, 105 мл диме- тилформамида и раствора метилата натрия (из 3,94 г (0,172 г-ат) натрия и 64 мл метанола) перемешивают и отгоняют метанол в вакууме. К остатку добавляют 45,8 г (0,175 моль) 96,5%-ного дибутилового ацеталя
бромуксусного альдегида и кипятят 1 ч. Охлаждают до 70°С, добавляют 95 мл воды и 65 мл бензола. Осадок (не вступивший в реакцию III) отфильтровывают, раствор переносят в делительную воронку, куда пред- 5 варительно заливают 320 мл воды. Водный слой экстрагируют бензолом (3x150 мл). Бензольный экстракт объединяют и упаривают в вакууме. К остатку добавляют 120 мл уксусной кислоты и 79 г уксуснокислого ам- 10 мония. Кипятят 3 ч, охлаждают, выливают в воду и экстрагируют эфиром (3x150 мл), эфирные экстракты упаривают, остаток растворяют в четыреххлористом углероде и добавляют эфирный раствор хлористого 15 водорода. Осадок отфильтровывают, промывают четыреххлористым углеродом, сушат. Растворяют осадок при кипячении в воде, добавляют уголь и отфильтровывают. К охлажденному фильтрату прибавляют 20 25%-ный водный раствор аммиака до рН 9-10. Экстрагируют эфиром, эфирный экстракт упаривают.
Получают 25,5 г (51 %) V, в виде кристаллического вещества желтого цвета, раство- 25 римого в органических растворителях, например спирте, гексане, бензоле, неустойчивого при длительном хранении на свету, т.пл. 110-111°С.
Найдено. %: С 82,73; Н 7,63; N 9,33. 30
C20H22N2
Вычислено, %: С 82,72; Н 7.64; N 9,65.
УФ-спектр (в спирте), А макс (Igs) нм: 266(4,73).
Г, Получение целевого продукта (I).35
Смесь 25,5 г (0.088 моль) V. 22 г пасты никеля Ренея, 500 мл абсолютного этилового спирта гидрируют при 60-70 атм и 50- 70°С. По окончании реакции катализатор отфильтровывают и промывают этиловым 40 спиртом. Фильтрат упаривают в вакууме (на 2/3 объема) и к горячему раствору добавляют концентрированную соляную кислоту до полноты выделения гидрохлорида (I). Осадок охлаждают, отфильтровывают, промы- 45 вают ацетоном. Получают 23,9 г (82,5%) вещества (I) в виде белого кристаллического вещества с кремовым оттенком. Перекри- сталлизовывают из 80%-ного метилового спирта.50
Получают 15,5 г (53,5%) вещества (I), т.пл. 249-251°С.
Найдено, %: С 72,73; Н 8,10; С 10,68; N 8,12.55
C20P27CIN2
Вычислено, %: С 72,58; Н 8,22; С 10,7; N . 8.4. .
Исследование соединений проводилось по методам, принятым для оценки и отбора антидепрессивных средств.
Изучали способность соединений уменьшать депрессивные эффекты резерпина (птоз), усиливать стимулирующее действие фенамина (стереотипия). возбуждающее действие 5-окситриптофана (встряхивание головой), судорожную активность триптамина, уменьшить судорожное действие ареколина и никотина, усиливать снотворное действие гексенала. Опыты проводили на мышах и крысах. Кроме того, в опытах на наркотизированных крысах исследовали влияние соединений на прессор- ное действие тирамина.
Каждое соединение при взаимодействии его с каждым из перечисленных нейрот- ропных веществ вводили шести интактным мышам или крысам и одной наркотизирова- ной крысе. Исследовали 2-3 дозы каждого соединения. Опыты повторяли 2-3 раза. Для сравнения в аналогичных условиях опыта вводили известные психотропные (антидепрессивные) средства: имипрамин - антидепрессант, применяемый во всем мире в качестве эталонного средства и пирази- дол.
Острую токсичность исследовали при введении соединений внутрь белым мышам.
Все соединения малотоксичны. Все они, кроме трет-бутильного аналога (соединение 2, где R - третбутил) менее токсичны, чем пиразидол.
Результаты опытов по отдельным показателям суммировали и обрабатывали статистически. Определяли ЗДбо - дозу, в которой соединения на 50% изменяли исследуемый эффект.
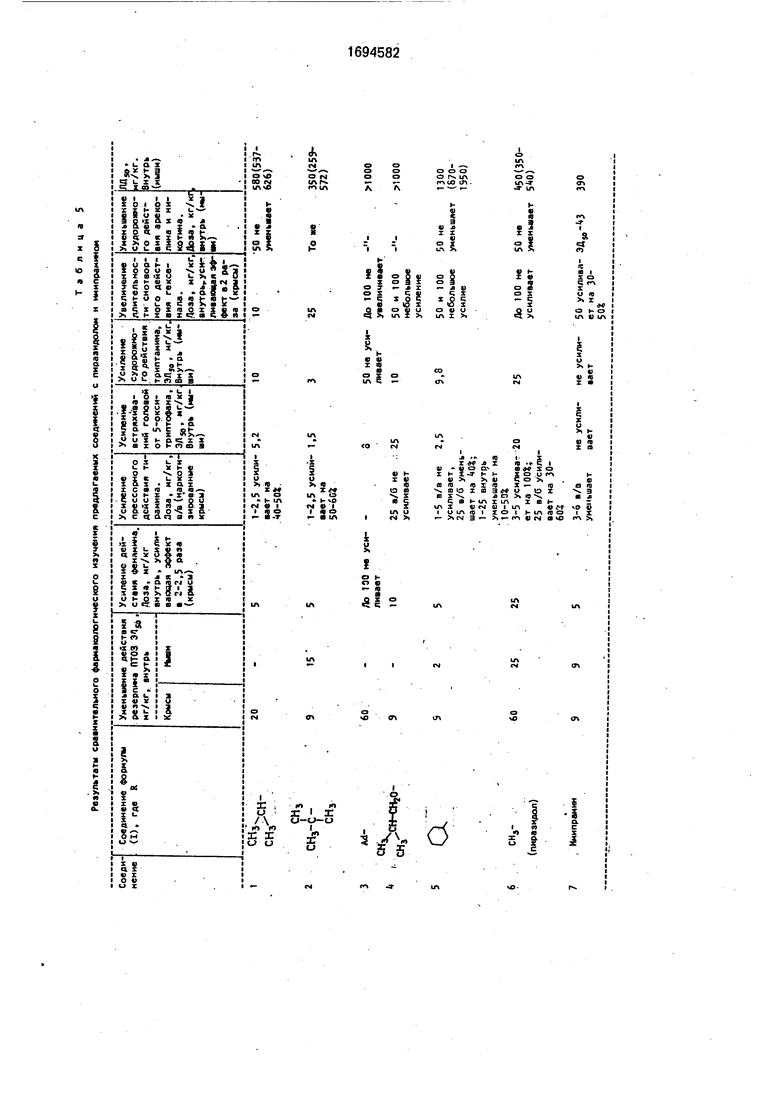
Результаты представлены в табл. 5.
Из табл. 1-5 видно, что все исследованные соединения превосходят пираэидол по активности по одному или нескольким показателям антидепрессивного действия.
Все исследованные соединения з большей степени, чем пиразидол усиливают судорожную активность 5-оксйтриптофана и триптамина, что v свидетельствует об их большей, чему пираэидола ингибирующеймоноаминоксидазу активности. Но ингибирующая моноаминоксидазу активность непродолжительна и обратима.
Способность ингибировать моноаминоксидазу отличает изученные соединения отимипрамина и подобных ему антидепрессантов, обладающих иным механизмом действия. В отличие от имипраминоподобных антидепрессантов, изученные соединения не оказывают холинолитического действия и обнаруживают лишь незначительный кард(|ютоксическийй эффект (и то в больших дфзах).
Гидрохлорид 2,3,За,4,5,6-гексагидро-8- циклогексил-1Н-пиразино-(3,2,1,1)-карба- зола более активен по сравнению с пирази- дфлом по антагонизму с резерпином (ЭДбО- мг/кг); по усилению эффекта фенамина ( мг/кг); п,о усилению судорожного дей- ctBHfl триптамина (9,8-25 мг/кг). Высокая активность по этим показателям может сви- детельствовать о более сильном влиянии aforo соединения по сравнению с пиразидо- лфм на моноаминергические процессы мозга, что может сказаться на терапевтическом действии соединения.
Данное соединение оказалось специфическим ингибитором моноаминооксида- зЫ А, Отличительным свойством этого ингибитора МАО от пиразидола является отсутствие потенцирующего действия на прессорные эффекты тирамина.
Отличительным свойством данного соединения является большая субстратная ши- рЬта окислительного дезаминирования, что мЬжет определить его эффективность при различных депрессиях.
По сравнению с пиразидолом оно менее токсично при приеме внутрь (ЛДзо соответ- с|венно 1300 и 450 мг/кг).
Таким образом, исследованнные соеди- нения являются биологически высокоактивными.
По антидепрессивной активности изученные соединения превосходят пирази- дол.
Изученные соединения отличаются по механизму действия от имипрамина, который не тормозит активности моноаминокси- дазы, и с этим скорее всего связано их значительно меньшее кардиотоксическое действие, чем у имипрамина.
Данные соединения отличаются от имипрамина также отсутствием холиноли- тического действия, вызывающего у больных нежелательные побочные эффекты (нарушение сердечной проводимости, задержка мочеиспускания, запоры, нарушение аккомодации и др.).
Соединения общей формулы (I) были изучены по влиянию на активность моно- аминоксидазы. .
В опытах In vitro и In vivo было установлено, что соединения (изопропил, трет- бутил, изобутоксил-циклогексил) избирательно тормозят дезаминирование серотонина - специфического субстрата моноаминоксидазы типа А и не влияют на дезаминирование Д-фенилэтиламина - специфического субстрата моноаминоксидазы типа Б. Это указывает на то, что эти соединения являются избирательными ингибиторами моноаминоксидазы типа А. В опытах In vivo соединения в более низких концентрациях, чем пиразидол, тормозят дезаминирование серотонина тканями мозга и печени крыс.
Большая антимоноаминоксидазная активность соединений может объяснить их большую фармакологическую активность по сравнению с пиразидолом.
Формула изобретения
Гидрохлориды8-замещенных
2,3,За,4,5,6-гексагидро-1Н-пиразино-{3,2,1- j,k)-Kap6a3onoB общей формулы
R
NHнее ,
где R - изопропил, трет-бутил, адамантил, изобутоксил, циклогексил, обладающие психотропным действием.
НеAd98
rir Э сн-сн2о-71
СН3
ЧХ. н о
(II)
209-211 (из 78,32 8,18 8,51 смеси мета- нов/бензолт , 1:5}
150-15270,36 8,20 10,30
(из ДМФА)
С42Нг8Н2078,53 8,39 8,3316553240
70,20 8,12. 10,23 16303240
О Ј
5
00
го
Физико-химические данные 6-Н-замещенных-3, -дигидрокарбазол-1-(2Н)-онов общей формулы
. ог.
л frit
Из смеси метаноя:бензол - 1:5. Из смеси ДМФА:спирт - 3:1.
Таблица 2
Аиэико-химические данные 5,6-дигидро-8-К-4Н-пира3ино-(3,2,1-;ьК)-карОазоло8 общей формулы
ТЪ$
(V)
CHv64
1 СН3Х
Ad- 26
сн-сн2оСН3
Таблица 3
(V)
111-113 (из метанола)
186-189
146-148 (из этанола)
81,83 7,60 10,83 MgHMN281,78 7,62 1C,60 264(4,75)
84,35 7,27 7,43 СмпввКг 77,13 7,30 9,77 C,8HZON20
84,Т7 7,65 8,18 77,11 7,19 9,99
S
и
со м
270(4,59)
Таблица 4 Физико-химические данные 2,3,За,,5,6-гексагияоо-3-П.-1Н-пиразино-(3,2,1 ,К)-карбазола гидрохлорид
иет$ - (1),
,
Из метанола. из 65%-ного водного ацетона.
CH3v., СН3
:СНСН3
СН3-С; СН3
Ad(пиразирол)
Ииипрамин
20
1-2,5 усили- 5.2 вает на 40-50
10
10
50 не580(537уменымет 626)
15
1-2,5 усилй- 1,5 лет на 50-60
25
То же
350(259- 572)
60
з
До 100 не уси- - ливает
10
О со
-Сь СЛ 00
го
60
25
25
| Машковский М.Д | |||
| и др Новый антидепрессивный препарат пиразидол | |||
| - ХФЖ, 1974, №3, с | |||
| Способ получения молочной кислоты | 1922 |
|
SU60A1 |
| Машковский М.Д., Полежаева А.И | |||
| К фармакологии имизина (тефранила) нового нейтронного вещества | |||
| - Невропатология и психиатрия им | |||
| Корсакова, 1959, № 8, с | |||
| Вагонный люковый затвор | 1924 |
|
SU964A1 |
Авторы
Даты
1991-11-30—Публикация
1981-06-18—Подача