(5) АНТИПИРИЛБИГУАНИДЫ, ПРОЯВЛЯЮЩИЕ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ



| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИАГРЕГАЦИОННОЙ АКТИВНОСТЬЮ | 1991 |
|
RU2061481C1 |
| N-(4-ХЛОРБЕНЗОЛ)СУЛЬФОНИЛ- N -[7-(1,3,5-ТРИАЗААДАМАНТИЛ)МОЧЕВИНА, ОБЛАДАЮЩАЯ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 1984 |
|
SU1254698A1 |
| БИС-(3,5-ДИ-ТРЕТ-БУТИЛ-4-ГИДРОКСИФЕНИЛ)ПРОПИЛ)СЕЛЕНИД, ОБЛАДАЮЩИЙ АНТИОКСИДАНТНОЙ И ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2586067C1 |
| БИС[3-(4-ХЛОРФЕНИЛ)-1-(4-МЕТИЛФЕНИЛ)КАРБОКСАМИДО-1,3-ПРОПАНДИОНАТО]ОКСОВАНАДИЙ, ОБЛАДАЮЩИЙ ГИПОГЛИКЕМИЧЕСКОЙ И АНТИГИПОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2010 |
|
RU2432355C2 |
| Производные соединений бигуанида,проявляющие гипогликемическую активность | 1981 |
|
SU992512A1 |
| Способ получения -замещенных производных бензгидрола или их солей | 1976 |
|
SU649306A3 |
| (±)-ЦИС-3-(2'-БЕНЗИМИДАЗОЛИЛ)-1,2,2-ТРИМЕТИЛЦИКЛОПЕНТАНКАРБОНОВАЯ КИСЛОТА, ПРОЯВЛЯЮЩАЯ САХАРОСНИЖАЮЩЕЕ И АНТИДИАБЕТОГЕННОЕ ДЕЙСТВИЕ | 2000 |
|
RU2205826C2 |
| ОКСОВАНАДИЕВЫЕ КОМПЛЕКСЫ L-ЯБЛОЧНОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ГИПОГЛИКЕМИЧЕСКУЮ АКТИВНОСТЬ | 1996 |
|
RU2101287C1 |
| 2-ГИДРОКСИ-4-ОКСО-4-ФЕНИЛ-2-БУТЕНОАТ БЕНЗОТИАЗОЛИЛАММОНИЯ, ОБЛАДАЮЩИЙ ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2412177C2 |
| Способ получения 1-оксо-1-алкокси2-оксимино-4-нитро-3-фосфоленов | 1978 |
|
SU771108A1 |

-ООС(СН2)зНН2
О
cJoo HNили
ч
О
N
Н
проявляющим гипогликемическую активно ность.
Указанное свойство позволяет предполагать возможность применения этих соединений в медицине. ипирилбигуанидам общей форулы I: C - NHo , R sf C)з при п 1 и 3 Ближайшим структурным соединений общей формулы gszsi 4 аналогом пикрат антипирилбигунида формуV. является лы 11 1
ci d-ir-c -№i-c -uH2
t.o NH
к
V
бН5
Однако в литературе нет сведений о его биологической активности.
Известен широко применяемый антидиабетик - инсулин, основными недостатками которого являются относительно непродолжительное сахароснис Нз(ен2)
iNH. Цель изобретения - расширение арсенала средств воздействия на живой организм. Поставленная цель достигается новыми антипирилбигуанидами общей формулы 1 в качестве веществ, обладающи гипогликемическим действием. Способ получения антипирилбигуани дов общей формулы 1 основан на известной реакции взаимодействия гидрйхлоридов соответствующих аминов с дициандиамидом при нагревании с последующей обработкой реакционной смеси щелочью и выделением оснований антипирилбигуанидов Cl J Соответствующие кислотно-аддитивные соли получают далее взаимодействием эквимолярных количеств соответствующих оснований антипирилбигуанидов с соответствующей кислотой. Пример. Получение -бигуанидоантипирина (соединение Ici). Раствор 60,75 г (Oj25 моль) гидрохлорида аминоантипирина и 21, г (0,25 моль) дициандиамида в 380 мл этилацетата и 380 мл абсолютного спирта нагревают в трехгорлой колбе, снабженной мешалкой, термометром и обратным холодильником, до кипения и кипятят в течение 10 ч. Затем раст вор упаривают досуха в вакууме, раст воряют в 150 мл воды, обрабатывают углем и отфильтровывают. При охлаждении к раствору приливают 30 мл АО -ного раствора NaOH. При этом выделяется свободное основание Ц - бигуанидоантипирина lot в форме кристал
жающее действие и необходимость, применения в виде инъекций 2 J,
Широкое применение в медицине в качестве синтетического перорального гипогликемического препарата группы бигуанидов находит гидрохлорид 1-бутилбигуанида (адебит)формулы III 3.
JiCl
БНг
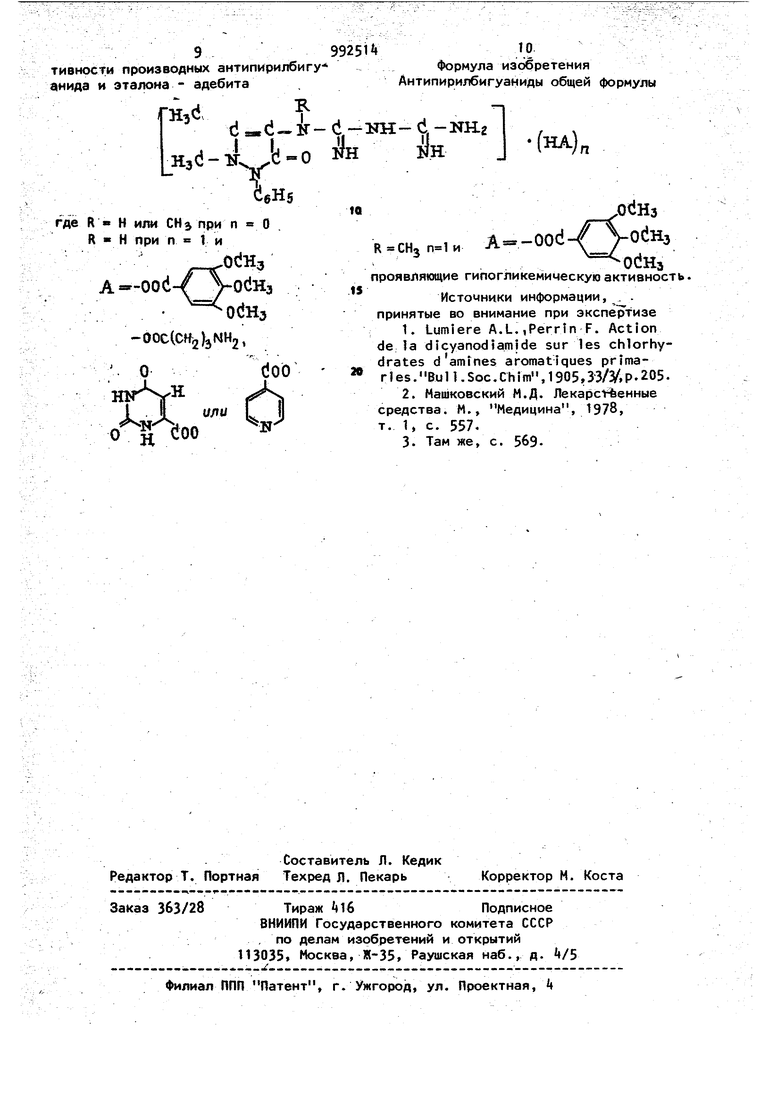
1ТН.IHов, которые дважды перекристаллизоывают из водного изопропилового пирта. Выход очищенного продукта 36,9 г 50,6% от теории). Т.пл. 205,5°С. Найдено, %: С 5,38; Н 6,12; 33,t ЧэН.1М Вычислено, %: С 5, Н 5,9б; 3,12 Уф-спектр снят в метаноле (С 5,9 10 моль) А (6) 207 (1,97-10); 238 (2,13-1СГХ Пример 2. Получение 4-метил- -бигуанидоантипирина (соединение 15). Тщательно перетертую в ступке смесь 12,69 г (0,05 моль) гидрохлорида -метиламиноантипирина и k,2 г (0,05 моль) дициандиамида переносят в колбу, которую помещают в предварительно нагретую до 200-205°С песчаную баню. Реакционная смесь расплавляется, расплав выдерживают 5 мин при 200-205С, затем охлаждают до комнатной температуры. Реакционную массу растворяют в минимальном количестве воды, греют с активированным углем, фильтруют. К фильтрату прибавляют раствор щелочи до рН 8-9, выделившийся осадок отфильтровывают. Получают 12,5 г (78,28% от теории) -метил- -бигуанидоантипирина 15 в виде моногидрата, т.пл. 138,5 1tO°C (из смеси спирта с петролейнЫм эфиром). Найдено, %: С 52,83; Н 6,80; N 30,28 HgO Вычислено,4: С 52, Н 6,63; N 30,69 УФ-спектр снят в метаноле (С 5,008ЧО- моль) Д(е) 206 (2,); 239 (2,31-1 П р и м .е р 3. Получение 3,,5 -триметоксибензоата 4-бигуанидоант гтирина (соединение I в), 16 г (0,0557 моль) основания f-б гуанидоантипирина la растворяют в 300 мл метанола, фильтруют, охлажд до комнатной температуры.и присыпаю 11,8 г (0,0557 моль) ЗЛ,5-тримет:о бензойной кислоты. Метанол упариваю в вакууме,, остаток растворяют в 50 хлороформа, фильтруют. Фильтрат выл вают в охлажденный холодной водой эфир (250 мл). Выпавший белый осадо 3,,5 триметоксибензоата -бигуанид антипирина 1в отфильтровывают, пром вают эфиром, сушат в вакуум-эксикат ре. г (91,7%). Т.пл. 131 Выход 25,8 С 55,; Н 6,29; Найдено, %: N 18,62 1°fe %: С 55,29; И 5,85; Вычислено, 19,-21 метаноле (С УФ-спектр снят в 3,58-10- моль) 208 Ci,75-10); 2 (2,7 П р и м е р 4. Получение 3,,5- т риме то КС ибе нзоата|-метил-А-бигуанидоантипирина (соединение г). Аналогично описанному в примере получают моногидрат 3,,5 триметокс бензоата 4-метил- -бигуанидоантипирина It из 3,19 г (0,01 моль) -метил- М-бигуанидоантипирина 1Б и 2,12 г (0,01 моль) 3,,5-триметокси бензойной кислоты. Выход 5,3 г (99 от теории), 11б-118 с. С 53,83; Н 6,28; Найдено, %: N 18,9 C24H3,N,0 Вычислено, %: С 5,23; Н 6,26; N 18, УФ-спектр снят в метаноле (С З,) д(е) 210 (k,), 2k (2,67-10 Пример 5. Получение | -амино бутирата -бигуанидоантипирина (сое динение Id). Аналогично описанному в примере 3 получают моногидрат J-аминобутирата -бигуанидоантипирина Id из 1,35 г (0,05 моль) 1а и 5,15 г (0,05 моль) у-аминомасляной кислоты. Выход I,2 г (69,53 от теории), 182-183°С. С 50,25; Н 6,81; Найдено, %; N 27,27 : С 9,98; Н 6,90; Вычислено, N 27,A3 УФ-спектр снят в метаноле (С 5,76 ). Л() 207 (1,267-10); 238 (1,736 хЮ); 270 (1,076-10). Пример 6, Получение оротата 4-бигуанидоантипирина (соединение |ё). В 100 мл воды растворяют 5,7 г (0,02 моль) соединения la, фильтруют, добавляют 3, г (0,02 моль) оротовой кислоты, упаривают в вакууме. Получают 7,9 г (89,67 от теории) оротата ii-бигуанидоантипирина I е, Т.пл. 19А-19б°С ,(после переосаждения из водногоацетона). Найдено, %: С А6,39; И 5,28 ,N90,y-i Вычислено, %: С 6,35; Н 5,03 УФ-спектр снят в этаноле (С 1,97 10- моль). А(е) 207 (2,36-10); 239 (2,13 ЧО); 276 (1,73-10). Пример7. Получение изоникотината -бигуанидоантипирйна (соединение }ж), Аналогично; описанному в примере 3 олучают полуторогидрат изоникотйнаа 4-бигуанидоантипирина I из ,7 г (0,02 моль) соединения lot 2,k6 г (0,02 моль) изоникотиновой ислоты. Выход 5,38 г (61,83 от теории) осле переосаждения из хлороформа фиром, Т.пл. 130-132 9. Найдено, %: С 52,18; Н 5,81 CygHgaN Oa . , . Вычислено, : С 52,16; Н 5,76 УФ-спектр снят в этаноле (С 1,8610- моль) А(е) 256 (2,3656-10); 238 (2,20113 104) Все синтезированные соединения бщей формулы I представляют собой елые или белые с кремоватым оттеном кристаллические вещества, раствоимые в воде, спиртах, хлороформе. Проведение фармакологических исследований. Острую токсичность соединений общей формулы I изучали на белых мышах с определением по f.H. Першину при внутрибрюшинном введении соединений в крахмальной слизи. Внутрибрюшинное введение соединений белым мышам в токсических дозах приводит к развитию у животных практически одинаковой картины отравлеП р и W е ч а н и Гипогликемизирующую активность изучали на белых крысах с эксфериментальным аллоксановым диабетом, вызван ным однократным подкожным введением аллоксангидрата в дозе 170 мг/кг. Опробование соединений общей формулы 1 начинали после развития диабета, о чём свидетельствовало появление полидипсии, полиурии, полифагии и устой чивого повышения сахара крови, содер жание которого определяли ортотолуидиновым методом.. Животных лишали пищи на 12 ч до опыта, уровень гликемии характеризовали непосредственно до, а также через 6 ч после применения исследуемого препарата. Все соединения общей формуль) I, а в контроле соответствующий объем.воды вводили через рот. Сахароснижающую активность соединений сравнивали с таковой е. Все соединения вводились крысам с аллоксановым диабетом через рот в дозе, равной 0,2 . Достоверность снижения гликемии в опыте по сравнению с контролем ,05. Достоверность снижения гликемии в опыте по сравнению с контролем 0,01. ния с выраженным тремором, одышкой, общим возбуждением. Гибель наступает в ближайшие мин на фоне клонико-тонических судорог. Результаты испытаний, приведенные в таблице, показывают, что все препараты (1а-1) обладают значительно меньшей токсичностью, чем эталон - абедит, который является лучшим прег аратом группы бигуанида. эталона - адебита, широко используемого в терапевтической практике перорального антидиабетического средства. Введение исследуемых препаратов крысам с аллоксановым диабетом через рот в эквитоксической дозе, равной 0,2 ДЛ5О, обусловило снижение гликемии различной степени выраженности, не вызывая изменений общего состояния животных (см. таблицу). Полученные результаты свидетельствуют о том, что соединения 1с5|-1ж обладают сахароснижающей активностью, в ряде случаев превосходящей по степени выраженности таковую эталонного препарата (адебита). Сравнительная характеристика острой токсичности и сахароснижающей активноСти производных антипирил анида и эталона - адебита d«c H3d-K.,ciтгде R Н или СНз при п 0 R Н при п 1 и А -ood-/ -o(iH3 -ООС(СН2)зМН2, . Оdoo 7.. о to Формула изобретения Антипирилбигуаниды общей формулы H-(i-NIl2 (НА)„ да .ОЙНз -ood CH. AV odHs роявляющие гипогликемическуюактивность. Источники информации, . . принятые во внимание при экспер тизе 1.Lumiere A.L.,Perrfn F. Action de la dicyanodiamlcle sur les chlorhydrates damfnes aromatiques primarles.BulKSoc.Chiffl,1905,.205. 2.Машковский М.Д. Лекарс-НЬенные средства. М., Медицина, 1978, т. 1, с. 557. 3.Там же, с. 5б9
Авторы
Даты
1983-01-30—Публикация
1981-07-15—Подача