Изобретение относится к органической химии, конкретно к усовершенствованному способу получения изомерных аминофенилперфторалкилсульфидов общей формулы (Ia-Iв)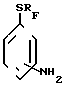 где RF=CF3, C3F7,
где RF=CF3, C3F7,
NH2 в положениях 2 (Ia), 3 (Iб), 4 (Iв).
Указанные соединения являются ценными промежуточными продуктами для синтеза различных практически полезных веществ. Например, м-аминофенилтрифторметилсульфид (Iб, RF= CF3) используется для получения 2-(3' -трифторметилтиоанилино)никотиновой кислоты и ее эфиров, обладающих аналгетичной и жаропонижающей активностью. п-Аминофенилтрифторметилсульфид (Iв, RF=CF3) является промежуточным соединением в синтезе антибактериальных агентов, а также антибластических препаратов. Для синтеза последних применяется также и п-аминофенилгептафторпропилсульфид (Iв, RF=C3F7).
В литературе описаны способы получения этих соединений. Синтезировались они различными путями. Так, о-аминофенилтрифторметилсульфид (Ia, RF=CF3) получают, например, трифторметилированием о-аминотиофенола при УФ облучении в растворе жидкого аммиака [1]. Учитывая то, что исходный о-аминотиофенол обычно получают из 2-меркаптобензтиазола с выходом 67-72% [2], общий выход целевого продукта составляет ≈ 50%.
м-Аминофенилтрифторметилсульфид (Iб, RF=CF3) получали хлорированием и фторированием м-нитротиоанизола с последующим восстановлением образовавшегося м-нитрофенилтрифторметилсульфида [3]. Исходный м-нитротиоанизол синтезировали исходя из м-нитророданбензола через промежуточный м-нитротиофенолят натрия.
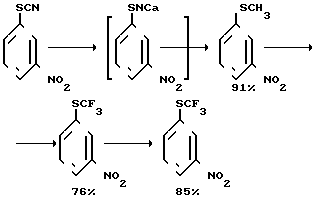
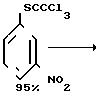
Итоговый общий выход 56%.
Описан также синтез п-аминофенилтрифторметилсульфида (Iв, RF= CF3) аналогично орто-изомеру фотохимическим перфторалкилированием п-аминотиофенола в растворе жидкого аммиака [4]. Несмотря на то, что эта стадия обеспечивает высокую степень превращения, с учетом синтеза исходного п-аминотиофенола [5] общий выход целевого продукта не превышает 60%.
По такому методу получен также п-аминофенилгептафторпропилсульфид (Iв, RF=C3F7) с общим выходом 50% [6].
Недостатками известных способов являются:
сравнительно низкая производительность метода. Для получения целевых продуктов (Iа-Iв) по известным способам необходимо заранее синтезировать, выделять и очищать промежуточные аминотиофенолы, и хотя методы для некоторых из них имеются, выходы в среднем составляют 70%. Поэтому несмотря на то, что непосредственный процесс перфторалкилирования довольно результативен (выхода 70-90% ), с учетом синтеза аминотиофенолов продуктивность метода в целом, составляет 50-60%.
необходимость работать с чрезвычайно зловонными, вредными для организма человека и токсичными аминотиофенолами.
недоступность ряда мета-аминофенилперфторалкилсульфидов (Iб) вследствие отсутствия эффективного и простого метода синтеза м-аминотиофенола. В то время как для синтеза орто- и пара-аминотиофенолов имеются достаточно хорошо разработанные методики, получение мета-аминотиофенола остается малодоступным.
Таким образом, из приведенного следует, что основные трудности при синтезе аминофенилперфторалкилсульфидов связаны с получением, выделением и очисткой промежуточных аминотиофенолов, с необходимостью с этими не только легко окисляющимися, но и мерзко пахнущими и токсичными веществами. С целью устранения указанных недостатков прототипа в задачу настоящего изобретения входит разработка такого способа получения изомерных аминофенилперфторалкилсульфидов (Ia-Iв), при котором генерируемые in situ аминотиофенолы использовались бы для синтеза целевых продуктов без выделения путем непосредственного их перфторалкилирования в первичной реакционной среде.
Поскольку процесс фотохимического перфторалкилирования тиофенолов должен протекать в щелочной среде, в частности в растворе жидкого аммиака, для достижения поставленной цели синтез аминотиофенолов необходимо осуществлять тоже в растворе жидкого аммиака.
По нашему мнению наиболее простым и универсальным методом получения всех изомерных аминотиофенолов могло бы оказаться восстановление промышленно доступных и легко синтезируемых в лаборатории динитродифенилдисульфидов. Вообще такие методы известны, однако они осуществляются не в жидком аммиаке. Например, используется действие цинка или олова в соляной и уксусной кислотах, амальгамы натрия в спирте, а также каталитическое гидрирование в диоксане при повышенной температуре и давлении. Ясно, что ни один из них не может быть использован для решения поставленной задачи, т.к. все они требуют выделения и очистки получаемых аминотиофенолов.
Целью изобретения является разработка нового универсального метода синтеза аминофенилперфторалкилсульфидов, упрощающего технологический процесс за счет устранения стадии выделения и очистки промежуточных аминотиофенолов, исключающего контакт человека и окружающей среды с токсичными и зловонными аминотиофенолами, что создает основу для организации экологически безопасного производства, а также повышающего выхода целевых продуктов.
Поставленная цель достигается заявляемым способом: постепенное прибавление металлического лития, натрия или кальция к суспензии симм.-динитродифенилдисульфида в жидком аммиаке в присутствии алифатического спирта и последующее УФ облучение образовавшегося раствора вместе с добавленным в него перфторалкилиодидом приводит к получению целевых соединений (Ia-Iв) с высоким выходом.
Новизна заявляемого изобретения выражена, во-первых, в новом методе синтеза промежуточных аминотиофенолов, заключающемся в восстановительном расщеплении соответствующих динитродифенилдисульфидов активными металлами в среде жидкого аммиака, а во-вторых, в совмещении в одном технологическом процессе двух различных стадий: синтез аминотиофенолов и их перфторалкилирование.
Предлагаемый способ имеет два существенных отличия: объединение в одной реакционной среде двух ранее раздельных и не связанных стадий: синтез промежуточных аминотиофенолов и их перфторалкилирование и использование в качестве исходных соединений не зловонных и токсичных аминотиофенолов, а изготовляемых в промышленности и экологически безопасных динитродифенилдисульфидов. Именно эти отличия позволили устранить все описанные недостатки.
П р и м е р. м-Аминофенилтрифторметилсульфид. В четырехгорлый реактор из стекла пирекс, снабженный механической мешалкой, холодильником глубокого охлаждения, термометром и охлаждаемый низкотемпературной баней, помещают 10 г (0,032 моль) 3,3' -динитродифенилдисульфида, 26 мл (0,64 моль) метанола, конденсируют 100-120 мл жидкого аммиака и при температуре от -50оС и до кипения аммиака малыми порциями прибавляют 5,3 г (0,76 моль) металлического лития, следя за тем, чтобы реакционная смесь не слишком бурно вскипала. Полученную смесь выдерживают при этой температуре 20-30 мин до обесцвечивания раствора, конденсируют в нее 19-25 г (0,1-0,13 моль) трифторметилиодида и освещают лампой ПРК-4 в течение 1 ч.
После удаления аммиака оставшуюся массу разбавляют водой, продукт извлекают бензолом, бензольный раствор промывают водой до рН 7 и сушат над K2CO3. Бензол отгоняют с дефлегматором, продукт перегоняют в вакууме.
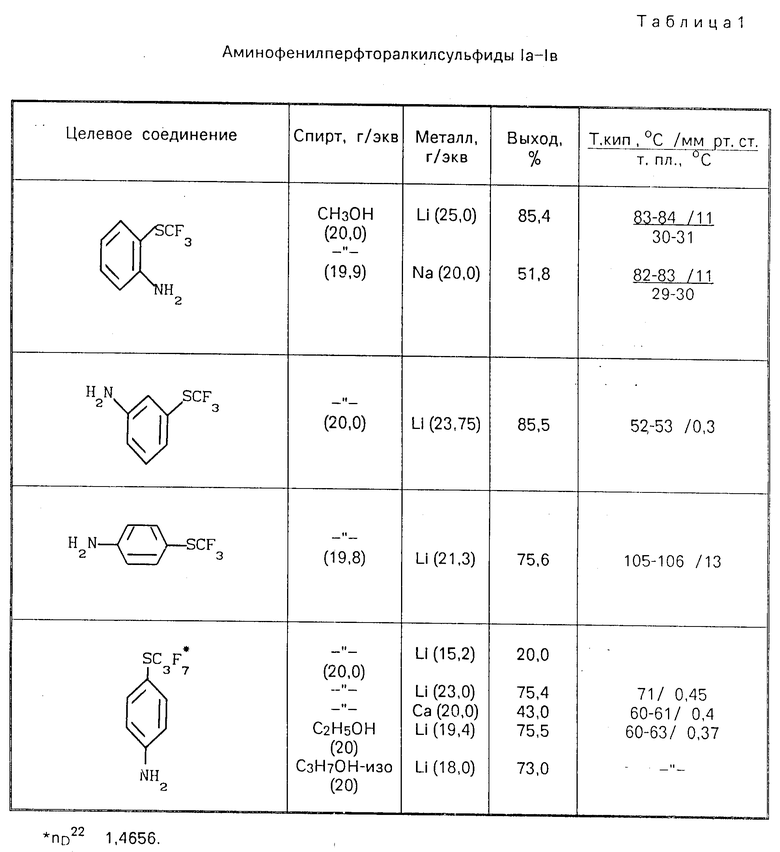
Аналогично получают все изомерные аминофенилперфторалкилсульфиды (Ia-Iв). Выходы, т. кип., т.пл. приведены в табл. 1. п-Аминофенилтрифторметилсульфид (Iв, RF=CF3) и п-аминофенилгептафторпропилсульфид (Iв, RF=C3F7) идентифицированы методом ГЖХ сравнением с заведомыми образцами (носитель Хроматон N-AW-ДМСS с 5% силикона SE 30; длина колонки 2,4 м, температура 175оС, газ-носитель гелий, расход 15 мл/мин).
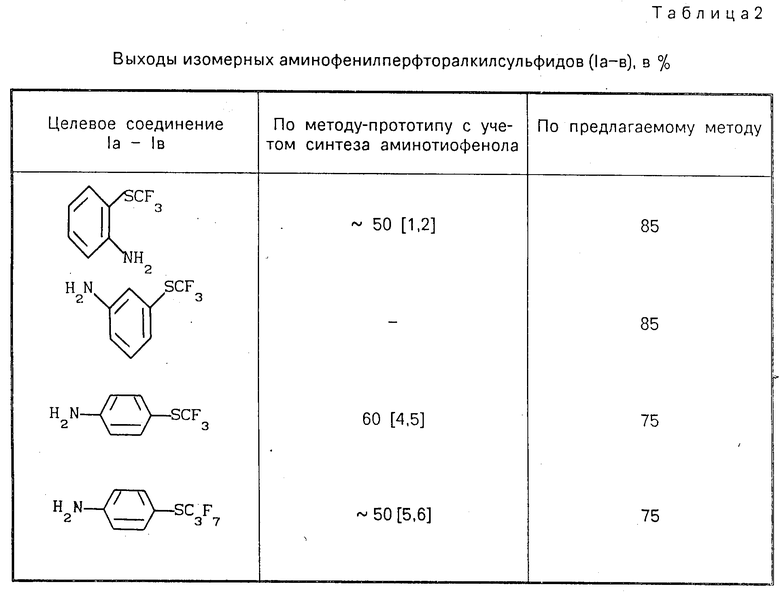
Таким образом, предлагаемый способ является универсальным, позволяющим получать все изомеры целевых продуктов. Весь процесс может быть реализован в одном реакторе. Способ не требует значительных технологических проработок, позволяет значительно снизить материальные затраты, обеспечивает безопасность и экологическую чистоту процесса за счет устранения стадии выделения и очистки зловонных и токсичных аминотиофенолов. Предлагаемый способ позволяет значительно повысить выходы целевых соединений (табл. 2).
Изобретение касается замещенных сульфидов, в частности получения изомерных аминофенилперфторметил-или пропилсульфидов, применяемых в синтезе лекарственных препаратов. Цель - создание универсального и безопасного синтеза указанных соединений с лучшим выходом. Синтез ведут обработкой соответствующих динитродифенилдисульфидов щелочным или щелочно-земельным металлом в жидком аммиаке и последующим УФ-облучением образовавшегося раствора вместе с добавленным в него перфторалкилиодидом. Эти условия повышают выход целевых продуктов с 50-60 до 75-85% при исключении стадий выделения и очистки опасных аминотиофенолов. 2 табл.
СПОСОБ ПОЛУЧЕНИЯ АМИНОФЕНИЛПЕРФТОРАЛКИЛСУЛЬФИДОВ общей формулы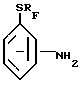
где RF - CF3 или C3F7,
с использованием реакции перфторалкилирования соответствующими перфторалкилиодидами при УФ-облучении в среде жидкого аммиака, отличающийся тем, что, с целью повышения выхода целевых продуктов и создания универсальной и безопасной технологии процесса, сим. -динитродифенилдисульфид подвергают обработке щелочным или щелочноземельным металлом в жидком аммиаке и в присутствии алифатического спирта с последующим непосредственным перфторалкилированием.
| Gilman H., Gainer G.C | |||
| Приспособление для точного наложения листов бумаги при снятии оттисков | 1922 |
|
SU6A1 |
| Автоматическое или полуавтоматическое телефонное устройство | 1925 |
|
SU1949A1 |
Авторы
Даты
1995-03-10—Публикация
1990-02-14—Подача