Изобретение относится к способам получения капролактамата натрия, используемого в качестве катализатора анионной полимеризации лактамов, для получения поликапрамида и его сополимеров.
Известен способ (1) получения капролактамата натрия, взаимодействием металлического натрия с капролактаматом при 100-120оС
Na+KлH __→ NaKл+0,5H2 где Kл=H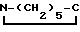 =0 . Этот способ при его кажущейся простоте имеет ряд недостатков. Помимо пожароопасности выделяющийся водород частично восстанавливает лактам до циклогексилимина, циклогексанола и других соединений, которые в целом снижают каталитическую активность капролактамата натрия. Следствием этого является невоспроизводимость ряда физико-химических и прочностных характеристик поликапрамида.
=0 . Этот способ при его кажущейся простоте имеет ряд недостатков. Помимо пожароопасности выделяющийся водород частично восстанавливает лактам до циклогексилимина, циклогексанола и других соединений, которые в целом снижают каталитическую активность капролактамата натрия. Следствием этого является невоспроизводимость ряда физико-химических и прочностных характеристик поликапрамида.
Наиболее близким по технической сущности и достигаемому результату к изобретению является способ получения (2) капролактамата натрия взаимодействием гидрида натрия с капролактамом по реакции в среде органических растворителей
NaH+H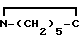 =0 __→ NA
=0 __→ NA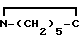 =0+H
=0+H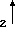
Однако и этот способ не лишен недостатков.
Гидрид натрия, получаемый в СССР, по чистоте не превышает 90%. Значительную часть примесей составляют алкильные производные натрия, которые являются инициаторами протекания побочных реакций, с образованием различных продуктов восстановления и конденсации, снижающих каталитическую активность капролактамата натрия.
Целью изобретения является способ получения капролактамата натрия.
Поставленная цель достигается тем, что для получения капролактамата натрия используют смешанный гидрид натрия и алюминий, выбранный из группы NaH˙AlH3, NaH˙ (AlH3)2 или (NaH)3 ˙AlH3, а в качестве растворителя применяют диэтиловый эфир.
Исходные гидриды NaH˙AlH3, NaH ˙(AlH3) или (NaH)3 ˙AlH3 получают по известному способу (3).
Химический анализ полученных смешанных гидридов представлен ниже.
Найдено,%: Na 42,3; Al 49,5; H 7,25.
NaH ˙AlH3
Вычислено,%: Na 42,5; Al 50; H 7,4.
Найдено,%: Na 27,5; Al 70,9; H 7,3.
NaH ˙(AlH3)2
Вычислено,%: Na 27,3; Al 71,4; H 7,2.
Найдено,%: Na 70,72; Al 25,9; H 5,85.
(NaH)3 ˙AlH3
Вычислено,%: Na 70,6; Al 26,5; H 5,92.
Затем полученные исходные смешанные гидриды NaH ˙(AlH3)nиспользуют для получения капролактамата натрия.
Взаимодействие их с ε-капролактамом проводят в среде диэтилового эфира, при комнатной температуре и перемешивании по реакции при соотношении реагентов:
NAH·AlH3+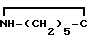 =0=1:1
=0=1:1
NAH·(AlH3)2+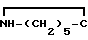 =0=1:1
=0=1:1
(NAH)3·AlH3+N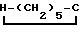 =0=1:3 в течение 2-5 ч, осветленный раствор отделяют от осадка упаривают при Т-200оС/вак.
=0=1:3 в течение 2-5 ч, осветленный раствор отделяют от осадка упаривают при Т-200оС/вак.
Процесс отражается уравнениями
NAH·AlH3+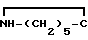 O __→ NA
O __→ NA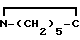 O+AlH3+H2 (1)
O+AlH3+H2 (1)
NAH·(AlH3)2+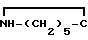 O __→ NA
O __→ NA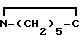 O+2AlH3+H2 (2)
O+2AlH3+H2 (2)
(NAH)3·AlH3+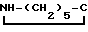 O __→ NAN-(CH2)5-CO+AlH3+3H2 (3)
O __→ NAN-(CH2)5-CO+AlH3+3H2 (3)
Например, в синтезе по уравнению (1)
к суспензии 2 г (0,0037 моля) NaH ˙AlH3 в Et2O дозируют 100 мл раствора Et2O, содержащего 4,2 г (0,037 моля ε-капролактама).
Реакционную смесь отфильтровывают от NaH˙AlH3 и упаривают в вакууме при 20оС. Получено 49 г (98%) капролактамата натрия, представляющего собой белое кристаллическое вещество, расплывающееся на открытом воздухе, поэтому синтезированный капролактамат натрия хранят в закрытых ампулах в атмосфере аргона.
Найдено,%: С 52,5; Н 7,3; N 10,2; Na 16,5.
NA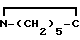 O
O
Вычислено,%: С 52,9; Н 7,4; N 10,3; Na 16,9.
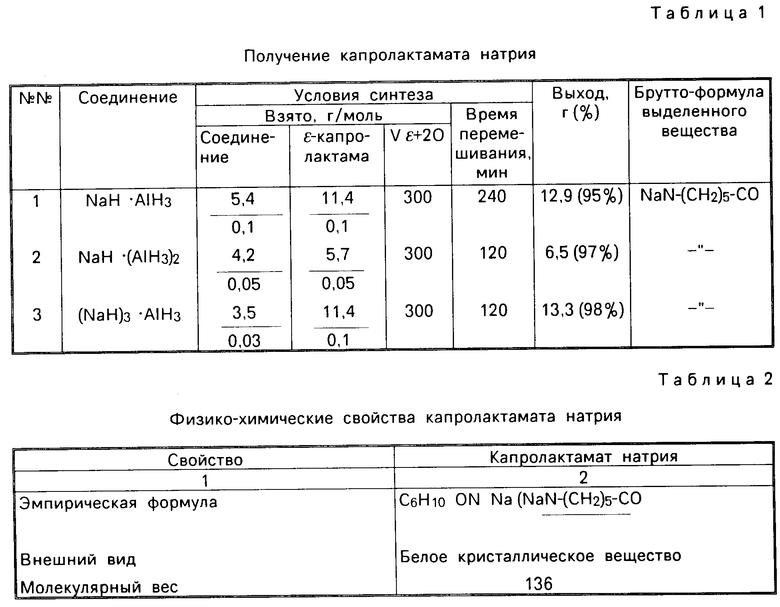
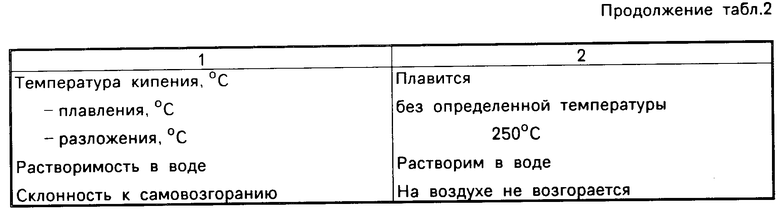
В табл. 1 и 2 приведены результаты синтеза капролактамата натрия и его физико-химические свойства.
Таким образом, получен капролактамат натрия с выходом 95-98%, чистотой 99,5%. Процесс прост в исполнении и для синтеза используют доступные исходные вещества, позволяющие повысить качество капролактамата натрия, т. е. его каталитическую активность.
Одним из важнейших преимуществ предлагаемого способа является получение в качестве побочного продукта гидрида алюминия, который нейтрализует отрицательное действие Н2 на получаемый капролактамат натрия, выражающееся в восстановлении капролактамата натрия, что приводит к снижению его каталитической активности. Кроме того, гидрид алюминия используют в качестве реагента для получения исходных водородных соединений алюминия и натрия.
Другим преимуществом рассматриваемого метода по сравнению с прототипом и аналогом состоит в том, что производство капролактамата натрия по предлагаемому способу дает возможность обеспечить выполнение следующих требований:
получить наиболее чистый и высокоэффективный катализатор полимеризации лактаматов;
повысить уровень безотходности за счет сведения к минимум бракованных партий поликапрамида, вследствие повышения чистоты капролактамата натрия, применяемого в качестве катализатора анионной полимеризации при его производстве.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ПОЛИМЕРИЗАЦИИ ЭПСИЛОН-КАПРОЛАКТАМА | 2012 |
|
RU2522540C1 |
| Способ получения катализаторов полимеризации лактамов | 1990 |
|
SU1779245A3 |
| Способ получения катализатора анионной полимеризации лактамов | 1990 |
|
SU1754203A1 |
| Способ получения алюмогидридов щелочноземельных металлов | 1981 |
|
SU1043105A1 |
| Способ получения лактамоалюминатов натрия | 1976 |
|
SU739070A1 |
| Способ получения катализаторов полимеризации лактамов | 1990 |
|
SU1774940A3 |
| МЕТАЛЛИРОВАННЫЙ ЛИГАНД, КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ ПРИ ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА | 2014 |
|
RU2658831C2 |
| БИС-ИМИН-ТИТАНОВЫЙ КОМПЛЕКС, КАТАЛИТИЧЕСКАЯ СИСТЕМА, ВКЛЮЧАЮЩАЯ ЭТОТ БИС-ИМИН-ТИТАНОВЫЙ КОМПЛЕКС, И СПОСОБ (СО)ПОЛИМЕРИЗАЦИИ СОПРЯЖЕННЫХ ДИЕНОВ | 2018 |
|
RU2772242C2 |
| Способ получения гидрида натрия | 1980 |
|
SU905190A1 |
| ЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ ЖЕЛЕЗА В КАЧЕСТВЕ КАТАЛИЗАТОРА ОКИСЛЕНИЯ ЛЕЙКОСОЕДИНЕНИЙ ТРИАРИЛМЕТАНОВЫХ КРАСИТЕЛЕЙ И СПОСОБ ПОЛУЧЕНИЯ ТРИАРИЛМЕТАНОВЫХ КРАСИТЕЛЕЙ | 1993 |
|
RU2045531C1 |
Использование: капралактамат натрия, катализаторы анионной полимеризации лактамов. Сущность изобретения: капролактамат натрия получают металлированием гидридом натрия ε-капролактама в среде апротонного растворителя при 20-80 °С и перемешивании в течение 2-5 ч, при этом используют смешанный гидрид алюминия и натрия, выбранный из группы NaH·AlH3, NaH·(AlH3)2 : (NaH)3·AlH3. Продукт отделяют, упаривают, сушат в вакууме. 2 табл.
СПОСОБ ПОЛУЧЕНИЯ КАПРОЛАКТАМАТА НАТРИЯ металлированием Е-капролактама гидридом металла при 20 - 80oС путем перемешивания в среде апротонного растворителя в течение 2-5 ч, отделения осветленного раствора с последующим упариванием и сушкой в вакууме, отличающийся тем, что в качестве гидрида металла используют смешанный гидрид натрия и алюминия, выбранный из группы NaH · AlH3, NaH · (AlH3) или (NaH)3 · AlH3, а в качестве растворителя используют диэтиловый эфир.
| Гарбузова И.А | |||
| и др | |||
| Известия АН СССР сер | |||
| хим | |||
| Способ приготовления консистентных мазей | 1919 |
|
SU1990A1 |
Авторы
Даты
1995-03-10—Публикация
1991-12-09—Подача