Изобретение относится к способам получения эфиров акриловой кислоты и может быть использовано для получения метилакрилата дегидрированием метилового эфира пропионовой кислоты.
Метилакрилат является ценным продуктом промышленности органического синтеза и широко используется в производстве органических стекол, волокон, смол и других продуктов.
Для получения акриловой кислоты и эфиров в промышленности используется циангидринный метод [1] При этом первой стадией процесса является катализируемое едким натром или содой взаимодействие синильной кислоты и ацетальдегида (20-40оС).
CH3CHO+HCN ____→ CH3-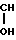 -CN Обработка циангидрина 100%-ной серной кислотой при 80-85оС приводит к образованию амида акриловой кислоты
-CN Обработка циангидрина 100%-ной серной кислотой при 80-85оС приводит к образованию амида акриловой кислоты
CH3-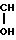 -CN+H2SO4 ____→ CH2=CH-C
-CN+H2SO4 ____→ CH2=CH-C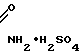
При добавлении воды и метанола протекает этерификация амида с образованием метилакрилата
CH2=CH-C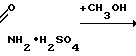 CH2=CH-C
CH2=CH-C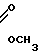 +NH4HSO4
+NH4HSO4
Суммарный выход метилакрилата достигает 70-80% Из-за все время увеличивающейся стоимости синильной кислоты и необходимости утилизации большого количества сернокислого аммония (в два раза больше, чем основного продукта) циангидринный метод не может обеспечить необходимый прирост потребности метилакрилата и не имеет перспектив в будущем [2]
Один из современных способов синтеза метилакрилата базируется на использовании акрилонитрила [3]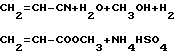 SO4 ____→
SO4 ____→
Реакцию проводят при 80-90оС, постепенно добавляя акрилонитрил или серную кислоту к смеси остальных реагентов и возвращая конденсат в реактор. Выход метилакрилата превышает 90%
Недостатком данного способа является использование синильной кислоты для синтеза акрилонитрила и образование отходов сульфата аммония.
Наиболее близким по технической сущности и достигаемому эффекту к изобретению является способ получения метакриловой кислоты или ее эфиров путем окислительного дегидрирования изобутановой кислоты или ее метилового эфира. Процесс протекает в газовой фазе при 300-500оС в присутствии катализатора следующего состава
FeP1-2V0,02-1OX где М кобальт, лантан, теллур или серебро, Х количество атомов кислорода, что отвечает степеням окисления других элементов катализатора. Концентрация исходного субстрата в газовом потоке составляет 0,1-20 мол. время контакта 0,05-3,0 с.
Недостатком данного способа является сложность его осуществления в промышленности. Процесс протекает при высоких температурах, катализатор не производится серийно. Кроме того, процесс характеризуется низкой селективностью по эфиру (56%).
Целью изобретения является упрощение процесса.
Поставленная цель достигается тем, что метилакрилат получают дегидрированием метилового эфира пропионовой кислоты на медьсодержащем катализаторе марки СНМ-1 (ТУ 6-03-370-78) согласно уравнения реакции
CH3CH2COOCH3 ____→ CH2= CH-COOCH3+H2 Процесс ведут в газовой фазе при 240-280оС. Катализатор имеет следующий состав, мас. CuO 53 ± 3 ZnO 26 ± 2 Al2O3 5,5 ± 0,7 Fe2O3 0,06 ± 0,02 NiO 0,03 ± 0,02 WO3 0,06 ± 0,02 Na2O 0,03 ± 0,02 Графит 2 ± 1 CO2 5 ± 1 Газовую реакционную смесь разбавляют азотом до объемного соотношения субстрат инерт от 0,5 1 до 2 1. Время контакта составляет 1-3 с.
П р и м е р 1. Методика проведения эксперимента.
В реактор трубчатого типа загружают 12 см3 катализатора СНМ-1 (ТУ 6-03-370-78). Температуру в реакторе поднимают до 240оС и подают в испаритель метилпропионат со скоростью 25,2 см2/ч на протяжении часа. Газовую реакционную смесь разбавляют азотом. Объемное соотношение эфир/азот 1 1. Время контакта составляет 2 с.
Полученную реакционную смесь конденсируют и разделяют на препаративной хроматографической колонне диаметром 30 мм и высотой 2 м, заполненной полиэтиленгликолем 35000, нанесенный в количестве 5 мас. на полихром-1 фракции 0,25-0,50 мм. Расход газа-носителя (азот) составляет 300 л/ч. Колонна работает при температуре 80оС.
Конверсия метилпропионата составила 5,1%
Выход метилакрилата 1,11 г (т.кип. 79,7оС, n 1,377520).
Выход метилакрилата на конвертированный метилпропионат 94%
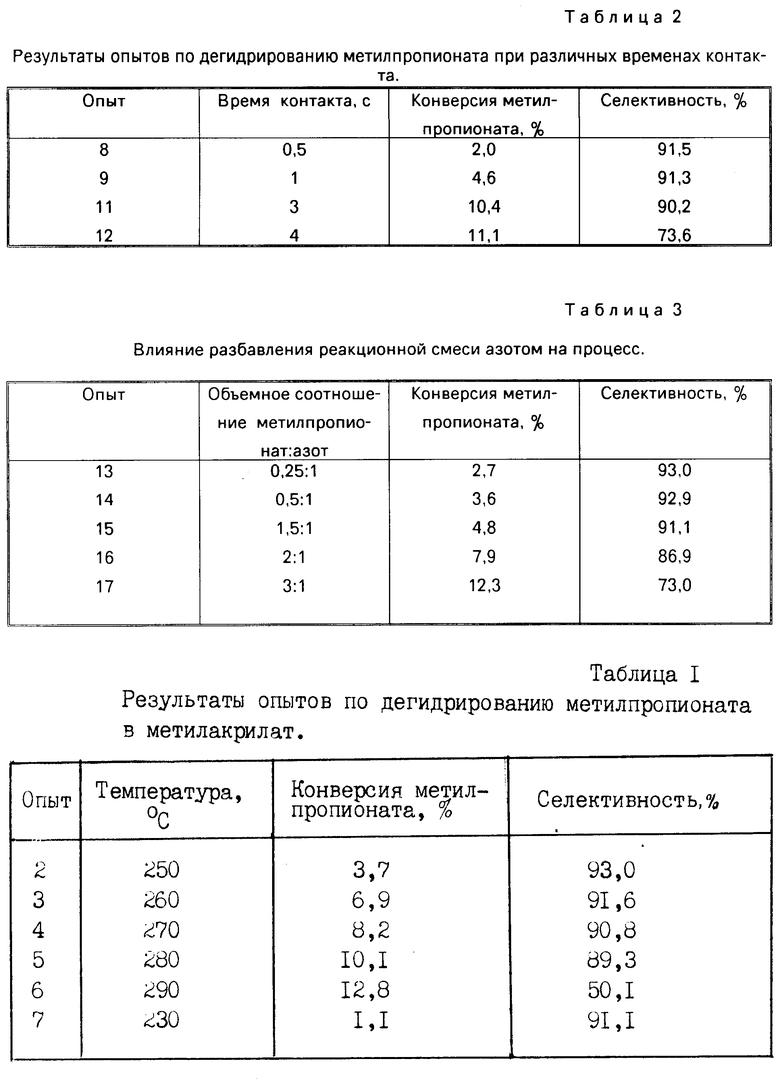
Результаты остальных опытов по изучению влияния температуры на процесс приведены в табл. 1. Время контакта во всех опытах составляло 2 с. Степень разбавления азотом 1 1.
Как видно из табл. 1, снижение температуры процесса ниже 240оС приводит к уменьшению конверсии матилпропионата, а повышение температуры выше 280оС приводит к снижению выхода метилакрилата.
Результаты опытов по влиянию времени контакта на процесс приведены в табл. 2. Температура в реакторе 270оС, соотношение субстрат инерт 1 1.
Как видно из табл. 2, при снижении времени контакта до 0,5 с существенно снижается конверсия эфира, а при увеличении времени контакта до 4 с снижается селективность процесса.
Результаты опытов по влиянию разбавления реакционной смеси азотом приведены в табл. 3. Температура в реакторе -270оС, время контакта 2 с.
Как видно из табл. 3 при увеличении соотношения эфир/инерт выше 2 1 снижается селективность процесса, уменьшение указанного соотношения ниже 0,5 1 практически не приводит к увеличению селективности процесса при одновременном снижении конверсии эфира. Таким образом, оптимальное соотношение метилпропионат/азот находится в пределах от 0,5 1 до 2 1.
Результаты опытов показывают, что предлагаемый способ позволяет получить метилакрилат с высокой селективностью, при низких температурах, используя промышленный катализатор.
Использование: производство мономеров, эфиры акриловой кислоты. Сущность изобретения: получение металакрилата ведут дегидрированием метилпропилового эфира в газовой форме в присутствии инертного газа над оксидным катализатором состава, мас.%: CuO 53 ± 3; ZnO 26 + 2; Al2O3 5,5 ± 0,7; Fe2O3 0,06 ± 0,02; NiO 0,03 + 0,02; WO3 0,06 ± 0,02; Na2O 0,03 ± 0,02; CO2 5 ± 1, графит - до 100% , при 240 - 280°С, объемном отношении метилпропионат: инертный газ = (0,5 - 2) : 1 при продолжительности контакта 1 - 3 с, селективность 91 - 93%. 3 табл.
СПОСОБ ПОЛУЧЕНИЯ МЕТИЛАКРИЛАТА дегидрированием эфира насыщенной карбоновой кислоты при повышенной температуре в газовой фазе над оксидным катализатором в присутствии инертного газа в качестве разбавителя, отличающийся тем, что, с целью упрощения процесса, в качестве эфира карбоновой кислоты используют метилпропионат, а в качестве катализатора смесь оксидов состава, мас.
CuO 53 ± 3
ZnO 26 ± 2
Al2O3 5,5 ± 0,7
Fe2O3 0,06 ± 0,02
NiO 0,03 ± 0,02
WO3 0,06 ± 0,02
Na2O 0,03 ± 0,02
CO2 5 ± 1
Графит Остальное до 100%
и процесс ведут при 240-280oС, объемном отношении метилпропионат: инертный газ, равном (0,5-2):1, продолжительности контакта газовой смеси с катализатором 1-3 с.
| Патент ФРГ N 3143152, кл | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
1995-04-10—Публикация
1990-12-25—Подача